根据国家癌症中心发布的《中国癌症报告》,乳腺癌是我国女性发病率最高的恶性肿瘤,每年发病约30.4万人。而其中HER-2阳性乳腺癌占总数的20% ~ 30%。乳腺癌患者应尽早明确HER-2状态,若提示HER-2扩增,则应持续进行抗HER-2治疗。而在抗HER-2治疗过程中,靶向药物需要与化疗联用,以获得最大获益。本文分享一例抗HER-2靶向联合口服长春瑞滨病例的诊疗思路。

浙江大学附属邵逸夫医院肿瘤内科
主治医师
致力于乳腺癌及等恶性肿瘤的内科诊疗
诊疗经过
患者,女性,51岁,2018年5月23日因“发现左乳肿块10天余”入院。既往10余年前曾行腹腔镜下胆囊切除术,2018年5月,发现子宫多发肌瘤。
专科查体
神清,精神可。双乳外形对称,双乳头无内陷、挤压无溢液,左乳9点距乳晕边缘约3.0 cm可触及一直径约1.0 cm大小类圆形肿块,质硬,边界尚清,活动度一般。肿块表面局部皮肤无红肿破溃、皮温正常。双乳皮肤酒窝征阴性,橘皮征阴性。右乳未及明显肿块。双腋下及锁骨上淋巴结未触及。
辅助检查
1.乳腺超声:双乳小叶增生;左乳多发结节,BI-RADS 4a-4b;右乳多发结节,BI-RADS 3;左腋下多发淋巴结肿大,转移可能,右侧腋下多发淋巴结可及。
2.胸部CT平扫(图1):两肺小结节,部分淡薄;左肺舌段纤维灶;左乳占位伴皮肤增厚。双侧腋下淋巴结显示,右侧腋下一肿大淋巴结。左乳可见数个结节影,较大者位于左乳头后方,大小约21.7 mm × 17.4 mm,伴左乳晕周围皮肤增厚。双侧腋下淋巴结显示,右侧腋下一肿大淋巴结,短径约13.6 mm。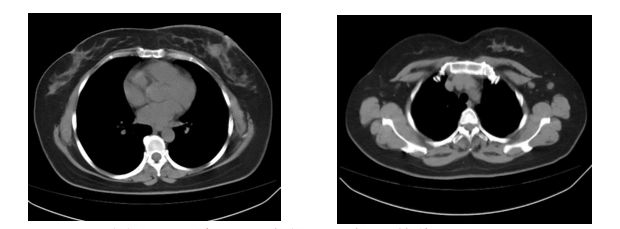
图1 2018年5月 胸部CT平扫(基线)
3.肝胆胰脾彩超:头颅MRI及骨ECT未见转移病灶。
4.病理检查:2018年5月22日,局麻下B超引导core针穿刺结果提示:(左乳11点结节CORE针穿刺)&(左乳9点结节CORE针穿刺)浸润性癌,(左腋下淋巴结CORE针穿刺)见癌转移。免疫组化A片左乳11点结节:HER-2(3+)、ER(-)、PR(-)、Ki-67(约40%+)、CK5/6(-)、Myosin(-)、Actin(-)、P63(-)、P120(膜+)、E-Cadherin(膜+)、EGFR(部分+)。D片左乳9点结节:HER-2(3+)、ER(-)、PR(-)、Ki-67(约40%+)、CK5/6(部分-)、Myosin(-)、Actin(-)、P63(部分-)、P120(膜+)、E-Cadherin(膜+)、EGFR(少量+)。
因外院已行MRI检查,本院未能留取基线乳腺MRI影像。
诊断(2018年5月):左乳浸润癌 (cT1N2M0 HER-2阳性型)
制定肿瘤治疗方案及疗效评估
新辅助治疗方案:AC-TH
2018年5月25—2018年7月28日行4周期AC方案治疗:脂质体多柔比星60 mg ig d1+ 环磷酰胺 1000 mg ig d1,q3w,过程顺利。
2018年8月18日—2018年10月28日行11次TH周疗:曲妥珠单抗针145mg ig d1(首次290 mg)+ 脂质体紫杉醇120mg ig d1,qw。期间临床查体评价病灶略缩小,影像评价最佳疗效:SD。
2018年10月30日复查乳腺MRI(图2):左乳乳腺癌复查,较前(2018年7月10日)部分肿块略饱满。双侧腋下淋巴结肿大,较前相仿。双乳小叶增生,右乳多发小结节灶,BI-RADS 3,较前相仿。
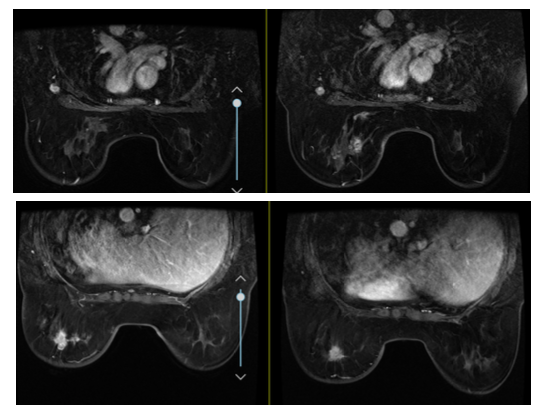
图2 第一次进展 2018年10月30日(均为右图)MRI对比2018年7月10日(均为左图)乳腺MRI
2018年10月30日,B超:脂肪肝,肝多发钙化灶,肝内中等偏低回声结节,血管瘤或不均质脂肪肝。
2018年11月5日,复查肝脏增强MRI(图3,4):肝脏多发结节灶,长T2长T1信号,DWI呈高信号,转移瘤考虑,其中右肝Ⅷ段包膜下及Ⅶ段腔静脉旁各见一T2高信号灶,大小分别约27 mm × 24 mm,11.5 mm × 9.8 mm;脂肪肝。
疗效评价:PD。
2018年11月7日,行超声引导下肝肿物切割式穿刺活检术,病理结果示:(右肝穿刺)浸润性癌,结合病史及免疫组化,考虑乳腺来源;免疫组化:ER(-)、PR(-)、HER-2(3+)、EGFR(少量+)、Ki-67(40%+),E-Cadherin(+)、P120(+)、Hepatocyte(-)、Arginase-1(-)、CK19(+)、CK20(-)。
2018年11月9日,PET/CT检查示:①a.“左侧乳腺癌化疗后”复查:左乳腺实质内多发结节,FDG代谢异常增高,考虑乳腺癌;右侧乳腺增生伴小结节,考虑BI-RADS 3类。b.两侧腋窝(右侧一枚、左侧两枚)肿大淋巴结,FDG代谢增高,考虑转移;余两侧腋窝多发小淋巴结,FDG代谢未见异常,考虑炎性淋巴结,建议密切随访。c.肝VII段近包膜侧、肝VII段腔静脉旁肿块和结节,FDG摄取增高,考虑转移瘤。②全身中轴骨FDG代谢弥漫性增高,考虑骨髓反应性增生,建议随访。③a.右肺上叶前段(IM274)水平裂胸膜下磨玻璃小结节,FDG代谢未见异常,考虑原位腺癌(AIS)可能,建议3个月后HRCT复查。b.右肺中叶内侧段、左肺上叶下舌段少许纤维化灶。④双侧上颌窦少许炎症。慢性咽喉炎。双侧颈部多发炎性小淋巴结。⑤主动脉弓少许钙化。⑥两肾结石。⑦子宫增大伴肌瘤。盆腔少许积液。⑧胃窦局部胃壁增厚,FDG代谢轻度增高,考虑炎症,建议胃镜复查。肠道炎症。⑨脊柱退行性改变。⑩颅脑FDG代谢未见异常。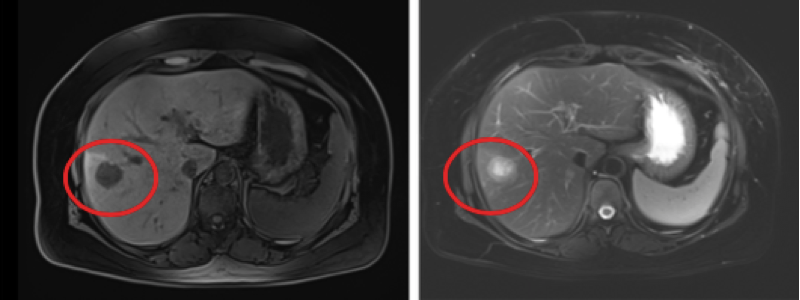
图3,4 2018年11月5日 第一次进展 肝脏增强MRI
诊断(2018年11月):左乳浸润癌 (cT1N2M1 HER-2阳性型) ,肝转移。
考虑患者在曲妥珠单抗治疗过程中病情进展,故予以二线抗HER-2治疗。 于2018年11月15日开始行第一周期“LN”方案治疗:长春瑞滨 100 mg po d1/d8+拉帕替尼 1250 mg po qd,q3w。治疗后主要发生不良反应:恶心、呕吐及腹泻,CTCAE Ⅱ级;粒细胞减少伴发热,CTCAE Ⅳ级,均经对症治疗后有好转。2018年12月6日行第2周期“LN”方案减量治疗:长春瑞滨 90 mg po d1/d8+拉帕替尼 1250 mg po qd,q3w,并预防性予以重组人粒细胞集落刺激因子等支持治疗后,无明显不良反应发生。2周期后复查CT,2018年12月20日胸部CT增强(图6)示:两肺淡薄小结节,较前(2018年5月22日)部分结节不明显,余相仿;左肺舌段纤维灶;左乳乳晕后方皮肤增厚,较前肿块影不明显、两腋下淋巴结缩小。2018年12月20日上腹部CT增强(图6)示:肝Ⅷ段结节灶,稍低密度结节,边缘稍模糊,径约15 mm,增强后边缘似见强化;脂肪肝;双肾小结石;胆囊术后。
综上显示乳腺病灶及肝脏转移灶均缩小,疗效:PR。后继续本方案治疗至2019年6月,期间定期复查评估,疗效仍为PR。
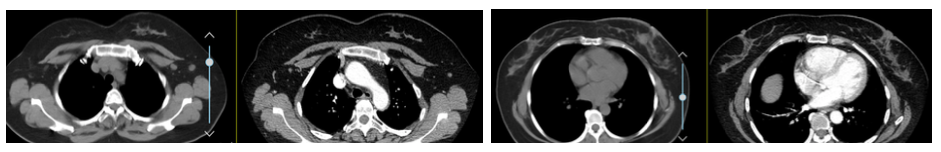
图5 2018年12月20日 LN方案后第一次疗效评价 胸部CT增强
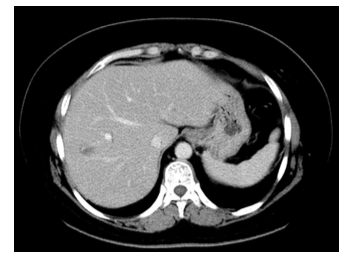
图6 2018年12月20日 LN后第一次疗效评价 上腹部CT增强
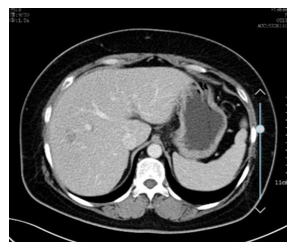
图7 2019年3月29日 上腹部CT增强

图8 LN方案治疗期间 患者血肿瘤标记物变化趋势
2019年6月5日胸部及上腹部CT增强示:两肺磨玻璃密度小结节,较前(2019年3月29日)大致相仿;左肺舌段纤维灶;动脉硬化;置管后;左乳多发结节,乳晕后方皮肤增厚;肝Ⅷ段结节灶,较前2019年3月29日增大,肝V段类似病灶新发,结合病史,转移考虑。疗效评估:PD。
2019年6月18日起行“PX”方案治疗:吡咯替尼400 mg qd+卡培他滨片1500 mg bid d1-14,q21d。主要不良反应:轻中度腹泻,手足综合征。因手足综合征明显,后卡培他滨减量至1000 mg/1500 mg口服。最佳疗效为:SD。至2019.11月复查胸部及上腹部CT增强,提示肝脏原病灶增大,同时有新发病灶,乳腺病灶稳定。疗效评估:PD。现拟入组DS8201临床研究。
点评

主任医师 博士生导师
浙江大学医学院附属邵逸夫医院肿瘤内科副主任兼乳腺疾病诊治中心副主任
学术任职:
中国医药教育协会临床抗肿瘤用药评价专委会副主任委员
中国抗癌协会遗传肿瘤学组委员
浙江省抗癌协会肿瘤转移专委会副主任委员
浙江省抗癌协会精准治疗专委会副主任委员
浙江省转化医学会精准医学分会副主任委员
浙江省中西医学会肿瘤学专委会副主任委员
浙江省抗癌协会肿瘤内科专委会常委
浙江省抗癌协会乳腺癌专业委员会委员
国家自然科学基金和北京市自然科学基金等基金评审专家等
患者中年女性,未绝经。分析患者的既往治疗,并结合美国国立综合癌症网络指南(national comprehensive cancer network guidelines,NCCN)2019 V2乳腺癌指南和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019)》对病例进行分析:
(1)HER-2阳性乳腺癌全程抗HER-2治疗
临床上会根据乳腺癌的患者病理组织切片中基因表达及蛋白水平将乳腺癌大致分成四类:Luminal A型、Luminal B型、HER-2阳性和三阴性乳腺癌(triple negative breast cancer, TNBC)。而乳腺癌中HER-2基因的扩增或过表达,素来被认为是最凶险的。临床研究表明,既往标准化疗治疗乳腺癌,HER-2阳性乳腺癌人群预后较差,复发风险高。抗HER-2药物出现改善这类患者的预后。该患者初诊为ⅢA乳腺癌,原发病灶穿刺病理免疫组化提示HER-2(3+),在后续治疗中及时进行化疗联合靶向抗HER-2治疗是正确且规范的。在抗HER-2的治疗中遵循了一线曲妥珠单抗、二线拉帕替尼的阶梯治疗策略,思路清晰。此外,对于该患者,早期病情进展迅速,在新辅助阶段给予标准含曲妥珠单抗的AC-TH方案,但抗HER-2治疗过程中发生疾病进展,因此后续给予LN方案作为晚期二线抗HER-2标准治疗方案。如果药物可及,在新辅助治疗阶段也可以考虑应用抗HER-2双靶方案,以尽早达到保乳、降期、保腋窝的目的。
(2)联合化疗,相得益彰
对于HR-/HER-2阳性乳腺癌患者治疗而言,积极的抗HER-2治疗是一方面,如何选择合适的化疗药物,做到抗HER-2和化疗二者强强联合、相辅相成,起到相得益彰的协同作用也至关重要。对于患者在新辅助阶段内出现疾病进展转移,一方面是因为HER-2通路未能够被有效抑制,另一方面可能是化疗药物出现的原发耐药。目前对于蒽环类、紫杉类药物耐药而言,并没有标准的化疗方案可以予以参考。可考虑的药物有卡培他滨、长春瑞滨、吉西他滨、顺铂等与之联合二线抗HER-2药物。
长春瑞滨(vinorelbine,NVB)[1-2]是一种半合成长春花生物碱,有广谱抗肿瘤活性,主要是通过影响微管或微管蛋白的动态平衡, 使肿瘤细胞的分裂在有丝分裂中期停止, 从而导致进入分裂间期或分裂后期的细胞死亡。与其他药物相比,长春瑞滨与曲妥珠单抗的联合指数最低,仅0.34,提示长春瑞滨与曲妥珠单抗具有最佳协同作用。长春瑞滨对于乳腺癌一线单药治疗的有效率为40% ~ 50%,中位至治疗失败的时间(time to treatment failure, TTF)和有效时间与蒽环类相似。在一项针对252例局部复发或转移,蒽环类和紫杉类经治的晚期乳腺癌研究中[3],吉西他滨联合长春瑞滨与长春瑞滨单药显示中位PFS联合组优于单药组(6个月vs 4.2个月,P = 0.002),但两组的中位OS并没有区别(联合组15.8个月vs单药组16.4个月),且两组非血液学毒性相似。两组耐受性均较好,神经毒性和肠道毒性相仿。此外,Ⅲ期HERNATA研究[4]显示,曲妥珠单抗联合多西他赛或长春瑞滨作为一线方案治疗HR-/HER-2+的晚期乳腺癌。两种方案虽然在中位肿瘤进展时间(TTP)、总生存期(OS)上相当,但长春瑞滨组中位至治疗失败时间(TTF)显著长于多西他赛组,提示多西他赛组因治疗相关不良事件导致的中止率高于长春瑞滨组,长春瑞滨组显示出更好的耐受性。两组患者均达到了3年左右的总生存期 ,一年生存率均为88%。该研究证实了长春瑞滨可作为紫杉类的一线替代化疗药物,联合曲妥珠单抗使用,为临床医师提供了一个可选的方案。此外,长春瑞滨的口服制剂在生物等效性研究结果显示, 80 mg/m2、60 mg/m2的口服剂量分别与静脉应用的长春瑞滨注射液30 mg/ m2、25 mg/ m2有着相近的血药浓度,临床疗效及安全性相当[5~7],但重要的一点是,口服制剂可大大提高患者的依从性,减少了患者住院的次数及治疗成本。
综上,口服长春瑞滨联合拉帕替尼即使在晚期二线也可以给患者带PFS长达8个月的临床获益,两者的联用确实起到了相辅相成、相得益彰的作用。该病例是基于指南规范,同时又结合临床实践合理治疗的成功病例,值得临床借鉴和学习。
1.Pierre Fumoleau, Joanne L. Blum, Peter Reichardt. Weekly vinorelbine is an effective palliative regimen after failure with anthracyclines and taxanes in metastatic breast carcinoma[J]. 98(6):1325-1326.
2. Lobo F , Virizuela J A , Dorta F J , et al. Gemcitabine/vinorelbine in metastatic breast cancer patients previously treated with anthracyclines: results of a phase II trial.[J]. Clinical Breast Cancer, 2004, 4(1):46-50.
3. Morabito A , Filippelli G , Palmeri S , et al. The Combination of Gemcitabine and Vinorelbine is an Active Regimen as Second-Line Therapy in Patients with Metastatic Breast Cancer Pretreated with Taxanes and/or Anthracyclines: a Phase I–II Study[J]. Breast Cancer Research and Treatment, 2003, 78(1):29-36.
4. Andersson, M, Lidbrink, E, Bjerre, K, et al. Phase III Randomized Study Comparing Docetaxel Plus Trastuzumab With Vinorelbine Plus Trastuzumab As First-Line Therapy of Metastatic or Locally Advanced Human Epidermal Growth Factor Receptor 2-Positive Breast Cancer: The HERNATA Study[J]. Journal of Clinical Oncology, 29(3):264-271.
5.Bonneterre J, Chevalier B C, Mauriac L, et al. Phase I and pharmacokinetic study of weekly oral therapy with vinorelbine in patients with advanced breast cancer (ABC)[J]. Annals of Oncology, 2014, 12(12):1683-1691.
6. M. Marty, P. Fumoleau, A. Adenis, Y. Rousseau, Y. Merrouche, G. Robinet, I. Senac and C. Puozzo. Oral vinorelbine pharmacokinetics and absolute bioavailability study in patients with solid tumors.[J]. Annals of Oncology Official Journal of the European Society for Medical Oncology, 2001, 12(11):1643.
7. Bourgeois H, Vermorken J, Dark G, et al. Evaluation of oral versus intravenous dose of vinorelbine to achieve equivalent blood exposures in patients with solid tumours.[J]. Cancer Chemotherapy & Pharmacology, 2007, 60(3):407-413.















 苏公网安备32059002004080号
苏公网安备32059002004080号


