胃癌(GC)早期症状不典型且缺乏有效筛查手段,导致多数患者确诊已是晚期,预后较差。传统血清标志物在早期诊断中敏感性和特异性不足。tRNA衍生小RNA(tsRNAs)是一类新型非编码RNA(ncRNAs),因其在体液中具有高稳定性,被认为是潜力巨大的液体活检指标。本研究旨在识别和验证胃癌血清中的差异表达tsRNAs,以期为早期诊断提供新方向[1]。【肿瘤资讯】特整理研究内容,以飨读者。
研究背景
尽管临床实践中一直在利用传统血清肿瘤标志物(如CEA、CA19-9、CA72-4等)进行监测和辅助诊断,但这些标志物在早期胃癌诊断中普遍存在灵敏度低、特异性差的局限性,难以有效区分早期癌症与良性疾病,无法满足临床上对精准早期筛查和实时动态监测的迫切需求。因此,寻找新型、高稳定性、特异性更强的分子标志物,并将其与现有指标联合应用,是提高胃癌早期诊断准确率的关键挑战。
近年来,tsRNAs作为一类新型的ncRNAs,因其结构稳定,在体液循环中具有相对高丰度和强耐受性,已被视为极具潜力的“液体活检”生物标志物。越来越多的研究揭示tsRNAs参与了多种癌症的发生、发展和转移过程,提示其有望成为弥补传统标志物不足的新型工具。
本研究正是在传统标志物效能受限和新型生物标志物探索成为趋势的背景下进行的。研究旨在系统性地识别和验证在胃癌患者血清中具有诊断和预后价值的tsRNAs分子,并重点探讨其中差异显著的tRF-18-HR05X6D2的临床应用价值、与临床病理参数的相关性以及促癌机制,以期为提高胃癌的早期诊断精度和精准治疗提供坚实的科学依据。
研究方法
研究设计与样本采集
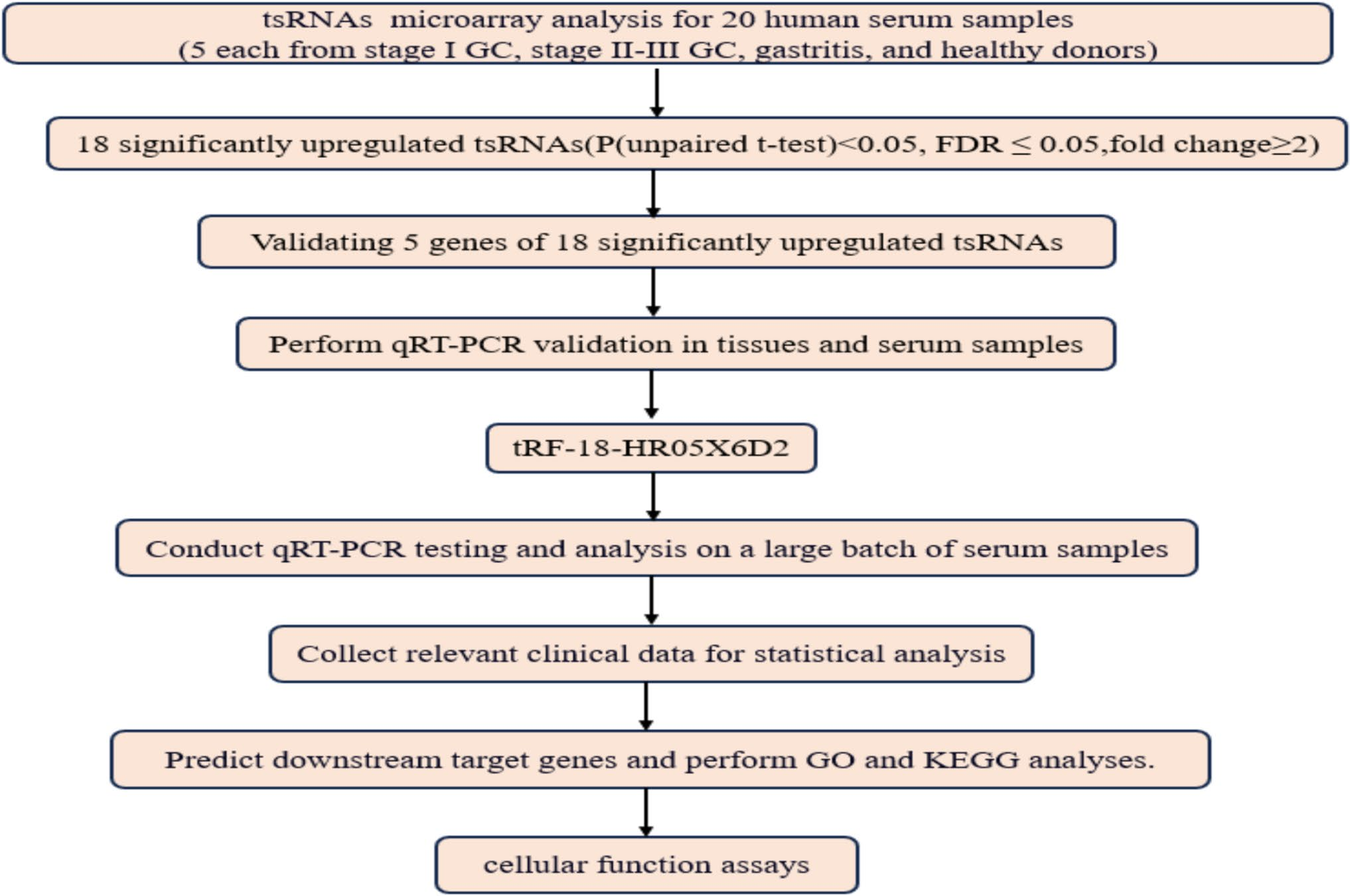
本研究旨在探究 tRF-18-HR05X6D2 作为GC诊断生物标志物的潜力及其病理机制。研究首先采用微阵列检测技术,对来自5例I期GC患者、5例II–III期GC患者、5例浅表性胃炎患者和5例健康捐献者的血清样本进行初步分析,以筛选差异表达的tsRNAs。随后,采用定量实时聚合酶链反应(qRT-PCR)对血清、组织和细胞系中的目标分子tRF-18-HR05X6D2进行进一步验证和定量分析。大规模临床样本采集自南通大学附属医院:(1)血清样本:包括116例术前GC患者、80例胃炎患者、28例术后GC患者和88例健康捐献者。此外,还收集了20例肝细胞癌(HCC)、20例结直肠癌(CRC)和20例乳腺癌(BC)患者的血清样本以评估特异性。(2)组织样本:收集了12对GC组织及其相邻非癌组织。所有GC患者在样本采集前均未接受放疗或化疗。
标志物特性评估与细胞实验
分子特性评估:通过室温孵育和重复冻融循环实验,评估tRF-18-HR05X6D2检测性能的稳定性。利用琼脂糖凝胶电泳(AGE)和Sanger测序对qRT-PCR产物进行鉴定。
功能研究:通过CCK-8实验评估tRF-18-HR05X6D2抑制剂对GC细胞增殖的影响。通过Transwell实验检测其抑制剂对GC细胞迁移和侵袭能力的影响。
下游机制预测:利用miRanda、RNAhybrid、TargetScan和RIsearch 等数据库进行生物信息学分析,预测 tRF-18-HR05X6D2 的下游靶基因,并进行 GO 和 KEGG 富集分析。
诊断效能评估
通过受试者工作特征(ROC)曲线和曲线下面积(AUC)评估血清 tRF-18-HR05X6D2单独使用以及与传统标志物(CEA、CA19-9、CA72-4)联合使用在区分GC患者与健康个体及胃炎患者时的诊断效能。
统计学分析
采用Mann-Whitney U检验进行两组独立样本比较。使用Wilcoxon符号秩检验分析术前与术后血清以及GC组织与癌旁组织的表达差异。采用χ2检验分析tRF-18-HR05X6D2表达水平与患者临床病理参数(如肿瘤大小、TNM 分期、淋巴结转移和血管侵犯)的相关性。P<0.05被认为具有统计学意义。
研究结果
tsRNA微阵列分析与目标筛选
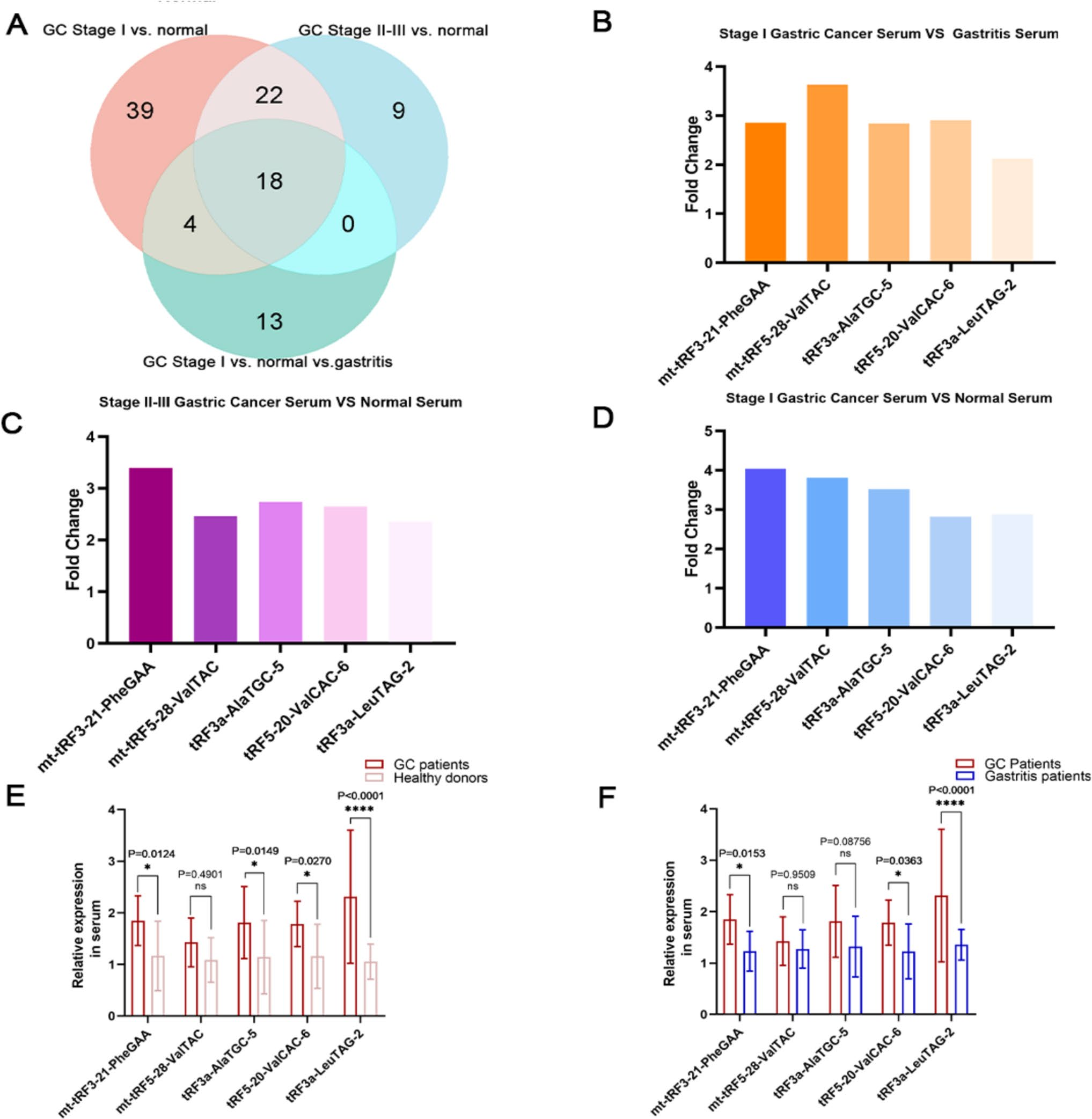
研究首先对来自GC患者、胃炎患者和健康捐献者的20例血清样本进行了tsRNA微阵列分析。结果显示,与健康对照组相比,I期GC患者血清中有83个tsRNAs显著上调;II–III期GC患者血清中有49个tsRNAs显著上调。将这些结果与胃炎患者血清中的上调tsRNAs进行交叉比对,最终确定了18个在三组比较中均显著上调的tsRNAs。
随后,研究通过qRT-PCR对5个候选tsRNAs进行了验证,结果表明mt-tRF3-21-PheGAA、tRF3a-AlaTGC-5、tRF5-20-ValCAC-6和tRF3a-LeuTAG-2在GC患者血清中的表达水平均显著高于健康捐献者。其中,tRF3a-LeuTAG-2(即tRF-18-HR05X6D2)在GC组织和多数GC细胞系中也表现出显著升高的表达,并且其在血清和组织中的表达水平呈正相关。最终,tRF-18-HR05X6D2 被选定用于后续的深入研究。
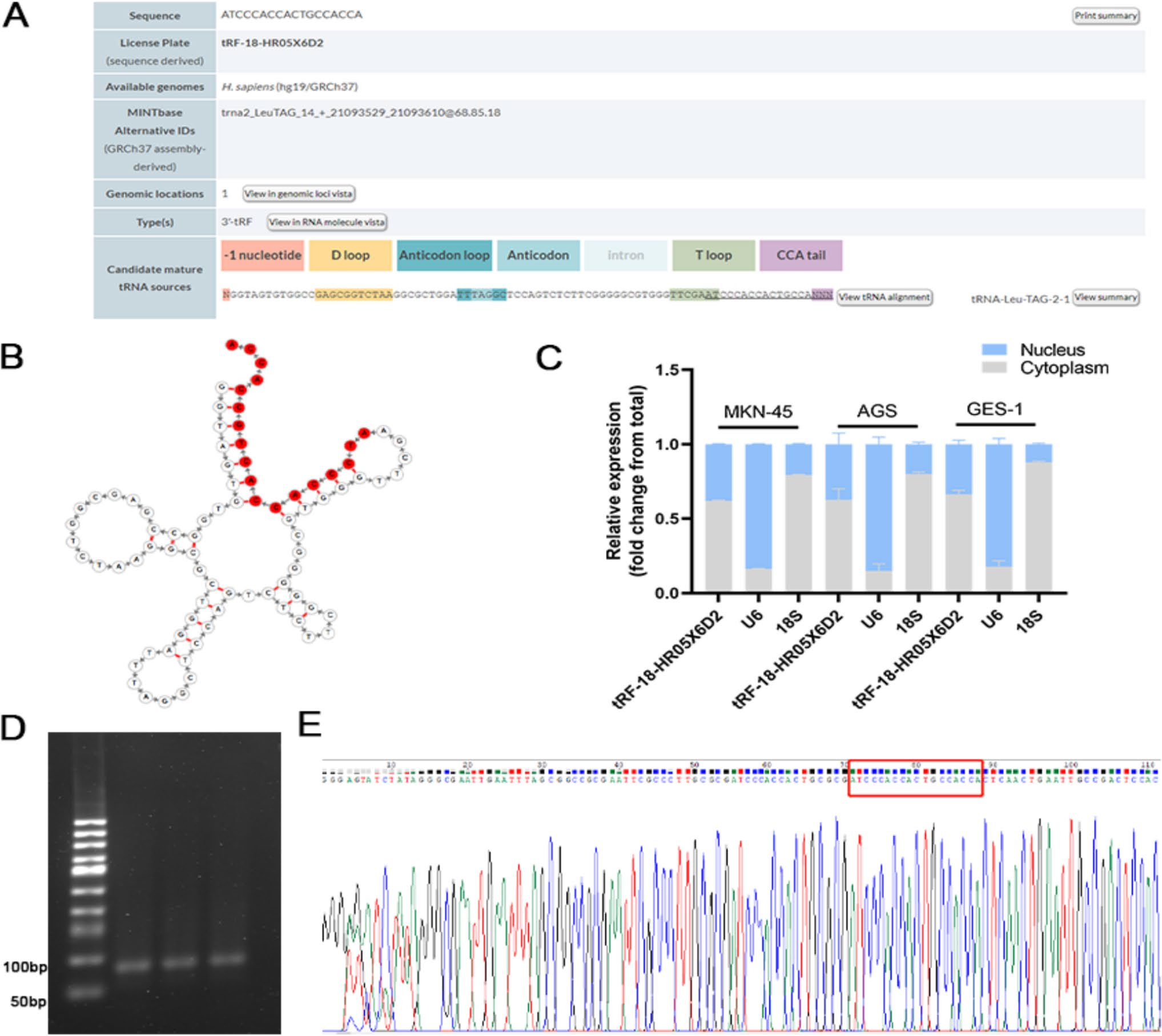
tRF-18-HR05X6D2的特性与稳定性
通过MINTbase v2.0数据库分析,tRF-18-HR05X6D2被确认为一个18核苷酸的 3'-tRF。细胞核质分离实验显示,该分子主要定位于细胞质中。方法学评估方面,该分子的批内变异系数(Intra-assay CV)为 1.55%,批间变异系数(Inter-assay CV)为2.01%。此外,血清样本在室温孵育24小时或经历10次冻融循环后,tRF-18-HR05X6D2的Ct值均无显著变化,表明其检测方法稳定可靠。
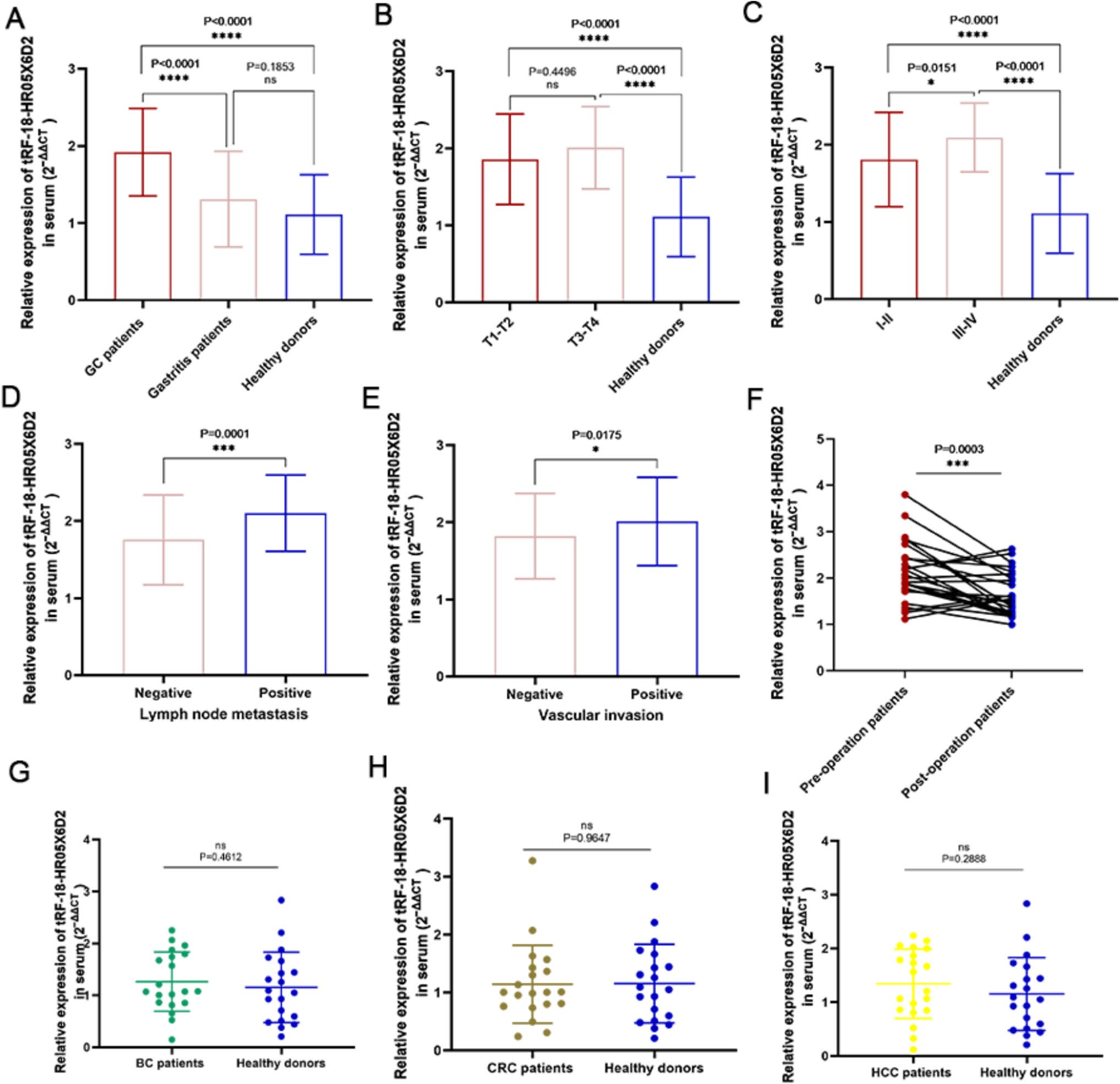
临床病理相关性分析
在对116例GC患者、80例胃炎患者和88例健康对照者的大规模血清样本队列中,tRF-18-HR05X6D2的表达水平在GC患者中显著高于胃炎患者和健康对照组(P<0.0001)。与临床病理参数的χ2检验分析结果显示:
肿瘤特征:tRF-18-HR05X6D2高表达与肿瘤大小(≥5cmvs.<5cm,P=0.009)、浸润深度(T3-T4 vs. T1-T2,P=0.014)、TNM分期(III-IV期vs.I-II期,P =0.004)、淋巴结转移(P=0.002)和血管侵犯(P=0.003)呈显著正相关。
术后变化:28例GC患者在手术治疗后,血清tRF-18-HR05X6D2表达水平显著下降(P=0.0003)。
特异性:tRF-18-HR05X6D2在BC、CRC和HCC患者血清中的表达与健康对照组相比无显著差异。
诊断效能评估
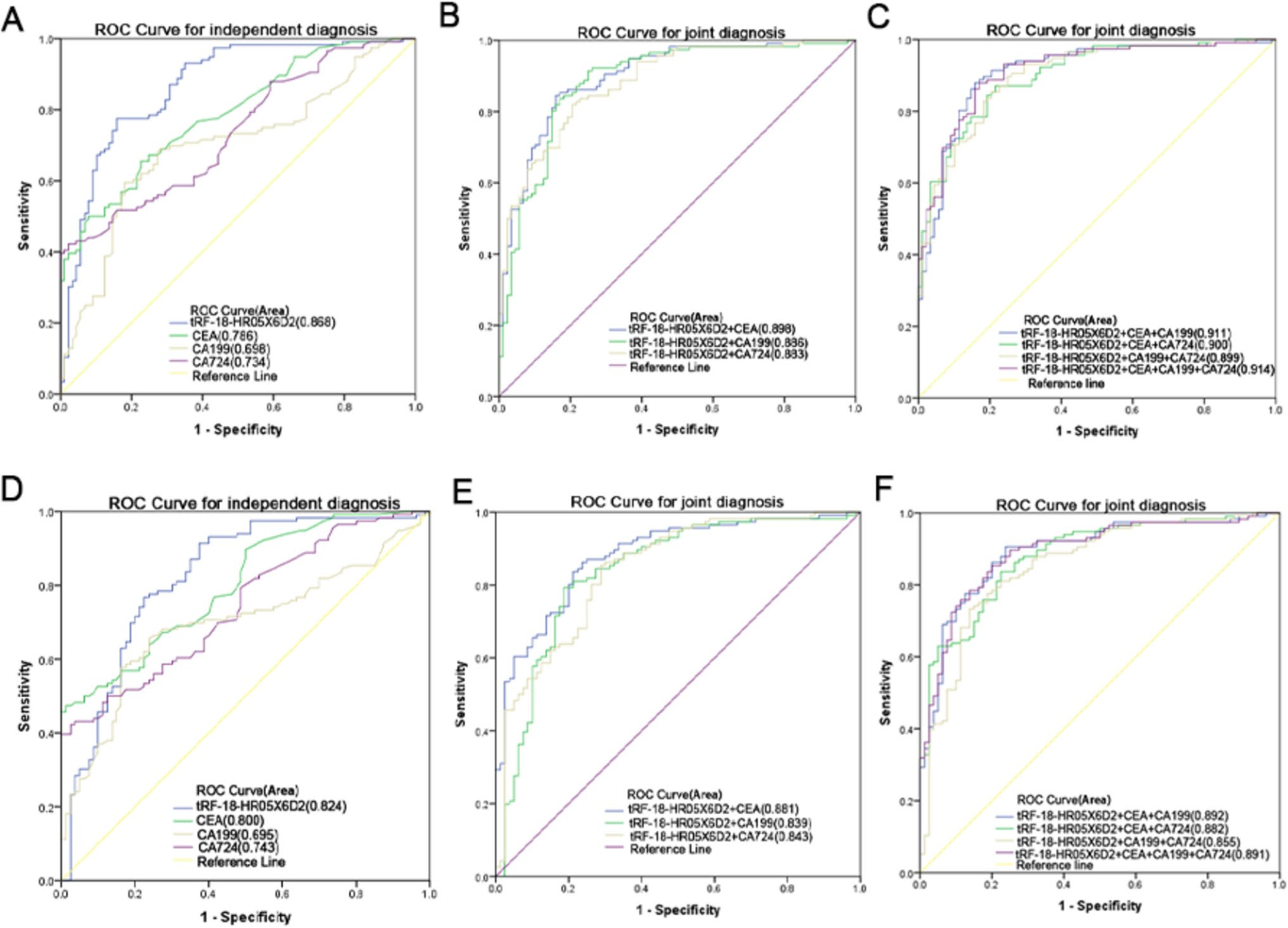
区分GC与健康对照:tRF-18-HR05X6D2单独诊断GC的AUC为0.868,优于CEA(0.786)、CA19-9(0.698)和CA72-4(0.734)。当tRF-18-HR05X6D2与所有三个传统标志物联合诊断时,AUC达到最高值0.914。单用tRF-18-HR05X6D2的灵敏度(SEN)为77.59%、特异性(SPE)为84.09%;而四项标志物联合检测的SEN提高至96.55%。
区分GC与胃炎患者:tRF-18-HR05X6D2单独诊断的AUC为0.824,仍高于CEA(0.800)、CA19-9(0.695)和CA72-4(0.743)。四项标志物联合检测的AUC达到0.891。
机制预测
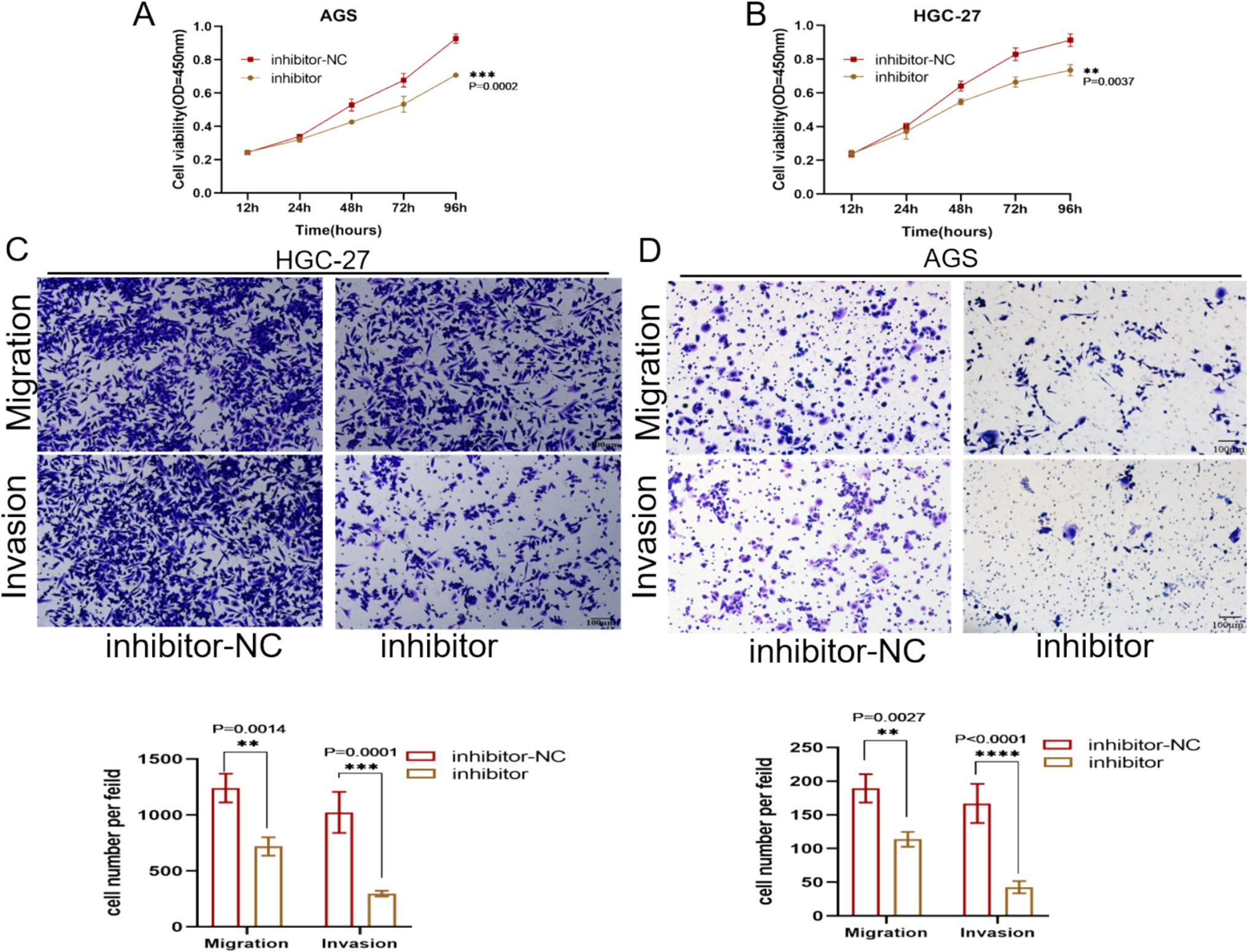
生物信息学分析预测的tRF-18-HR05X6D2下游靶基因主要富集于癌症细胞信号转导和代谢等通路,特别是ErbB信号通路,提示该分子可能通过调控此通路影响GC进展。细胞功能实验结果支持了这一预测,抑制tRF-18-HR05X6D2可显著抑制GC细胞(AGS和HGC-27)的增殖、迁移和侵袭能力(P<0.05)。
结论
这项基于大规模临床血清样本的研究结果初步表明,血清tRF-18-HR05X6D2有望作为GC诊断和预后评估的潜在生物标志物。研究证实,tRF-18-HR05X6D2的表达水平在GC患者血清中显著升高,并且与淋巴结转移、TNM分期以及血管侵犯等多种不良临床病理特征呈正相关。本研究通过ROC曲线分析证实,tRF-18-HR05X6D2单独检测具有较高的诊断效能(AUC达0.868),且当其与传统肿瘤标志物(CEA、CA19-9、CA72-4)联合检测时,能够显著提高胃癌的诊断敏感性和准确性(联合检测AUC最高达0.914)。此外,细胞功能实验结果进一步揭示tRF-18-HR05X6D2具有促进GC细胞增殖、迁移和侵袭的能力,提示其可能参与胃癌的发生发展。这一发现不仅为胃癌的早期非侵入性诊断提供了新的分子靶标,也指明了未来深入探索其在ErbB等信号通路中的调控机制方向。未来需要更大规模的多中心前瞻性研究来建立标准化的检测程序和诊断阈值,并进一步验证其在临床转化中的价值。
[1]Li X, Zhang W, Chen Y, et al. Serum tRF-18-HR05X6D2 may serve as a promising potential diagnostic biomarker for gastric cancer. Clin Exp Med. Published online November 18, 2025. doi:10.1007/s10238-025-01938-y.
审批编号:CN-174151 有效期:2027-4-12
声明:本材料由阿斯利康提供,仅供医疗卫生专业人士进行医学科学交流,不用于推广目的。
排版编辑:肿瘤资讯-Alex











 苏公网安备32059002004080号
苏公网安备32059002004080号


