著名BOLERO-2研究证明,靶向乳腺癌(BC)PI3K/AKT/mTOR途径有获益,但由于治疗毒性及费用,必需确定哪些患者可从此类治疗中获益最多。PI3K/AKT/mTOR途径可由多种因素激活,如PIK3CA、PIK3R1、PTEN、AKT等癌基因改变,其中部分异常改变作为PI3K抑制剂(PI3Ki)的治疗反应标志物已广泛研究。Brandão教授最近发表综述,全面讨论了雌激素受体(ER)阳性BC采用PI3Ki治疗时可用于预测治疗反应的标志物,同时还评估了PI3Ki的联合治疗。

预测 PI3Ki获益的潜在标志物
PIK3CA基因改变和PI3K途径活化
临床前研究表明,PIK3CA突变(PIK3CA-mut)BC细胞对PI3Ki更敏感,但临床评估其预测价值的研究结果相互矛盾,新辅助治疗时,PIK3CA-mut对泛PI3Ki pictilisib(OPPORTUNE研究)或α选择性PI3Ki alpelisib(NEO-ORB研究)治疗无预测价值,但似对β型PI3Ki taselisib治疗有预测作用。
进展期疾病的PIK3CA-mut的预测作用也存有矛盾,部分泛PI3Ki研究显示,血液与组织中检测到PIK3CA-mut时具有预测作用,但也有研究认为无预测作用,但总体而言PIK3CA-mut可以预测患者可从β型PI3Ki taselisib和α选择性PI3Ki alpelisib治疗中获益,PIK3CA-wild肿瘤不能从这些治疗中获益。
研究还探讨了PIK3CA两个突变最频繁区域(外显子9螺旋结构域和外显子20激酶域)作为治疗反应标志物的能力。新辅助治疗研究表明,与外显子20突变相比,第9外显子突变使得pictilisib的治疗敏感性更高,但大型SOLAR-1研究却显示,PIK3CA-mut肿瘤采用alpelisib治疗获益与突变类型无关。
PIK3CA突变预测疗效的矛盾结果可能源于可变的致癌潜能,导致肿瘤细胞对PI3K/AKT/mTOR途径活化依赖的程度不同。Mertins的研究显示,某些PIK3CA-mut乳腺肿瘤并无下游途径激活,证明PIK3CA-mut可变的致癌潜力。肿瘤可能需要另一次打击才能使得途径完全激活,这一点最近已被证明,与单一热点突变相比,顺式PIK3CA双突变导致乳腺肿瘤PI3K途径和下游信号途径活化增加,此外双突变使得肿瘤对α选择性PI3Ki更加敏感。
PIK3CA-mut肿瘤存在多种PI3Ki耐药机制,包括激活驱动细胞增殖的途径(MAPK,ER,HER2,AXL,PIM-1,FOXO转录因子);某个特定亚基被阻滞时通过其他PI3K异构体传导信号;激活PI3K途径的下游效应子,如AKT和mTOR;PI3K信号调节子缺失,如PTEN;PI3K和ER途径表观基因组间交联,导致通过PI3K抑制上调ER依赖性转录(图1)。据此,很多研究将“激活的PI3K途径” 状态作为标志物,分析转移性BC从PI3Ki治疗中的获益,虽不同研究中采用的定义不同,但通常都是联合DNA与蛋白表达进行评估,不过研究均未显示“激活的PI3K途径”的预测价值。
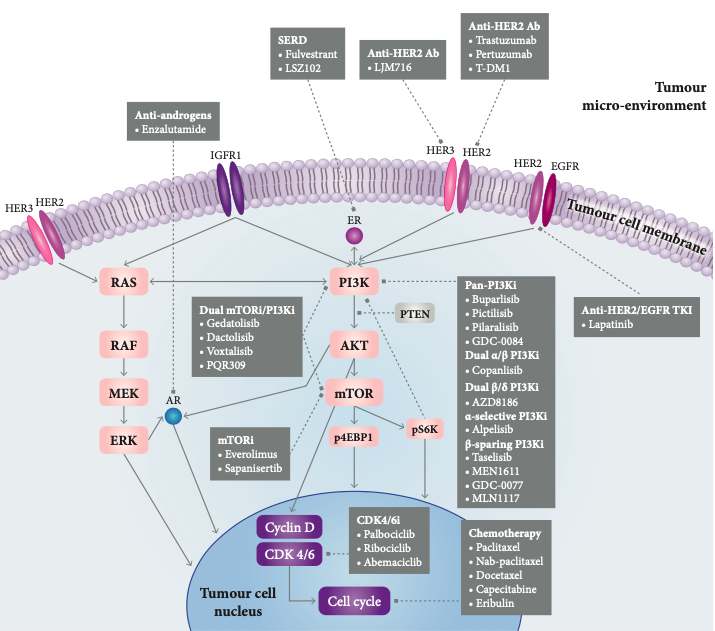
图 雌激素受体阳性乳腺癌PI3K抑制剂耐药机制以及PI3K抑制剂的联合治疗
肿瘤异质性也可解释上述矛盾结果,某些情况下,PIK3CA突变可能并非早期克隆事件,而是作为亚克隆驱动突变存在于部分转移性病灶,因此针对该途径治疗并不是非常有效。但AURORA研究显示,PIK3CA-mut在原发肿瘤与转移灶中高度一致,提示多数情况下检测到的PIK3CA-mut是克隆性的。另一方面,预测作用可能会因靶向药物不同而有变化,α选择性PI3Ki和β型PI3Ki的研究都证明PIK3CA-mut的预测作用,但不是所有泛PI3Ki研究都证明PIK3CA-mut的预测作用。此外PIK3CA突变的预测价值也可能取决于疾病背景,其致癌潜能在早期BC中的作用不如在进展期BC中重要,进展期BC的PIK3CA突变对内分泌治疗耐药具有重要作用,因此可作为内分泌治疗耐药进展期肿瘤从PI3Ki治疗获益的预测指标,但在初治肿瘤中无预测作用,如新辅助治疗时。
18F FDG-PET/CT
一项Ib研究采用buparlisib联合来曲唑治疗,18F FDG-PET/CT扫描显示无早期代谢反应者(2周)疾病迅速进展,而早期有代谢反应者治疗时间更长,提示肿瘤代谢减少预示着PI3Ki的治疗反应。目前有更大型研究对上述结果进行验证。
其他预测治疗反应的潜在标志物
OPPORTUNE研究表明孕激素受体阴性患者或luminalB型肿瘤更可能获益于pictilisib治疗,因为该药具有抗增殖作用,但在NEO-ORB研究中未证明这一点。
PI3Ki耐药的潜在标志物
PTEN表达缺失
临床前数据表明,PTEN表达缺失细胞对AKT/PI3K抑制剂(PI3Ki)更敏感。Jurice也报告一名患者在alpelisib治疗时进展,所有进展后的转移灶都携带新发PTEN表达损失,由不同基因改变所致。对该患的PTEN阴性异种移植物进行功能性分析,也提示对alpelisib耐药。已知PTEN缺失肿瘤依赖PI3Kb信号途径,可能解释了为什么OPPORTUNE研究中患者获益于泛PI3Ki pictilisib,因该药同时也可靶向PI3Kb,因此无论肿瘤是否表达PTEN均有治疗作用。目前评估“PTEN状态”仍具有挑战性,因其“缺失”可由PTEN基因缺失所致,也可能是PTEN蛋白或其他下游标志物的免疫组化表达缺失所致,如磷酸化Akt。而且这些研究使用的PTEN抗体不同,PTEN状态的定义也不一致,这使得数据间很难进行比较。
高胰岛素水平
众所周知,PI3K介导细胞对胰岛素的反应,受抑后可导致高血糖。报道显示,PI3Ki引起的高血糖可导致胰岛素释放增加,这足以使小鼠肿瘤模型中PI3K信号重新激活,即使存在PI3Ki,也最终导致治疗耐药。研究还显示,这种胰岛素反馈可采用生酮饮食预防或减轻,钠-葡萄糖共转运体抑制剂也有治疗作用,均可提高PI3Ki疗效。应注意的是,外源性胰岛素控制高血糖可进一步激活肿瘤细胞中的PI3K信号,削弱PI3Ki疗效。
上述假说可部分解释为什么SANDPIPER研究中taselisib疗效在不同地区存在差别,亚洲风险比0.38,西欧/美国/加拿大/澳大利亚0.57,拉丁美洲/东欧1.18。患者胰岛素耐药程度、饮食和高血糖治疗的不同可以解释这种差异。
目前还缺少临床数据支持上述假说,但可通过对PI3Ki临床研究数据库的探索来进一步明确,一些PI3Ki研究建议优先使用口服药物治疗高血糖。如果上述假说被证明,将会影响到PI3Ki临床研究设计,对患者选择以及随访也均有重要影响。
其他耐药的潜在标志物
数据表明,PI3Ki耐药细胞株中存在低水平Akt信号,通过使用AKTi MK-2206可使细胞对PI3Ki重新敏感,但一项I期研究中,MK-2206联合来曲唑新辅助治疗PIK3CA-mut肿瘤,结果显示不完全靶抑制,缺少对Ki67的抑制。另一项Ib研究显示,少数FGFR1/2扩增、KRAS或TP53突变患者并不能从来曲唑联合alpelisib治疗中获益,这需要更多研究证实。
标志物研究的限制性
尽管对预测PI3Ki治疗反应的标志物进行了大量研究,但目前只有PIK3CA突变 (组织或血液中检测到)获FDA批准作为alpelisib疗效预测标志物。此外,PIK3CA突变作为获益于α选择性PI3Ki的预测标志在ESCAT乳腺癌基因组改变中为IA类证据。
几个原因可以解释PIK3CA-mut对其他PI3Ki没有确定的预测作用或其他标志物为什么缺少预测作用。首先,许多分析为回顾性、探索性,只是基于少数患者。一些被检测的基因改变(如PTEN突变)频率低,统计有困难,并存在过度分析的风险。最近有研究前瞻性评估了PIK3CA-mut状态或PI3K途径激活的预测作用,PIK3CA-mut的预测作用仅在α选择性PI3Ki和β型PI3Ki的研究中得到证实。这可能部分源于泛PI3Ki耐受性较低,常因毒性而减量,导致抑制不充分,因此出现矛盾结果。
其次,测序方法和突变类型评估的差异也可能影响结果。最后,标志物大多只在基线时作了评估,CDK4/6i研究数据显示,肿瘤基因组在选择性治疗压力下可能会发生改变,因此应随着PI3Ki治疗时间推移实时评估基因改变,循环肿瘤(ct)DNA是比较便利的评估方法。
评估的时机也很重要,多数研究都是采用存档组织评估标志物,通常是原发性乳腺肿瘤。部分研究评估了组织PIK3CA-mut与ctDNA间的一致性,符合率70%~83%。BELLE-2研究中,21%原发肿瘤PIK3CA-wild的患者在开始PI3Ki治疗时ctDNA中可检测到PIK3CA-mut,提示肿瘤出现进展,因此PIK3CA-mut应在PI3Ki治疗起始时采用血液或最近的组织活检标本同时进行检测。SOLAR-1研究中,ctDNA PIK3CA-mut患者数量低于存档组织PIK3CA-mut患者数量(186和341例),表明一定比例组织PIK3CA-mut患者不能检测到ctDNA PIK3CA-mut,这与AURORA研究结果吻合,该研究超过半数转移灶中携带PIK3CA-mut患者的ctDNA中无PIK3CA-mut,因此FDA建议阴性ctDNA PIK3CA-mut患者应接受肿瘤活检评估PIK3CA-mut。SOLAR-1研究中,ctDNA PIK3CA-wild型患者未获益于alpelisib治疗,HR 0.8,进一步分析alpelisib在ctDNA PIK3CA-wild型但组织PIK3CA-mut患者的获益就显得更有意义。
未来的研究
PI3Ki研究中采用基因组学、转录组学和蛋白质组学评估乳腺肿瘤标本的结果应公开,以便更好地理解进展期BC中PIK3CA-mut及其他基因改变的预测和预后作用。今后研究中应前瞻性地评估标志物,并贯彻疾病始终,正在进行的前瞻性研究CIPLADES就是纵向评估ctDNA中的ESR1、PIK3CA和AKT1突变在一线内分泌治疗期间的变化,以评估其预测价值。免疫治疗正在成为BC的治疗选择,应该评估不同PI3Ki对肿瘤微环境的不同影响以及对肿瘤治疗反应的影响。最后,PI3Ki联合治疗正在研究中,预测其获益的标志物也是应探索的内容。
含有PI3Ki的联合治疗
临床前研究中PI3Ki的抗肿瘤活性令人鼓舞,已证明α选择性PI3Ki和β型PI3Ki对PIK3CA-mut转移性BC有效,但PI3Ki治疗过程中,疾病不可避免会进展,因此需要克服耐药、改善预后的治疗策略。根据已发现的耐药机制,PI3Ki联合治疗成为研究重点,同时抑制其他途径或阻滞PI3K下游,从而克服耐药(图)。
临床前模型中HER2阳性的BC细胞,PI3K途径激活可诱导耐药,PI3Ki治疗可恢复抗HER2治疗敏感性,因此联合PI3Ki与抗HER2治疗具有协同抗肿瘤活性。HER2阳性BC患者如携带PIK3CA-mut,对新辅助治疗反应较差。
I/II期研究证实了PI3Ki联合抗HER2治疗的总体可行性。一项II期研究纳入HER2阳性、曲妥珠单抗耐药转移性BC,给予buparlisib和曲妥珠单抗联合治疗,总的治疗反应率10%,3级毒性率70%。NeoPHOEBE研究中HER2阳性BC患者随机分入新辅助曲妥珠单抗/紫杉醇±buparlisib治疗,因严重肝毒性发生率明显增加,招募50名患者时研究中断,病理完全缓解率在二组并无差别,但buparlisib组和安慰剂组的Ki67有显著差别,分别为75%和26.7%,提示PI3Ki在HER2阳性BC中具有治疗活性,但高频严重毒性令人担忧。因为异构体选择性PI3Ki可能毒性更小,目前有研究采用其与抗HER2药物联合治疗HER2阳性BC。
PI3Ki与化疗联合
PI3K途径激活可诱导BC细胞化疗耐药,多数以PIK3CA-mut作为BC化疗反应预测因子的研究中,PIK3CA-mut患者较PIK3CA-wild者的治疗反应率更差。 因此,有研究正在评估PI3Ki与化疗联合以克服耐药。
PI3Ki与CDK4/6抑制剂联合
细胞周期素依赖性激酶(CDK)参与细胞周期调控,其异常激活是内分泌治疗耐药机制之一。临床前研究表明,BC细胞携带PI3KCA-mut时,CDK4/6抑制剂(CDK4/6i)的抗肿瘤作用因PI3K/AKT/mTOR途径激活而被削弱,CDK4/6i和PI3Ki联合治疗较单独PI3Ki更有效,提示PI3K激活是抗CDK4/6i耐药的潜在机制。早期研究显示,BC中CDK4/6i和PI3Ki联合具有治疗活性,目前有研究正在探索二者的协同效应。
PI3Ki与新型内分泌药物联合
ER阳性BC细胞的生存和增殖高度依赖ER信号,即使内分泌治疗时,ER途径仍具有活性,主要通过ESR1基因突变或其他激酶如PI3K、HER2和MAPK活化下游效应子实现。选择性ER调节剂/降解剂(SERMs/SERDs)可以结合ER,阻断信号和/或增加降解,新的SERRDs/SERMs可与突变ER结合,有效恢复阻断ESR1突变BC细胞的ER途径。ESR1-mut和PIK3CA-mut都参与内分泌治疗耐药,有研究正在评估新的SERD(LSZ102)与alpelisib联合治疗内分泌耐药的BC患者。
同时靶向PI3K/AKT/mTOR途径的多个靶点
虽然PI3Ki能有效阻滞PI3K并下调对细胞增殖的刺激作用,但BC细胞能通过激活下游效应子,如AKT和mTOR,重新激活PI3K/AKT/mTOR途径,对PI3Ki产生耐药。克服这一耐药机制的潜在策略就是多重抑制PI3K/AKT/mTOR途径,因此有研究正在评估同时阻滞PI3K/AKT/mTOR途径多个位点以克服BC治疗耐药。
高达40%表达雄激素受体(AR)的BC携带PIK3CA-mut,PI3K激酶结构域突变的BC较PIK3CA-wild BC表达更高的AR。Luminal和三阴性BC的临床前模型中,PI3K与AR途径间有交叉。表达AR的三阴性BC细胞系和异种移植模型中,PI3Ki和AR抑制剂有协同作用,联合抗肿瘤作用优于每种药物单独使用。基于临床前数据,α选择性PI3Ki alpelisib与enzalutamide(AR拮抗剂)联合治疗HER2阴性转移性BC的研究正在进行中,BC的免疫组化检查均表达AR和PTEN。
结语
尽管进行了大量研究,但目前只有PIK3CA突变在进展期BC治疗中可以预测α选择性PI3Ki和β型PI3Ki的治疗作用 。采用复合标志物可以更准确地评估PI3K/AKT/mTOR途径的激活。随着新药与PI3Ki联合应用的增多,标志物的寻找更加紧迫,以更好的指导治疗。
Brandão M, Caparica R, Eiger D, etal. Biomarkers of response and resistance to PI3K inhibitors in estrogen receptor-positive breast cancer patients and combination therapies involving PI3K inhibitors. Ann Oncol. 2019; DOI:10.1093/annonc/mdz280
排版编辑:肿瘤资讯-Ervin















 苏公网安备32059002004080号
苏公网安备32059002004080号


