每年,乳腺癌领域会有大量的新研究数据出台,医生也会花大量的时间精力学习理解。但新的研究结果是否迅速地转化成了专业知识,这些新知识在临床实践上到底给予了医生怎样的价值和意义?
让我们从一个病例说起:
【病例汇报】
2014年11月 ,49岁的胡女士在我院被确诊为乳腺癌,接受了左乳癌改良根治术(T3N2M0,IIIA期),分子分型为luminal B型(HER-2阴性)。患者术后接受了ddEC-2wP的辅助化疗及常规胸壁、锁骨上下区域放疗,并于2015年初开始口服他莫昔芬治疗,常规随访。
2016年11月,当内分泌治疗接近2年时,胡女士忽然出现剧烈的左腿疼痛,连行走都极为困难。她在家人陪同下前来我院接受检查,结果提示全身多发骨转移,除了左侧股骨头、股骨颈及左侧髋臼骨质明显破坏外,右侧肩胛、多处肋骨及椎骨、耻骨等也出现了转移。接着我们采取了骨活检,病理确诊乳腺癌骨转移,分子分型依然是ER、PR阳性,HER2阴性。
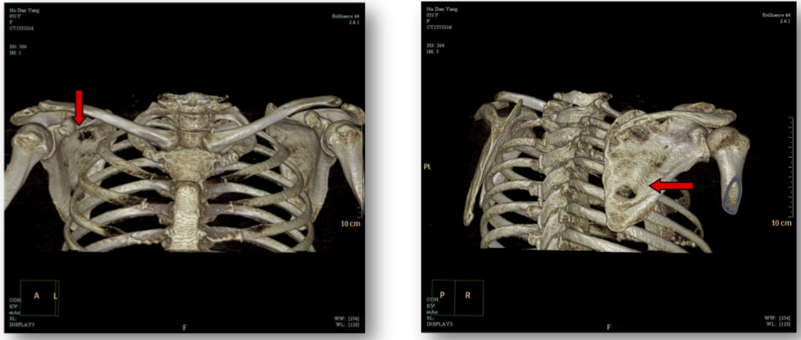
图一:2016-11-19 肩胛骨CT平扫+三维重建:右侧肩胛骨多发骨质破坏。
【诊断】
左乳癌术后多发骨转移(DFS 24月)
【治疗】
我们对胡女士的病情进行了MDT讨论,考虑到胡女士目前骨痛症状严重,并且辅助内分泌治疗不足两年,可能存在原发内分泌耐药的情况,讨论决定给予她NP方案及唑来膦酸的治疗。经历了4个周期的化疗,她的骨痛情况明显好转,恢复正常行走,肩胛骨CT平扫+三维重建提示右侧肩胛骨骨质破坏较前好转。但此时胡女士已无法耐受化疗的各种不良反应,提出停止化疗的要求。
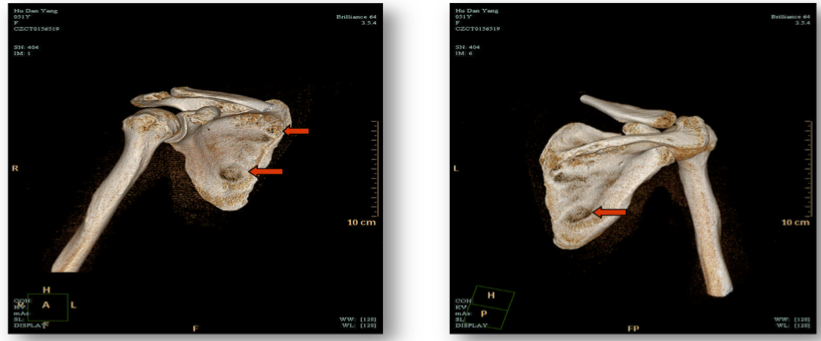
图二:2017.3.8肩胛骨CT平扫+三维重建:右侧肩胛骨骨质破坏较前好转。
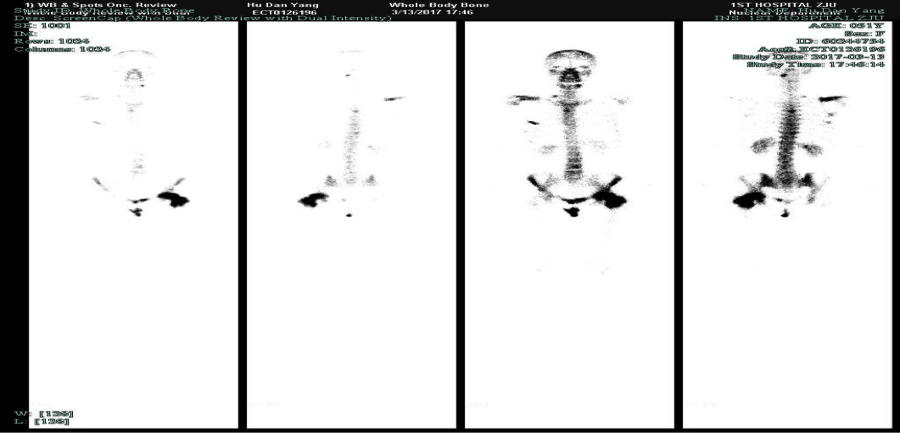
图三:2017.3.13骨骼ECT提示:颈椎上段左缘、右侧肩胛骨、右侧1后肋及5前肋、胸5、10椎体、双侧耻骨及左侧股骨上段见示踪剂分布异常浓聚。
于是我院再次组织MDT讨论,选择戈舍瑞林+氟维司群作为内分泌维持治疗方案(经检查确认胡女士尚未绝经),并继续给予唑来膦酸。患者耐受性良好。2017年7月骨骼ECT复查提示部分骨病灶代谢较前有所降低。
至今胡女士已接受戈舍瑞林+氟维司群治疗8+月,未出现任何身体不适,疗效评价SD。
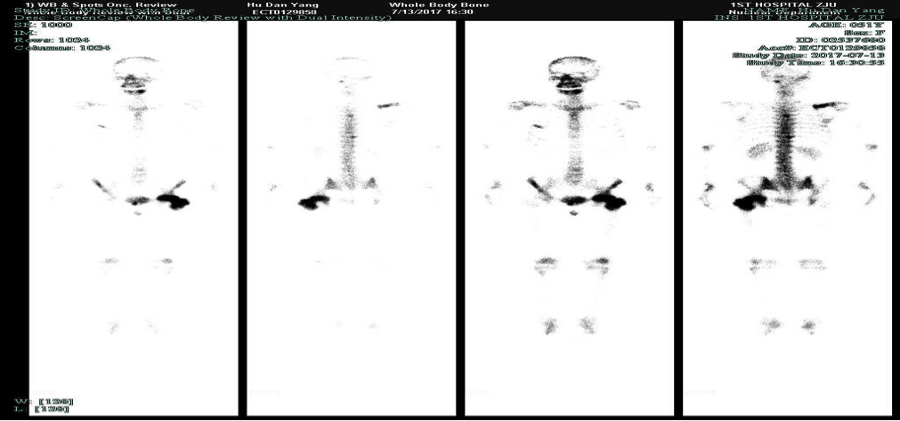
图四:2017.7.13骨骼ECT:骨骼(颈椎上段左缘、右侧肩胛骨、右侧1后肋及5前肋、胸5、10椎体、双侧耻骨及左侧股骨上段见示踪剂分布异常浓聚)骨质代谢活跃,对照本院2017-03-13ECT片,部分病灶代谢较前有所降低。
【病例小结】
52岁女性,未绝经,3年前行 “左乳癌改良根治术” ,术后接受化疗(ddEC-2wP)、放疗及他莫昔芬内分泌治疗。术后2年出现多发骨转移,予NP方案化疗4个周期。因患者不能继续耐受化疗,改用戈舍瑞林+氟维司群维持内分泌治疗8+个月,疗效评估SD。
【专家点评】

主任医师,外科学博士
浙江大学附属第一医院乳腺疾病诊治中心主任
中国抗癌协会乳腺癌专业委员会委员
中国临床肿瘤学会乳腺癌专家委员会委员
中国医师协会乳腺外科医师委员会委员
中国医药教育协会乳腺疾病专业委员会常委
中国医疗保健国际交流促进会乳腺疾病分会常委
浙江省抗癌协会乳腺癌专业委员会副主任委员
浙江省中西医学会乳腺病专业委员会副主任委员
尽管晚期乳腺癌治疗指南推荐:“内分泌治疗是ER+乳腺癌的优选治疗方案”。但该患者在辅助他莫昔芬治疗两年左右出现多发骨转移,不能排除内分泌原发耐药可能,而且从疾病发展角度看骨转移数目众多,部分骨质破坏严重,临床症状明显,已不能行走,存在着快速缓解症状的需要。

因此,虽然该患者不合并内脏转移且不直接构成生命威胁,我们仍然一线选择了化疗。但短暂的化疗以后(仅完成了4个周期的NP方案),由于患者不能耐受,拒绝继续化疗。这时摆在我们面前的就是:一线化疗获益之后的晚期患者能否使用内分泌维持治疗?该如何选择合适的方案?
对于药物的合理选择,我们回顾了既往研究的数据,并向今年新公布的临床研究寻求答案和循证医学证据。
尽管近两年内CDK4/6抑制剂联合内分泌药物的晚期一线研究提示了可喜的结果,但目前国内尚不可获得CDK4/6抑制剂。
通过回顾既往研究的数据,我们发现一项临床前的研究显示氟维司群对于他莫昔芬耐药的细胞株可以起到抑制作用。
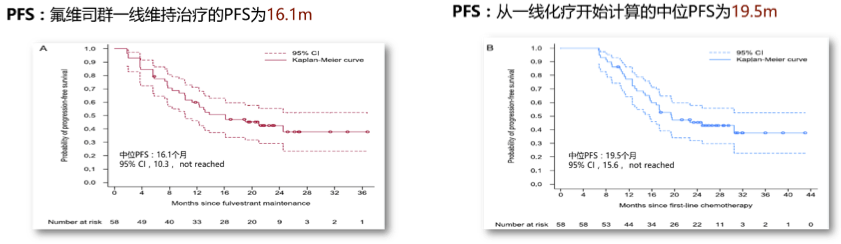
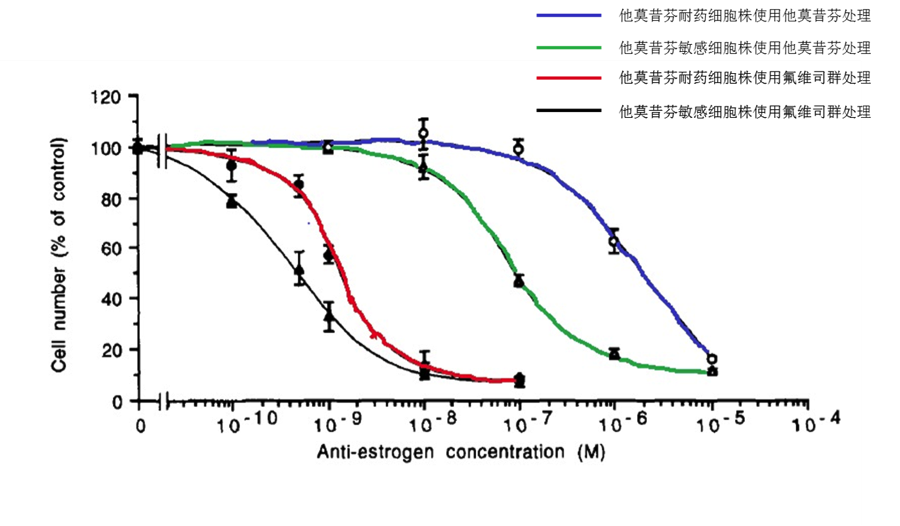 而今年ASCO发表的FANCY研究中58%的患者用过他莫昔芬,31%的患者在辅助内分泌治疗期间进展,但一线化疗后采用氟维司群维持治疗的PFS达到了16.1个月。
而今年ASCO发表的FANCY研究中58%的患者用过他莫昔芬,31%的患者在辅助内分泌治疗期间进展,但一线化疗后采用氟维司群维持治疗的PFS达到了16.1个月。
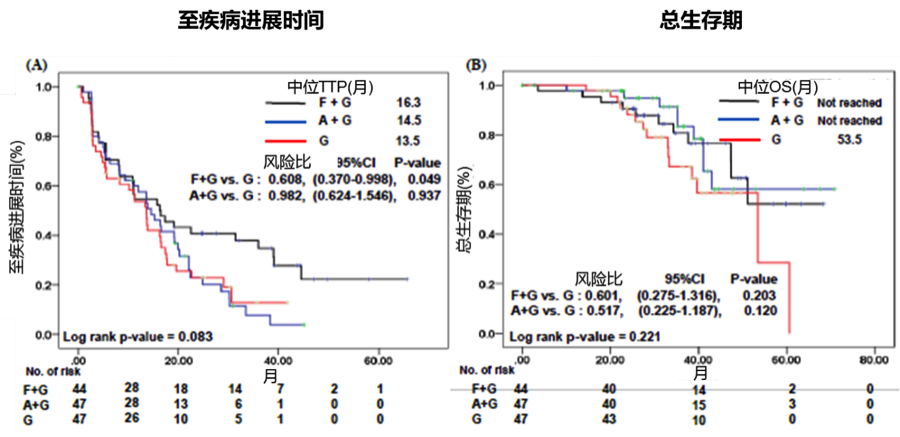
 对于未绝经患者的药物选择,同样在今年ASCO上发表的II期随机开放性临床研究KCSG BR10-04结果也显示:Tam经治的绝经前晚期乳腺癌中氟维司群+戈舍瑞林组的TTP达到16.3个月,优于阿那曲唑+戈舍瑞林和戈舍瑞林单药组。证实氟维司群联合戈舍瑞林对他莫昔芬经治的绝经前HR+晚期乳腺癌患者是有效的治疗方式。
对于未绝经患者的药物选择,同样在今年ASCO上发表的II期随机开放性临床研究KCSG BR10-04结果也显示:Tam经治的绝经前晚期乳腺癌中氟维司群+戈舍瑞林组的TTP达到16.3个月,优于阿那曲唑+戈舍瑞林和戈舍瑞林单药组。证实氟维司群联合戈舍瑞林对他莫昔芬经治的绝经前HR+晚期乳腺癌患者是有效的治疗方式。
基于以上的研究结果,我们选择了OFS+氟维司群,内分泌维持治疗有可能进一步提高一线化疗的疗效,并且相比于化疗维持毒副反应低,具备更好的耐受性。
当然对于这个病例我们也进行了反思。该患者初诊时49岁,术后病理提示左腋窝淋巴结转移达到5/16 ,肿块最大径达到6.5CM,WHOⅢ级,乳腺癌术后复发风险评估属高危,那么我们在完成常规的化疗后仅给予三苯氧胺单药是否存在内分泌治疗的不足呢?这也许需要在以后的类似患者中寻找答案。
明代著名思想家、哲学家王阳明说过:“未有知而不行者。知而不行,只是未知”。我们希望通过上述病例资料的回顾,体现如何在临床工作中将理念和实践合二为一,做到真正的知行合一,为乳腺癌患者提供更规范的治疗。
【大咖点评】

复旦大学附属肿瘤医院主任医师
教授,博士研究生导师
复旦大学附属肿瘤医院肿瘤内科主任和药物临床试验机构常务副主任
上海抗癌协会乳腺癌专业委员会副主委
上海市疾病预防控制中心乳腺癌防治专业委员会副主委
中国抗癌协会乳腺癌专业委员会常委兼秘书长
国家食品药品监督管理局审评中心审评专家
中国抗癌协会癌症康复和姑息治疗委员会常委等
我们常说要用临床研究的结果指导临床实践,做到知行合一。从傅佩芬教授分享的病例中,我们不仅看到了使用新的研究结果对既往治疗进行了反思,也看到利用最新发表的数据对后续治疗进行了指导。这是一个初诊49岁的患者;伴5个腋窝淋巴结转移;肿块大小:6.5X3.5CM;WHOⅢ级;ER(++,80%),PR(++,60%),Ki-67(约15%),乳腺癌术后复发风险分组属高危患者,STEEP评分为2.71分,为复发中高危人群。如果在辅助内分泌治疗阶段能够联合OFS,相较于仅使用他莫昔芬可以延长至疾病进展时间。但由于当地医院对辅助内分泌治疗的认识不够,他莫昔芬治疗仅1+年的时间就出现了原发耐药和疾病进展(多发骨转移),因此患者接受了化疗,但由于不能耐受化疗的毒副反应,在仅完成了4个周期的NP化疗后便要求更换治疗方案。通过对既往研究的回顾,发现氟维司群对于他莫昔芬耐药的细胞株也具有抑制作用,这可能与氟维司群独特的作用机制有关。因为相较于他莫昔芬,氟维司群的化学结构与雌激素高度相似,与雌激素受体的亲和力达89%,与他莫昔芬相比(2.5%)明显增加。并且相较于他莫昔芬仅抑制雌激素受体AF2,氟维司群可以同时阻断AF1和AF2,抑制二聚体的形成,并能阻断和降解ER,从而阻断了雌激素受体信号通路。ER与氟维司群结合后引起构象改变,促进ER的快速降解,最终降低细胞中的ER水平。而今年ASCO最新发表的FANCY研究中,31%的患者在辅助内分泌治疗期间进展,但采用氟维司群维持治疗的PFS达到了16.1个月。KCSG BR10-04研究的结果则进一步为氟维司群+戈舍瑞林提供了理论基础,氟维司群+戈舍瑞林组的TTP达到16.3个月,优于阿那曲唑+戈舍瑞林组和戈舍瑞林单药组。
基于以上研究的结果,患者接受了戈舍瑞林+氟维司群治疗,至今已8+月,且仍然在线,最新骨扫描显示部分病灶代谢较前有所降低,病情稳定。
HR+/HER2-晚期乳腺癌患者化疗后的内分泌维持治疗,在临床实践中被广泛应用,是一个合理的选择。但仍然缺乏高级别的前瞻性研究数据的支持。我们相信随着越来越多临床专家认识到内分泌维持治疗的有效性和重要性,会产生越来越多的数据来填补这一空白。
另外,这个病例的治疗验证了一个结论:今年ABC4会议和刚刚更新的NCCN指南第3版,都强调绝经前患者在采取去势的基础上,可以接受和绝经后乳腺癌一样的治疗。
正所谓“行是知之始,知是行之成”。
对于这样的病例,我们也希望听到您的建议意见,所以,诚邀您参与专家投票














 苏公网安备32059002004080号
苏公网安备32059002004080号


