肝内胆管癌(ICC)作为一种高度恶性的胆道肿瘤,其隐匿的发病特征和极高的复发转移率一直是临床治疗的难点。对于晚期不可切除的ICC患者,传统的标准化疗方案生存获益有限。近年来,免疫治疗联合靶向治疗及化疗的“三药联合”模式虽在生存期上取得了突破,但其复杂的给药方式和潜在的毒副作用限制了部分体能状态较差患者的应用。
近日,复旦大学附属中山医院樊嘉院士、周俭院士团队在BMC Medicine上发表了一项题为“Anti - PD1 antibody toripalimab combined with lenvatinib, or GEMOX chemotherapy combined with lenvatinib as first - line therapy in patients with advanced intrahepatic cholangiocarcinoma: a randomized, open, two - cohort Phase 2 Study”的重磅研究成果。该研究前瞻性地评估了“特瑞普利单抗+仑伐替尼”(“去化疗”方案)与“仑伐替尼+GEMOX化疗”两种双药联合方案一线治疗晚期ICC的疗效与安全性。
研究结果显示,特瑞普利单抗联合仑伐替尼方案取得了令人瞩目的生存获益,中位总生存期(mOS)长达20.3个月,且安全性良好。这一发现为无法耐受高强度三药联合治疗的晚期ICC患者提供了极具潜力的“去化疗”一线治疗新选择。

研究背景
ICC是起源于二级胆管及其分支上皮细胞的原发性肝脏肿瘤,其发病率在全球范围内呈上升趋势,尤其在东南亚及中国地区高发。由于缺乏特异性的早期症状,多数患者确诊时已处于晚期,失去了手术根治的机会。既往晚期ICC的标准一线治疗为吉西他滨联合顺铂(GemCis),但其中位总生存期仅约11.7个月。尽管TOPAZ - 1和KEYNOTE - 966研究将免疫检查点抑制剂引入一线治疗,将mOS提升至12.7 - 12.8个月,但患者的长期生存需求仍未得到充分满足。
研究团队此前曾开展一项II期单臂研究,探索了“特瑞普利单抗+仑伐替尼+GEMOX”的三药联合方案,取得了80%的客观缓解率(ORR)和22.5个月的mOS。然而,三药方案虽然疗效强劲,但高强度的治疗可能增加不良事件风险,未必适用于所有患者。
基于此,研究团队设计了本项随机、开放标签的II期临床试验,旨在通过“做减法”,探索在保留两种药物(靶向+免疫 或 靶向+化疗)的情况下,是否能在维持一定疗效的同时降低毒性,从而为不同耐受程度的患者提供优化的治疗策略。
研究方法
1. 研究设计与入组标准
本研究(ClinicalTrials.gov ID: NCT04361331)是一项单中心、随机、开放标签的II期临床试验。入组对象为年龄18 - 75岁、经组织病理学确认的不可切除或术后复发转移的ICC患者。患者需符合ECOG评分0 - 1分,Child - Pugh A级,且既往未接受过系统性治疗。
2. 治疗分组
研究共纳入61例患者,按1:1比例随机分配至两个队列:
A组(靶免联合组,n = 31): 接受特瑞普利单抗(240 mg,静脉注射,每3周一次)联合仑伐替尼(体重<60kg者8mg,≥60kg者12mg,口服,每日一次)。
B组(靶化联合组,n = 30): 接受仑伐替尼(剂量同上)联合GEMOX化疗方案(奥沙利铂 85 mg/m² D1 + 吉西他滨 1000 mg/m² D1, D8,每3周一次,共6 - 8周期)。
3. 评估终点
研究的主要终点是根据RECIST 1.1标准评估的客观缓解率(ORR)。次要终点包括治疗相关不良事件(TRAEs)、总生存期(OS)及无进展生存期(PFS)。同时,研究还对患者外周血中的免疫细胞及细胞因子进行了动态监测,以探索疗效预测标志物。
研究结果
1. 基线特征
两组患者基线特征均衡。A组和B组的中位年龄分别为58.4岁和59.2岁。值得注意的是,入组患者中乙肝病毒感染比例较高(约77%),且约半数患者伴有CA19 - 9水平升高(≥37 U/mL),这符合中国ICC患者的流行病学特征。
表1 患者基线特征

2. 疗效分析:A组生存获益显著
截至2023年9月1日的数据截止日,中位随访时间为18.2个月。
A组(特瑞普利单抗+仑伐替尼):
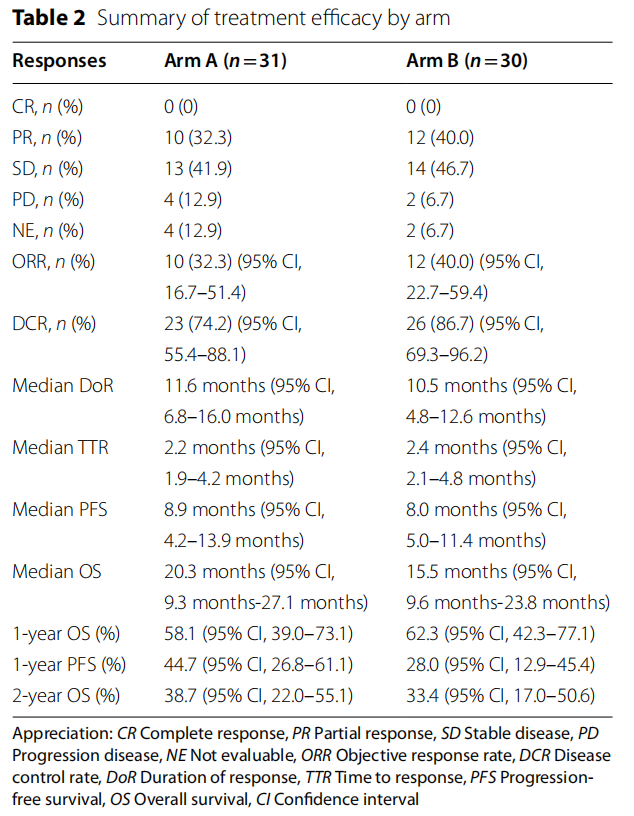
客观缓解率(ORR): 32.3%(10/31),其中包含10例部分缓解(PR)。
疾病控制率(DCR): 高达74.2%。
生存数据: 中位OS达到20.3个月(95%CI: 9.3~27.1),1年OS率为58.1%,2年OS率为38.7%。中位PFS为8.9个月。
降期转化: 令人欣喜的是,A组中有3例患者在治疗后肿瘤显著缩小,成功接受了手术切除。
B组(仑伐替尼+GEMOX):
客观缓解率(ORR): 40.0%(12/30)。尽管ORR数值上略高于A组,但并未转化为更长的生存获益。
生存数据: 中位OS为15.5个月(95%CI: 9.6~23.8),中位PFS为8.0个月。
降期转化: B组有1例患者接受了挽救性手术。
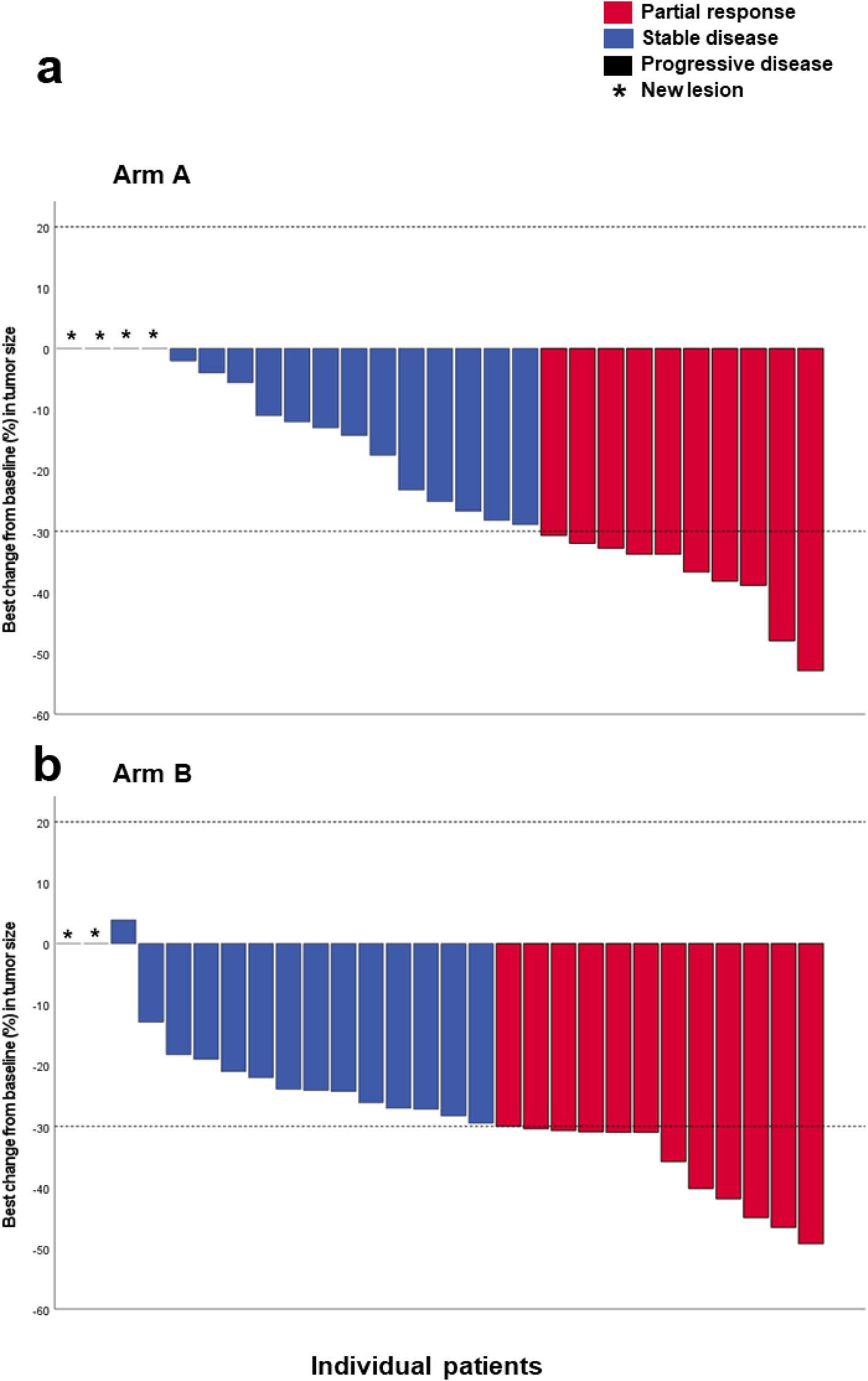
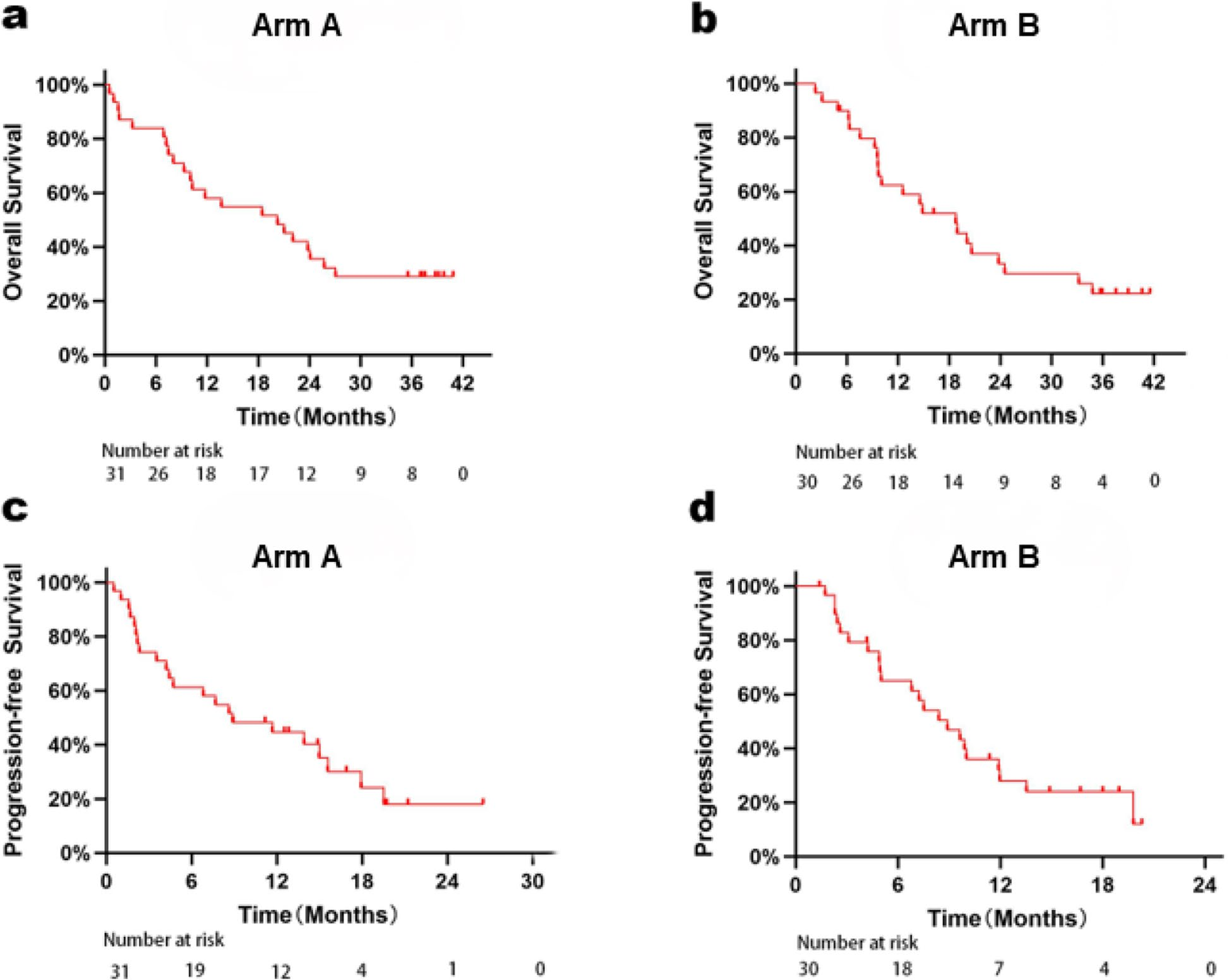
图1 ORR、OS、PFS
表2 疗效汇总
3. 安全性分析
两组治疗耐受性总体良好,未发生导致死亡(5级)的不良事件。
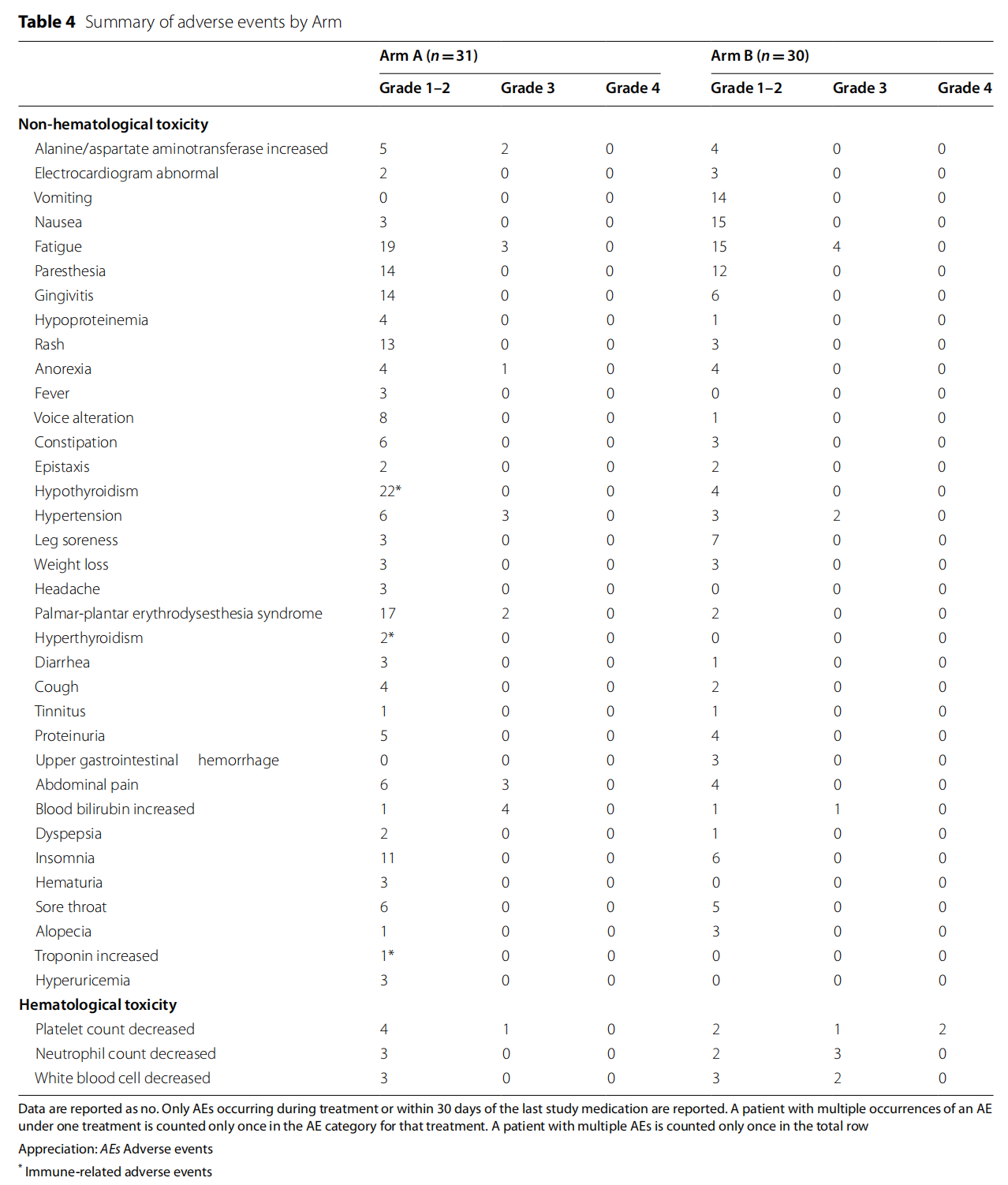
A组: 最常见的不良事件为疲劳(71%)、感觉异常(45%)和免疫相关的甲状腺功能减退(71%)。3 - 4级不良事件发生率为35.5%。
B组: 由于包含化疗药物,B组表现出更多的血液学毒性,包括血小板减少、中性粒细胞减少等。3 - 4级不良事件发生率为40.0%。
总体而言,A组的“去化疗”方案避免了化疗常见的骨髓抑制和严重的消化道反应,安全性特征更易于长期管理。
表3 不良事件
4. 探索性生物标志物分析
研究团队对外周血标志物分析发现,A组中获得PR的患者,其基线中性粒细胞比例及计数显著高于未缓解者(P<0.05)。此外,治疗有响应的患者在中位治疗后表现出IL - 8水平的下降。这提示基线中性粒细胞水平可能作为特瑞普利单抗联合仑伐替尼治疗疗效的潜在预测因子,而IL - 8的下降则可能反映了免疫微环境中促肿瘤炎症的缓解。
临床意义
1. 证实了“去化疗”策略的可行性
靶向联合免疫组合在晚期ICC中展现出强大的生存获益,说明对于部分患者,或许不需要联合高毒性的化疗药物即可获得长期生存。
2. 提供了分层治疗的依据
对于体能状态良好、追求极速缩瘤的患者,三药联合可能仍是首选;但对于无法耐受化疗或追求生活质量的患者,特瑞普利单抗联合仑伐替尼提供了一个疗效确切且更加温和的替代方案。
3. 揭示了潜在机制
中性粒细胞和IL - 8的变化为理解抗血管生成药物与免疫治疗的协同机制提供了线索,即仑伐替尼可能通过重塑免疫微环境增强了PD - 1抗体的疗效。
结论与展望
本研究是首个前瞻性比较仑伐替尼联合PD - 1单抗或仑伐替尼联合GEMOX化疗一线治疗晚期ICC的II期临床试验。研究结果表明,特瑞普利单抗联合仑伐替尼的“去化疗”方案均显示出令人鼓舞的抗肿瘤活性,尤其是20.3个月的中位OS。综上所述,特瑞普利单抗联合仑伐替尼方案为晚期肝内胆管癌患者的一线治疗提供了新的希望。
Huang XY, Shi GM, Zheng ZT, et al. Anti-PD1 antibody toripalimab combined with lenvatinib, or GEMOX chemotherapy combined with lenvatinib as first-line therapy in patients with advanced intrahepatic cholangiocarcinoma: a randomized, open, two-cohort Phase 2 Study. BMC Med. 2025;23(1):573. Published 2025 Oct 21. doi:10.1186/s12916-025-04404-4
排版编辑:肿瘤资讯-Skye











 苏公网安备32059002004080号
苏公网安备32059002004080号


