引言:肺癌是全球癌症相关死亡的首要原因,其中非小细胞肺癌(NSCLC)占比超85%,EGFR突变在东亚肺腺癌患者中发生率约为50%。EGFR酪氨酸激酶抑制剂(TKIs)的出现显著改善了这类患者的预后,但治疗相关不良事件及疗效个体差异仍是临床面临的挑战。本研究基于184例接受EGFR-TKIs治疗的NSCLC患者的回顾性数据,探讨基线白蛋白-胆红素(ALBI)分级与肝毒性、治疗失败时间(TTF)的关联,为临床精准评估治疗效果、优化用药策略提供参考。
背景
EGFR-TKIs已成为EGFR突变NSCLC患者的基石治疗药物,其药物相关不良事件包括皮疹、腹泻、肝毒性和间质性肺病等,部分患者因这些不良反应被迫停药,其中肝毒性是主要停药原因之一。根据不良事件通用术语标准(CTCAE),EGFR-TKIs治疗患者中3级及以上肝毒性发生率为5.4%-18.0%,二、三代EGFR-TKIs的肝毒性发生率低于一代药物。
已有研究表明,第一代EGFR-TKIs相关肝毒性的常见危险因素包括肝转移、EGFR外显子19缺失突变、合并使用抑酸药物(AS)或细胞色素P450(CYP)3A4诱导剂、肝炎病毒感染等,但目前关于EGFR-TKIs肝毒性的预测仍需更多证据支持。
白蛋白-胆红素(ALBI)评分/分级最初是为评估肝细胞癌(HCC)患者肝功能和预后而提出的工具,基于血清白蛋白(Alb)和总胆红素(T-Bil)这两个客观指标,相比Child-Pugh评分具有更简洁、客观且鉴别性更强的优势,改良ALBI(mALBI)评分的精细分层可准确预测HCC患者预后。虽尚未被广泛认知,但ALBI评分可能与药物诱导的肝损伤相关,ALBI分级与NSCLC患者EGFR-TKIs治疗相关肝毒性的关系尚未完全明确。
近年来研究发现,ALBI评分与部分恶性肿瘤的肿瘤学结局密切相关,但ALBI分级与NSCLC患者EGFR-TKIs治疗疗效的关联仍需进一步阐明。本研究旨在评估基线ALBI评分对接受EGFR-TKIs治疗的NSCLC患者的临床影响,回顾性分析其与肝毒性发生率及治疗失败时间(TTF)的关联。
研究方法
本研究采用opt-out方式获取知情同意。研究为回顾性设计,纳入2010年1月至2020年6月期间接受吉非替尼、厄洛替尼、阿法替尼、奥希替尼的NSCLC患者。排除标准包括:无ALBI评分、TKIs给药前未记录天冬氨酸转氨酶(AST)和丙氨酸转氨酶(ALT)水平、TKIs给药前AST/ALT水平达到CTCAE 5.0版2级及以上、在观察期外或其他机构开始治疗的患者。
通过电子病历收集患者开始EGFR-TKI治疗时的基线特征和实验室检查数据,包括性别、年龄、BMI、吸烟史、肝炎病毒感染史、肝转移情况、EGFR突变类型、实验室检查结果及合并用药等。BMI根据世界卫生组织标准及既往研究分为体重不足(<18.5kg/m²)、正常体重(18.5-25kg/m²)和超重(≥25kg/m²)。实验室检查数据包括Alb、T-Bil、AST、ALT、γ-谷氨酰转肽酶(GGT)、碱性磷酸酶(ALP)、乳酸脱氢酶(LDH)和血清肌酐,采用Cockcroft-Gault公式计算肌酐清除率(Ccr)。合并用药包括AS药物和CYP3A4诱导剂。
ALBI评分计算公式为:0.66×log10 [T-Bil(mg/dl)×1.71]-0.085×10×[Alb(g/dl)],分级标准为:1级(评分≤-2.60)、2a级(评分>-2.60且<-2.27)、2b级(评分≥-2.27且≤-1.39)、3级(评分>-1.39),参考既往研究将患者分为ALBI 1/2a级组和2b/3级组。肝毒性定义为AST或ALT水平升高至2级及以上,或医师开具保肝药物,参考既往研究监测治疗开始后180天内的AST和ALT水平。TTF定义为从首次给予EGFR-TKIs至末次给药或死亡的时间。
研究结果
患者基线特征
本研究最终纳入184例患者进行分析。患者中位年龄72岁(范围36-94岁),男性占37.5%,有吸烟史者占39.7%,无吸烟史者占52.2%,12.0%有肝炎病毒感染史,13.6%存在肝转移。EGFR突变类型中,外显子19缺失占42.4%,21外显子L858R突变占36.4%,其他突变占21.2%。治疗药物方面,吉非替尼占54.9%,厄洛替尼占31.0%,奥希替尼占9.8%,阿法替尼占4.3%。ALBI分级分布为1级50.0%、2a级22.8%、2b级22.8%、3级4.3%。
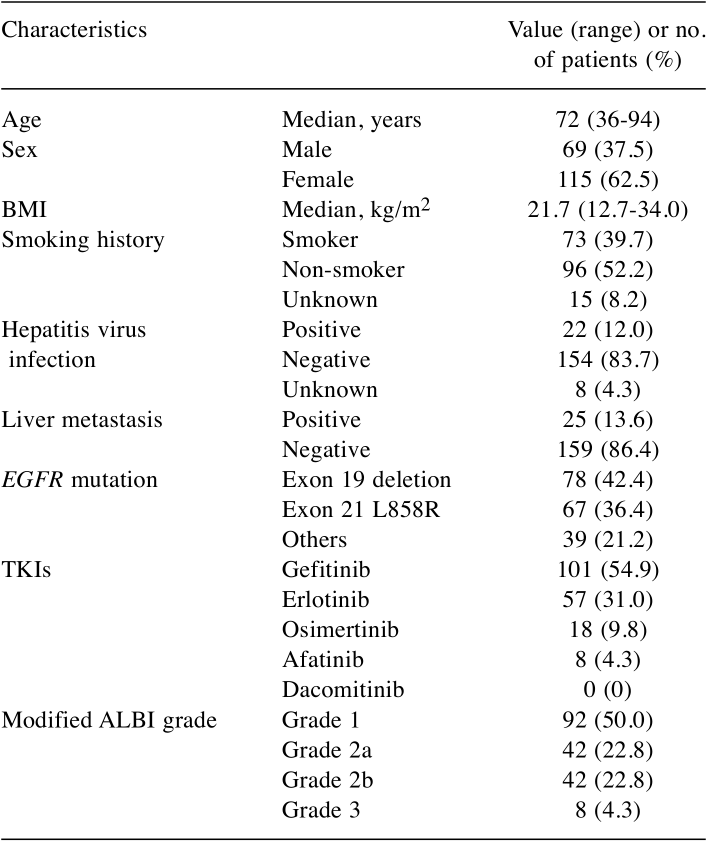
ALBI分级与临床特征的关联
分析显示,ALBI 2b/3级与BMI(p<0.01)和肝转移(p=0.02)显著相关。ALBI 2b/3级组中正常体重(BMI 18.5-25kg/m²)患者比例显著更低,体重不足(BMI<18.5kg/m²)患者比例显著更高。实验室数据显示,ALBI 2b/3级组血清白蛋白水平更低,总胆红素水平无显著差异,而GGT(p<0.01)、ALP(p<0.01)和LDH(p=0.03)水平显著升高。
ALBI分级与肝毒性的关联
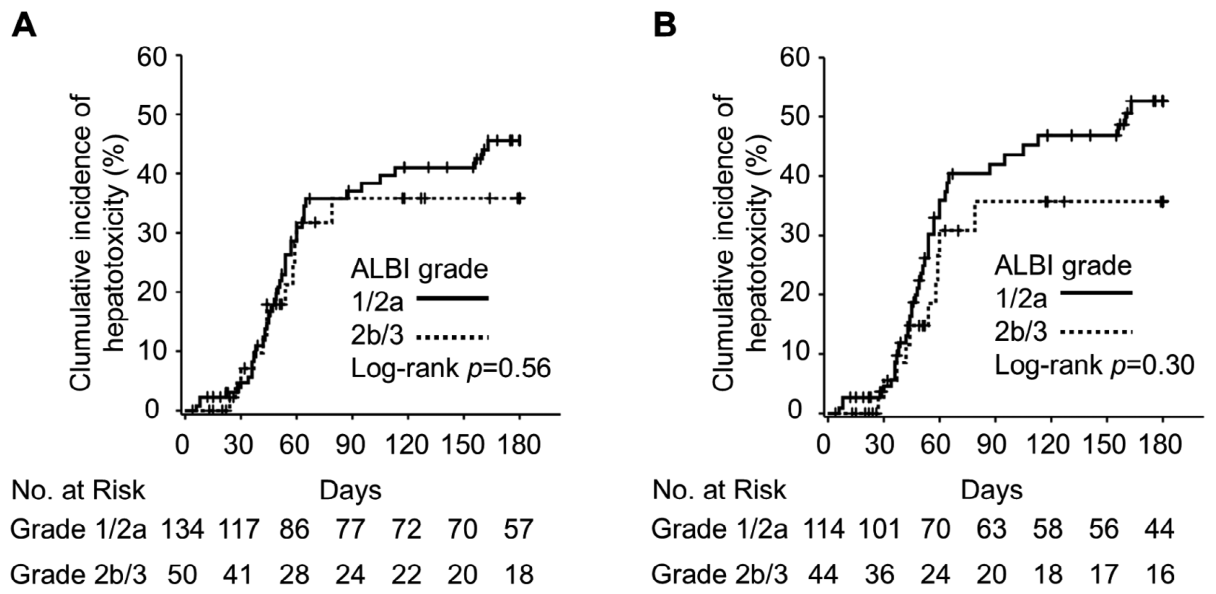
治疗开始后180天内,55例患者(29.9%)发生肝毒性,其中33例(17.9%)为3/4级肝毒性。ALBI 1/2a级组肝毒性发生率为32.1%,2b/3级组为24.0%;3/4级肝毒性发生率分别为19.4%和14.0%。Kaplan-Meier单因素分析显示,ALBI分级与肝毒性无显著相关性(log-rank p=0.56)(图1A)。
针对接受第一代EGFR-TKIs治疗的158例患者进行肝毒性相关因素分析,单因素分析显示ALBI分级与肝毒性无显著关联(p=0.30)(图1B),而合并使用AS药物与肝毒性风险降低显著相关(HR=0.50,95%CI=0.27-0.94,p=0.03),这一关联在多因素分析中仍显著(HR=0.50,95%CI=0.27-0.94,p=0.03)。
ALBI分级与TTF的关联
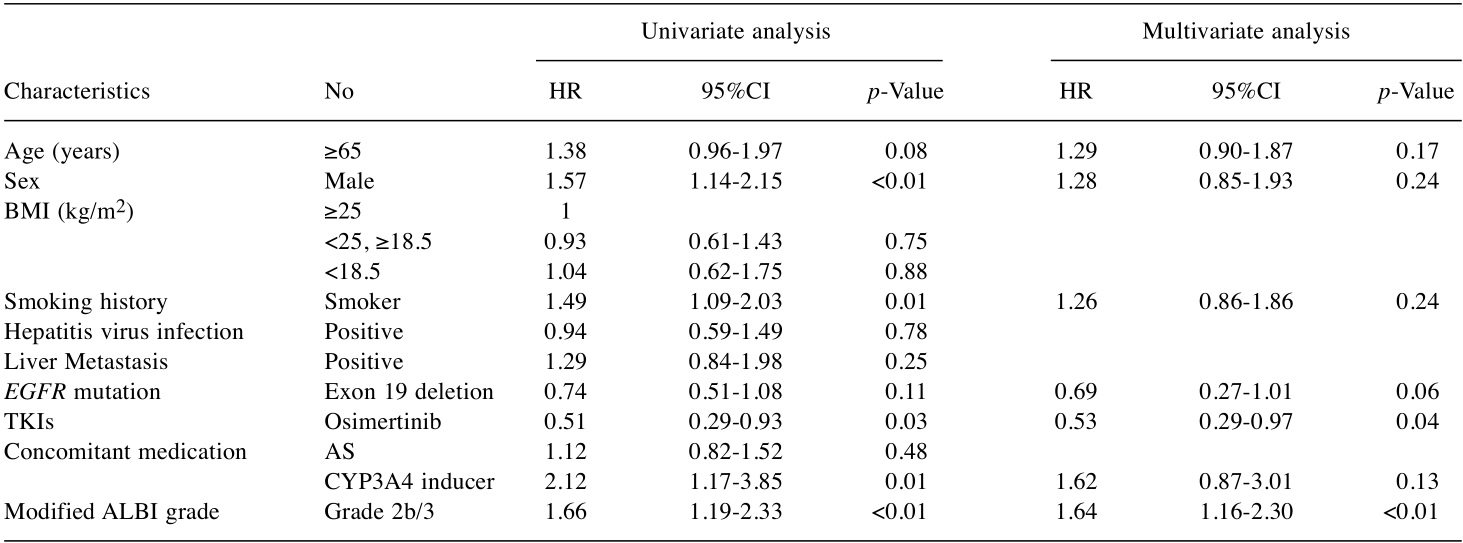
所有患者的中位TTF为8.4个月(95%CI=6.4-10.4)。Kaplan-Meier单因素分析显示,ALBI 1/2a级组中位TTF为10.6个月,显著长于2b/3级组的5.8个月(HR=1.66,95%CI=1.19-2.33,p=0.003)。单因素分析还显示,男性(p<0.01)、有吸烟史(p=0.01)、合并使用CYP3A4诱导剂(p=0.01)与TTF缩短相关。多因素分析证实,ALBI 2b/3级(HR=1.64,95%CI=1.16-2.30,p<0.01)是TTF缩短的独立预测因素,第三代EGFR-TKIs治疗(HR=0.53,95%CI=0.29-0.97,p=0.04)是TTF延长的独立预测因素。
表2 TTF相关预后因素的单因素和多因素Cox回归分析
结论
本研究通过对184例接受EGFR-TKIs治疗的NSCLC患者进行回顾性分析,发现基线ALBI分级与患者肝毒性无显著关联,但与治疗失败时间密切相关,ALBI 2b/3级是TTF缩短的独立预测因素,而第三代EGFR-TKIs治疗则与TTF延长相关,同时合并使用抑酸药物可降低第一代EGFR-TKIs治疗患者的肝毒性风险。这表明,作为评估肝功能和营养状况的工具,基线ALBI分级可有效预测EGFR-TKIs治疗NSCLC的疗效,为临床治疗决策提供参考。
然而,本研究存在一定局限性,首先为回顾性研究设计,缺乏酒精摄入、基础疾病等可能影响肝功能的相关数据,且未收集PS状态、脑转移等已知的NSCLC患者EGFR-TKIs疗效预后因素,可能存在未纳入的混杂变量影响结果,需通过随机前瞻性研究进一步验证;其次,治疗药物的样本量存在偏倚,解读结果时需谨慎;此外,研究未评估药代动力学效应,且仅基于治疗开始前的ALBI分级进行分析,未考虑治疗过程中肝功能和营养状况变化对ALBI分级及治疗结局的影响,未来需进一步开展相关研究以完善结论。
Arihara H, Nagamatsu H, Hayakawa Y, Mase H, Araya T, Kita T. Association of Pretreatment Albumin-bilirubin Grade With Hepatotoxicity and Efficacy in EGFR-TKIs Therapy for NSCLC. Cancer Diagn Progn. 2025;5(1):95-104. Published 2025 Jan 3. doi:10.21873/cdp.10417。
审批编号:CN-171622
过期日期:2026-02-11
声明:本材料由阿斯利康提供支持,仅供医疗卫生专业人士参考
排版编辑:肿瘤资讯-Sally











 苏公网安备32059002004080号
苏公网安备32059002004080号


