早期乳腺癌(BC)是指肿瘤病灶局限于乳腺、伴或不伴区域淋巴结转移(≤3个)的肿瘤。尽管早期BC预后相对良好,但要对患者进行精准风险分层以指导个体化临床决策,仍存在显著挑战——核心原因是目前缺乏能整合多类风险因素的明确预测工具。传统组织学标准是早期BC的重要预后指标,而激素受体(HR)、HER2及BRCA1/2等关键生物标志物的状态检测,也为风险分层提供了重要参考。近年来,适用于液体活检样本的组学技术快速发展,大幅拓展了早期BC的评估手段。随着风险分层相关因素的不断丰富,尽早构建基于多因素的综合病理模型,建立早期乳腺癌风险分层的标准化评估方法,已成为临床亟待解决的关键问题。
本文摘自发表在Cancers(Basel)的综述文章Advances in Early Breast Cancer Risk Profiling: From Histopathology to Molecular Technologies,旨在系统梳理当前早期BC的风险分层策略。
病理报告分析
1. 组织病理学
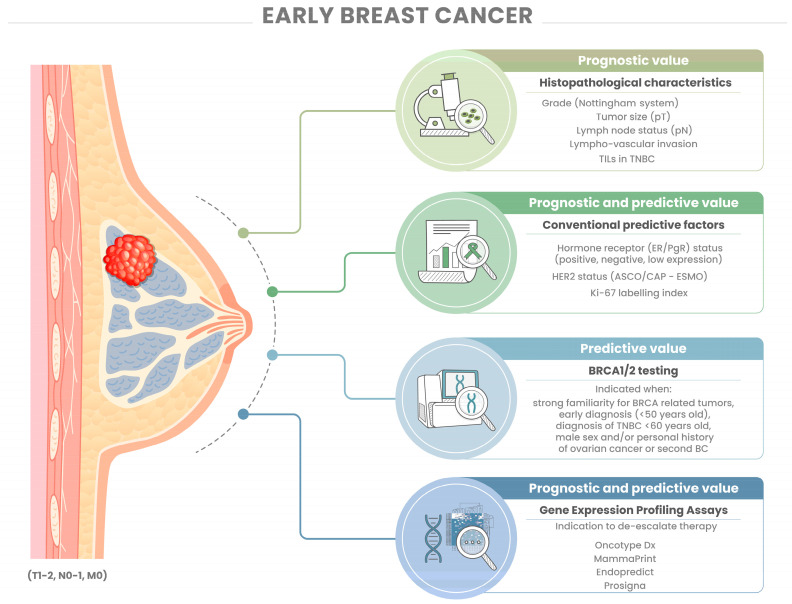
肿瘤形态学分析是BC临床决策的基石,其核心特征涵盖肿瘤类型、大小、组织学分级、淋巴结状态及脉管侵犯情况。其中,低风险组织学类型(如管状癌、黏液癌等)往往复发率低、疾病进展呈惰性,患者预后更佳;而肿瘤体积越大、组织学分级越高(通过腺管形成、细胞核多形性、有丝分裂计数三项指标评估)、受累淋巴结数量越多,或存在脉管侵犯,均提示患者复发风险更高、远期预后更差。
2. 生物标志物
1)激素受体
通过免疫组化(IHC)评估雌激素受体(ER)和孕激素受体(PR)的状态是BC管理的核心。ER阳性(定义为肿瘤细胞核阳性比例>10%)是患者能否从内分泌治疗中获益的关键决定因素;PR阳性(定义为肿瘤细胞核阳性比例≥1%)则可补充更精细的预后信息,还能为内分泌治疗方案的选择提供参考。值得注意的是,2020年ASCO/CAP指南引入了“ER低表达”(1-10%)这一类别——这类肿瘤常伴随更强的侵袭性,其临床管理和治疗策略仍是当前面临的挑战。
2)Ki-67
Ki-67指数是衡量BC细胞增殖活性的关键指标。高Ki-67水平通常与肿瘤表型更具侵袭性、患者预后更差相关,因此该指数能帮助临床区分两类患者:一类是可能从额外辅助治疗中获益的患者,另一类是可避免不必要治疗干预的患者。目前国际上对用于治疗决策的Ki-67临界值尚未达成完全共识,但临床中常以20%作为界值——既用于区分HR阳性/HER2阴性BC Luminal A型与Luminal B型,也辅助判断患者是否需要接受辅助化疗。根据ASCO指南,当Ki-67水平极低(<5%)或极高(>30%)时,Ki-67指数的预后价值尤为明确。
3)HER2
约15-20%的BC患者存在HER2过表达或基因扩增,这类患者的肿瘤临床进程通常更具侵袭性。然而,随着HER2靶向药物的临床应用,HER2阳性患者的治疗结局已得到显著改善。近年来,“HER2低表达”(FISH检测阴性,且IHC检测结果为1+或2+)的概念备受关注——它定义了新型抗体药物偶联物(ADC)的潜在获益人群。尽管目前HER2状态不影响早期乳腺癌的治疗决策,但准确评估并动态监测HER2状态,仍具有重要临床意义。
3. TILs
肿瘤浸润淋巴细胞(TILs)已成为三阴性乳腺癌(TNBC)和HER2阳性乳腺癌中重要的预后标志物。其中,高水平的间质TILs与新辅助化疗后更高的病理学完全缓解(pCR)率及更佳的生存结局显著相关,还与辅助治疗后的疗效改善存在关联。尽管其临床价值已获广泛认可,2019年圣加仑共识也明确推荐对TILs进行常规报告,但90%专家不建议仅依据TILs水平来制定治疗策略,其临床实用性仍需更多研究进一步证实。
分子分型与基因表达谱
1. 基因表达谱检测
基因表达谱检测,如Oncotype Dx、MammaPrint等,已成为HR阳性/HER2阴性早期BC个体化治疗的关键工具。基因表达谱检测工具通过分析一组特定基因的表达水平,可提供超越传统病理因素的预后与预测信息,其核心价值在于精准评估患者远期复发风险,并预测患者从辅助化疗联合内分泌治疗中的获益情况。ASCO与ESMO指南并未对特定基因表达谱检测方法有所偏好,而是强调这类检测在选择最佳辅助治疗方案中的临床价值,如用于少数淋巴结阳性(1-3个)的Luminal B型BC患者的治疗决策。
2. BRCA1/2突变
BRCA1/2胚系突变是重要的遗传性BC风险因素。携带该突变的患者不仅终生患癌风险显著升高,患有TNBC等更具侵袭性肿瘤的概率也更高;同时,BRCA1/2突变会影响治疗敏感性。OlympiA试验已证实,在携带BRCA1/2胚系突变的HER2阴性高危早期BC患者中,辅助奥拉帕利治疗相较安慰剂可显著改善生存。因此,对具有高危因素(如早发、高危家族史等)的患者进行BRCA1/2检测,对于指导治疗选择、评估未来风险以及其家人的遗传咨询,均具有重要临床意义。
总结与临床启示
早期乳腺癌的风险分层已从单纯依赖组织病理学,演变为整合病理学、关键生物标志物及分子基因组学信息的多维度综合评估体系。其中,病理学特征构成了预后评估的基础框架;激素受体、HER2和Ki-67等标志物进一步细化了分子亚型并直接指导治疗;基因表达谱检测则在特定人群中助力化疗决策的精准化。此外,TILs和BRCA1/2突变等新兴或特定标志物,分别为免疫治疗和靶向治疗提供了新的视角。未来的挑战在于:一方面需要建立标准化的检测与判读流程,确保信息的可靠性;另一方面需将多组学数据与机器学习等新技术相结合,构建更精准的预测模型,从而持续优化早期乳腺癌的个体化管理策略,最终实现疗效最大化和毒性最小化的治疗目标。
Pescia C, Guerini-Rocco E, Viale G, Fusco N. Advances in Early Breast Cancer Risk Profiling: From Histopathology to Molecular Technologies. Cancers (Basel). 2023;15(22):5430. Published 2023 Nov 15. doi:10.3390/cancers15225430
审批编号:CN-172764
过期日期:2026-11-24
声明:本材料由阿斯利康提供支持,仅供医疗卫生专业人士参考
排版编辑:肿瘤资讯-Sally











 苏公网安备32059002004080号
苏公网安备32059002004080号


