多年来,晚期肝细胞癌(HCC)的一线系统治疗一直以索拉非尼和仑伐替尼为代表的口服多酪氨酸激酶抑制剂(TKIs)为主。近期免疫联合治疗模式开启了HCC一线治疗的新纪元,但仍有相当比例的患者在一线治疗后出现疾病进展或药物不耐受,需要进行二线治疗。目前获批的二线治疗方案主要针对索拉非尼治疗失败后的患者,包括瑞戈非尼、免疫检查点抑制剂单药等。近期发表的一项韩国研究中,研究者在索拉非尼治疗失败后的患者中,对比了纳武利尤单抗和瑞戈非尼作为晚期HCC二线治疗的临床结果[1]。
研究方法
这项研究纳入了2017年8月至2021年12月期间,在该中心接受瑞戈非尼或纳武利尤单抗作为索拉非尼失败后的二线系统治疗的晚期HCC患者。索拉非尼失败后使用瑞戈非尼或纳武利尤单抗的决定由医学专家根据每位患者的具体临床情况做出。瑞戈非尼使用者每天口服160mg瑞戈非尼,每4周周期的前3周给药,允许在14天内中断治疗,并允许剂量减少(先降至120mg,再降至80mg)以管理毒性。纳武利尤单抗每2周通过静脉注射给药,每次剂量为3mg/kg。当患者出现明确的疾病进展、不可接受的毒性、系统性恶化(包括肝功能下降)或死亡时,停止治疗。主要研究终点为总生存期(OS),次要终点为无进展生存期(PFS)。
此外,为了考虑可能影响主治医生选择二线治疗方案的因素,研究者进行了1:1倾向评分(PS)匹配,以平衡治疗组之间患者的基线特征。PS模型中的协变量包括基线年龄、性别、HCC病因、肝硬化、高血压、糖尿病、既往肝切除术、既往局部区域治疗、索拉非尼维持治疗、索拉非尼失败原因、肿瘤行为、血小板计数、凝血酶原时间、总胆红素、血清白蛋白、天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶、碱性磷酸酶(ALP)、甲胎蛋白(AFP)、维生素K缺乏或拮抗剂诱导的蛋白以及Child-Pugh评分。研究还采用稳定化逆概率治疗加权(IPTW)以保留原始数据的样本量。
研究结果
基线特征
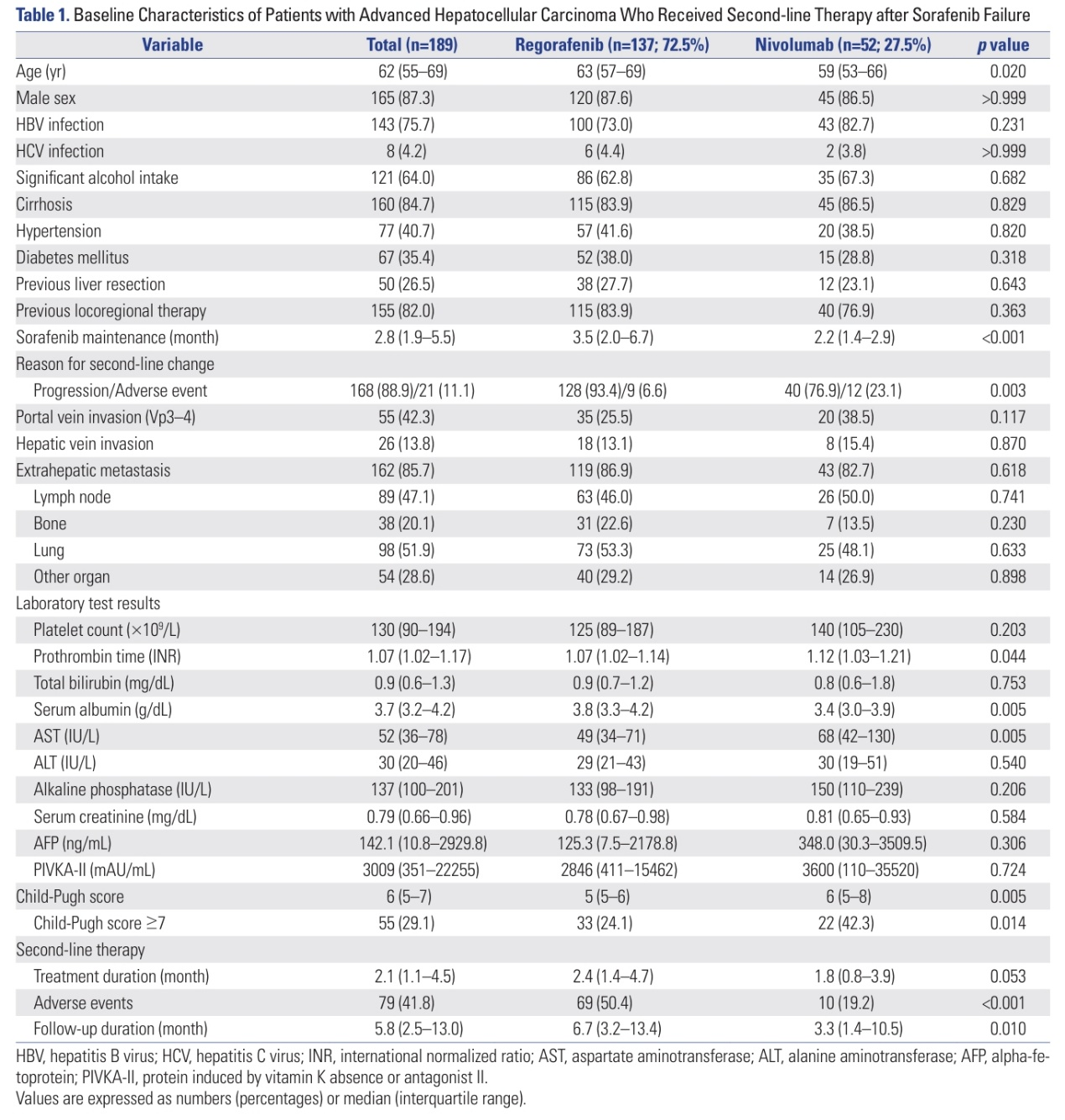
研究者将137例(72.5%)瑞戈非尼使用者和52例(27.5%)纳武利尤单抗使用者纳入统计分析。其中,大多数患者为男性(n=165,87.3%),患有肝硬化(n=160,84.7%)、乙型肝炎病毒(HBV)感染(n=143,75.7%)和酗酒(n=121,64.0%)。索拉非尼在维持2.8个月后因疾病进展(n=168,88.9%)并停用。
在二线治疗开始时,所有患者中分别有55例(42.3%)和26例(13.8%)患者有Vp3-4门静脉癌栓形成和肝侵犯,162例(85.7%)患者有肝外转移。纳武利尤单抗使用者对比瑞戈非尼使用者更年轻(中位年龄:59岁vs. 63岁),索拉非尼维持时间更短(中位时间:2.2个月vs.3.5个月),Child-Pugh评分≥7的比例更高(42.3% vs. 24.1%,所有p<0.05)。
表1. 患者基线特征
总体肿瘤缓解
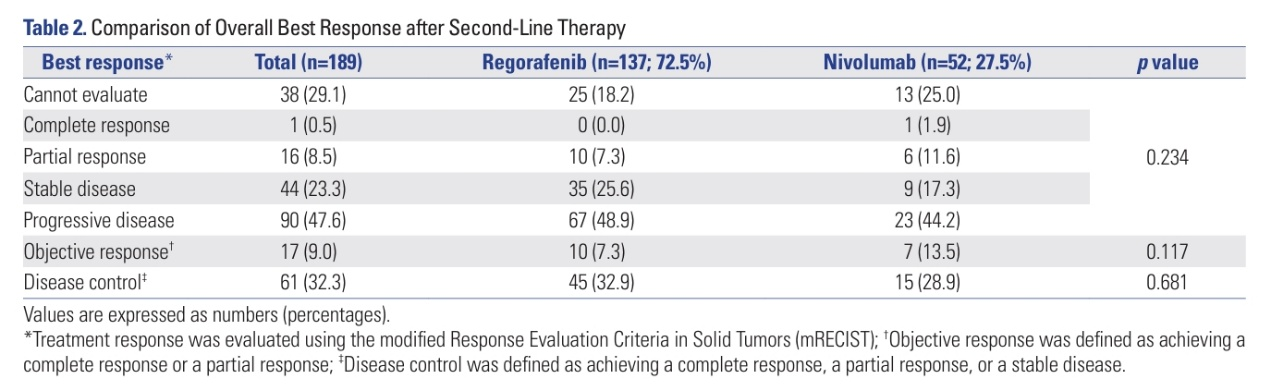
瑞戈非尼组和纳武利尤单抗组中分别有25例(18.2%)和13例(25.0%)患者因不良反应导致的早期停药、死亡、失访等原因导致无法评估肿瘤缓解。两组间的客观缓解率(ORR)差异无统计学意义(13.5%vs.7.3%,p=0.117),疾病控制率(DCR)总体相似(32.9% vs. 28.9%)。
表2. 肿瘤缓解情况
治疗结局
在随访期间,共有147例(77.8%)患者死亡,其中瑞戈非尼组104例(75.9%),纳武利尤单抗组43例(82.7%),两组的中位随访时间分别为6.7个月(IQR=3.2-13.4;最大值=40.0)和3.3个月(IQR=1.4-10.5;最大值=48.8)(p=0.010)。
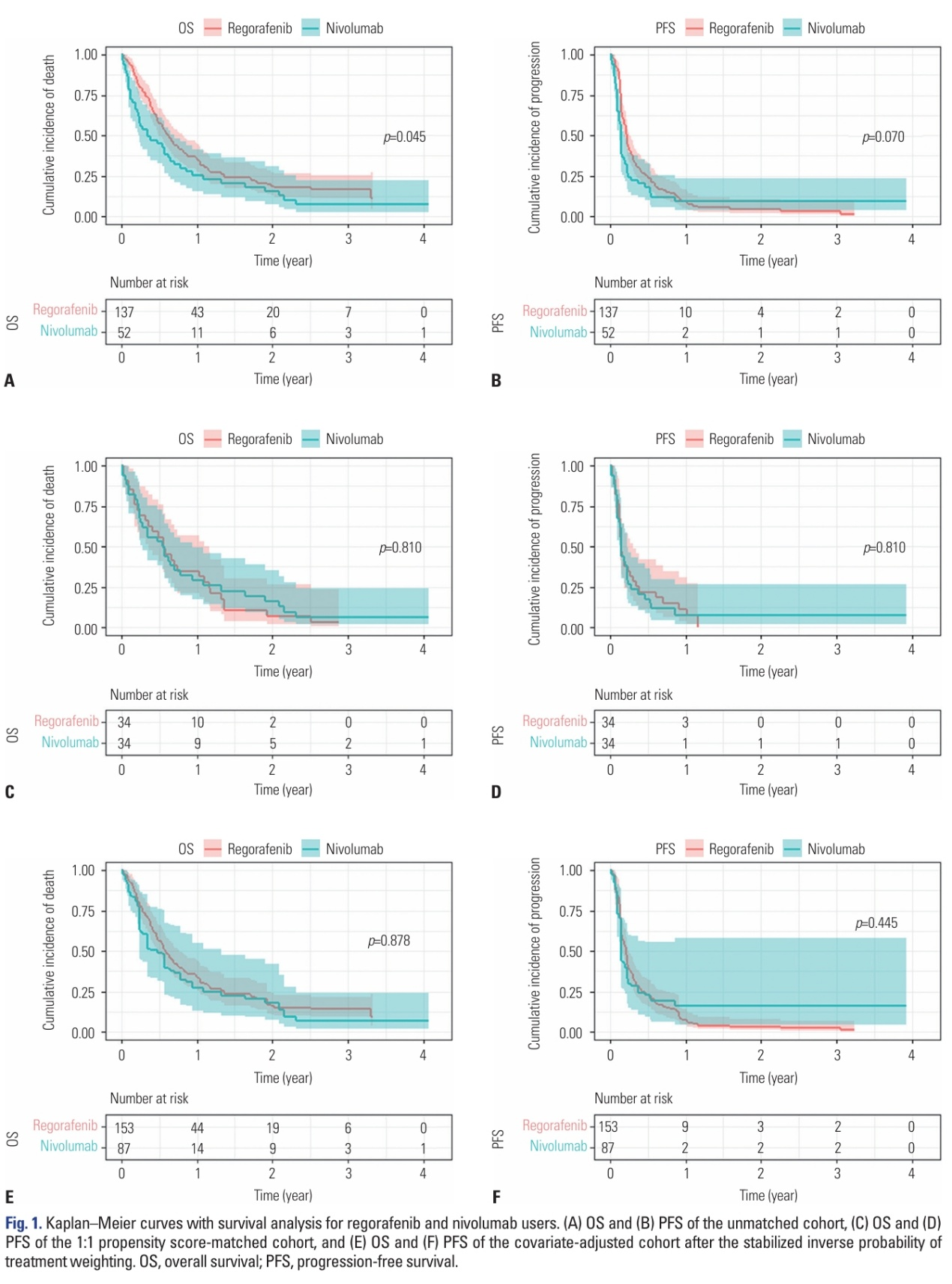
所有患者的中位OS和PFS分别为6.9个月(95%CI=5.7-8.3)和2.4个月(95%CI=1.9-2.7)。匹配前,瑞戈非尼组的中位OS为7.4个月(95%CI 5.9-9.9),显著高于纳武利尤单抗组的4.2个月(95%CI 2.7-8.5;p=0.045)。瑞戈非尼组(2.7个月;95%CI 2.2-3.2)和纳武利尤单抗组(1.8个月;95%CI=1.5-2.4)之间的中位PFS无差异(p=0.070)。
在多变量分析中,使用纳武利尤单抗(与瑞戈非尼相比)与降低OS无独立关联,但在单变量分析中显示出显著关系(HR=1.436;95%CI=1.006-2.050;p=0.046)。其他与OS独立相关的变量包括淋巴结转移、AST水平、ALP和Child-Pugh评分≥7,以及实现客观缓解(HR=0.216)和疾病控制(HR=0.228)(所有p<0.05)。纳武利尤单抗(与瑞戈非尼相比)的使用与PFS无关,无论是在单变量(p=0.068)还是多变量分析中(p=0.377)。与PFS独立相关的因素包括HBV感染、AST水平和实现客观缓解(所有p<0.05)。
倾向评分匹配后的结果对比
两组匹配后在PS模型中包含的几乎所有配对的基线协变量之间均达到接近平衡(ASMDs<0.2),仅血清肌酐除外(ASMD=0.253)。在匹配的瑞戈非尼和纳武利尤单抗组之间,匹配后的中位OS(中位:6.7个月;95%CI 4.3-13.1 vs. 中位:6.7个月;95%CI 3.4-11.2;p=0.810)和PFS(中位:1.8个月;95%CI 1.6-3.6 vs. 中位:1.8个月;95%CI 1.6-2.8;p=0.810)相似。
在PS匹配队列中,匹配后的纳武利尤单抗使用者的ORR更高,但差异无统计学意义(17.6% vs. 2.9%,p=0.105),DCR则相似(瑞戈非尼:32.4% vs. 纳武利尤单抗:35.3%)(p>0.999)。
在纳入稳定化IPTW后(ASMDs<0.2,丙型肝炎病毒(HCV)感染除外,ASMD=0.300),加权后的瑞戈非尼(n=153;63.7%)和纳武利尤单抗使用者(n=87;36.3%)在基线特征上无统计学差异。加权后的瑞戈非尼和纳武利尤单抗组之间的中位OS相似(7.4个月 vs. 4.2个月;p=0.445),两组之间的中位PFS也相似(2.6个月vs. 1.8个月;p=0.878)。
在IPTW队列中,瑞戈非尼组和纳武利尤单抗组的ORR(5.9% vs. 13.6%,p=0.187)和DCR(31.4% vs. 35.2%,p=0.848)相似。在IPTW后,纳武利尤单抗(与瑞戈非尼相比)的使用与OS和PFS均无显著关联。OS与AST、ALP、AFP(仅当包括客观缓解时)水平以及Child-Pugh评分≥7独立相关,同时实现客观缓解(HR=0.265)和疾病控制(HR=0.222)也与OS独立相关(所有p<0.05)。PFS与HBV感染(HR=1.991)、HCV感染(HR=0.274)、AST水平(HR=1.007)以及实现客观缓解(HR=0.269)独立相关(所有p<0.05)。
研究结论
这项研究显示,在索拉非尼治疗失败的晚期HCC患者中,瑞戈非尼和纳武利尤单抗两种治疗方案的疗效并无显著差异。总结以往对比瑞戈非尼和纳武利尤单抗临床结果的研究,通过适当的匹配和加权分析减少选择偏差后,预后并无显著差异,尽管纳武利尤单抗相对瑞戈非尼更多地用于肝功能较差的患者,并且在实现客观缓解方面或许表现出更大的变化。纳武利尤单抗使用者的ORR倾向于更高(13.5% vs. 7.3%),不过差异并没有统计学意义(p=0.117)。
瑞戈非尼使用者的中位OS显著更长(7.4个月 vs. 4.2个月,p=0.045),这可能是由于纳武利尤单抗使用者中Child-Pugh B级肝功能患者比例更高(42.3% vs. 24.1%)。然而,在1:1 PS匹配和稳定化IPTW后,瑞戈非尼和纳武利尤单抗使用者之间的ORR和DCR并无差异。
此外,PS匹配和IPTW队列中的协变量调整Cox回归分析还显示,二线治疗的选择与临床结果无关,而肝功能降低、疾病侵袭性(如淋巴结转移)以及实现客观缓解/疾病控制与患者预后相关,尽管在个别分析中存在一些细微差异。此外,由于早期死亡和严重不良事件,相当一部分患者无法评估其治疗反应(29.1%)。
这项研究存在一定局限性,例如由于当地医保政策的影响,治疗方案的选择可能并非是最佳选择,此外,纳武利尤单抗单药治疗作为二线系统治疗的适应证在2021年4月底被美国FDA撤销,这可能限制了本次研究结果的临床应用,仅可暂时作为临床医生的参考。
总之,在二线治疗中,瑞戈非尼和纳武利尤单抗在索拉非尼失败后的晚期HCC患者中显示出相似的OS、PFS和DCR。具体的临床决策应基于患者的具体情况,包括肝功能和疾病转移情况等。
[1] Lee HJ, Lee JS, So H, Yoon JK, Choi JY, Lee HW, Kim BK, Kim SU, Park JY, Ahn SH, Kim DY. Comparison between Nivolumab and Regorafenib as Second-line Systemic Therapies after Sorafenib Failure in Patients with Hepatocellular Carcinoma. Yonsei Med J. 2024 Jul;65(7):371-379. doi: 10.3349/ymj.2023.0263. PMID: 38910299; PMCID: PMC11199178.
排版编辑:肿瘤资讯-jyy











 苏公网安备32059002004080号
苏公网安备32059002004080号


