肢端肥大症是一种由生长激素(GH)长期过量分泌引起的慢性内分泌疾病,其中约95%的患者是由于分泌GH的垂体腺瘤所致。持续升高的GH及其介导的胰岛素样生长因子-1(IGF-1)水平可影响全身多个器官和系统,导致一系列并发症,如心血管疾病、糖代谢紊乱、骨关节病变等,严重影响患者的健康状况、生活质量及寿命。因此,肢端肥大症的早期诊断和早期治疗至关重要。
目前,肢端肥大症的主要治疗手段包括手术、放射治疗及药物治疗,其中,手术切除垂体GH腺瘤是首选治疗方式。然而,研究显示,尽管手术能够有效减少GH分泌,但术后仍有43.2%的患者生化指标未达标,进而影响长期生存率及生活质量。对于这些患者,生长抑素被推荐为一线药物,可有效控制GH及IGF-1水平,缓解临床症状,并进一步提高手术治疗的获益。
本文通过分析三例因垂体腺瘤引起的肢端肥大症患者的病例,探讨奥曲肽微球在术后治疗以及保守治疗中的疗效,及其对患者生化指标和临床症状的改善情况,以期为垂体腺瘤的治疗提供新的临床借鉴。
病例一
病例汇报:
孙芳教授 昆明医科大学第一附属医院
病例点评:
续岭教授 遵义医科大学附属医院
刘克君教授 惠州市第一人民医院
昆明医科大学第一附属医院
毕业于北京大学医学部
从事内分泌及代谢疾病工作9年
擅长糖尿病、甲状腺疾病、肾上腺疾病等内分泌疾病的诊治
病例介绍
1. 患者基本情况
一般资料:男,35岁。
主诉:主因“肢端增粗2年,垂体瘤术后2月余”收住我科。
现病史:患者2年前出现额头增宽、口唇增厚、手指、足趾增粗、鞋码增大,偶感双上肢指间关节、膝关节胀痛、紧绷感,伴心悸、乏力,无头痛、头晕、恶心、呕吐,无视力下降、视野缺损,无怕冷、浮肿、腹胀、便秘、记忆力减退,无性功能减退、毛发脱落,无多尿、烦渴、多饮,未重视。
2月前至我院就诊,查GH >50 ug/L,甲功、ACTH、COR节律、Prol、LH、FSH水平正常,垂体MRI提示:鞍区占位(1.8×1.8×1.9cm),并于2024年3月27日行:经鼻蝶垂体瘤切除术,术后病理提示垂体生长激素瘤,术后患者自觉面容、肢端增粗无明显改善,关节胀痛、紧绷感稍缓解。
术后病理:支持垂体GH细胞瘤
术后1周复查GH>50 ug/L,垂体MRI提示右侧鞍旁占位术后改变。20天前至我科门诊复查GH 31.3 ng/ml,现患者为进一步诊治门诊以“肢端肥大症、垂体生长激素瘤术后”收住我科。患者精神、饮食可,睡眠稍差,大小便正常,近期体重无明显变化。
既往史:2型糖尿病病史6年,目前口服二甲双胍缓释片2片/次 2次/日、达格列净片每天1片,血糖8-9 mmol/L。
个人史、家族史:无特殊。
体格检查:一般情况可,神情,反应可,回答切题,查体合作。全身皮肤黏膜无黄染、破溃,浅表淋巴结无肿大,甲状腺未触及肿大,心肺腹及神经系统查体无异常。眉弓突出,鼻翼及口唇肥厚,双手指、足趾粗短,手背、足背宽厚,体毛分布正常。
辅助检查:
下丘脑-垂体-肾上腺轴及甲状腺轴功能正常;GH 31.30 ng/ml(↑);PRL:30.29 ng/ml(↑);生长激素抑制试验示:GH未能被抑制。
心电图示:窦性心律。胸部CT示:双肺散在微结节,大致同前。腹部及泌尿系:肝脏多发钙化斑;肝脏多发实性结节(血管瘤可能);胆囊多发息肉。甲状腺彩超示:甲状腺实质回声欠均声像。心脏彩超、血管彩超:未见异常。胃肠镜示:食管胃粘膜异位;慢性非萎缩性胃炎(胃窦);十二指肠炎;内痔。肺功能:肺通气功能正常;弥散功能正常;残气量轻度增高。眼科会诊:视力、视野未见明显异常。
诊断:肢端肥大症;垂体生长激素瘤术后;2型糖尿病;肺结节;肝血管瘤可能;胆囊息肉;慢性胃炎 十二指肠炎。
2. 诊疗经过
糖尿病管理、生长抑素治疗
患者接受糖尿病管理+生长抑素治疗,包括:1、糖尿病饮食,适当运动;2、监测三餐前、三餐后2小时及睡前血糖;3、降糖:利格列汀片每天1片,二甲双胍缓释片每次2片,每天2次;4、抑制生长激素:生长抑素20mg每月一次肌肉注射。
患者于7月4日首次注射生长抑素治疗,注射前GH水平为37 ng/ml。首次注射后复查(7月31日),GH水平明显降至7.05 ng/ml。第二次注射前(8月26日)GH水平进一步降至3.97 ng/ml。患者IGF-1水平亦呈下降趋势,由治疗前的596 ng/ml降至治疗后的375 ng/ml。
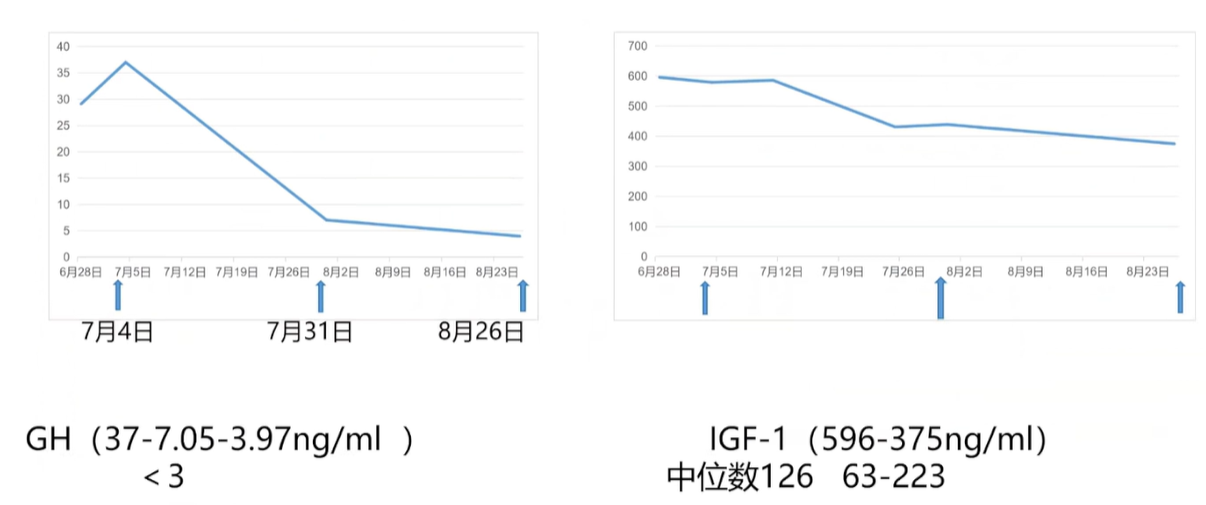
疗效评估和随访
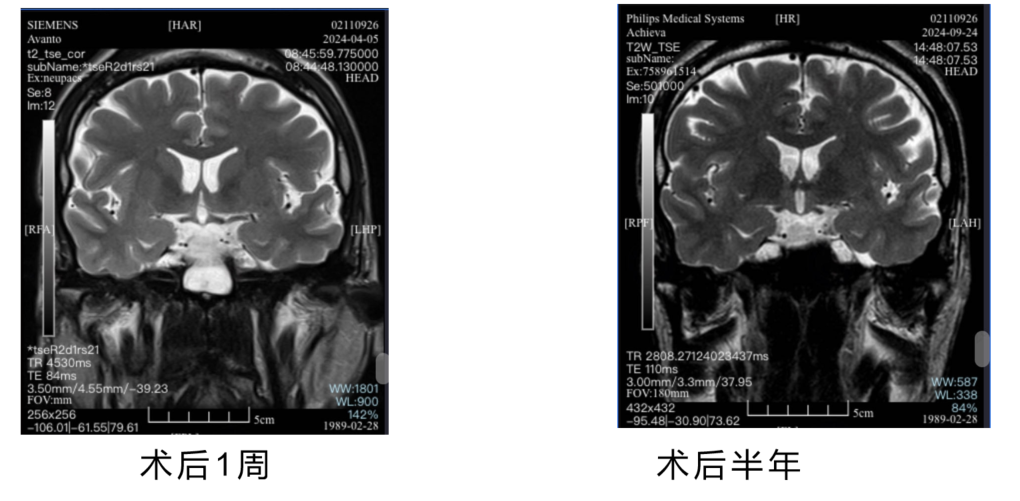
患者肝肾功能检测结果均在正常范围内,血糖水平较治疗前明显下降。影像学复查(术后6个月)示:术区混杂信号影较术后1周时明显缩小,提示病灶进一步改善。目前患者仍在规律使用生长抑素治疗。
病例小结
本例患者因“肢端增粗2年,垂体瘤术后2月余”入院。尽管接受经鼻蝶垂体瘤切除术,但术后GH水平仍明显较高(>50 ug/L),提示生化控制不达标。为进一步控制GH分泌,患者接受生长抑素治疗(生长抑素20 mg肌肉注射,每月一次)。治疗近1个月,GH水平由37 ng/ml 降至7.05 ng/ml;治疗近2个月后进一步降至3.97 ng/ml,同时IGF-1水平由596 ng/ml降至375 ng/ml,生化指标明显改善。影像学复查提示术区病灶较术后1周明显缩小,提示肿瘤进一步改善。患者治疗过程中耐受良好,未出现明显不良反应,血糖水平较治疗前亦有所下降。
本例提示,对于术后生化未达标的患者,奥曲肽微球可有效抑制GH分泌、降低IGF-1水平,并在一定程度上促进残留病灶的缩小。
遵义医科大学附属医院神经外科
贵州省医学会神经外科学分会神经内镜学组秘书(委员)
贵州省医学会神经外科学分会青年委员
贵州省中西医结合神经外科专业委员会委员
中国民族卫生协会卫生健康技术推广专家委员会委员
遵义医科大学附属医院垂体瘤MDT专家组成员
《遵义医科大学学报》青年编委
成都高新医学会神经外科专业委员会委员
惠州市第一人民医院神经外科
神经外科硕士研究生、毕业于广州医科大学(原广州医学院)
广东省抗癌协会神经肿瘤专业委员会青年组常委
广东省精准医学应用学会神经肿瘤分会委员
惠州市医师协会神经外科分会委员及秘书
从事神经外科临床工作10余年,曾在中山大学附属肿瘤医院进修神经肿瘤专业,临床经验丰富
擅长颅脑肿瘤的综合治疗(显微手术及放化疗),包括脑转移瘤、脑膜瘤、胶质瘤、神经鞘瘤对三叉神经痛、面肌痉挛、脑积水、脑出血的诊治经验丰富
主持或参与市科技基金项目3项,获市科技进步“三等奖”1项,发表学术论著10余篇,中华系列期刊3篇,参编《家庭医学病患说明书.神经医学卷》1本
本例患者的诊治过程充分体现了神经外科与内分泌科的紧密合作,也反映了多学科(MDT)管理在垂体腺瘤治疗中的重要性。肢端肥大症的治疗不仅仅是手术切除垂体腺瘤,而是一个长期的综合管理过程,涉及术后生化指标监测、内分泌调控、影像学随访以及必要时的放射治疗干预。因此,神经外科与内分泌科的协同合作对于优化患者的长期预后至关重要。
目前,术后生长抑素治疗已成为术后生化未达标患者的重要管理策略。此外,该病例也反映了当前医保政策的优化对于患者治疗依从性的提升。由于肢端肥大症已被纳入罕见病管理,患者在门诊即可完成生长抑素的报销,而无需住院,极大地减轻了患者的经济负担,提高了长期治疗的可及性和便利性。
在生长抑素治疗过程中,放疗的介入时机是一个重要的临床决策点。目前的共识是,放疗的起效往往需要较长时间,因此,对于术后仍有残留病灶或生化未达标的患者,可先通过生长抑素进行控制,并在治疗过程中定期复查GH及IGF-1水平。一般来说,每3个月进行一次生化评估,若生长抑素治疗已达生化缓解,且患者愿意继续用药,可维持现有方案;若生长抑素剂量增加后仍未能有效控制GH水平,或肿瘤残留体积较大、存在占位效应,则需要与放疗科共同评估放疗介入的时机和必要性。此外,对于放疗的选择,还需同时关注可能的放疗副作用,如对视神经的影响等。目前,MDT模式已广泛应用于垂体腺瘤的治疗决策中。
病例二
病例汇报:
伍敏教授 贵州省人民医院
病例点评:
周帅教授 云南省第一人民医院
何娟教授 贵州医科大学附属医院
贵州省人民医院神经外科
颅底肿瘤专业方向,擅长内镜鼻颅底外科、显微颅底外科
主持国家自然科学基金1项、贵州省科技厅基础研究计划项目1项
以第一作者身份发表论文6篇,其中SCI论文3篇
病例介绍
1. 患者基本情况
一般资料:男,28岁。
主诉:四肢肢端增大、容貌改变5年。
体格检查:典型肢端肥大症面容。
辅助检查:
术前MRI:提示典型垂体瘤。
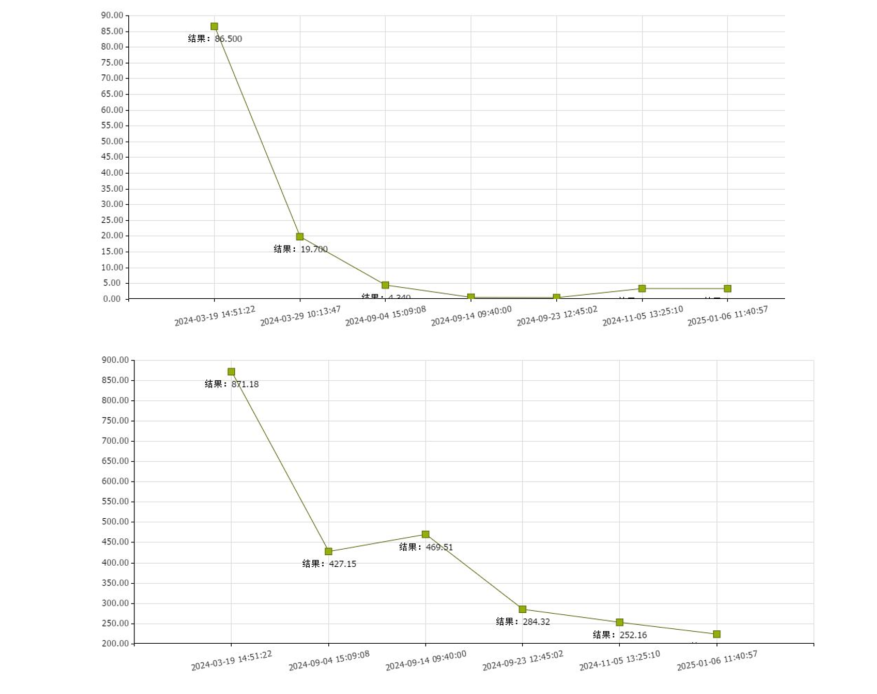
术前激素水平:GH 86.5 ng/ml(↑),IGF-1 871.18 ng/ml(↑);糖代谢:空腹血糖 8.98 mmol/L,120分钟血糖15.07 mmol/L;睡眠监测示:重度睡眠呼吸暂停低通气;血气分析示:Ⅱ型呼吸衰竭;心电图示:窦性心动过速。
2. 诊疗经过
术前药物治疗
患者于2024年3月至2024年9月行奥曲肽微球治疗6个月。治疗后内分泌功能检查示:GH由2024年3月19日的86.5 ng/ml降至2024年9月4日的4.340 ng/ml;IGF-1由871.18 ng/ml降至427.15 ng/ml。MRI检查示:治疗后瘤体较前缩小。此外,患者心率较前明显好转,睡眠呼吸暂停及低氧症状明显改善。
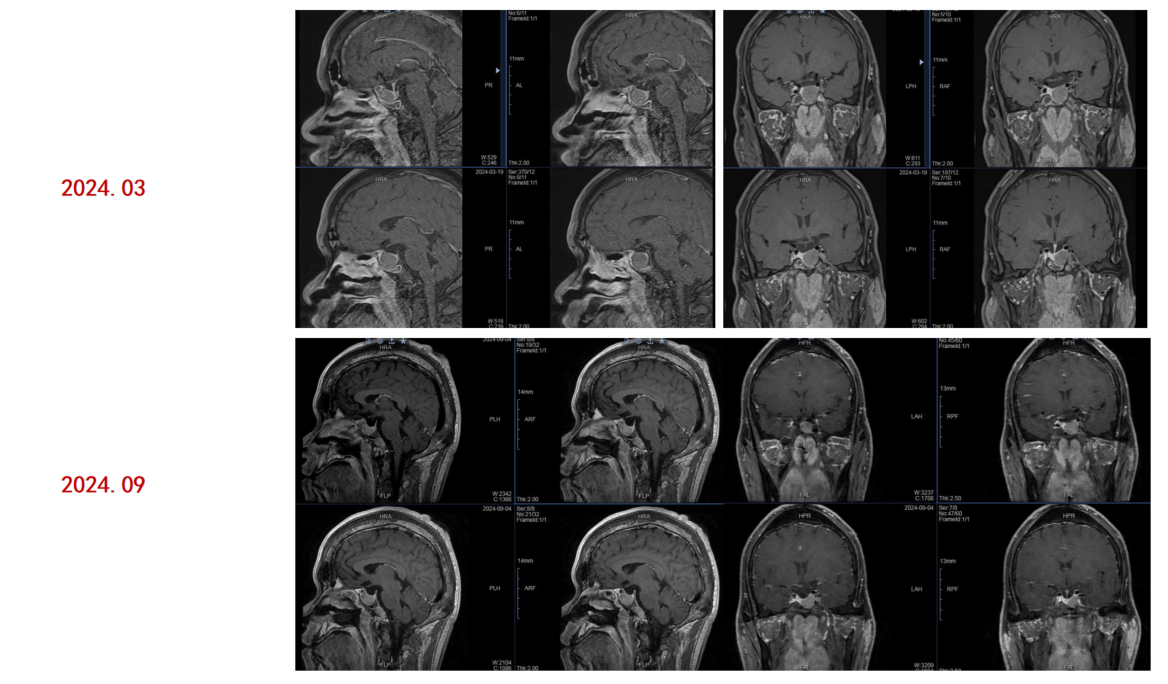
手术治疗
患者于2024年9月行假包膜外切除术,术后MRI示肿瘤切除满意,正常垂体组织保护良好;术后第1天GH降至0.3 ng/ml,IGF-1恢复至正常水平;术后第3天出现阵发性室上心动过速,经相应处理后症状明显改善。
疗效评估和随访
出院时患者处于生化治愈状态。术后随访过程中GH水平有所回升,但IGF-1仍保持在正常范围内。
病例小结
本例患者因“四肢肢端增大、容貌改变5年”入院,体格检查及影像学检查均提示典型肢端肥大症,术前GH及IGF-1显著升高,合并糖代谢异常、重度睡眠呼吸暂停低通气综合征及Ⅱ型呼吸衰竭,提示疾病已造成多系统影响。
患者术前接受奥曲肽微球治疗6个月,GH水平由86.5 ng/ml降至4.34 ng/ml,IGF-1水平由871.18 ng/ml降至427.15 ng/ml,同时瘤体体积明显缩小,心率、睡眠呼吸暂停及低氧症状均明显改善,充分体现了奥曲肽微球在术前优化中的重要作用。随后患者接受假包膜外切除术,术后MRI显示肿瘤切除满意,正常垂体组织保护良好。术后第1天GH降至0.3 ng/ml,IGF-1恢复正常,达到生化治愈标准。
本例病例表明,奥曲肽微球在术前治疗中可有效缩小瘤体、改善代谢功能及相关并发症,并为手术创造更有利的条件。
云南省第一人民医院神经外科副主任主持工作、教学主任
云南省“兴滇英才支持计划”青年人才
云南省医学学科后备人才
中国抗癌协会康复会头颈分会全国委员
云南省康复会加速康复神经外科专委会副主任委员
云南省医师协会胶质瘤专业委员会常务委员
云南省医师协会神经调控专业委员会委员
2023 年度云南省科学技术进步三等奖(排名第一)
2019 年全国神经肿瘤 MDT 精英赛全国一等奖
贵州医科大学附属医院 内分泌代谢病科
上海交通大学(瑞金医院)内分泌学博士
中国医师协会内分泌代谢科医师分会第五届委员会青年委员
中国医药教育协会数字医疗专业委员会全国委员
贵州省医学会内分泌暨糖尿病学分会第七届委员会常务委员兼秘书
贵州省医学会内分泌暨糖尿病学分会第七届委员会垂体肾上腺学组副组长
贵州省医学会内分泌暨糖尿病学分会第七届委员会肥胖糖尿病学组组员
贵州省医学会骨质疏松暨骨矿盐疾病分会第六届委员会常委兼青年学组组长
贵州省基层医疗卫生机构卫生健康标准体系专家库成员
《中华糖尿病杂志》审稿人
主持并参与国家自然科学基金、省市级、横向课题多个科研项目,于《Frontiers in genetics》、《BMC Endocrine Disorders》等杂志发表论文
曾于美国哈佛医学院附属Joslin糖尿病中心短期进修
例患者的治疗过程无论从术前管理、手术策略,还是术后随访,都体现了非常成熟、规范的诊疗思路,尤其在手术方面,假包膜外切除技术的应用确保了肿瘤的完整切除,同时最大程度保护了正常垂体组织,从影像学及术后生化结果来看,手术效果令人满意。
术前奥曲肽微球治疗不仅有效缩小了瘤体,还改善了患者的代谢异常和睡眠呼吸暂停综合征,为手术创造了良好条件。术后短期内GH显著下降,IGF-1恢复正常,达到生化治愈标准。然而,在随访过程中,GH水平出现一定程度的回升,而IGF-1仍维持在生化缓解范围内。GH的测定易受多种因素影响,包括个体的体重、性别、年龄及体质等,因而可能存在一定的变异性。当前国际上普遍将IGF-1作为评估GH瘤术后生化缓解的关键指标。本例患者的磁共振复查显示肿瘤切除彻底,无复发或残留,因此GH的回升可能更多地受到个体因素或检测方法学的影响,而非疾病活动的真实反映。后续仍需定期随访,结合生化指标和影像学检查,确保长期疗效稳定,并在必要时调整治疗策略。
病例三
病例汇报:
陈刘教授 陆军军医大学西南医院
病例点评:
段剑教授 南昌大学第一附属医院
李德培教授 中山大学肿瘤防治中心
陆军军医大学西南医院内分泌科
现任重庆市医学会糖尿病学专业委员会委员
重庆市医师协会内分泌代谢科医师分会第一届委员会内分泌高血压学组副组长
重庆市医学会骨质疏松及骨矿盐疾病专业委员会委员
重庆市中西医结合学会糖尿病专业委员会委员
重庆市医学会糖尿病学分会第七届委员会糖尿病足学组委员
病例介绍
1. 患者基本情况
一般资料:女,45岁。
主诉:颈部、双足怕冷1年,发现甲功异常2天。
现病史:患者近1年来无明显诱因感颈部、双足部怕冷,伴食欲不佳、疲倦感,无多汗,多饮多尿、消瘦,无畏寒、发热,无手抖、突眼,无脱发、体毛稀疏,无心悸、腹泻、腹痛。我院门诊查甲功:T3 4.20 nmol/L,T4 204.00 nmol/L,FT3 14.40 pmol/L,FT4 54.50 pmol/L,TSH 4.980 ulU/ml。为进一步诊治收入院。
既往史:自诉2012年孕期因在xx医院诊断为“甲亢”、服用“丙硫氧嘧啶”治疗近10个月。2020年因“颈部触痛”在xx医院诊断为“亚甲炎”、“甲状腺结节”,服用“泼尼松”治疗3个月。2012年剖腹产时大出血,输血900ml。否认“高血压、糖尿病”等病史。
个人史、家族史:无特殊。
婚育史:已婚,育有二子。
体格检查:体温 36.5℃,脉搏 102次/分,呼吸 20次/分,血压 108/67mmHg,身高 145cm,体重 61kg,BMI 29.01kg/m²,口唇稍增厚,心肺腹等一般查体无特殊。
辅助检查:
皮质醇节律、ACTH、性腺激素正常。生长激素轴:IGF-1升高(436.4 ng/ml),OGTT抑制试验GH最低1.01 ng/ml。糖代谢:120分钟血糖10.83 mmol/L。奥曲肽试验:ΔGH(0-12h)=79.4%(≥80.51%可认为治疗能较好地控制GH水平)。心脏超声:左房稍大。肠镜检查:结直肠多发息肉。甲状腺超声:甲状腺结节。
垂体MRI示:鞍区见异常信号肿块影,大小约2.4x1.9x1.9cm,增强扫描可见轻度强化,垂体柄偏移,鞍底下陷,向下侵袭入蝶窦,紧贴左侧颈内动脉双侧海绵窦未见异常信号,视交叉无明显受压。奥曲肽抑制试验示:TSH抑制率84.8%。溴隐亭敏感试验示:服用溴隐亭后TSH持续下降(4.32 ulU/ml→2.72 ulU/ml)。
甲状腺显像示:1. 甲状腺两叶血供丰富、摄99m锝功能增强,呈现甲状腺功能亢进征象。2. 甲状腺两叶放射性分布欠均匀。基因检测:未发现阳性基因突变,排除中枢甲状腺激素抵抗综合征。
MDT会诊意见:
鞍区病变有侵袭性,影像学表现为垂体瘤,向下侵袭入蝶窦,紧贴左侧颈内动脉。功能上考虑TSH瘤合并GH瘤可能性大,有手术指征,建议手术切除。患者奥曲肽试验TSH抑制率84.8%,ΔGH(0-12h):79.4%,如果患者拒绝手术,也可以选择生长抑素类似物治疗后观察。
2. 诊疗经过
保守治疗(患者拒绝手术)
住院期间短效奥曲肽(0.1 mg皮下注射q8h)治疗,TSH持续下降。出院后患者于2024年5月28日首次注射奥曲肽微球20 mg,随后每月一次。2024年6月11日复查:甲功、IGF-1恢复正常。2024年8月21日垂体MRI:肿瘤明显缩小。
2024年5月11日垂体MRI:鞍区见异常信号肿块影,大小约2.4x1.9x1.9cm,增强扫描可见轻度强化,垂体柄偏移,鞍底下陷,向下侵袭入蝶窦,紧贴左侧颈内动脉双侧海绵窦未见异常信号,视交叉无明显受压。2024年8月20日垂体MRI:鞍区见异常信号肿块影,大小约1.6x1.8x2.3cm,边界欠清,增强扫描不均匀强化,局部突入左侧蝶窦,视交叉无明显受压。
疗效评估和随访
生化指标达标:甲功、生长激素轴均恢复正常,肾上腺皮质轴、性腺轴正常。肿瘤缩小:治疗3个月后MRI提示瘤体缩小,内科治疗有效。目前患者甲功、IGF-1正常,生化达标,继续随访观察。
病例小结
本例患者因“颈部、双足怕冷1年,发现甲功异常2天”入院。既往有妊娠期甲亢病史,曾接受抗甲状腺药物治疗,并在2020年因“亚甲炎”服用糖皮质激素。此次入院检查发现TSH异常分泌,同时伴有生长激素轴异常,垂体MRI提示鞍区肿瘤,影像学表现符合垂体瘤,且肿瘤具有一定侵袭性,MDT团队综合分析后考虑TSH瘤合并GH瘤的可能性较大,建议手术切除。
由于患者拒绝手术,遂选择药物治疗。住院期间短效奥曲肽治疗后TSH水平下降,出院后改为奥曲肽微球(20mg/月)治疗。随访过程中,患者甲状腺功能及IGF-1水平恢复正常,治疗3个月后复查MRI显示肿瘤明显缩小,提示内科治疗有效。目前患者生化指标达标,甲状腺功能及生长激素轴正常,肿瘤体积较基线缩小,提示药物治疗在本例患者中取得良好效果。
南昌大学第一附属医院
中国医师协会神经外科医师分会内镜专业委员会工作秘书
中国医药教育协会脑出血内镜救治分会副秘书长
江西省康复医学会颅脑创伤专业委员会主委
江西省医师协会神经外科分会常委兼秘书
江西省整合医学会神经外科分会副主委
江西省整合医学学会神经外科分会青年学组主委
专业方向:脑出血,脑肿瘤,神经内镜
中山大学肿瘤防治中心神经外科
医学博士、于中山大学附属肿瘤医院完成神经肿瘤外科的专科培训
目前专注于神经肿瘤的临床诊疗,方向为内镜神经外科
主持省部级科研项目2项,作为第一/通讯作者在J Neuro-Oncol、Int J Clin Oncol等学术期刊发表论文十多篇,研究成果入选SNO、EANO等国际学术会议交流,获国家发明/实用新型专利各1项
兼任广东省抗癌协会神经肿瘤青委会秘书、广东医学会神经肿瘤分会青委委员、广东省基层医药学会脑胶质瘤专委会委员等
本例患者的诊治过程非常严谨,经过系统分析,逐步理清病情,在生化指标方面取得了比较理想的治疗效果,同时影像学提示肿瘤缩小,内科治疗可谓取得了良好成效。针对这类垂体瘤,药物治疗在某些患者中确实能够达到生化缓解,但是否需要长期用药仍需结合患者的病情特点、肿瘤残留情况以及长期随访的动态评估。对于这类患者,治疗策略应结合个体化情况,动态调整。从外科的角度来看,垂体瘤,尤其是TSH瘤合并GH瘤的病例,如果条件允许,外科治疗仍然是首选方案。随着神经内镜技术的发展,手术切除的精准度大幅提高,可以在最大程度上保护垂体功能的同时实现肿瘤全切,提高生化治愈率。
总之,对于可完整切除的患者,手术仍然是最直接、最有效的治疗手段,可以减少长期药物依赖,并降低肿瘤复发的风险。因此,在病例讨论中,我们也需要综合考虑患者的个体情况、肿瘤的手术可切除性以及患者的意愿,来制定最优的治疗方案。本例患者的诊治过程充分体现了MDT的价值,在个体化治疗的基础上达到了良好的生化缓解。从长期管理的角度来看,患者仍需定期随访,动态评估生化指标和影像学变化,以确保病情的长期稳定。如果未来肿瘤有进展,仍可结合手术等进一步干预手段,实现最佳治疗效果。
总结
奥曲肽微球在术前治疗中不仅能够有效缩小瘤体,还可改善代谢功能及相关并发症,为手术创造更有利的条件。对于术后生化未达标的垂体瘤患者,奥曲肽微球可显著抑制GH分泌、降低IGF-1水平,并在一定程度上促进残留病灶的缩小。生长抑素类药物在垂体瘤术后管理中发挥着重要作用,可作为长期控制疾病进展的有效治疗策略,提高患者的生化缓解率和长期预后。
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


