宫颈癌在全球范围内是女性中第四常见的癌症[1],也是导致女性癌症死亡的主要原因之一。历经一线标准治疗失败的复发或转移性患者,在二线及以上治疗选择有限。近年来,以免疫检查点抑制剂为代表的免疫治疗运用于宫颈癌治疗越来越受到重视,但也面临着疗效或安全性有待提升等诸多挑战。
艾托组合抗体(艾帕洛利托沃瑞利单抗)是由齐鲁制药通过自主研发的MabPairTM技术平台设计生产的首个抗PD-1和抗CTLA-4的双功能组合抗体,其II期研究(DUBHE-C-206)结果于2024年欧洲妇科肿瘤学大会(ESGO)重磅发布,引起了业内广泛的关注与期待。本文特邀中山大学肿瘤防治中心刘继红教授,聚焦双免疫创新疗法,深入解读DUBHE-C-206研究,揭示艾托组合抗体的治疗潜力。
克服宫颈癌二线治疗的难题,艾托组合抗体展现治疗潜力
复发或转移性宫颈癌主要以系统治疗为主,现有的治疗方案仍存在诸多限制。包括化疗在内的传统治疗手段,虽然在一定程度上能够缓解症状、延长生存期,但往往伴随着较大的副作用和有限的疗效持续性。
随着对肿瘤免疫微环境认识的深入,以免疫检查点抑制剂为代表的免疫治疗作为一种革命性的治疗手段,开始在宫颈癌治疗中展现出潜力;用于复发或转移性宫颈癌的二线及以上治疗时,其疗效和安全性仍有待进一步的优化和突破。其中,PD-1单抗作为近年来的研究热点,主要被批准用于PD-L1阳性的复发或转移性宫颈癌患者治疗;对于PD-L1阴性患者如何从免疫检查点抑制剂治疗中获益,仍是临床上面临的问题。而PD-L1单抗虽然可用于不区分PD-L1表达状态的全人群治疗,但临床研究结果显示其单药在肿瘤缓解效果上还有待进一步提升。
针对这些挑战,研究者们开始探索更为有效的治疗方案。其中,联合使用两种不同“作用环节”的免疫检查点抑制剂的“双免疫疗法”,可以通过解除对免疫细胞的双重抑制,更全面地激活患者的抗肿瘤免疫反应,起到协同增效的作用。尽管这一策略在一些研究中显示出了“1+1>2”的潜力,但在真实世界临床应用中仍面临着现实的挑战,如抗CTLA-4抗体带来的免疫相关不良反应增加,导致患者耐受性不佳,以及两种药物联用的给药频率不同会影响患者依从性等。
在这一背景下,艾托组合抗体(QL1706)的研发和临床研究为复发或转移性宫颈癌的治疗带来了新的希望。作为一种新型的双功能组合抗体,它集合了抗PD-1和抗CTLA-4的双重作用,旨在克服单一疗法的局限性。艾托组合抗体在I期研究中已经展现出了良好的安全性和初步的疗效信号,特别是在未经免疫治疗的复发或转移性宫颈癌患者中ORR达到了28.3%,疾病控制率(DCR)达到55%,中位PFS达到4.2个月;此外,在安全性方面,艾托组合抗体≥3级TRAE的发生率为17%,其中因TRAE导致停药的发生率仅为6%[4]。
相较于传统治疗和单药免疫治疗,艾托组合抗体显示出了令人鼓舞的治疗潜力和可管理的安全性,不仅为复发或转移性宫颈癌患者提供了新的治疗选择,也为未来的临床治疗策略提供了重要的参考和启示。
研究设计科学严谨,入组患者具有广泛代表性
该研究主要针对一线含铂化疗(±贝伐珠单抗)失败且未接受过免疫治疗的复发或转移性宫颈癌患者,接受艾帕洛利托沃瑞利单抗5mg/kg,静脉注射,每3周一次,持续至疾病进展、出现无法耐受的毒性、治疗暂停>84天、失访、死亡或退出研究。
研究的主要终点是独立审查委员会(IRC)基于RECIST 1.1评估的客观缓解率(ORR),次要终点包括疾病控制率(DCR)、缓解持续时间(DoR)、无进展生存期(PFS)、总生存期(OS)、安全性等(图1)。
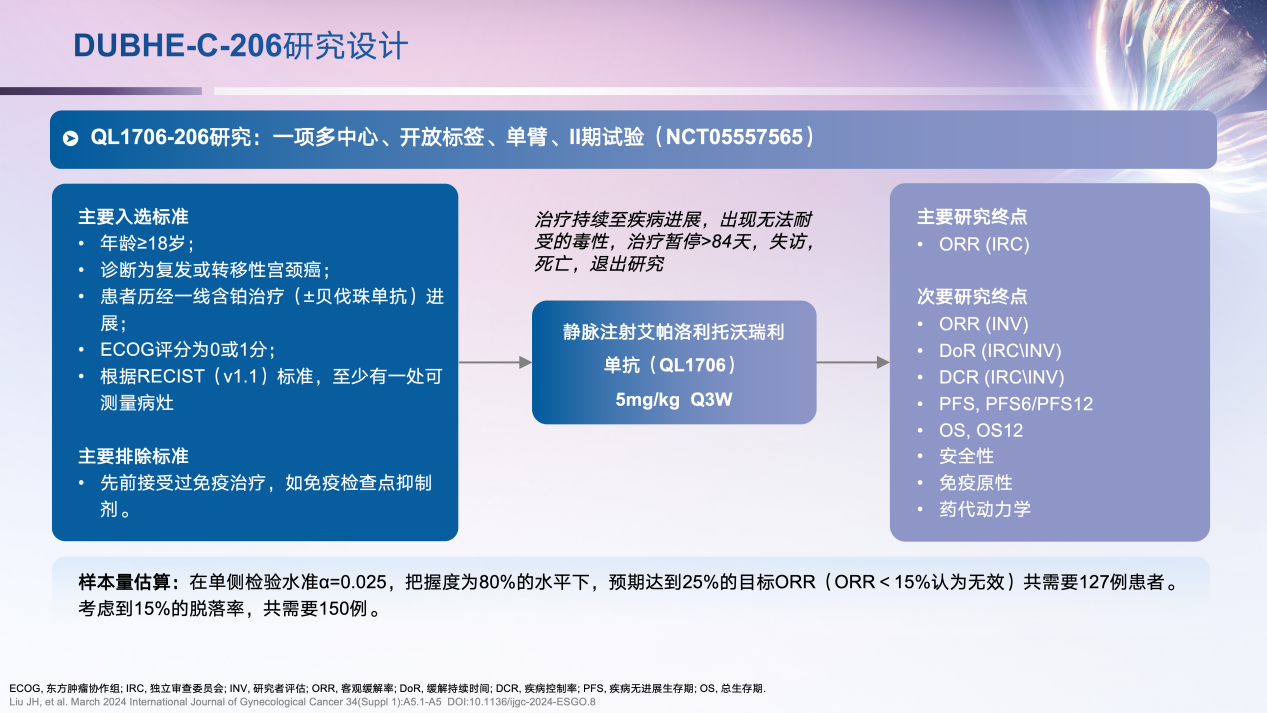
图1. DUBHE-C-206研究设计
该研究共纳入148例患者,中位年龄为53.0岁,其中89.2%(132例)患者为鳞状细胞癌,73.6%(109例)的ECOG PS评分为1;在PD-L1表达水平方面,29.1%(43例)的患者CPS<1。此外,39.9%的患者有贝伐珠单抗治疗史,37.2%的患者在全身性治疗阶段至少接受过两线治疗(图2)。
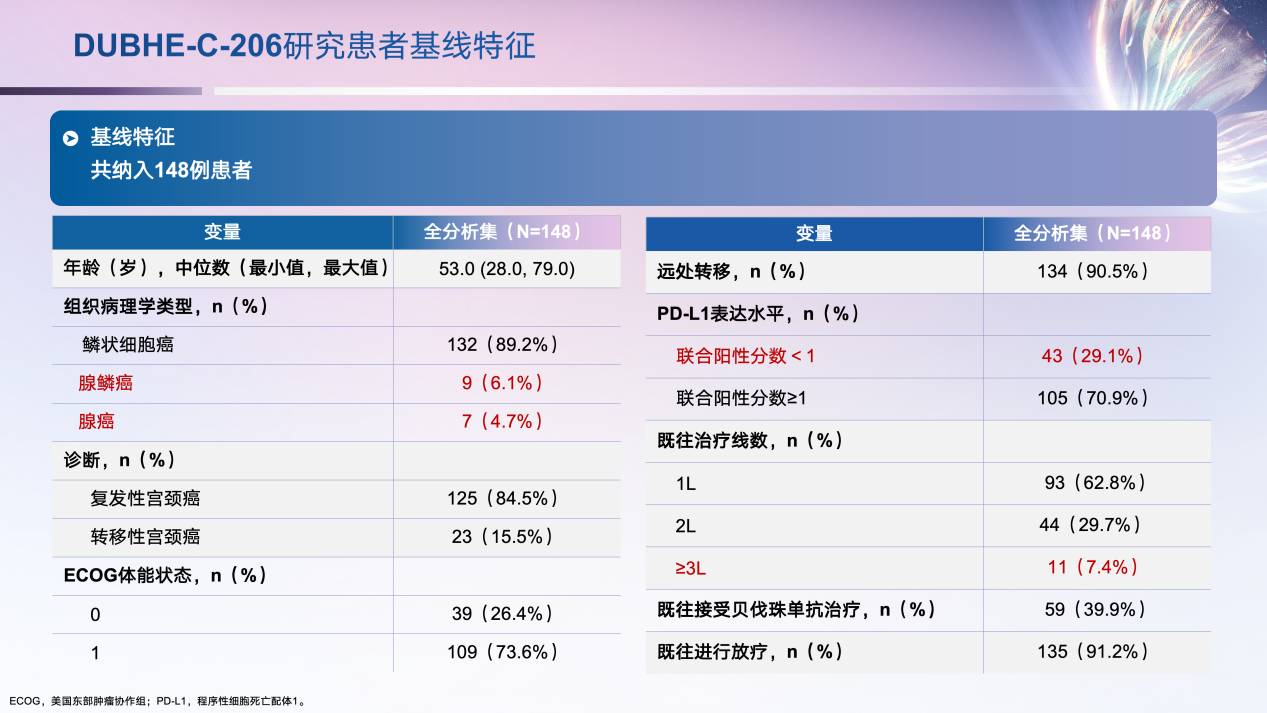
图2. DUBHE-C-206研究患者基线特征
整体而言,DUBHE-C-206的研究设计科学严谨,而患者基线特征的详细记录为DUBHE-C-206研究结果提供了坚实的基础,使得研究结果更具说服力,为临床应用提供科学依据。
研究结果令人惊艳,生存与生活兼顾、疗效与安全并重
根据IRC的评估,艾托组合抗体治疗的ORR为33.8%(95% CI: 26.2%-42.0%),DCR为64.9%(95% CI,56.6%-72.5%),表明超过半数的患者在接受治疗后疾病得到了控制。截至2023年4月28日,DoR尚未达到中位数,表明艾托组合抗体可能具有较长的疗效持续时间。(图3)。
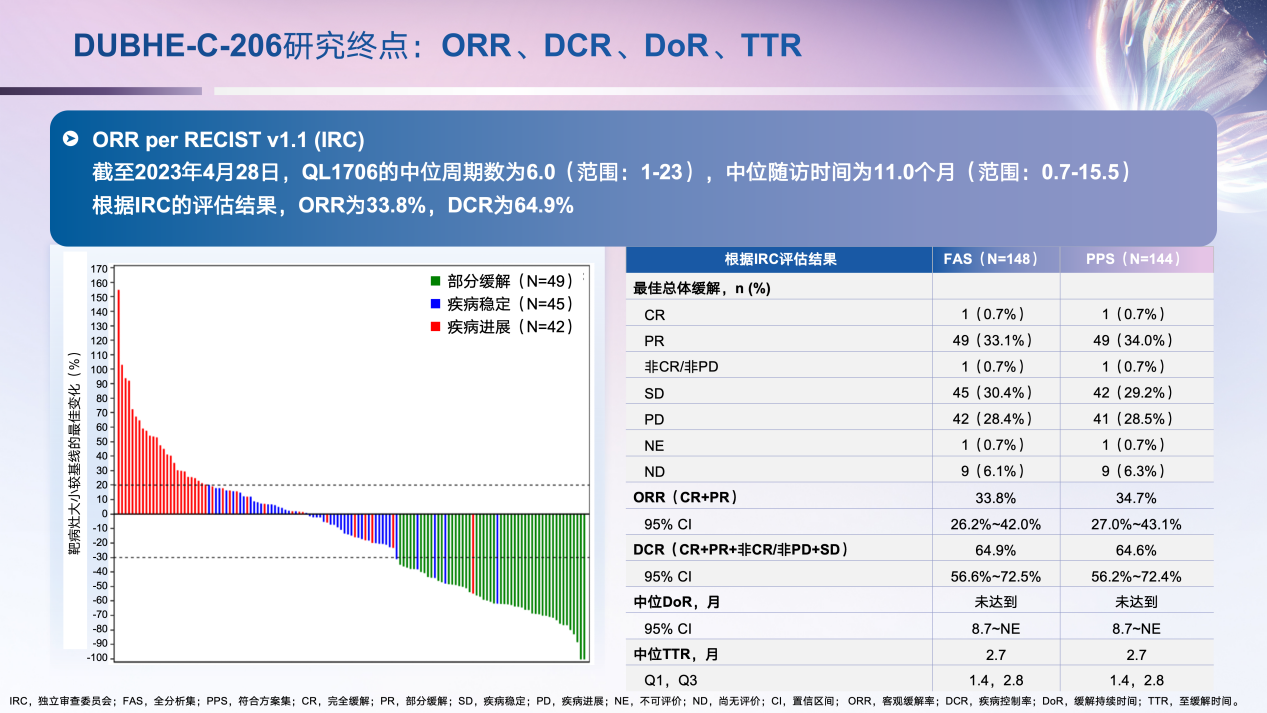
在生存获益方面,根据IRC的评估结果,50%的患者在5.4个月内疾病未进展(中位PFS:5.4个月;95%CI:3.9-6.9),45%的患者在治疗后6个月疾病未进展(6个月PFS率:45.0%;95% CI:36.4%-53.3%),为艾托组合抗体治疗能够有效控制疾病进展提供了证据(图4)。在数据分析时,本研究的中位OS尚未达到,12个月PS率达65.4%,接受治疗患者有较好的生存获益(图5)。
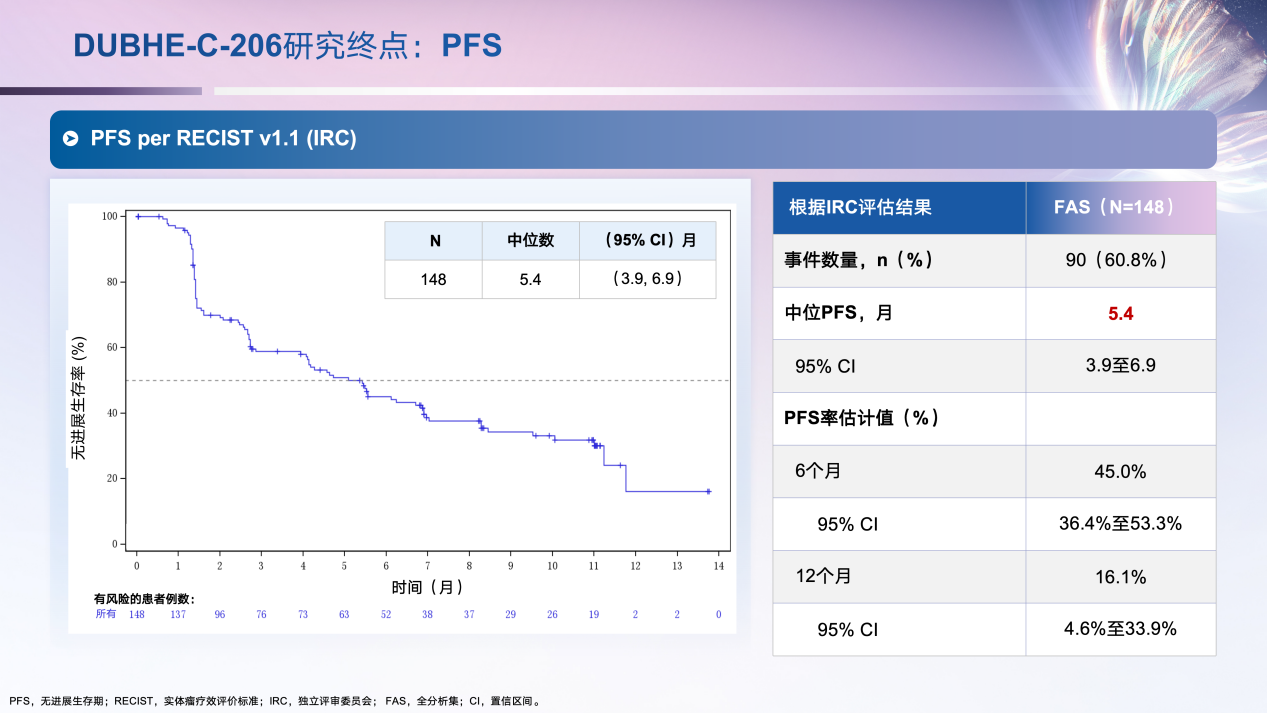
图4. DUBHE-C-206研究PFS结果
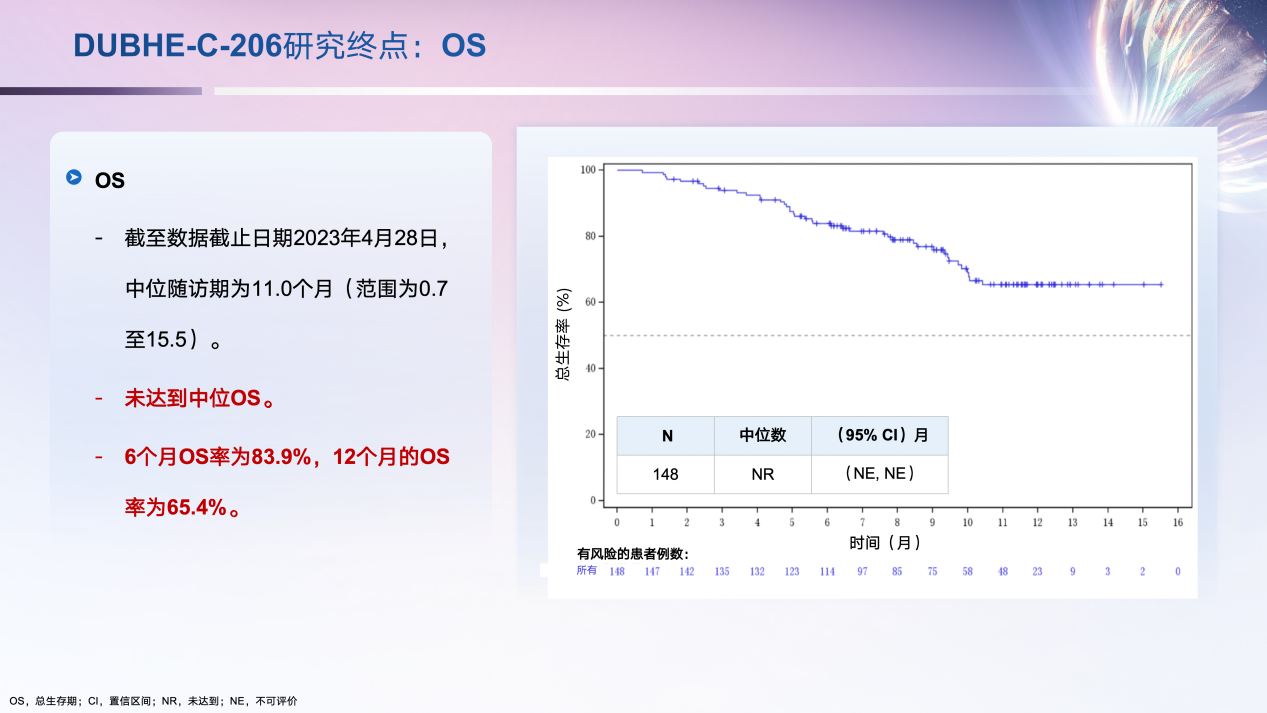
图5. DUBHE-C-206研究OS结果
148例患者的安全性分析结果显示,治疗相关不良事件(TRAEs)发生率为70.3%,其中24.3%为≥3级,3例(2.0%)患者因TRAE终止治疗。尽管艾托组合抗体治疗中有一定比例的患者经历了不良事件,但大多数不良事件是可控的,并且没有导致治疗相关死亡(图6)。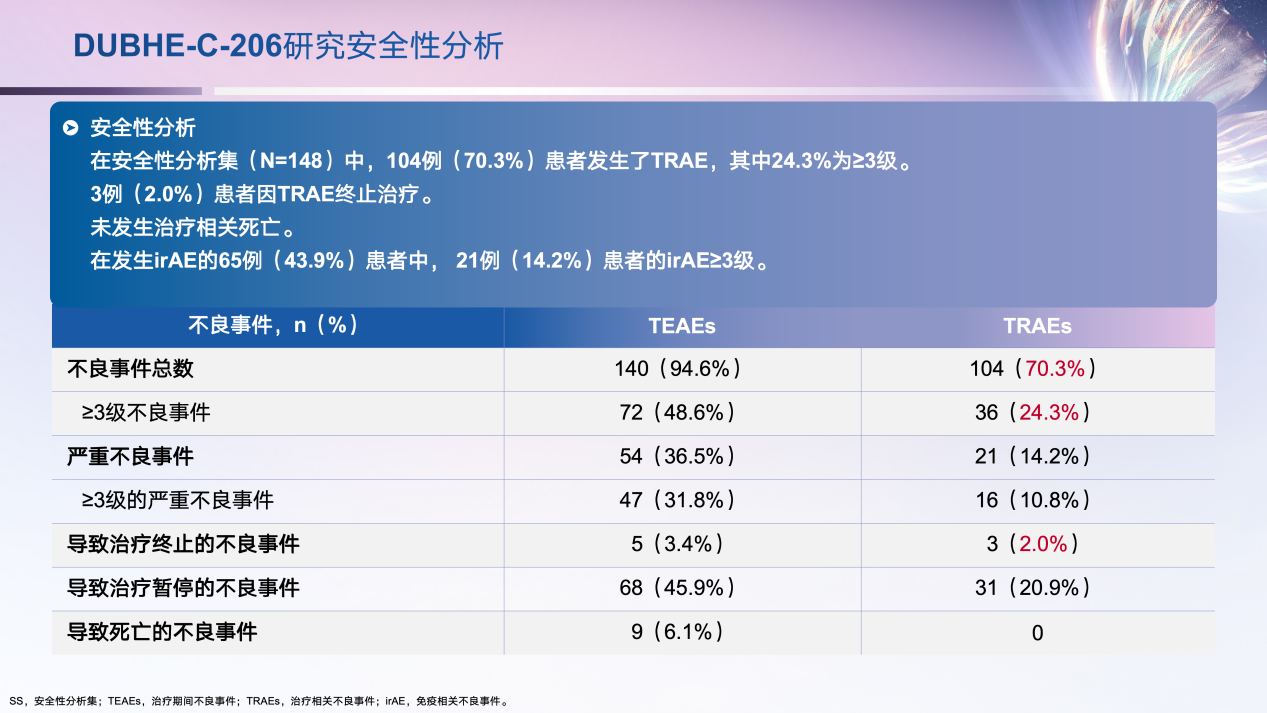
图6. DUBHE-C-206研究安全性结果
亚组分析同样喜人,多线治疗疗效不减
本研究进一步对不同的患者群体进行了亚组分析,获得与总人群同样显著的疗效。结果显示,PD-L1 CPS≥1和<1的患者ORR分别为37.1%和25.6%。此外,即使患者既往经过三线及以上的多线治疗,艾托组合抗体仍旧疗效不减,ORR达到30.9%。在病理类型、ECOG体能状态、既往接受贝伐珠单抗治疗、既往接受放疗方面,结果与整体研究人群的ORR数据一致(图7)。
这些亚组分析结果表明,艾托组合抗体在不同类型的复发或转移性宫颈癌患者中均显示出令人鼓舞的治疗效果,为临床医生提供了关于患者选择和治疗决策的宝贵信息。
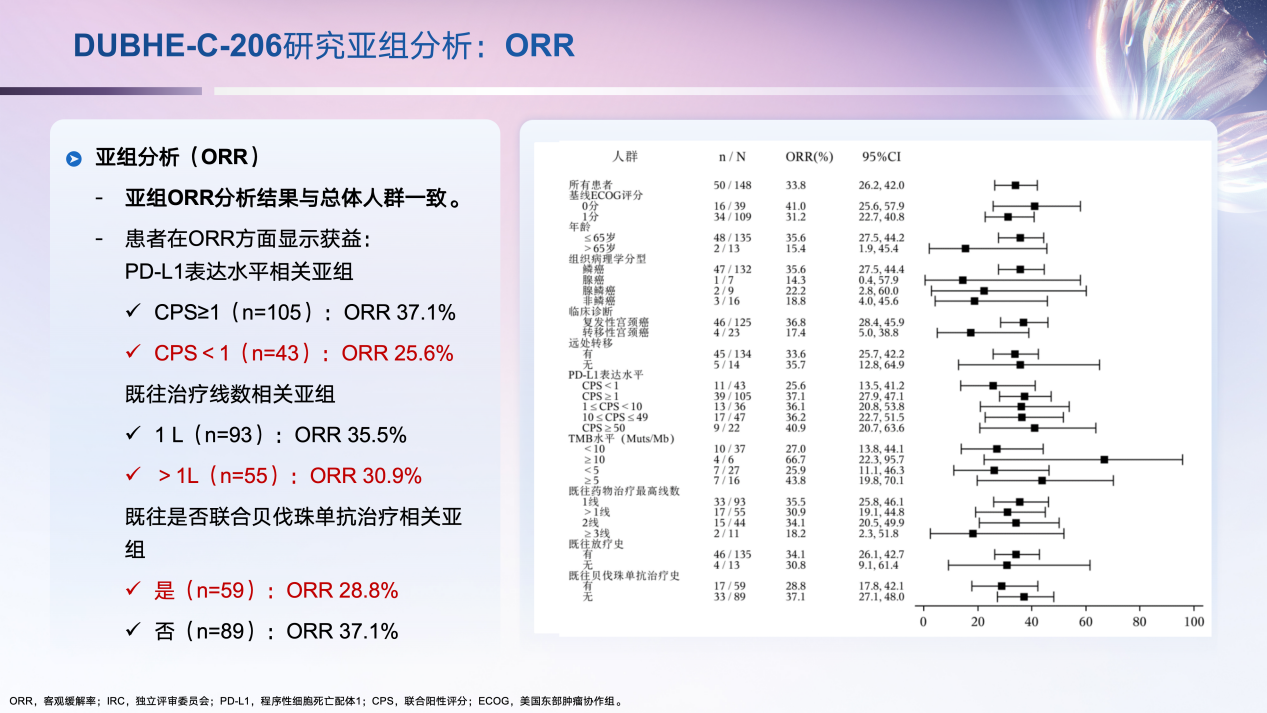
图7. DUBHE-C-206研究亚组分析ORR结果
艾托组合抗体未来可期,开启免疫治疗崭新篇章
艾托组合抗体作为一种创新的双功能组合抗体,其在I期的102研究中展示了良好安全性和积极的疗效信号,为该药物的进一步研究和应用奠定了基础。II期研究DUBHE-C-206进一步验证了艾托组合抗体在复发或转移性宫颈癌患者中的疗效和安全性,其中位PFS达到5.4个月,ORR为33.8%,而且艾托组合抗体表现出可管理的安全性和耐受性。
随着免疫治疗的不断进步和对药物作用机制的深入理解,我们有理由相信,艾托组合抗体将为宫颈癌患者提供更多的治疗选择。特别是在PD-L1表达水平不高或对现有治疗反应不佳的患者群体中,艾托组合抗体为临床提供了新的治疗思路,期待其在研III期研究能够再次闪耀全球,在更广泛的患者群体中发挥更大的作用,为患者提供更有效、更安全的治疗选择,显著提高他们的生存率和生活质量。这不仅是医学科技的一次重要突破,也是人类抗击疾病、追求健康生活的坚定证明!
[1] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024.
[2] Hyun Cheol Chung, et al. Efficacy and Safety of Pembrolizumab in Previously Treated Advanced Cervical Cancer: Results From the Phase II KEYNOTE-158 Study. J Clin Oncol. 2019 Jun 10;37(17):1470-1478.
[3] David A Reardon, et al. Treatment with pembrolizumab in programmed death ligand 1-positive recurrent glioblastoma: Results from the multicohort phase 1 KEYNOTE-028 trial. Cancer. 2021 May 15;127(10):1620-1629.
[4] Jihong Liu, Naifu Liu, Danbo Wang, Dapeng Li, Cheng Fang. Efficacy and safety of QL1706, a novel dual immune checkpoint blockade containing a mixture of anti-PD1 IgG4 and anti-CTLA4 IgG1 antibodies, for advanced cervical cancer: Cohort data from a phase 1b trial. J Clin Oncol 40, 2022 (suppl 16; abstr 5535).
[5] Liu JH, et al.Efficacy and safety of iparomlimab and tuvonralimab in previously treated patients with recurrent or metastatic cervical cancer: a multicenter, open-label, single-arm, phase 2 clinical trial (DUBHE-C-206). International Journal of Gynecologic Cancer Mar 2024, 34 (Suppl 1) A5.
排版编辑:肿瘤资讯-Zika











 苏公网安备32059002004080号
苏公网安备32059002004080号


