近年来,我国前列腺癌发病率呈逐年上升趋势,初诊时中晚期病例比例较高,20%~35%处于高危或局部进展期[1-2],约54%的患者已伴有远处转移[3]。此种情况下,术前实施新辅助治疗成为改善者生存预后的探索方向。
既往激素剥夺治疗(ADT)是前列腺癌新辅助治疗的主要方案之一,但单纯的ADT治疗仍面临着耐药或疾病复发、进展的挑战。随着新型药物的不断涌现,以达罗他胺为代表的新型雄激素受体抑制剂(ARi)为前列腺癌患者的治疗提供了新的有力武器。本期特邀何志嵩教授、杨恺惟教授、谌诚教授、蔡林教授、虞巍教授、范宇教授就前列腺癌新辅助治疗的研究进展特此进行整理讨论,以飨读者!
前列腺癌新辅助治疗进展
高危前列腺癌与较高的生化复发率、临床复发率、转移率和前列腺癌特异性死亡相关[4],此类患者接受根治性前列腺切除术(RP)后,5年内生化复发率大于50%[5-6],患者的生存及预后均不佳。多项研究表明,与单纯的根治性手术相比,前列腺癌接受局部治疗前进行新辅助治疗能够有效降低手术切缘阳性率、前列腺肿瘤病灶体积、病理分期以及淋巴结阳性率[7-9],从而降低了手术难度、增加了患者根治性治疗的机会。
ADT疗法是晚期前列腺癌治疗的基石
目前,前列腺癌新辅助治疗主要包括新辅助内分泌治疗(NHT)、新辅助化疗(NCT)和新辅助内分泌治疗联合化疗(NCHT)等。基于前列腺癌发生发展往往存在雄激素依赖性的分子机制,ADT构成了晚期前列腺癌治疗体系的基石,是前列腺癌应用最广泛、使用时间最久的治疗方式。在过去的二十年中,以RP术前新辅助治疗领域展开了多项以ADT为基础的研究,包括ADT单药治疗,NHT单药治疗,ADT联合NHT等方案。这些研究的结果已证实ADT治疗在前列腺癌患者新辅助治疗中可以达到缩瘤降期、降低术后切缘阳性率等效果,为局晚期不可切除前列腺癌患者带来了手术治愈的希望。但在肿瘤学终点(总生存率和癌症特异性生存率)中并没有观察到有统计学意义的临床获益[10]。
ARi+ADT策略实现了前列腺癌非转移和转移阶段全覆盖
随着治疗理念的进步,以ADT治疗为主的联合治疗为前列腺癌患者新辅助效果的提高带来新的希望。2015年,多西他赛加入ADT形成首个标准强化治疗方案[11],开启了转移性激素敏感前列腺癌(mHSPC)双药强化治疗时代。此后,NHA的出现使双药强化治疗方案得到了进一步丰富[12-14]。
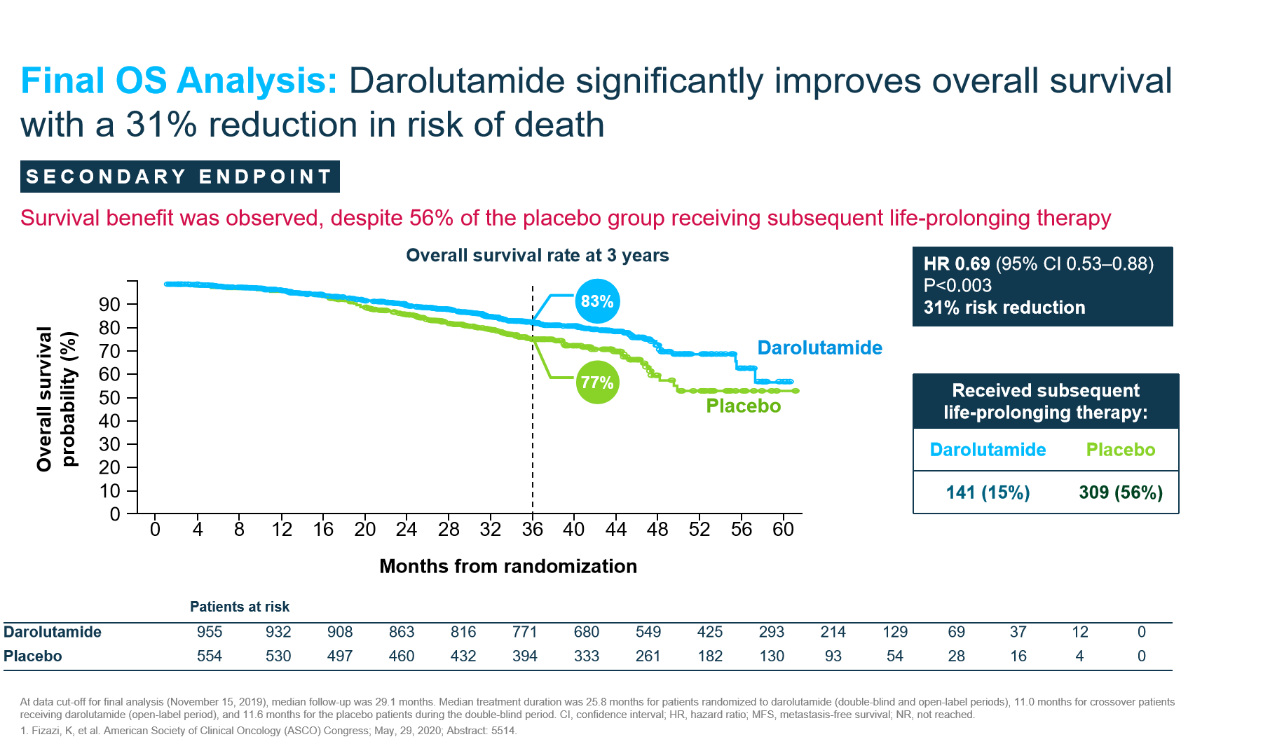
2019-2020年发表在《新英格兰杂志》的ARAMIS研究结果证实[15,16],具有独特分子结构的新一代ARi达罗他胺+ADT组患者的中位无转移生存期(MFS)为40.4个月,显著高于安慰剂+ADT组的18.4个月,MFS生存期获益接近2.2倍。研究揭盲之后,虽然对照组中有55%的患者后续接受了达罗他胺或其他治疗,但达罗他胺组仍可显著降低31%的死亡风险。该研究奠定了以达罗他胺为基础的AR抑制剂在nmCRPC治疗中的关键地位。自此,以达罗他胺为代表的新型AR抑制剂已成为nmCRPC的标准治疗药物,改变了nmCRPC的治疗格局。
在mHSPC领域,目前,9项Ⅲ期临床试验[GETUG-AFU 15、CHAARTED (E3805)、STAMPEDE group C和group G、LATITUDE、ARCHES、TITAN、ENZAMET、PEACE-1和ARASENS研究]探索了ADT联合治疗策略在mHSPC中的疗效与安全,且多项研究已证实ADT+多西他赛、ADT+ARi和ADT+ARi+多西他赛较单纯ADT可改善总生存期(OS)。
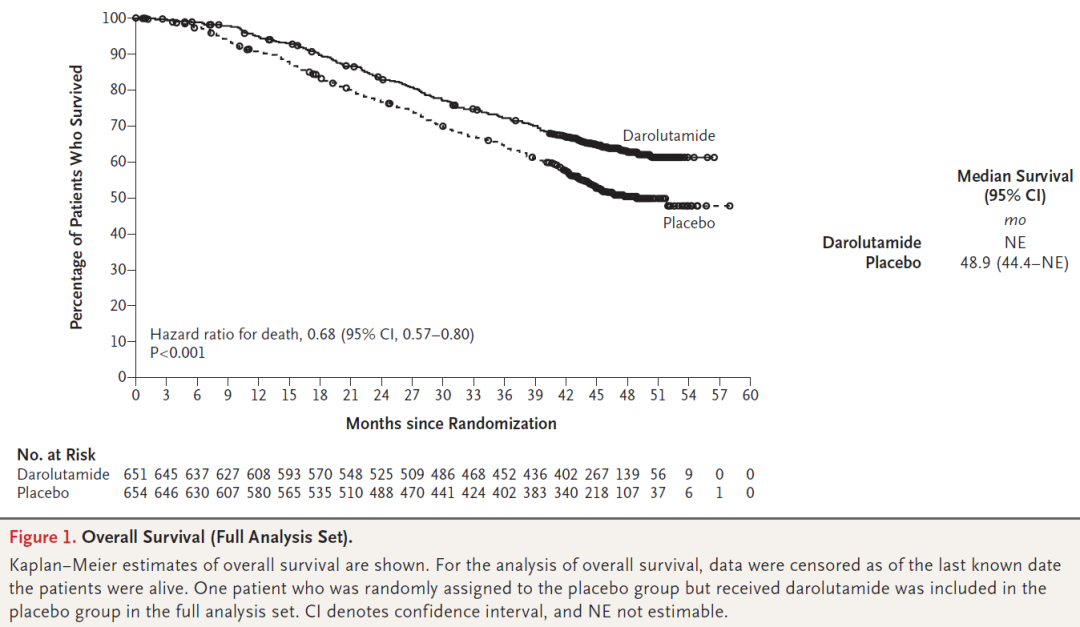
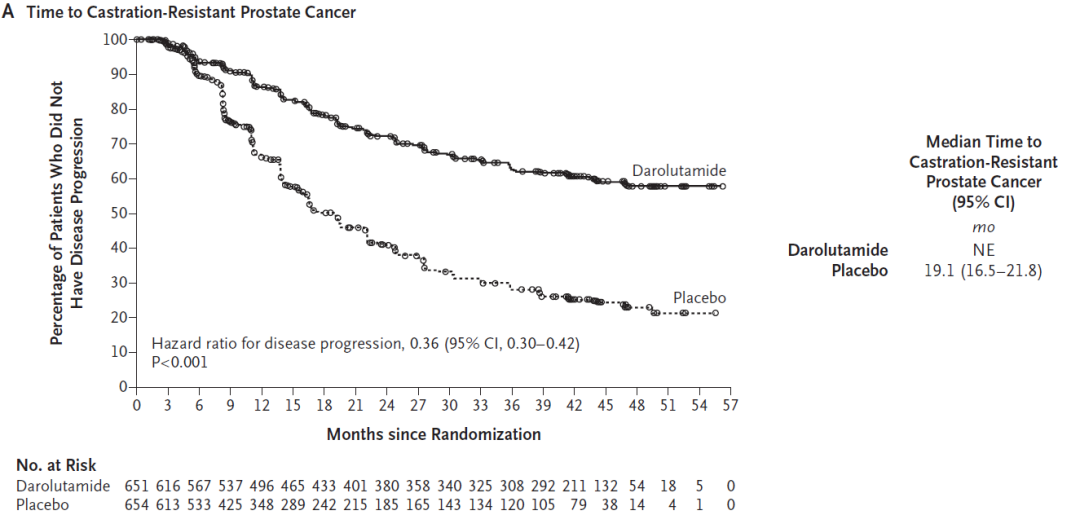
2022年,首个在mHSPC患者中验证三联治疗方案疗效和安全性的试验——ARASENS研究公布其阳性结果,数据表明[17],达罗他胺达罗他胺+ADT+多西他赛的三药方案较安慰剂+ADT+多西他赛能够显著降低mHSPC患者32.5%的死亡风险(HR 0.68,95%CI 0.57-0.80;P<0.0001));与安慰剂联合治疗组相比,达罗他胺“三联”治疗方案显著延迟了患者至去势抵抗性前列腺癌(CRPC)的时间(NE vs 19.1个月,HR 0.36,95%CI 0.30-0.42;P< 0.001),并显著延长患者的至疼痛进展时间(HR 0.79,95%CI 0.66-0.95;P=0.006),且在化疗的基础上并未增加安全性风险。而且,在高肿瘤负荷和高危/低危mHSCP患者中,达罗他胺+ADT+多西他赛带来了明显的生存获益,与研究总体人群一致。同时,达罗他胺的安全性在所有亚组中均得到证实。
有鉴于此,达罗他胺“三联”方案的成功标志着mHSCP正式进入三药强化治疗时代。2023年美国临床肿瘤学会年会(ASCO)公布了该研究根据肿瘤负荷进行分层后,患者的至疼痛进展时间,结果显示[18],达罗他胺“三联”方案能够显著延长mHSPC患者的至疼痛进展时间,尤其是在高瘤负荷患者(HR 0.75,95%CI 0.61-0.93)中。达罗他胺“三联”方案具有良好的安全性,且能够显著延长患者的预后生存,延缓疼痛进展,因此,推荐达罗他胺“三联”方案作为mHSPC治疗的新标准。
在2024年欧洲肿瘤内科学会(ESMO)大会上,一项全球多中心、随机、双盲、安慰剂对照的Ⅲ期临床试验ARANOTE,评估了达罗他胺+ADT“二联”方案在治疗mHSPC中的有效性及安全性。该研究的主要终点是放射影像学无进展生存期(rPFS)。结果显示[19],与安慰剂组相比,达罗他胺组在rPFS方面取得了显著提升,降低了46%的影像学进展或死亡风险(HR=0.54; 95%CI为0.41-0.71; P<0.0001)。在所有预先设定的亚组中都观察到一致的rPFS获益,无论是高/低瘤负荷的mHSPC患者。在安全性方面,达罗他胺组与对照组的治疗相关不良事件(TEAEs)发生率相似,且达罗他胺组疲乏与皮疹发生率更低,因TEAEs而中断治疗的比例也相对较低(6.1%对9.0%)。
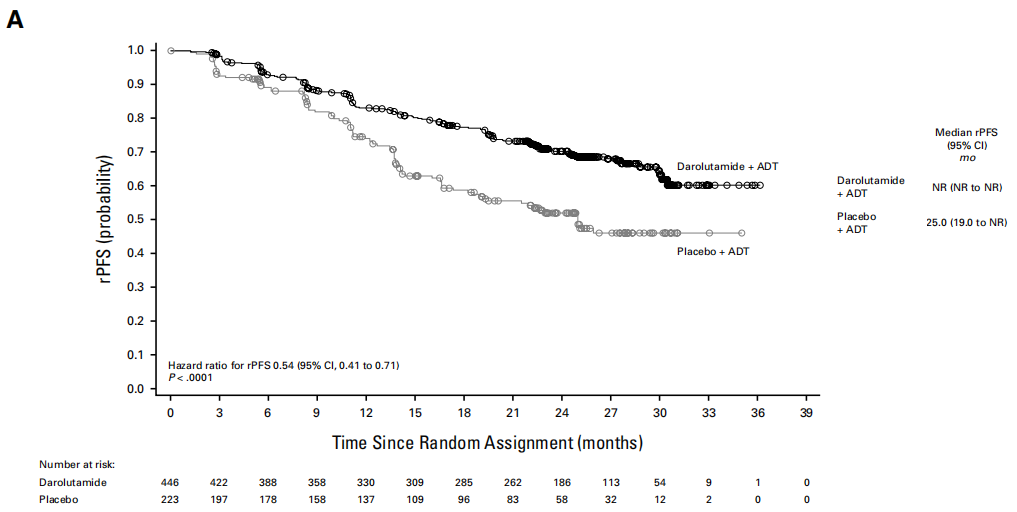
表1. ARANOTE研究的TEAE结果

此成果彰显了达罗他胺“二联”方案在前列腺癌治疗中具有显著疗效,为患者带来灵活的多元化用药策略,同时也为mHSPC的治疗构建了全新的全程化管理格局。
高危局限性前列腺癌症RP前达罗他胺+ADT的II期研究正在入组冲刺
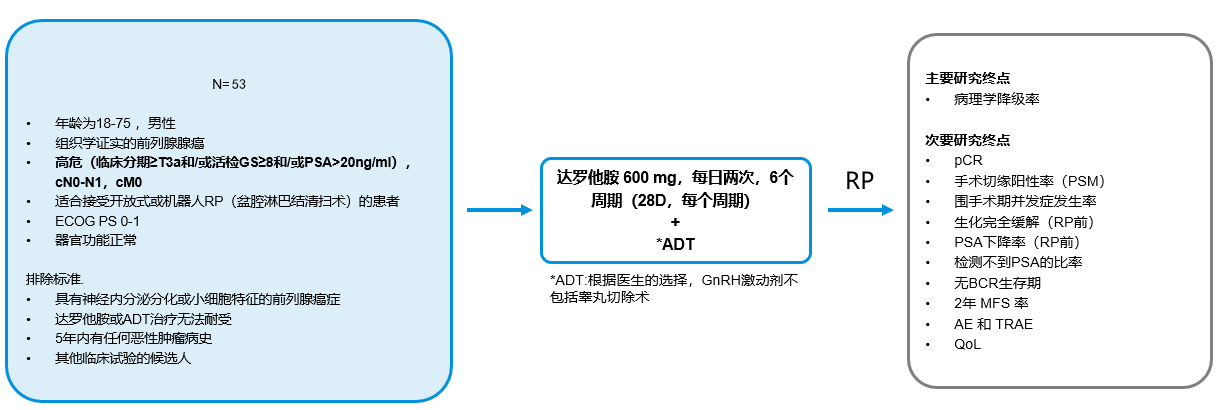
以上数据均显示出达罗他胺联合策略在晚期前列腺癌患者中的优异疗效,2023年欧洲肿瘤内科学会亚洲年会(ESMO Asia)上重磅公布了ARASENS研究中国亚组数据[20],这使得达罗他胺联合方案在中国mHSPC患者人群中的重要价值得到了再次肯定。为进一步证实达罗他胺联合策略在我国前列腺癌人群中的疗效与安全,由北京大学第一医院泌尿外科主导,西京医院参与的高危局限性前列腺癌症RP前达罗他胺+ADT的多中心、单臂、前瞻性、概念验证、II期研究正在紧锣密鼓地进行当中。
该研究计划招募接受RP作为最终治疗的高危局限性前列腺腺癌患者53例。其中,受试者必须至少具有以下特征之一,即PSA>20ng/ml,cT3疾病,Gleason评分为8-10的腺癌,可以包括盆腔淋巴结受累(N1)的受试者。如果患者之前接受过前列腺癌症的全身治疗,则不符合本研究的条件。
目前该项研究已经入随访阶段,期待研究成果的公布,以进一步为达罗他胺联合方案持续引领我国前列腺癌治疗的发展助力,不断为中国前列腺癌患者争取更高生存获益。相信随着以达罗他胺为基础的更多研究数据的公布和临床应用,前列腺癌的治疗必将步入一个更加个体化与精准化的新治疗时代,为更多前列腺癌患者带来生命的希望与光明。
1. Peyromaure M, Debré B, Mao K, et al. Management of prostatecancer in China: a multicenter report of 6 institutions[J]. J Urol, 2005,174:1794-1797.
2. Chen R,Ren S,Yiu MK, et al. Prostate cancer in Asia: a collaborative report[J]. Asian J Urol, 2014,1:15-29.
3. 中国抗癌协会泌尿男生殖系肿瘤专业委员会. 2018版转移性前列腺癌诊治中国专家共识[J]. 中华外科杂志,2018,56(9):646-652.
4. Ashrafi AN, Yip W, Aron M. Neoadjuvant Therapy in High-Risk Prostate Cancer. Indian journal of urology : vol. 36,4 (2020): 251-261.
5. Bergstrom CP, Ruffell B, Ho CM, et al. Docetaxel and mitoxantrone before radical prostatectomy in men with high-risk prostate cancer:10-year follow-up and immune correlates [J]. Anticancer Drugs,2017,28(1):120-126.
6. Kane CJ, Presti JJ, Amling CL, et al. Changing nature of high risk patients undergoing radical prostatectomy [J]. J Urol,2007,177(1):113-117.
7. Devos G, Devlies W, De Meerleer G, et al. Neoadjuvant hormonal therapy before radical prostatectomy in high-risk prostate cancer[J]. Nat Rev Urol, 2021,18(12):739-762.
8. Liu W, Yao Y, Liu X, et al. Neoadjuvant hormone therapy for patients with high-risk prostate cancer:a systematic review and meta-analysis[J]. Asian J Androl, 2021,23(4):429-436.
9. Ashrafi AN, Yip W, Aron M. Neoadjuvant therapy in high-Risk prostate cancer [J]. Indian J Urol,2020,36(4):251-261.
10. Bandini M, Fossati N, Gandaglia G, et al. Neoadjuvant and adjuvant treatment in high-risk prostate cancer. Expert review of clinical pharmacology vol. 11,4 (2018): 425-438.
11. Clarke NW, Ali A, Ingleby FC, et al. Addition of docetaxel to hormonal therapy in low- and high-burden metastatic hormone sensitive prostate cancer: long-term survival results from the STAMPEDE trial. Ann Oncol. 2019 Dec 1;30(12):1992-2003.
12. Fizazi K, Tran NP, Fein L, et al. Abiraterone acetate plus prednisone in patients with newly diagnosed high-risk metastatic castration-sensitive prostate cancer (LATITUDE): final overall survival analysis of a randomised, double-blind, phase 3 trial. Lancet Oncol. 2019 May;20(5):686-700.
13. Armstrong A ,et al. Annals of Oncology (2021) 32 (suppl_5): S1283-S1346.10.1016/annonc/annonc741.
14. Chi KN, Chowdhury S, Bjartell A, et al. Apalutamide in Patients With Metastatic Castration-Sensitive Prostate Cancer: Final Survival Analysis of the Randomized, Double-Blind, Phase III TITAN Study. J Clin Oncol. 2021 Jul 10;39(20):2294-2303.
15. Fizazi K, Shore N, Tammela T L, et al. Nonmetastatic, castration-resistant prostate cancer and survival with darolutamide[J]. New England Journal of Medicine, 2020, 383(11): 1040-1049.
16. 3.Fizazi K, Shore N, Tammela T L, et al. Darolutamide in nonmetastatic, castration-resistant prostate cancer[J]. New England Journal of Medicine, 2019, 380(13): 1235-1246.
17. Smith MR, Hussain M, Saad F, et al. Darolutamide and Survival in Metastatic, Hormone-Sensitive Prostate Cancer. N Engl J Med 2022; 386:1132-1142.
18. Smith MR, et al. Darolutamide and time to pain progression by disease volume in ARASENS. 2023 ASCO, e17075.
19. Efficacy and safety of darolutamide plus androgen-deprivation therapy (ADT) in patients with metastatic hormone-sensitive prostate cancer (mHSPC) from the phase 3 ARANOTE trial2. ESMO 2024.LBA68.
20. Wang, et al. Darolutamide (DARO) in combination with androgen-deprivation therapy (ADT) and docetaxel (DOC) in Chinese patients (pts) with metastatic hormone-sensitive prostate cancer (mHSPC) in the phase III ARASENS study. 2023 ESMO ASIA Congress . 255O.
排版编辑:肿瘤资讯-jyy











 苏公网安备32059002004080号
苏公网安备32059002004080号


