EGFR突变是NSCLC中最常见的驱动基因,其中,EGFR 20外显子插入(ex20ins)突变的发生率仅次于19号外显子缺失突变(ex19del)和21号外显子L858R点突变(L858R),是EGFR的第三大突变亚型。在我国,EGFR ex20ins占所有NSCLC突变类型的0.3%-2.9%,占EGFR突变的2%-5%。EGFR ex20ins突变NSCLC患者的治疗选择有限,其中一线治疗仍以化疗为主,但其疗效欠佳,因此亟需优化这部分人群的诊疗。PAPILLON研究是全球首个在EGFR ex20ins突变NSCLC一线治疗领域取得阳性结果的III期临床研究,基于此,埃万妥单抗联合化疗已经被NCCN非小细胞肺癌指南列为初治EGFR ex20ins突变NSCLC患者的优选一线治疗。更具里程碑意义的是,埃万妥单抗在2025年2月8日正式获得NMPA批准,为国内这一领域的诊疗打开了全新的治疗格局。基于此,【肿瘤资讯】特邀中国医学科学院肿瘤医院的段建春教授深入解读埃万妥单抗的研究数据及临床意义。
中国医学科学院肿瘤医院 肿瘤内科
CSCO理事
CSCO肉瘤专家委员会副主任委员
CSCO非小细胞肺癌专家委员会委员
CSCO免疫治疗专家委员会委员
CSCO青年专家委员会委员
国家抗肿瘤药物临床应用监测青年专家委员会副主任委员
北京医学奖励基金会肺癌医学青年专家委员会副主任委员
中国初级卫生保健基金会肺癌专业委员会 常务委员
北京肿瘤学会肺癌专业委员会常委
北京癌症防治学会肺癌免疫治疗专业委员会常委
北京医学会肿瘤学分会青年委员会委员
教育部“创新团队”骨干成员
国自然青年基金,国自然面上项目获得者
荣获“教育部科技进步一等奖”,“国家科技进步二等奖”,首届“国家优秀青年医师”,“2021 年度茅以升科学技术奖——北京青年科技奖”
长期致力于肺癌为主的胸部肿瘤的规范化个体化多学科综合治疗及转化研究。
任重道远,EGFR ex20ins突变NSCLC亟需探索新的诊疗模式
EGFR ex20ins是继EGFR ex19del和L858R两大敏感突变外EGFR的第三大突变亚型[1]。与EGFR敏感突变相似的是,EGFR ex20ins突变多见于亚裔、女性、不吸烟、肺腺癌患者[2];然而不同的是,EGFR ex20ins的空间结构存在明显的空间位阻,导致药物结合口袋缩小,使得EGFR ex20ins NSCLC对传统的EGFR-TKIs的获益有限,预后差。此外,EGFR ex20ins具有高度分子异质性,目前已报告检出200余种突变亚型[3],且不同的突变亚型也会影响传统EGFR-TKIs对这部分人群的治疗疗效,再次提示这部分人群更具挑战性。
近年来,EGFR ex20ins突变NSCLC备受国内外专家学者的关注,多项新型EGFR-TKI进行了诸多临床研究探索,然而结果却不尽如人意。其中EXCLAIM-2研究探索了莫博赛替尼一线治疗EGFR ex20ins突变NSCLC中的有效性和安全性,令人遗憾的是,相较含铂化疗,莫博赛替尼并未改善中位PFS(9.6个月 vs 9.6个月,HR=1.04 [95%CI 0.77-1.39], P=0.803)[4]。此外,舒沃替尼一线治疗EGFR ex20ins突变NSCLC的I/II期临床研究显示(N=28),整体人群的最佳ORR为71.4%,其中经确认的ORR为35.7%,显示出了初步的抗肿瘤疗效[5],有待随机对照研究进一步验证。因此,对于EGFR ex20ins突变NSCLC患者,仍需进一步探寻优化的诊疗模式。
独具匠心,埃万妥单抗的多重作用机制奠定了其疗效基础
埃万妥单抗是一种靶向EGFR和MET的全人源双特异性免疫球蛋白G1抗体,目前已被证实具有3种作用机制[6]:
免疫细胞导向活性:埃万妥单抗可募集免疫效应细胞,引起依赖NK细胞的抗体依赖性细胞毒性和依赖巨噬细胞的胞啃作用(即啃噬细胞膜);埃万妥单抗Fc区的岩藻糖含量较低,增强了这种免疫效应细胞募集作用
受体降解:以高亲和力与细胞外EGFR和MET结合也会诱导受体降解。通过细胞外结合,埃万妥单抗不受EGFR结合口袋共突变的影响
抑制配体结合:埃万妥单抗与细胞外EGFR和MET结合的亲和力高于其天然配体,因此可阻断这些受体的天然信号传递通路
在此基础上联合化疗可起到协同效应。化疗介导的肿瘤细胞凋亡,可释放抗原招募更多携带Fc的免疫细胞,进而协同增强埃万妥单抗的免疫细胞介导毒性(图1)。
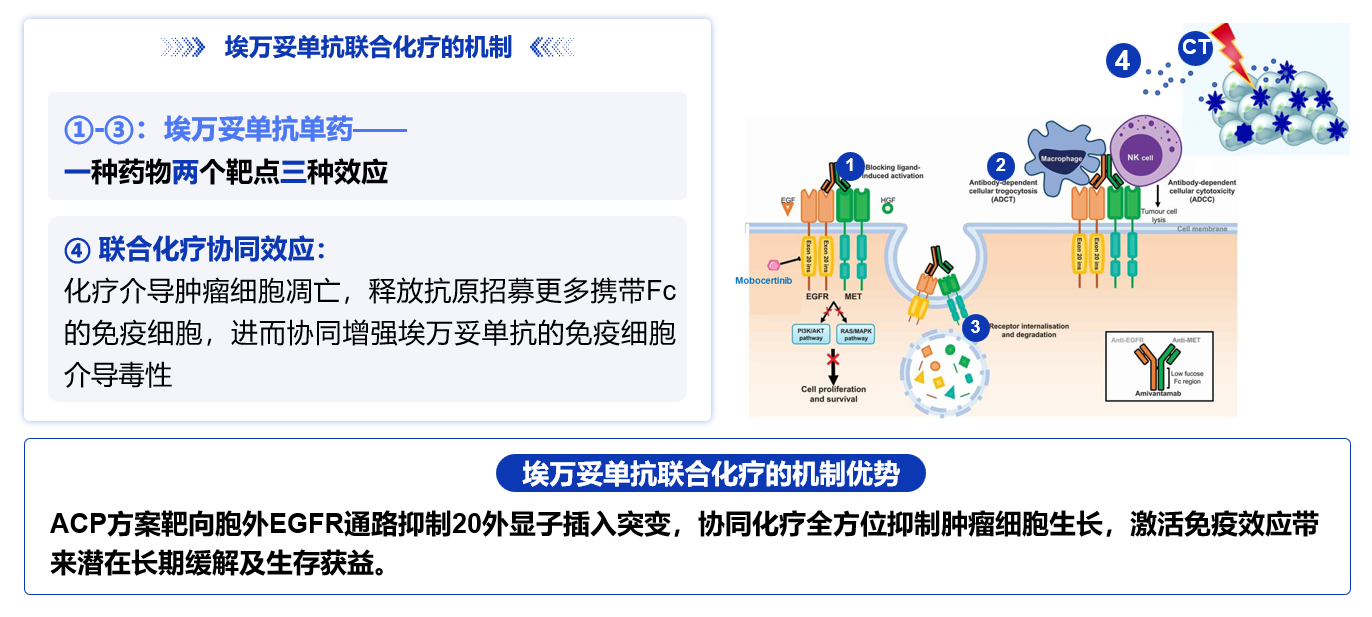
多重的作用机制为以埃万妥单抗为基础的治疗模式的出色疗效奠定了坚实的基础,目前埃万妥单抗联合化疗(ACP方案)以及联合兰泽替尼已经在国内外陆续获批相应适应症(表1)。

继往开来,埃万妥单抗开辟晚期EGFR ex20ins突变NSCLC新诊疗格局
PAPILLON研究是一项全球多中心、随机对照III期临床研究,旨在评估埃万妥单抗联合化疗(ACP方案)与单纯化疗在未经治疗的EGFR ex20ins突变晚期或转移性NSCLC患者中的疗效和安全性。主要终点是根据盲态独立中心评估(BICR)评估的PFS,关键次要终点包括ORR和OS[7](图2)。
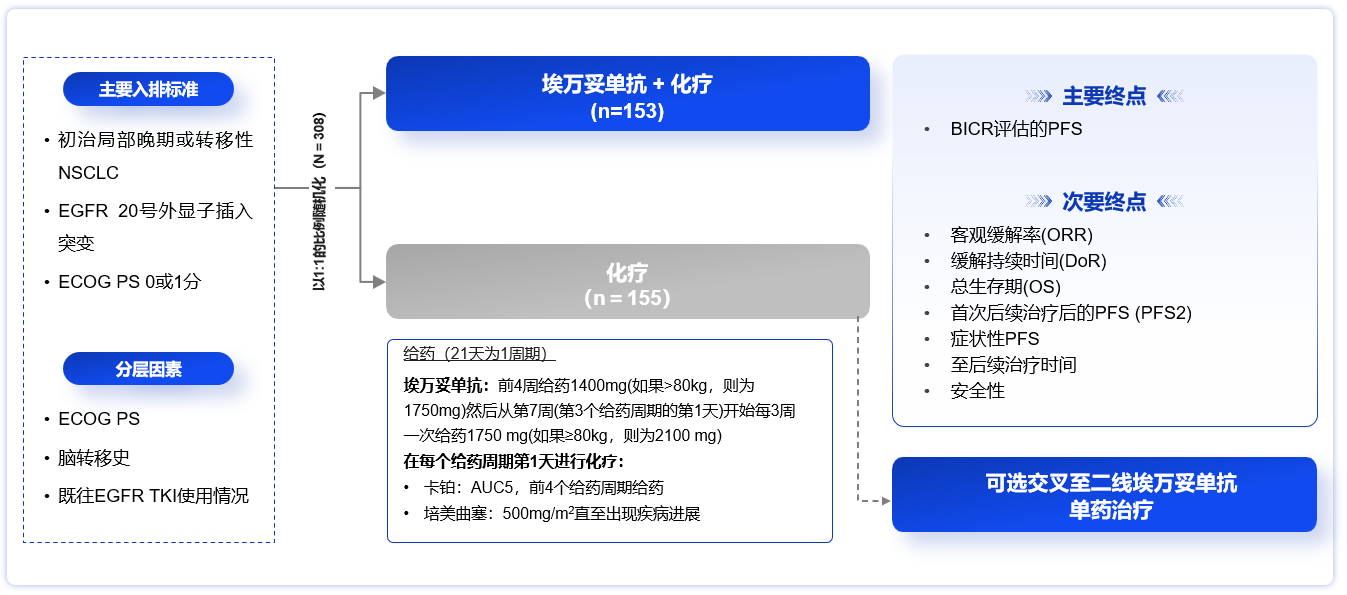
研究共纳入308例患者,ACP组和化疗组的基线特征均衡,其中基线伴脑转移患者均占23%。
数据截至2023年5月3日,整体人群的中位随访时间为14.9个月,ACP组为EGFR ex20ins突变NSCLC患者带来了具有统计学及临床意义的PFS显著获益。ACP组和化疗组经BICR评估的中位PFS分别为11.4个月和6.7个月;相较化疗组,ACP组降低了60%的疾病进展或死亡风险,且从生存曲线来看,两组的曲线早期即分离并显示出了长拖尾效应,两组18个月PFS率分别为31%和3%(图3);此外,研究者评估的中位PFS与BICR评估的获益一致(12.9个月 vs 6.9个月),疾病进展或者患者死亡的风险降低了62%[7]。
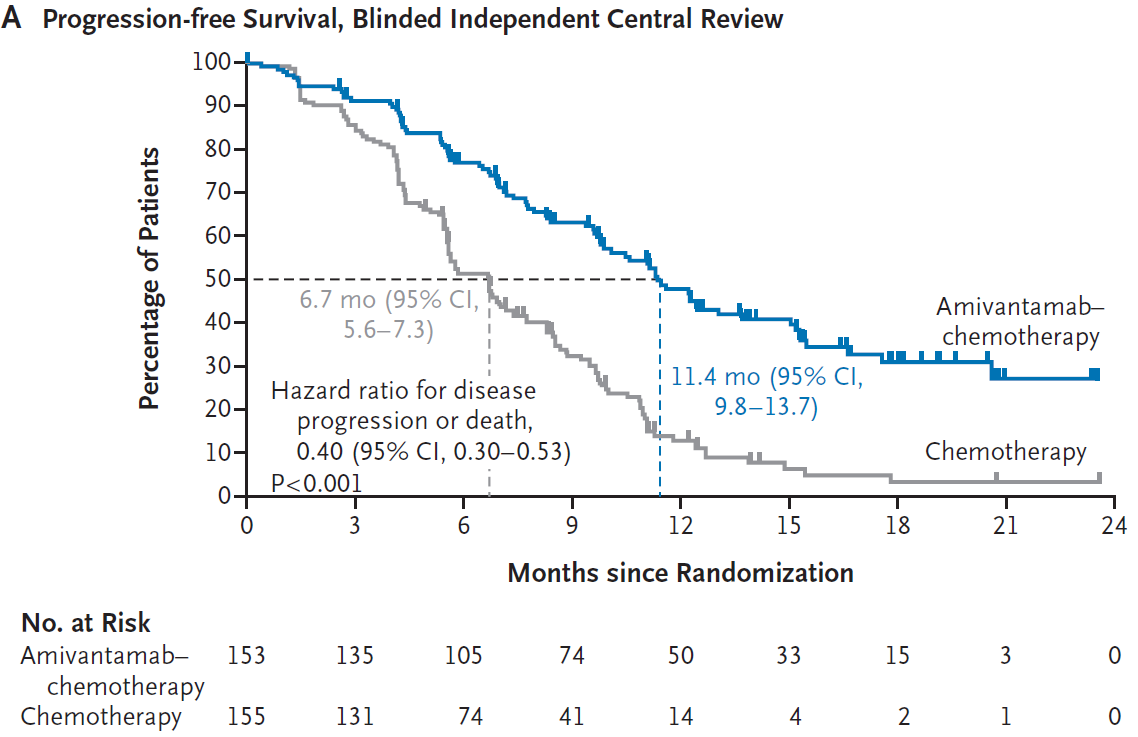
在肿瘤缓解方面,ACP组可快速且显著降低患者的肿瘤负荷。ACP组和化疗组的中位至肿瘤缓解时间分别为6.7周和11.4周。相较化疗组,ACP组的ORR提高了26%(73% vs 47%,OR=3.0 [95%CI 1.8-4.8],P<0.0001);且患者一旦达到肿瘤缓解,中位的缓解持续时间(mDoR)显著延长(9.7个月 vs 4.4个月)[7](图4)。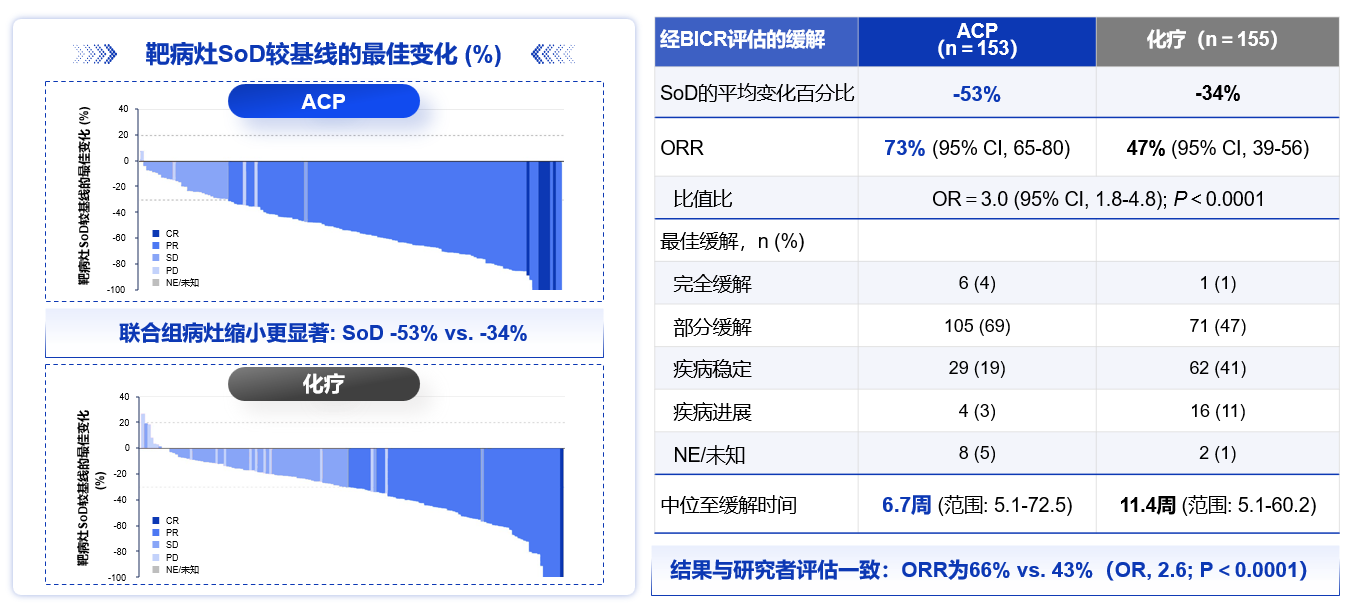
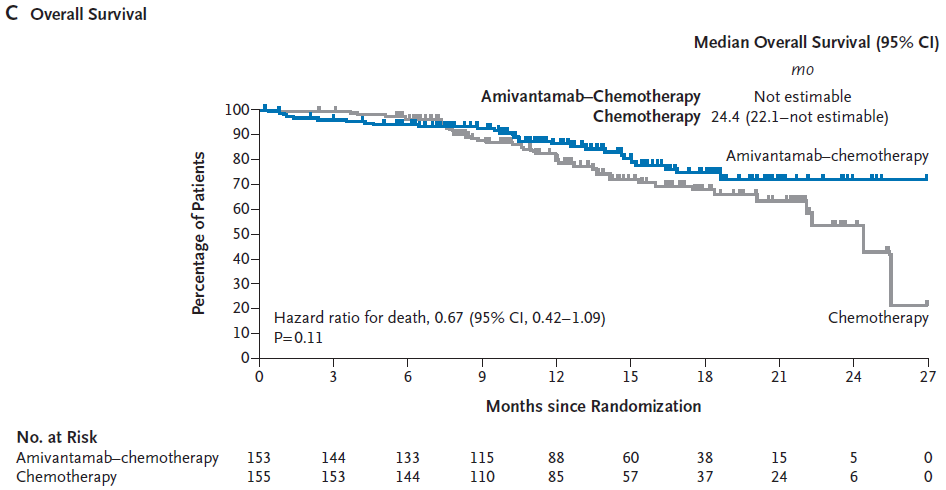
值得关注的是,尽管化疗组有66%的患者在疾病进展后交叉接受二线埃万妥单抗治疗,ACP组的OS依旧显示出获益趋势。相较化疗组,ACP组降低了33%的死亡风险(HR=0.67; 95%CI 0.42-1.09)[7](图5),期待未来更长时间随访后的最终分析结果。
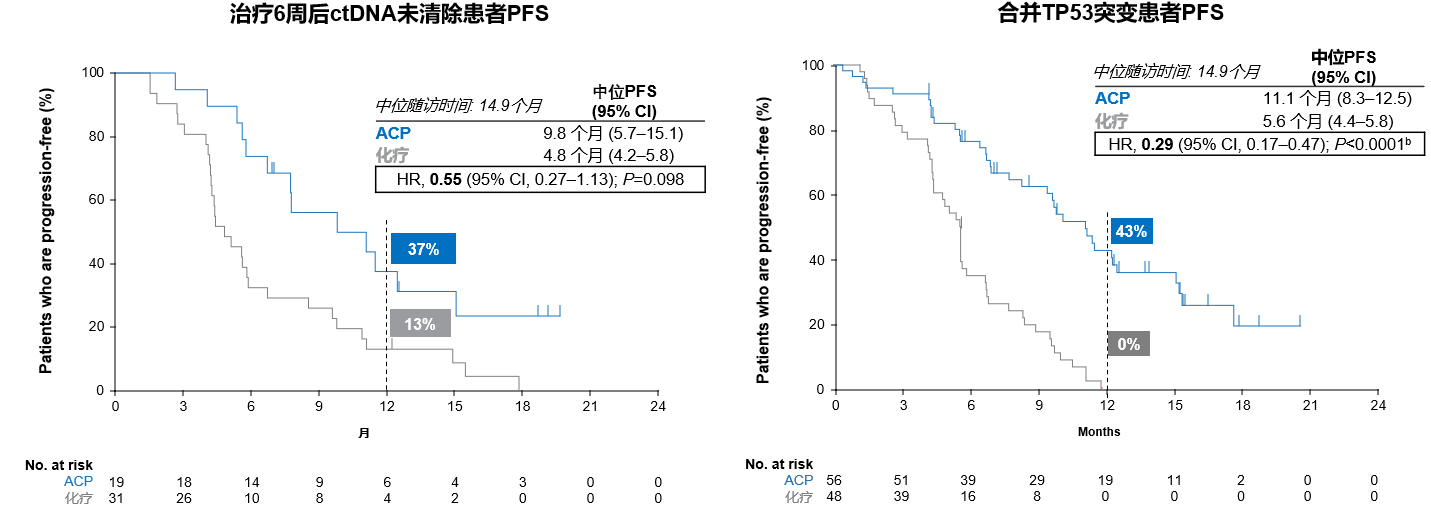
迎难而上,ACP组在高危亚组中同样展现出强劲的疗效优势。相较化疗组,ACP组在治疗6周后ctDNA未清除(HR=0.55,[95%CI 0.27-1.13])以及基线合并TP53突变(HR=0.29,[95%CI 0.17-0.47])患者中也具有明显的PFS获益趋势(图6)[8]。
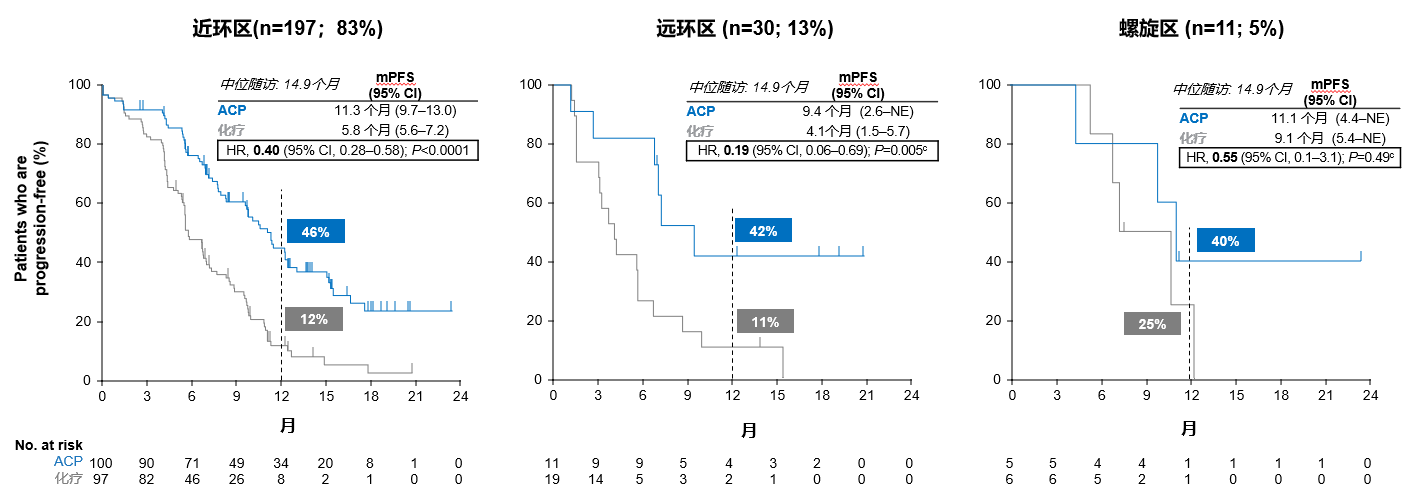
此外,无论ex20ins突变类型,与化疗组相比,ACP组均取得与整体人群一致的PFS获益[8]。
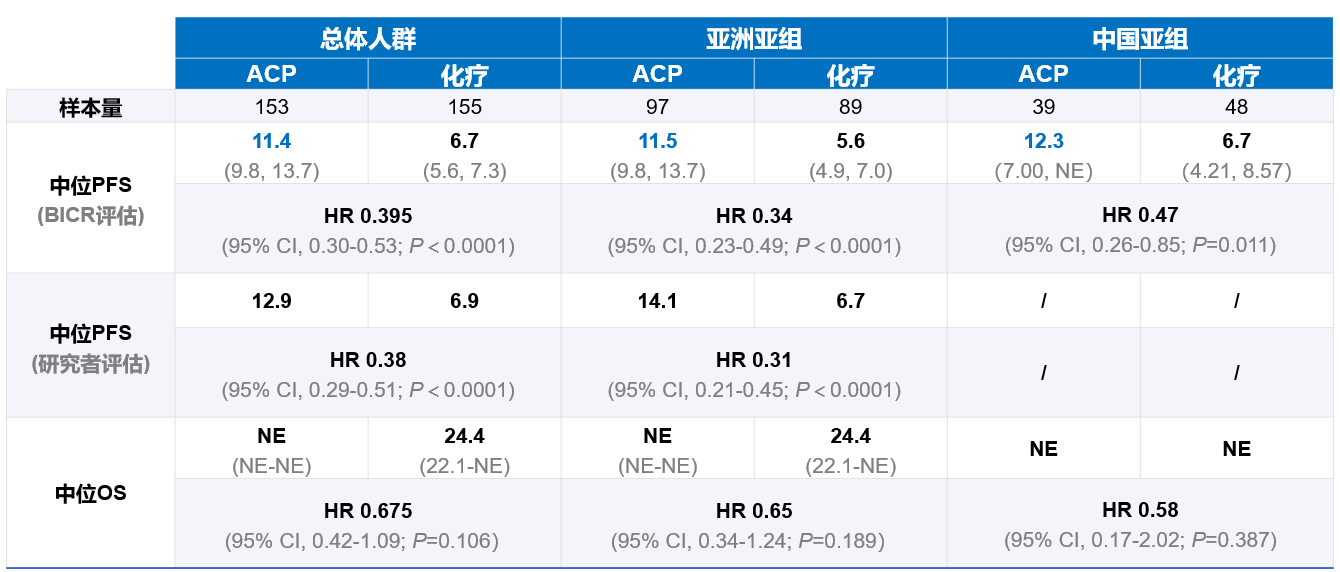
更为有意义的是,亚洲人群和中国人群的PFS结果与整体人群一致[9,10],相较化疗组,ACP组均明显降低了疾病进展或死亡风险。其中,在中国人群中,相比于化疗组,ACP组的中位PFS明显延长,分别是12.3个月和6.7个月,降低疾病进展或死亡风险达53%(HR=0.47; 95% CI, 0.26-0.85; P=0.011)(表2)。
安全性方面,ACP组整体耐受性良好,安全性可预测且可控,任何事件导致的埃万妥单抗相关停药率低(仅7%)[7]。
埃万妥单抗谱写国内EGFR ex20ins突变NSCLC诊疗新篇章
基于PAPILLON研究在初治EGFR ex20ins突变NSCLC人群取得的突破性进展,FDA已经批准其相应适应症,且埃万妥单抗联合化疗已经成为NCCN非小细胞肺癌指南优选的一线治疗方案。更具里程碑意义的是,基于PAPILLON研究的全球和中国亚组的研究数据,2月8日,NMPA正式批准埃万妥单抗联合化疗用于初治EGFR ex20ins突变NSCLC的一线治疗,标志着这部分人群正式迈入了精准治疗时代。
[1] Mao L, Zhao W, Li X, et al. Mutation Spectrum of EGFR From 21,324 Chinese Patients With Non-Small Cell Lung Cancer (NSCLC) Successfully Tested by Multiple Methods in a CAP-Accredited Laboratory. Pathol Oncol Res. 2021;27:602726. Published 2021 Apr 7. doi:10.3389/pore.2021.602726
[2] Zhang YL, Yuan JQ, Wang KF, et al. The prevalence of EGFR mutation in patients with non-small cell lung cancer: a systematic review and meta-analysis. Oncotarget. 2016;7(48):78985-78993. doi:10.18632/oncotarget.12587
[3] 中国抗癌协会肿瘤病理专业委员会分子病理协作组, 中国医师协会肿瘤多学科诊疗专业委员会. 非小细胞肺癌表皮生长因子受体20号外显子插入突变检测临床实践中国专家共识(2024版) [J] . 中华肿瘤杂志, 2024, 46(3) : 179-188. DOI: 10.3760/cma.j.cn112152-20230905-00125.
[4] Jänne PA, Wang BC, Cho BC, et al. First-Line Mobocertinib Versus Platinum-Based Chemotherapy in Patients With EGFR Exon 20 Insertion-Positive Metastatic Non-Small Cell Lung Cancer in the Phase III EXCLAIM-2 Trial. J Clin Oncol. Published online January 29, 2025. doi:10.1200/JCO-24-01269
[5] Yan Xu et al., Efficacy and safety of sunvozertinib in treatment naïve NSCLC patients with EGFR exon20 insertion mutations.. JCO 41, 9073-9073(2023). doi:10.1200/JCO.2023.41.16_suppl.9073
[6] Cho BC, Simi A, Sabari J, Vijayaraghavan S, Moores S, Spira A. Amivantamab, an Epidermal Growth Factor Receptor (EGFR) and Mesenchymal-epithelial Transition Factor (MET) Bispecific Antibody, Designed to Enable Multiple Mechanisms of Action and Broad Clinical Applications. Clin Lung Cancer. 2023;24(2):89-97. doi:10.1016/j.cllc.2022.11.004
[7] Zhou C, Tang KJ, Cho BC, et al. Amivantamab plus Chemotherapy in NSCLC with EGFR Exon 20 Insertions. N Engl J Med. 2023;389(22):2039-2051. doi:10.1056/NEJMoa2306441
[8] Goldman, J.W. et al. MA12.06 PAPILLON: TP53 Co-mutations, Sites of Insertion, and ctDNA Clearance Among Patients with EGFR Ex20ins-Mutated Advanced NSCLC. Journal of Thoracic Oncology, Volume 19, Issue 10, S102 - S103
[9] Zhou, C. et al. 513MO Amivantamab plus chemotherapy vs chemotherapy as a first-line treatment among Asian patients with EGFR exon 20 insertion-mutated advanced non-small cell lung cancer (NSCLC): PAPILLON subgroup analysis. Annals of Oncology, Volume 34, S1668 - S1669
[10] Ke-Jing Tang et al., Amivantamab plus chemotherapy vs chemotherapy as first-line treatment among patients with EGFR exon 20 insertion–mutated advanced non-small cell lung cancer (NSCLC): PAPILLON Chinese subgroup analysis.. JCO 42, 8606-8606(2024). doi:10.1200/JCO.2024.42.16_suppl.8606
CRC Code: EM-176449
Approved Date: 2025-2-16
排版编辑:肿瘤资讯-TJ
✅ “本资料仅用于医学、科学交流,可能涉及尚未在中国获批的产品和适应症。强生创新制药不支持、不鼓励任何未被批准的药品/适应症使用。”











 苏公网安备32059002004080号
苏公网安备32059002004080号


