在本期文献更新中,我们将探讨多项最新的研究成果,这些研究在癌症治疗和免疫疗法领域中具有重要意义。通过对不同治疗策略的深入分析,我们将揭示这些研究如何推动医学前沿的发展,并为临床实践提供新的视角和方法。
双特异性CD40激动抗体通过抗体-肽偶联物形成实现癌症特异性肽递送
本文亮点
本研究开发了一种新型双特异性CD40激动性抗体BiA9*2_HF,能够有效递送抗原肽,显著提高CD8+和CD4+ T细胞的增殖。该抗体在小鼠肿瘤模型中展示了优异的抗肿瘤疗效和安全性,能够完全清除肿瘤并产生远隔效应。BiA9*2_HF的设计结合了CD40激动活性和抗原递送功能,为癌症免疫治疗提供了新的可能性。
主要内容
本研究开发了一种新型双特异性CD40激动性抗体BiA9*2_HF,旨在通过抗体-肽偶联实现癌症特异性肽递送,从而增强小鼠的T细胞增殖和抗肿瘤免疫。BiA9*2_HF在病毒诱导和基于新抗原的肿瘤模型中表现出治疗效果和安全性,能够完全清除肿瘤并对肿瘤生长产生远隔效应。该药物候选物可用于为癌症患者量身定制免疫治疗。
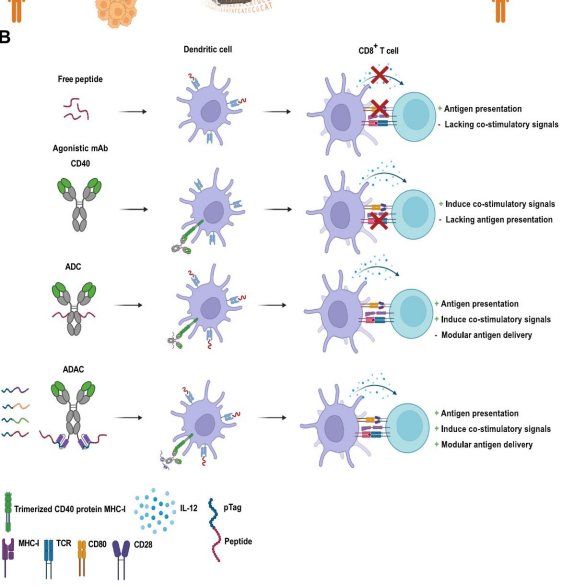
图1 - ADAC技术工作流程
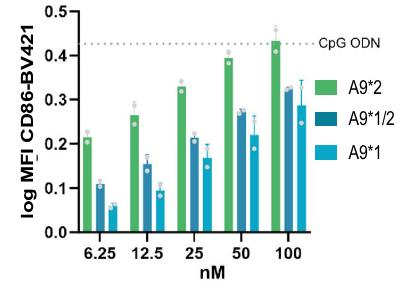
图2 - 新型克隆的激动活性
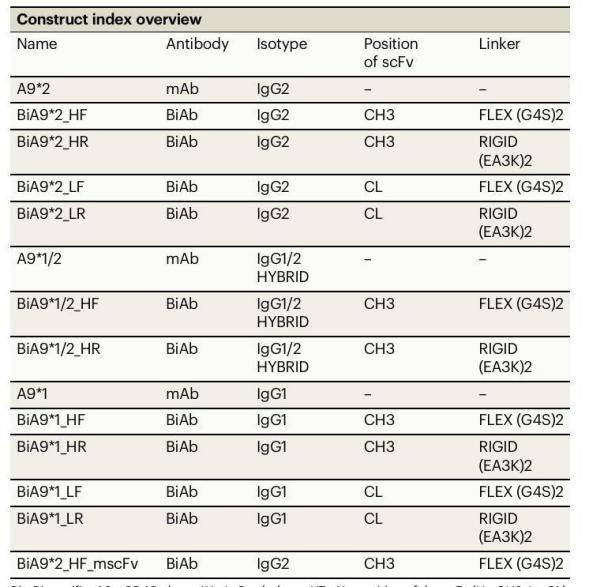
Bi = 双特异性,* = CD40抗体,1/2 = IgG亚类,_H = V = scFv的位置(H = CH3,L = CL),F = FLEX连接子,R = RIGID连接子。
表1 - mAb和双特异性抗体构建索引
CD25×TIGIT双特异性抗体通过选择性肿瘤内Treg细胞耗竭诱导抗肿瘤活性
本文亮点
本研究探讨了一种新型CD25-TIGIT双特异性抗体在肿瘤微环境中选择性耗竭调节性T细胞(Tregs)的潜力。研究表明,该抗体在小鼠模型中显著增强了肿瘤抑制效果,并在体外实验中优先消除CD25+ TIGIT+双阳性细胞。与单一抗体疗法相比,该双特异性抗体在不显著影响外周Tregs的情况下,展现出更强的抗肿瘤活性,提示其在临床应用中的潜在价值。
主要内容
本研究探讨了CD25和TIGIT双特异性抗体在选择性去除肿瘤内Tregs中的应用。研究表明,NSWm7210和NSWh7216抗体在小鼠和人类模型中均表现出增强的抗肿瘤活性,且对外周Tregs无明显毒性。NSWm7210在小鼠模型中显著抑制肿瘤生长,并通过去除肿瘤内Tregs和激活效应细胞(Teffs)来增强抗肿瘤活性。NSWh7216在CD25人源化小鼠中显示出对肿瘤内Tregs的高选择性结合能力,且不显著影响外周Tregs。
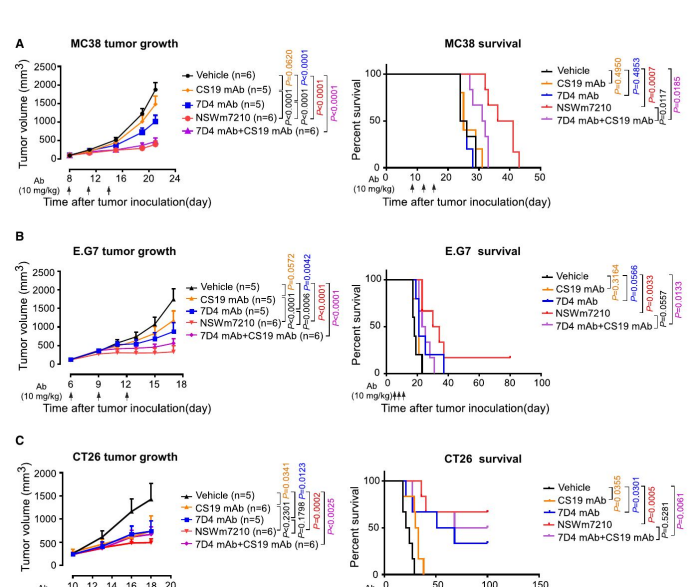
图3 - NSWm7210抑制肿瘤生长
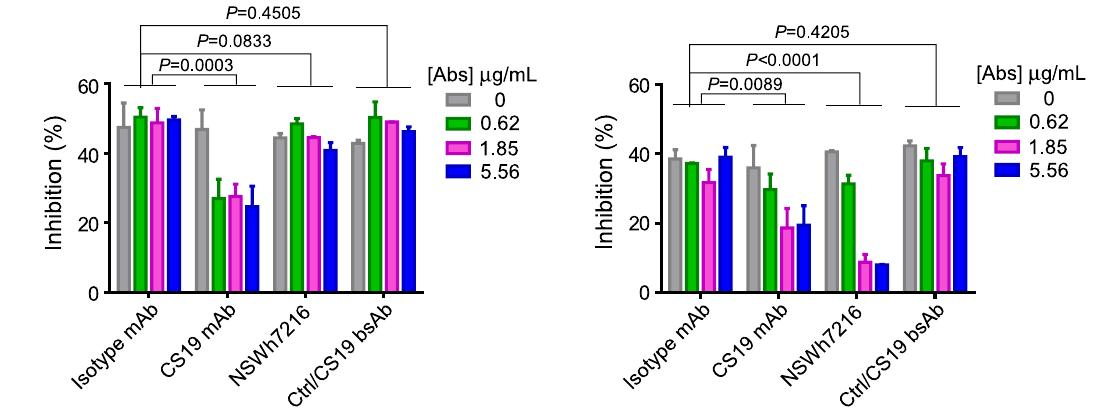
图4 - NSWh7216的构建与特性
费城染色体阳性急性淋巴细胞白血病中mini-hyper-CVD、贝林妥欧单抗和泊那替尼的二期试验
本文亮点
本研究探讨了mini-hyper-CVD、贝林妥欧单抗和泊那替尼联合治疗费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)的疗效。结果显示,新诊断患者的完全分子学缓解(CMR)率为78%,3年总生存(OS)率为72%。在复发/难治性患者和CML LBP患者中,所有可评估患者均达到完全缓解(CR),CMR率为71%。研究表明,该联合方案在Ph+ ALL和CML LBP患者中具有良好的疗效和安全性。
主要内容
在这项开放标签、单臂的二期试验中,研究了小剂量化疗联合泊那替尼和贝林妥欧单抗治疗新诊断或复发/难治性Ph+ ALL或慢性髓性白血病淋巴母细胞期(CML LBP)的可行性。主要结果显示,新诊断患者的CMR率为78%,3年OS率为72%。复发/难治性患者和CML LBP患者的CMR率为71%。研究表明,该联合方案在Ph+ ALL和CML LBP中具有良好的疗效和安全性。
阻断CCR5+ T细胞在肿瘤微环境中的积累优化抗TGF-β/PD-L1双特异性抗体
本文亮点
本研究揭示了抗TGF-β/PD-L1双特异性抗体YM101在多种肿瘤模型中的显著抗肿瘤活性。通过单细胞RNA测序分析,发现YM101治疗后肿瘤微环境中免疫细胞的显著变化,尤其是CCR5+ T细胞的积累。结合CCR5拮抗剂Maraviroc,能够有效抑制CCR5+ T细胞的积累,增强YM101的疗效。这一组合策略不仅提高了抗肿瘤免疫反应,还诱导了持久的免疫记忆,显示出在临床应用中的潜力。
主要内容
在本研究中,YM101在多种小鼠肿瘤模型中表现出显著的抗肿瘤活性。通过单细胞RNA测序分析,揭示了YM101治疗后肿瘤微环境的复杂变化,特别是免疫细胞亚群的重新分布。研究发现,YM101不仅增强了抗肿瘤免疫反应,还通过抑制CCR5+ T细胞的积累来优化免疫反应。结合CCR5拮抗剂Maraviroc,进一步提高了YM101的疗效,表明选择性靶向CCR5信号通路是增强YM101疗效的有效策略。
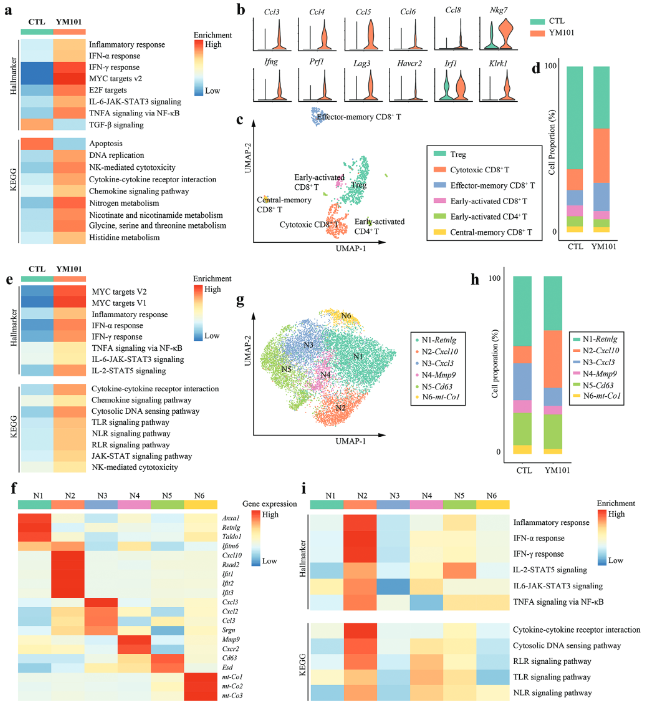
. 肿瘤浸润T细胞和中性粒细胞的二次分析。a) 热图显示总T细胞的GSEA结果。b) 小提琴图显示YM101组T细胞中显著上调的基因。c) 显示T细胞重聚类分析结果的UMAP图。d) 直方图显示CTL和YM101组中T细胞亚群的比例。e) 显示总中性粒细胞GSEA结果的热图。f) 显示常见中性粒细胞标记物表达水平的热图。g) 显示中性粒细胞重聚类分析结果的UMAP图。h) 直方图显示CTL和YM101组中中性粒细胞亚群的比例。i) GSEA描绘中性粒细胞亚群的内在特征。
图5- T细胞和中性粒细胞分析
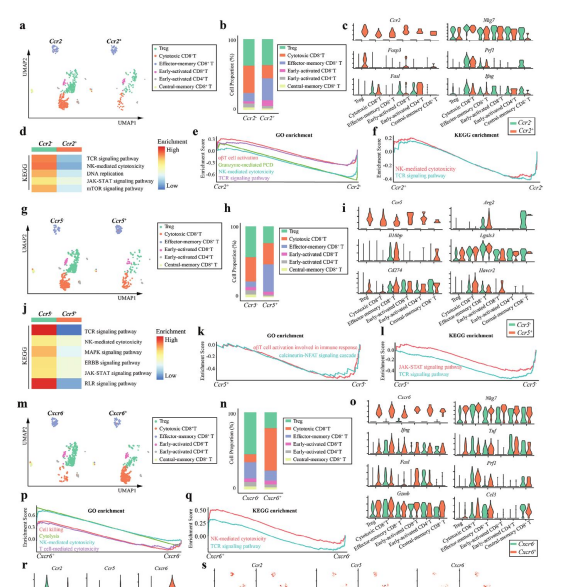
. YM101组Ccr2+, Ccr5+, Cxcr6+ T细胞的内在特征。a) YM101治疗后Ccr2−和Ccr2+ T细胞的UMAP聚类。总计692个T细胞中,495个为Ccr2− (71.5%),197个为Ccr2+ (28.5%) T细胞。b) 直方图显示YM101组Ccr2−和Ccr2+ T细胞中T细胞亚群的比例。c) 小提琴图显示T细胞激活相关标记物的表达水平。d) 显示YM101组Ccr2−和Ccr2+ T细胞富集分析结果的热图。e,f) GSEA富集图显示YM101组Ccr2−和Ccr2+ T细胞之间的差异。g) 显示根据Ccr5水平对T细胞重聚类分析结果的UMAP图。h) 直方图显示YM101组Ccr5−和Ccr5+ T细胞中T细胞亚群的比例。i) 小提琴图显示免疫抑制相关标记物的表达水平。j) 显示YM101组Ccr5−和Ccr5+ T细胞富集分析结果的热图。k,l) GSEA富集图显示YM101组Ccr5−和Ccr5+ T细胞之间的差异。m) 显示根据Cxcr6水平对T细胞重聚类分析结果的UMAP图。n) 直方图显示YM101组Cxcr6−和Cxcr6+ T细胞中T细胞亚群的比例。o) 小提琴图显示T细胞激活和细胞毒性相关标记物的表达水平。p,q) GSEA富集图显示YM101组Cxcr6−和Cxcr6+ T细胞之间的差异。r) 小提琴图显示CTL和YM101组T细胞中Ccr2, Ccr5, 和Cxcr6的表达水平。s) UMAP图显示CTL和YM101组T细胞中Ccr2, Ccr5, 和Cxcr6的表达。
图6 - Ccr2+, Ccr5+, Cxcr6+ T细胞特征
Epcoritamab在复发/难治性大B细胞淋巴瘤中的2年随访结果
本文亮点
Epcoritamab在复发/难治性大B细胞淋巴瘤(LBCL)中的长期疗效和安全性得到证实。研究显示,24个月的无进展生存(PFS)率为27.8%,总生存(OS)率为44.6%。完全缓解(CR)率为40.1%,其中64.2%的患者在24个月时仍保持CR。最常见的不良事件为细胞因子释放综合征(51.0%)和发热(24.8%)。这些结果表明,Epcoritamab在治疗难治性LBCL中具有显著的长期益处。

图7- 患者缓解持续时间
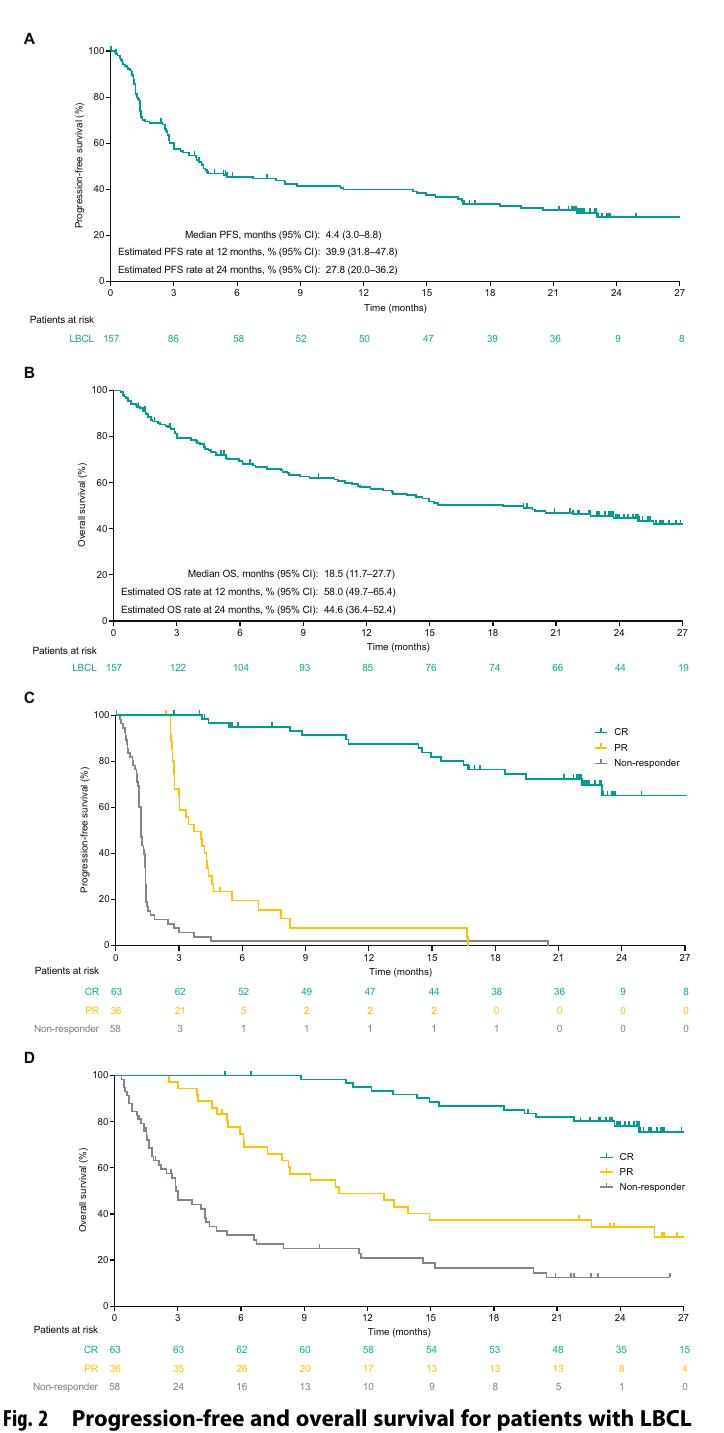
图8 - 无进展生存和总生存
主要内容
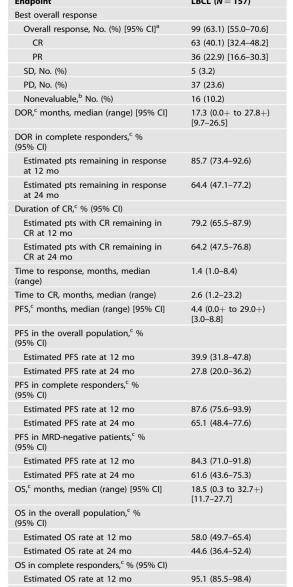
在EPCORE NHL 1试验中,Epcoritamab作为单药治疗复发或难治性LBCL显示出深度和持久的疗效。经过25.1个月的中位随访,总缓解率(ORR)为63.1%,CR率为40.1%。24个月的PFS率和OS率分别为27.8%和44.6%。在微小残留病灶(MRD)阴性患者中,45.4%显示出更长的PFS和OS。常见的不良事件包括细胞因子释放综合征(51.0%)和发热(24.8%)。这些结果表明Epcoritamab在治疗复发或难治性LBCL中具有长期益处。
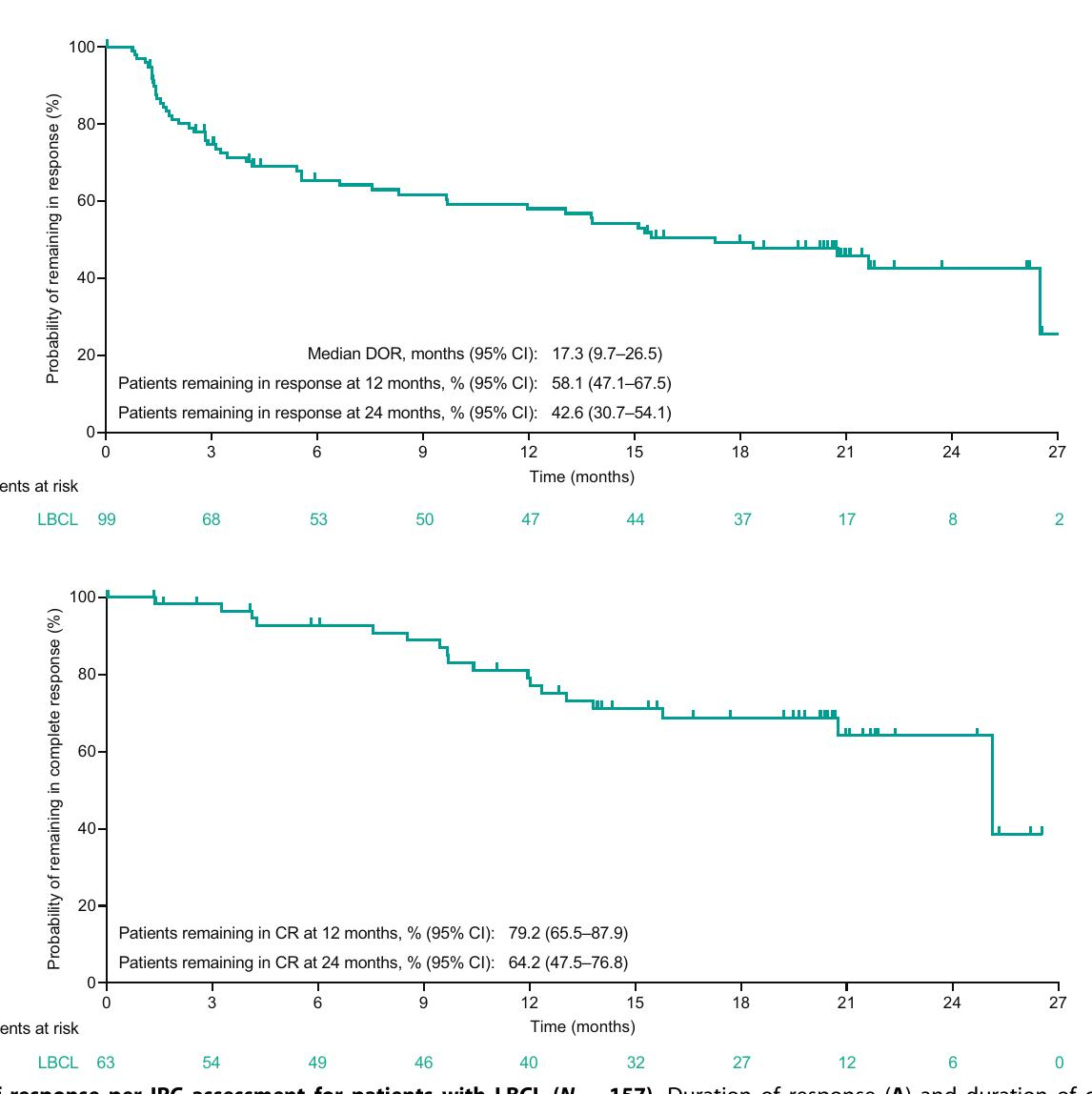
图9 - 缓解持续时间图
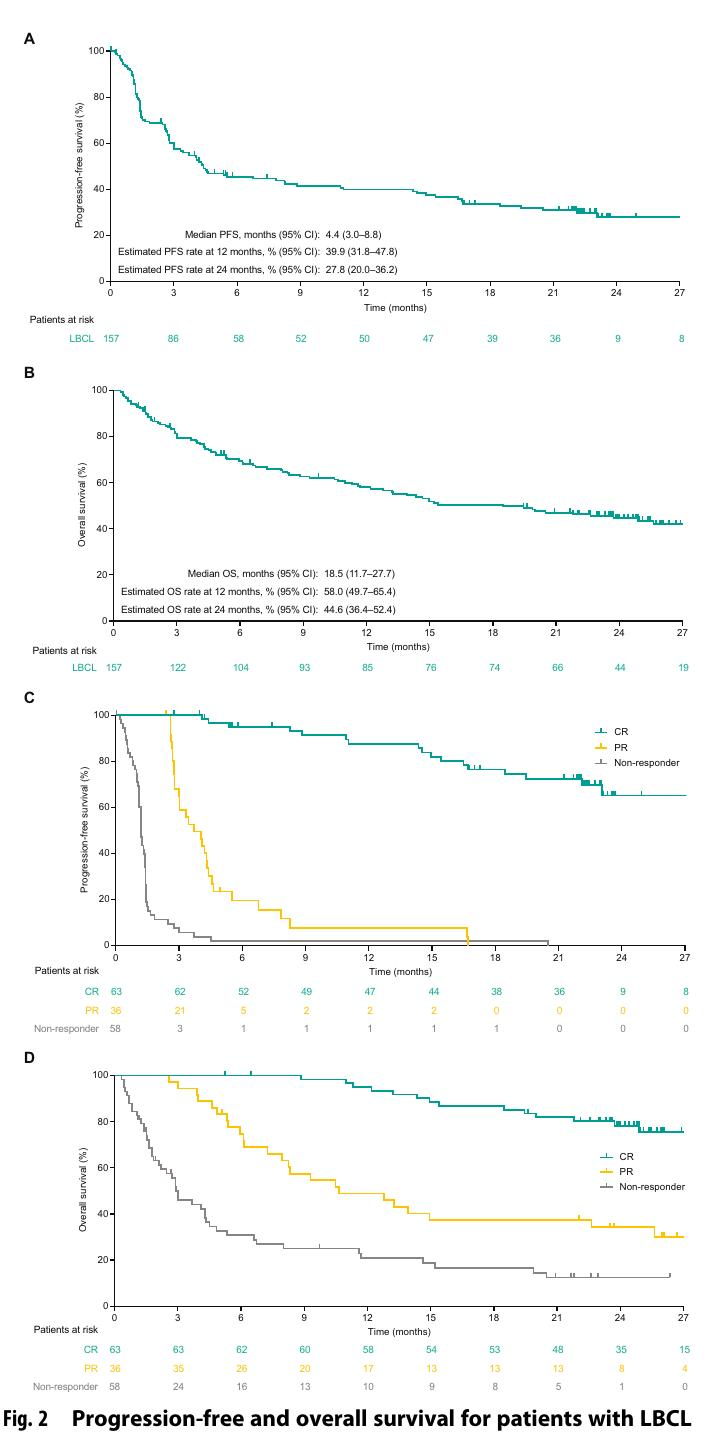
图10 - 无进展生存和总生存图
中位随访为25.1个月(95% CI:24.0-26.0)。CR完全缓解,DOR缓解持续时间,IRC独立审查委员会,LBCL大B细胞淋巴瘤,MRD最小残留病,OS总生存期,PD进展性疾病,PFS无进展生存期,PR部分反应,pts患者,SD稳定疾病。
表2 - 疗效终点总结
1. Mebrahtu A, Laurén I, Veerman R, Akpinar GG, Lord M, Kostakis A, Wells JA, Persson J, Persson H, Dönnes P, Dahllund L, Olsson A, Andersson O, Rockberg J, Mangsbo S. A bispecific CD40 agonistic antibody allowing for antibody-peptide conjugate formation to enable cancer-specific peptide delivery, resulting in improved T Cell proliferation and anti-tumor immunity in mice. Nat Commun. 2024;15(1):9542. doi:10.1038/s41467-024-53839-5
2. Wei X, Zhao L, Yang F, Yang Y, Zhang H, Du K, Tian X, Fan R, Si G, Wang K, Li Y, Wei Z, He M, Sui J. A CD25×TIGIT bispecific antibody induces antitumor activity through selective intratumoral Treg cell depletion. Mol Ther. 2024;32(11):4075-4094. doi:10.1016/j.ymthe.2024.09.0103. Jen WY, Jabbour E, Short NJ, et al. A phase 2 trial of mini hyper CVD, blinatumomab, and ponatinib in Philadelphia positive acute lymphoblastic leukemia. Am J Hematol. 2024;99:2229-2232. doi:10.1002/ajh.27463
4. Yi M, Li T, Niu M, Wu Y, Zhao B, Shen Z, Hu S, Zhang C, Zhang X, Zhang J, Yan Y, Zhou P, Chu Q, Dai Z, Wu K. Blockade of CCR5+ T cell accumulation in the tumor microenvironment optimizes anti-TGF-β/PD-L1 bispecific antibody. Adv Sci. 2024;11(38):2408598. doi:10.1002/advs.202408598
5. Thieblemont C, Karimi YH, Ghesquieres H, et al. Epcoritamab in relapsed/refractory large B-cell lymphoma: 2-year follow-up from the pivotal EPCORE NHL-1 trial. Leukemia. 2024;38:2653-2662. doi:10.1038/s41375-024-02410-8
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


