外周T细胞淋巴瘤(PTCL)是一种高度异质性的非霍奇金淋巴瘤(NHL),其多种亚型在发病机制、生物学行为、临床表现及预后方面存在显著差异。研究发现,几乎所有T细胞恶性肿瘤中都存在JAK-STAT通路的异常。戈利昔替尼是全球首个且唯一针对PTCL的高选择性JAK1抑制剂,具有出色的疗效及安全性。本文将通过上海交通大学医学院附属瑞金医院赵维莅教授团队的两例真实世界病例,探讨戈利昔替尼联合方案在复发/难治性(R/R)PTCL患者的实际疗效与安全性。
详情如下
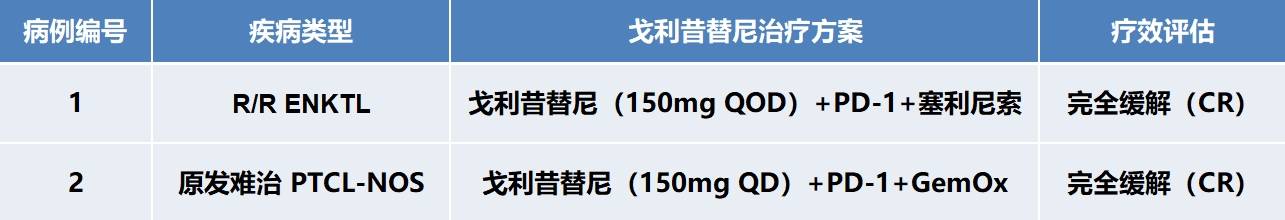
病例1:一例R/R ENKTL病例分享
病例简介
患者,男性,84岁,2023年3月出现鼻塞流涕,2024年初症状加重,就诊于外院,病理结果考虑为结外NK/T细胞淋巴瘤。为求进一步诊疗,该患者于2024年3月至上海交通大学医学院附属瑞金医院就诊。经过全面的病理和影像学检查,该患者最终被确诊为结外NK/T细胞淋巴瘤(AA IV期,PINK-E 2分),鼻腔、肌肉、皮肤、骨髓受累。
治疗概览
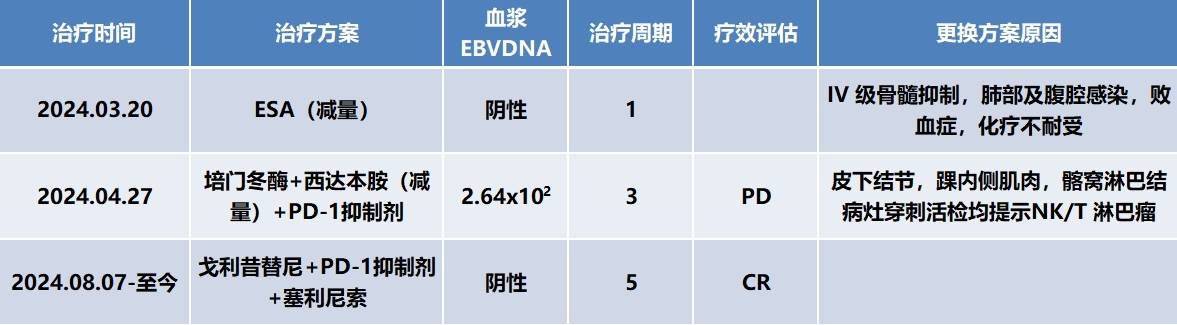
2024年6月26日,PET-CT显示:左侧小腿下段内侧肌间隙软组织结节,直径约1CM,代谢增高;右侧足底肌间隙低密度小结节,1.8×1.6CM,代谢增高。
2024年8月7日,更换治疗方案为戈利昔替尼+PD-1抑制剂+塞利尼索进行治疗。
2024年10月10日,PET/CT结果显示与之前相比,原高代谢结节消失或代谢降低,Deauville 评分:1分,脾脏大小正常,代谢分布均匀,骨髓腔内未见明显异常高代谢。原腿部皮下结节,皮损明显好转,疗效评估达到CR。
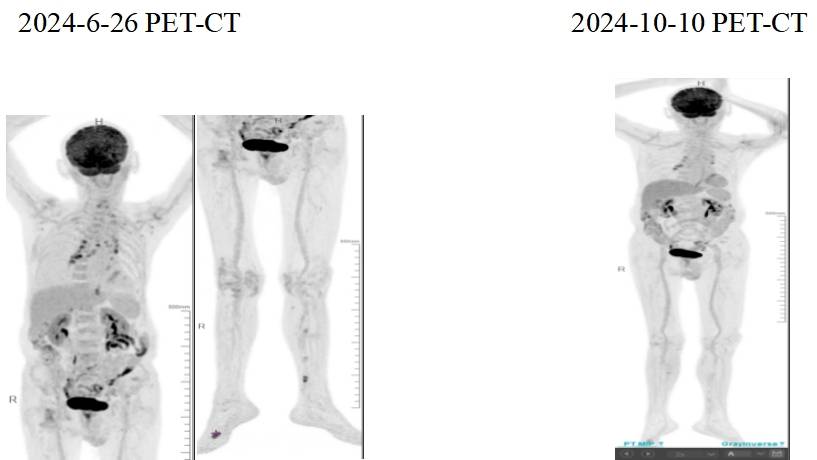
该患者在治疗期间出现2级骨髓抑制,积极对症支持治疗后可缓解,整体用药安全性良好,未出现严重不良反应,ECOG评分良好,精神状态佳,生活完全自理。
程澍教授用药体会分享
上海交通大学医学院附属瑞金医院血液科
中国抗癌协会淋巴瘤整合康复专业委员会常委
中国老年医学学会血液学分会淋巴瘤学组委员
中国女医师协会血液专业委员会委员
上海女医师协会血液分会秘书长
海峡两岸医药卫生交流协会血液学专委会委员
中国EBV相关疾病工作组成员
负责及主要参与国自然基金项目3项,主持上海市卫健委面上项目1项;以第一/通讯作者发表论文20余篇,SCI 论文10篇
ENKTL为高度侵袭性淋巴瘤,与EB病毒感染相关。一线治疗通常使用包含培门冬为基础的化疗方案1-2。晚期患者疾病进展迅速,治疗应答率低,容易出现耐药,预后不佳。本例为84岁高龄的晚期NK/T细胞淋巴瘤患者,伴有高血压等基础疾病,对常规治疗方案耐受性差,治疗选择受到极大限制。一线使用减量的ESA方案后出现IV度骨髓抑制及重症感染,经积极对症支持治疗后好转。换用西达本胺联合培门冬酶及PD-1单抗后,疾病进展,皮肤病灶有所增大,多处结外病变髌骨仍证实为淋巴瘤累及。基于患者高龄、体能状况差,既往治疗后出现重症感染,血浆EBVDNA水平有所升高等因素综合考虑,决定选择减量戈利昔替尼联合PD-1抑制剂及塞利尼索治疗。治疗3周期后,复查PET-CT结果显示原有高代谢病灶均消失,疗效评估达到CMR。整个治疗过程中,未发生药物相关的严重不良事件,患者未再出现活动性感染,耐受性良好,一般状况佳,可恢复正常生活状态。
由此可见,对于高龄、体能状况较差,无法耐受常规化疗的ENKTL患者,戈利昔替尼作为高选择性JAK1抑制剂联合免疫治疗及其他小分子靶向药物展示出显著的疗效和良好的安全性。未来,对于此类不耐受常规化疗的老年患者,戈利昔替尼联合免疫治疗可能成为一个有效且安全的治疗选择,值得在临床上进一步探索和应用。
病例2:一例R/R PTCL-NOS病例分享
病例简介
患者,女性,54 岁,该患者于2023年医美注射后出现左下颌、左眼睑、右眼睑反复肿胀。2024年3月感右上牙龈肿痛,行右上颌拔牙术后感右上颌肿物仍未消退。遂于2024年5月至当地医院取右上颌组织活检,病理结果提示考虑外周T细胞淋巴瘤(非特指型)。为进一步明确诊断与治疗,患者前来上海交通大学医学院附属瑞金医院就诊。经全面的病理和影像学检查,该患者最终被确诊为外周T细胞淋巴瘤(非特指型)(AA Ⅱ期,ECOG 0分,IPI 1分,TP53突变)。
治疗概览
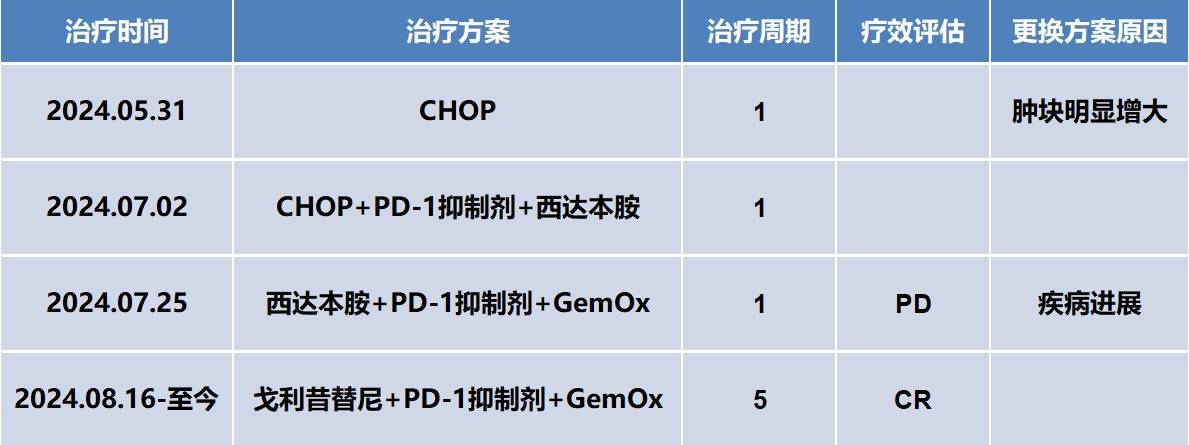
该患者此前接受多程化疗后,未获得缓解,右侧上颚新发肿物,口咽部肿块增大,并伴有发热,疾病持续进展。
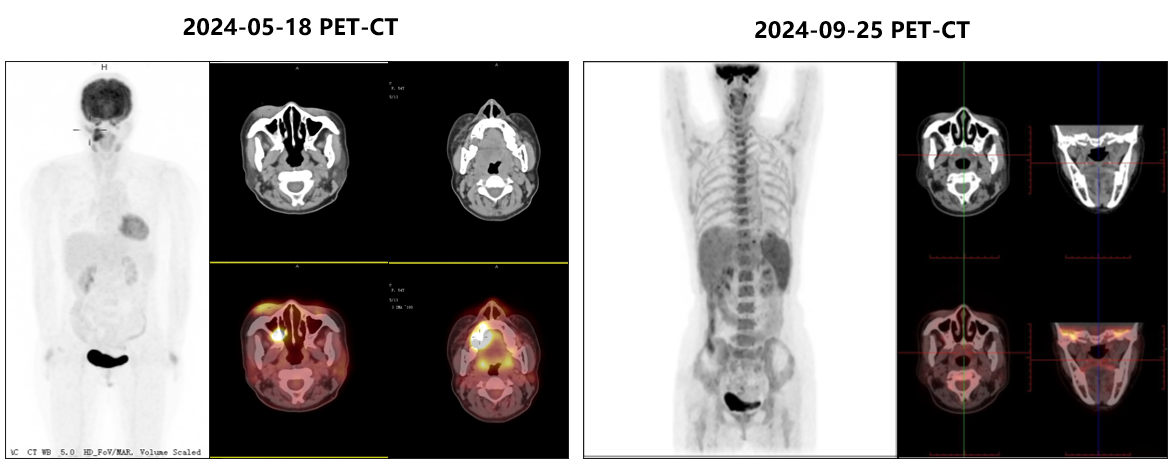
2024年8月开始更换治疗方案为戈利昔替尼+PD-1抑制剂+GemOx方案治疗。服药9天,右侧上颚肿物明显减小;服药24天,肿物持续消退;服药后45天,肿物基本消失;2024年09月25日,复查PET/CT结果回示,躯干及颅脑未见高代谢淋巴瘤累及瘤灶,Deauville评分:1分,疗效评估结果为CR。
安全性反馈:患者该方案治疗10天后出现III级血小板减少,未停药,给予特比澳升血小板治疗,一月后恢复正常。用药21天复查生化指标,丙氨酸氨基转移酶(60IU/L)和天门冬氨酸氨基转移酶(62IU/L)升高,出院带药甘草酸二铵肠溶胶囊,每日三次,每次两片使用。患者治疗期间,给予复发磺胺甲噁唑每天一片常规预防,目前情况较好,暂无异常。
许彭鹏教授用药体会分享
上海交通大学医学院附属瑞金医院血液科主任医师、医学博士、博士生导师
教育部青年长江学者、上海市青年东方英才
中华医学会血液学分会淋巴细胞疾病学组秘书
上海市抗癌协会淋巴瘤专业委员会青年委员会副主委
上海市医学会血液学分会青年委员会副主委
中国临床肿瘤学会抗白血病及抗淋巴瘤联盟青年委员
上海市血液内科临床质量控制中心秘书兼评审专家
上海市第八批援藏干部人才,曾任西藏自治区日喀则市人民医院血液科主任、中心实验室副主任
第一或通讯作者在《Cancer Cell》、《Lancet Haematology》、《Signal Transduction and Targeted Therapy》等发表论文
PTCL-NOS是PTCL中一种常见的亚型,约占30%~50%3。尽管以CHOP为基础的化疗方案仍是该病的“标准”治疗,但研究表明患者往往面临一线治疗效果不佳、反复复发及后续治疗选择有限等问题,其5年总生存(OS)率仅为20%~30%4。因此,亟需更有效的治疗方法来满足此类患者的治疗需求。
本例患者接受第一周期CHOP方案化疗半个月后疾病迅速进展,在原化疗方案基础上增加西达本胺和PD-1抑制剂治疗后,仍未缓解。二线更换化疗方案为西达本胺+PD-1抑制剂+GemOx,1疗程后疾病仍迅速进展,口咽部肿块迅速增长。考虑到该患者为原发难治性PTCL-NOS,疾病进展迅速,且对现有治疗方案不敏感,治疗难度极大。在三线治疗时,我们将原二线方案中的西达本胺替换为戈利昔替尼。令人惊喜的是,服用戈利昔替尼9天后,患者右侧上颚肿物肉眼可见持续缩小。40天后复查PET/CT:患者全身高代谢淋巴瘤病灶消退,颅脑及躯干未见病变累及,整体疗效达CR。在整个治疗过程中,患者曾出现III级血小板减少,给与支持治疗后恢复,未出现药物安全性相关剂量调整或停药。目前患者仍原方案治疗中,并定期随访。
该病例进一步验证了戈利昔替尼在PTCL-NOS患者中具有显著和持久的抗肿瘤活性,对于复发/难治性患者,戈利昔替尼联合化疗/免疫治疗或许可进一步提升疗效,且安全性可控。
赵维莅教授点评
上海交通大学医学院附属瑞金医院副院长
国家杰出青年科学基金获得者
教育部长江学者特聘教授
科技部万人计划领军人才
百千万人才工程国家级人选
上海市重中之重临床医学中心主任
上海血液学研究所所长
国家血液内科专业医疗质量控制中心(筹)共同主任
中华医学会血液学分会副主任委员
淋巴细胞疾病学组组长
中国病理生理学会理事、实验血液学专委会副主任委员
中国临床肿瘤协会抗淋巴瘤联盟副主席
致力于淋巴细胞恶性疾病的临床和基础研究,以通讯/第一作者在《The New England Journal of Medicine 》《CANCER CELL》、《NATURE GENETICS》、《BLOOD》《LANCET HAEMATOL》、《SIGNAL TRANSDUCT TARGET THER》、《J HEMATOL ONCOL》等国际权威杂志发表文章110余篇,总影响因子超过1600。相关成果以第一完成人获项,相关成果以第一完成人获国家科技进步奖创新团队奖1项,国家科学技术进步奖二等奖1项,省部级一等奖国家科技进步奖创新团队奖16项,获国家发明专利16项,主持国家科技部重点研发计划、863 重大项目、国家自然科学基金重点项目多项。先后荣获 “全国卫生系统先进工作者”、“全国三八红旗手”、中国青年女科学家奖、EBMT青年领袖奖、吴阶平医药创新奖、谈家桢生命科学奖、上海市科技精英等多项荣誉
目前,PTCL的治疗面临诸多困境,复发率高、预后差。据相关研究,在接受一线治疗的PTCL患者中,68%的患者会发展为复发难治,复发难治PTCL患者的中位OS仅5.8个月5-7。目前临床上还没有非常满意的治疗手段,尚不能满足PTCL的临床治疗需求。戈利昔替尼的上市为PTCL患者提供了新的治疗选择。作为我国自主研发的全球首个高选择性JAK1抑制剂,戈利昔替尼通过靶向抑制JAK/STAT信号通路异常激活,从根本上阻断了PTCL的病理进程。
JACKPOT8 B部分研究已充分证实了戈利昔替尼单药治疗R/R PTCL的优异疗效,ORR达到44.3%,CR率23.9%,且安全可控8。然而,R/R PTCL患者发病机制复杂,异质性强,预后差,因此真实世界临床使用时,以戈利昔替尼为基础的联合方案的探索极为必要。
关于JAK抑制剂与免疫检查点抑制剂联合的探索,此前已有多项研究对此进行佐证。今年6月发表在Science杂志的2项研究发现9-10,JAK/STAT通路在免疫介导的耐药机制中具有重要作用,阻断JAK/STAT信号通路,可降低肿瘤细胞表面T细胞抑制信号受体(TCIR)配体的表达(如PD-L1等),从而避免效应T细胞耗竭,持续发挥抗肿瘤作用,同时可增强PD-1抑制剂疗效或逆转PD-1抑制剂耐药。
结合我们团队的真实世界经验,以戈利昔替尼为基础的联合方案的治疗潜力在复杂临床场景中得到了充分验证。程澍主任和许彭鹏主任提供的两例病例展示了戈利昔替尼在复发难治性ENKTL和PTCL-NOS患者中的出色疗效,通过这两例病例我们更可以看到,戈利昔替尼联合化疗或免疫治疗具有充分的临床可行性,两例患者均实现了深度缓解,且安全可控。更令人欣喜的是,团队在实际使用过程中发现,戈利昔替尼不仅适用于这两类亚型患者,对于其他PTCL亚型患者同样表现出令人惊喜的疗效。例如,对于罕见难治性肠道T细胞淋巴瘤患者,以戈利昔替尼为基础的联合方案均表现出出色的疗效,显著缓解了临床治疗困境,成为PTCL治疗策略中的一大亮点。
此外,戈利昔替尼的Ⅲ期随机对照临床试验正在积极开展中,旨在进一步验证其疗效和安全性。期待未来更大样本量的研究数据发布,为其在不同PTCL亚型以及其他类型淋巴瘤中的应用提供更强有力的循证医学支持。这不仅将推动PTCL治疗领域的变革,也将为更多患者带来生存的希望与生活质量的提升。
1. He X, Gao Y, Li Z, Huang H. Review on natural killer/T-cell lymphoma. Hematol Oncol. 2023;41(2):221-229.
2. Reneau JC, Shindiapina P, Braunstein Z, Youssef Y, Ruiz M, Farid S, Hanel W, Brammer JE. Extranodal Natural Killer/T-Cell Lymphomas: Current Approaches and Future Directions. J Clin Med. 2022 May 10;11(10):2699.
3. Lone W, Alkhiniji A, Manikkam Umakanthan J, Iqbal J. Molecular Insights Into Pathogenesis of Peripheral T Cell Lymphoma: a Review. Curr Hematol Malig Rep. 2018;13(4):318-328.
4. Savage KJ, Ferreri AJ, Zinzani PL, Pileri SA. Peripheral T-cell lymphoma--not otherwise specified. Crit Rev Oncol Hematol. 2011;79(3):321-329.
5. Lansigan F, Horwitz SM, Pinter-Brown LC, et al. Outcomes for Relapsed and Refractory Peripheral T-Cell Lymphoma Patients after Front-Line Therapy from the COMPLETE Registry. Acta Haematol. 2020;143(1):40-50.
6. Biasoli I, Cesaretti M, Bellei M, et al. Dismal outcome of T-cell lymphoma patients failing first-line treatment: results of a population-based study from the Modena Cancer Registry. Hematol Oncol. 2015;33(3):147-151.
7. Lansigan F, Horwitz SM, Pinter-Brown LC, et al. Outcomes for Relapsed and Refractory Peripheral T-Cell Lymphoma Patients after Front-Line Therapy from the COMPLETE Registry. Acta Haematol. 2020;143(1):40-50.
8. KIM W, CAI Q, SONG Y, et al. Golidocitinib in treating reactory or relapsed peripheral T-cell lymphoma: primary analysis of the multinational pivotal study results (JACKPOT8) [J]. Hematol Oncol, 2023, 41(S2): 79-80.
9. Zak J, Pratumchai I, Marro BS, et al. JAK inhibition enhances checkpoint blockade immunotherapy in patients with Hodgkin lymphoma. Science. 2024;384(6702):eade8520.
10. Mathew D, Marmarelis ME, Foley C, et al. Combined JAK inhibition and PD-1 immunotherapy for non-small cell lung cancer patients. Science. 2024;384(6702):eadf1329.
* 随访至2024年2月22日,data on file
责任编辑:肿瘤资讯-Kaylee
排版编辑:TanRongbing











 苏公网安备32059002004080号
苏公网安备32059002004080号


