EGFR外显子20插入(Exon 20ins)突变具有异质性,插入位点可能影响药物和ATP结合,降低了突变患者对EGFR TKIs治疗的敏感度。现有的TKIs常不能使EGFR Exon 20ins晚期NSCLC患者获益;一二代TKIs治疗后,患者无进展生存较短,客观缓解率不高。面对上述困境,亟待新疗法来打破僵局。随着药物研发日新月异,给EGFR Exon 20ins突变NSCLC患者带来了希望。抗体类药物脱颖而出,如双特异性抗体amivantamab等;TKIs经典药物在阵痛中不断迭代,新型TKIs层出不穷,呈现出诸多亮点。我们盘点了2022年抗体类和EGFR TKIs相关重点药物在EGFR Exon 20ins领域的新进展,并诚邀吉林省肿瘤医院程颖教授对这些研究新进展进行点评。
一级教授,国家临床重点专科学科带头人
博士研究生导师,博士后工作站导师
享受国务院特殊津贴,卫生部突出贡献中青年专家
吉林省癌症中心主任
吉林省肿瘤医院恶性肿瘤临床研究一体化诊疗中心主任
吉林省肺癌诊疗中心主任
中国临床肿瘤学会(CSCO) 副理事长
CSCO小细胞肺癌专业委员会主任委员
CSCO临床研究专家委员会候任主任委员
中国抗癌协会肺癌专业委员会候任主任委员
CSCO非小细胞肺癌专业委员会副主任委员
CSCO肿瘤大数据专家委员会副主任委员
中华医学会肿瘤学分会肺癌专委会副主任委员
中国医师协会肿瘤多学科诊疗专委会副主任委员
中国医师协会肺癌培训专业委员会副主任委员
国家卫生、计生委常见肿瘤规范化诊疗专家组成员
吉林省医师协会肿瘤医师分会主任委员
吉林省医学会肿瘤专业委员会主任委员
从0到1 创新突破:抗体类药物
【Amivantamab的CHRYSALIS研究亮点频现】
EGFR/c-MET在肺癌领域是经验证的成药靶点。amivantamab(JNJ-372)是一款全人源靶向EGFR/MET双特异性抗体,通过与肿瘤细胞表面EGFR、c-Met受体结合,阻断EGFR、c-Met 信号通路的活化,促进EGFR、c-Met受体降解,并通过Fc 段介导的抗体依赖的细胞介导的细胞毒性作用(ADCC)、抗体依赖的细胞介导的吞噬作用(ADCP)以及胞啃作用杀伤肿瘤细胞。(图1)美国FDA 2021年5月21日基于CHRYSALIS研究结果,加速批准amivantamab上市,该药成为全球首款治疗EGFR Exon 20ins突变NSCLC双抗类药物。此前,Ⅰ/Ⅱ期CHRYSALIS研究Cohort D数据表明[1],amivantamab对经含铂类化疗后进展患者,中位总生存期(mOS)达22.8个月,客观缓解率(ORR)达40%,中位无进展生存期(mPFS)为8.3个月,中位缓解持续时间(mDOR)为11.1个月。治疗相关不良事件(TRAE)主要为1~2级,≥3级TRAE发生率为16%。(表1)
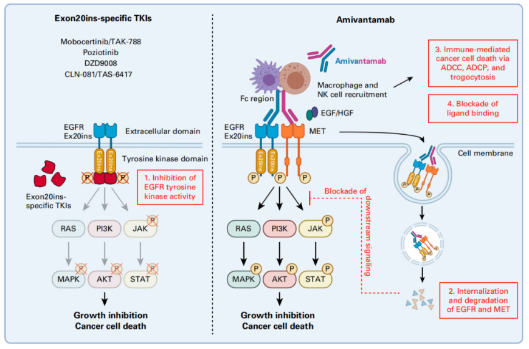 图1 Amivantamab作用机制
图1 Amivantamab作用机制
表1 Amivantamab单药CHRYSALIS研究Cohort D疗效数据
Amivantamab单药治疗使部分缓解(PR)或疾病稳定(SD)的晚期患者获益
2022ELCC大会(Girard N等,19P)[2]公布,截至2021年3月30日,amivantamab治疗的114例含铂化疗后进展患者,出现进展的仅12例,PR+为42(39%)例,SD为52(49%)例。死亡风险分别下降79%(PR+ vs PD)和67%(SD vs PD)。(表2、图2)无论治疗反应深度如何,amivantamab均可有效控制疾病。2022WCLC大会(EP08.02-163)上公布的美国MD安德森癌症中心[3]数据也支持该药对突变患者有着强大的抗癌活性和治疗潜力。
表2 Amivantamab单药治疗使PR或SD的晚期患者疗效数据
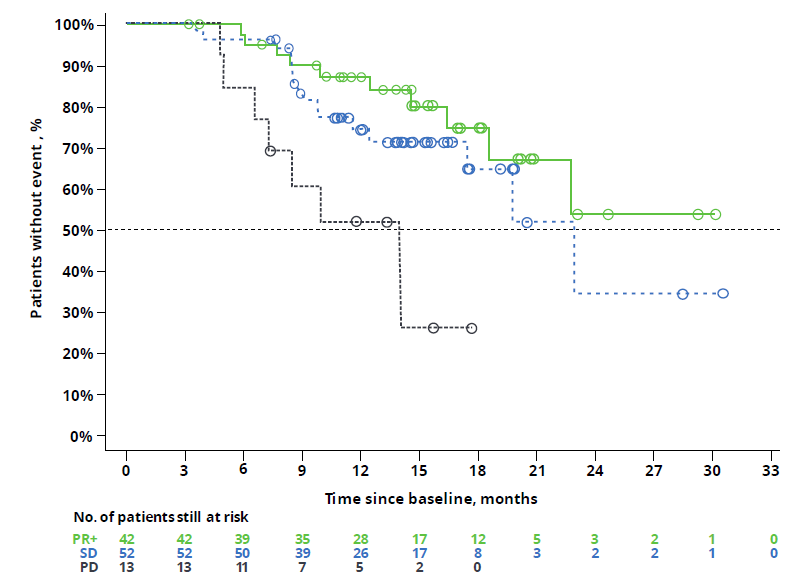
图2 PR或SD的晚期患者获益的生存曲线
Amivantamab单药治疗可控制有/无脑转移突变患者疾病进展
2022ELCC大会(J. Trigo 等,20P)[4]公布,上述114例经含铂化疗后进展患者,无论基线是否有脑转移,ORR分别可达45%(17/38)和42%(32/76)。仅17例(15%)患者出现颅内进展,其中13例(11.4%)单发脑转移。对脑转移患者继续采用amivantamab+立体定向放疗,显示出初步疗效且对患者可耐受。(图3、表3)
 图3 研究者第一次评估发生进展的部位
图3 研究者第一次评估发生进展的部位
表3 Amivantamab单药对基线有/无脑转移患者的疗效比较
亚洲人群中疗效和安全性与全球数据一致
2022JCLS大会(Goto等)[5]公布,amivantamab治疗53例经含铂化疗进展后的亚洲患者,ORR可达41%(95%CI 25%~58%),mPFS达9.7个月(95%CI 5.5%~14.0%)。(表4)TRAEs主要为1~2级(≥3级,13%),与治疗相关腹泻发生率为6%(≥3级,2%),导致治疗终止的TRAEs发生率仅为6%。(表5)
表4 亚洲患者亚组经治后疗效数据(中位随访9.7个月) 表5 亚组患者经治后不良反应数据
表5 亚组患者经治后不良反应数据
真实世界研究力挺突变患者生存获益
2022ESMO大会(T.M. Kim等,1109P)[6]公布了amivantamab对比日本经含铂化疗进展后患者真实世界研究方案结果。amivantamab组(全部患者、亚洲患者)OS、PFS、至后线治疗时间(TTNT)更长,ORR优势更为明显。在全部患者中,amivantamab组与外部对照(EC)组ORR为41.7% vs 14.1%(P<0.001);mPFS为6.7 vs 4.7个月(HR= 0.59);mOS为19.9 vs 14.1个月(HR= 0.59);mTTNT为12.2 vs 5.1个月(HR= 0.39)。分析亚洲患者亚组的数据发现,amivantamab组同样具有临床优势。大会(M. Okahisa等,1115P)[7]同期发布的对比日本经铂类治疗后患者真实世界研究方案数据,相比多西他赛(DOC)、TKI、免疫治疗(IO)等现有二线治疗手段,amivantamab治疗后ORR均显著优于EC组,PFS和OS疗效也得到提升。(表6、图4~6)
表6 Amivantamab对比DOC/TKI/IO治疗患者的ORR
 图4 Amivantamab与DOC治疗患者的OS(A)和PFS(B)对比
图4 Amivantamab与DOC治疗患者的OS(A)和PFS(B)对比

图5 Amivantamab与TKI治疗患者的OS(A)和PFS(B)对比

图6 Amivantamab与IO治疗患者的OS(A)和PFS(B)对比
迭代升级 蓄势而为:EGFR TKIs类药物
【Mobocertinib的EXLAIM队列在诸多研究中突围】
Mobocertinib(TAK-788)为口服EGFR Exon 20ins突变EGFR TKI。美国FDA 2021年9月16日批准该药用于NSCLC EGFR Exon 20ins突变经含铂类化疗进展后患者,无论以前是否接受过PD-1/PD-L1抗体免疫治疗。开放标签、非随机临床试验NCT02716116研究,由剂量递增、剂量扩展队列及单臂扩展队列(EXLAIM)3部分组成。114例经铂类治疗(PPP)队列,从剂量递增(n=6)、剂量扩展(n=22)和EXCLAIM(n=86)接受mobocertinib 160 mg qd。
安全性整体可控,TRAEs中腹泻或许是最大困扰
2022ESMO大会(S.S. Ramalingam等,988P)[8]公布了NCT02716116更新数据。疗效方面,截至2021年11月1日,PPP 队列(n=114例)中,cORR为28%,mDOR为15.8个月。mPFS为7.3个月(IRC),mOS为20.2个月。EXCLAIM扩展队列中(n=96)中,ORR为25%,1例CR;DCR为76%;中位DoR未达到。(表7)安全性方面,常见的TRAEs是腹泻(92%)、皮疹(46%)、甲沟炎(38%)、食欲下降(37%)、恶心(34%)、呕吐(32%)和皮肤干燥(31%)。在≥10%的患者中观察到的≥3级TRAE是腹泻(23%)。(表8、图7)
表7 Mobocertinib在PPP队列中的疗效数据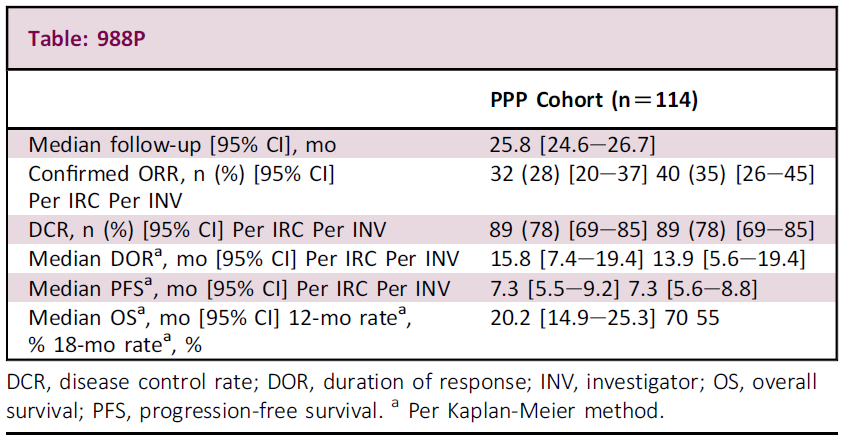
表8 Mobocertinib在PPP队列中总体不良反应情况(n=114)

图7 Mobocertinib在PPP队列中总体不良反应情况(n=114)
有限的颅内活性
2022ASCO大会(Pasi A. Janne等,Abs 9099)[9]公布了mobocertinib颅内活性情况。PPP队列(n=64)在接受160mg qd治疗后,21例(33%,21/64)首发疾病累及的部位是大脑,11例(17%,11/64)首发仅在大脑。43例患者第一个出现PD的部位不涉及大脑,其中28例(65%)继续使用mobocertinib治疗,4例(9%)至少持续6个月。考虑到脑中首次PD的频率较高(25%),mobocertinib在脑转移突变患者中的颅内活性有限。
真实世界研究显示为突变患者带来临床获益
2022ELCC大会(P. Christopoulos等,36P)[10]公布,114例经含铂类化疗进展后患者接受多种疗法,其中mobocertinib治疗相较真实世界方案在二线或后线治疗中有一定疗效, cORR为 35% vs 0%,mPFS为7.3 vs 2.5个月,mOS为24.0 vs 9.8个月。(表9)
表9 Mobocertinib真实世界研究数据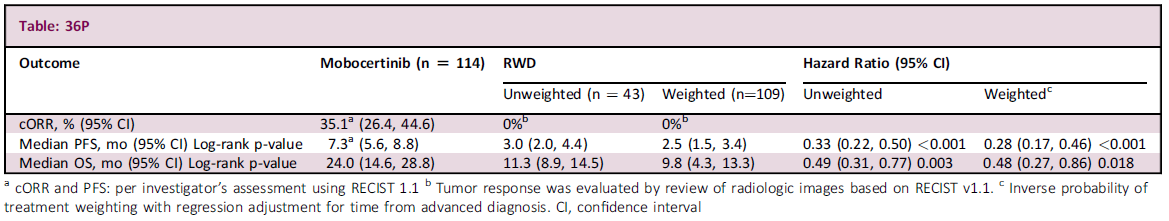
2022ESMO大会(V.H.F. Lee等,1111P)公布的EAP项目数据[11],在556例铂类化疗进展后患者中,287例(51.6%)接受过≥2 次 mobocertinib 治疗,预计中位至停药时间(TTD) 延长11个月(8.9~12.6个月),表明该药有临床获益(即缓解或疾病稳定)。
【CLN-081的剂量递增队列试验数据公布】
CLN-081(TAS6417或TPC-064)为不可逆的、广谱EGFR TKI,除了可用于EGFR Exon 20ins外,还可以适用于EGFR Exon18ins、21ins 等少见突变。美国FDA 2022年1月4日授予“突破性疗法”认定,用于治疗既往接受过铂类化疗后、且具有EGFR Exon 20ins突变的局部晚期或转移性NSCLC患者。2022ASCO大会( Helena Alexandra Yu等,9007P)[12]公布CLN-081剂量递增队列疗效数据,特别在100 mg bid剂量下表现出良好的临床表现。
疗效方面,截至2021年12月13日, 73例患者采用不同剂量(≤65mg,100mg,150mg)中,PR为28例(38.4%),SD 为42例(57.5%),PD为3例(4.1%),mDoR超10个月,mPFS为10个月。其中,39例100 mg bid时的PR为41.0%(16/39),DCR为97.4%(38/39),1例患者PD;mDoR超21个月,mPFS为12个月。(表10)
表10 CLN-081剂量递增队列疗效数据
安全性方面,出现较多的TRAEs(≥15%)为皮疹(74%)、腹泻(27%)、甲沟炎(25%)、疲劳(19%)、贫血(18%)、皮肤干燥(18%)和恶心(16%)。出现较多的≥3级TRAEs(≥4%)为贫血(10%)、ALT升高(4%)。(NCT04036682)
【Poziotinib研究之路道阻且长】
Poziotinib(HM781)为新型口服EGFR/HER2 exon 20ins突变EGFR TKI,适用于第一代EGFR TKI耐药且T790M/MET阴性的EGFR exon 20ins突变NSCLC晚期患者。
整体疗效尚好,3级以上不良反应较高
2022AACR大会(Xiuning Le等,Abs CT081)[13]公布了ZENITH20-1研究数据。疗效方面,115例突变患者口服16 mg/d,其中75例(65%)瘤体缩小。poziotinib虽能使65%患者肿瘤体积减小,但减少程度不够明显——有20%(7例)患者可达到疾病部分缓解(PR)。从亚组分析结果来看,先前未接受过EGFR TKIs治疗、无脑转移、体力状况良好的患者,ORR要好一些。如,脑转移患者ORR为8.3%,无脑转移患者ORR为15.5%。
安全性方面,以3级居多:皮疹(28%),腹泻(25%),口腔炎(9%)和甲沟炎(6%),4级有腹泻和皮炎各1例,无5级不良反应。整体上不良事件发生较多,也较严重——88%的患者暂停,68%减量,10%永久停药。针对其AE,研究者将进一步优化给药方式与剂量,最大程度减轻毒副作用。
抗肿瘤效应受插入位置影响
2022年,Yasir Y. Elamin等[14] Cancer Cell上公布的结果(NCT03066206)显示,poziotinib治疗50例突变肺癌患者,ORRs可达到 32%,mPFS也延长到5.5个月。研究人员还发现患者对poziotinib的敏感性依赖于插入的位点,即“近环端插入突变”比“远环端插入突变”更加敏感,ORRs分别为46%和0%(P=0.0015)。poziotinib在EGFR Exon20ins突变NSCLC患者中具有活性,但该活性受到插入位置的影响。(图8)

图8 插入位点的不同对疗效的影响
【DZD9008的WU-KONG系列研究成果颇丰】
DZD9008(舒沃替尼)为国产口服EFGR TKI。舒沃替尼正在进行多项临床研究,包括在全球多个国家和地区进行的Ⅱ期多中心注册研究WU-KONG1(NCT03974022)part B和在中国进行的Ⅱ期多中心注册研究WU-KONG6(CTR20211009),以进一步评估该药对EGFR Exon 20ins突变晚期NSCLC患者的疗效和安全性。(图9)
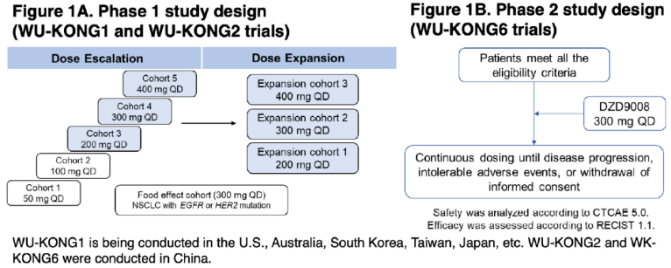 图9 舒沃替尼研究设计路线
图9 舒沃替尼研究设计路线
对基线有脑转移突变患者有一定抗肿瘤活性
2022年,Cancer Discov上Mengzhao Wang等[15]报告了WU-KONG1(NCT03974022)part A研究和中国多中心WU-KONG2(CTR20192097)研究结果,其中56例为EGFR Exon 20ins突变晚期患者(56/109)。疗效方面,在剂量≥100mg时,显示出对EGFR Exon 20ins各种突变亚型患者有效,对基线脑转移患者有一定抗肿瘤活性。研究推荐剂量300mg剂量组,脑转移患者ORR为48.4%,DCR为90.3%。2022 WCLC大会上更新了舒沃替尼三项I/II期多中心研究(WU-KONG1、WU-KONG2和WU-KONG6)的汇总分析。截至2022年4月30日,共纳入119例既往经铂类化疗失败的、EGFR Exon 20ins突变晚期NSCLC患者,300mg情况下ORR可达52.4%。(表11)安全性方面,最常见的TEAEs为腹泻和皮疹,可能与EGFR抑制有关。TRAEs大多为CTCAE 1级或2级。
表11 舒沃替尼不同剂量下疗效数据(截至2022年4月30日)
300 mg剂量下ORR表现亮眼
2022ESMO(M. Wang等,987P)公布了中国注册、多中心Ⅱ期WU-KONG6(CTR20211009)研究的初步结果[16]。疗效方面,截至2022年7月31日,97例既往含铂化疗后进展的晚期突变型患者,300 mg剂量条件下cORR为59.8%(58/97);基线有脑转移的患者中,cORR为48.4%(16/33)。在EGFR Exon 20ins 30种突变亚型中均有效。(图10~11)
 图10 插入位点的不同对疗效的影响
图10 插入位点的不同对疗效的影响
 图11 脑转移患者治疗前后影像学变化
图11 脑转移患者治疗前后影像学变化
安全性方面,根据正在进行的 WU-KONG1 和 WU-KONG2 研究及合并WU-KONG6的数据。在277例患者中,导致永久停药的TRAEs为6.1%。约19.5%的患者因不良反应需要减少剂量。≥3级TRAEs,血肌酸磷酸激酶升高是最常见的原因(11.2%),其次是腹泻(6.1%)。(表12~13)
表12 出现较多的≥3级TRAEs
表13 舒沃替尼TRAEs 汇总分析
回顾2022年的肺癌新药研究,NSCLC罕见靶点的研究可谓是最为耀眼的领域之一,各个罕见靶点的新药研究热度不减,呈现百花齐放的景象,使晚期NSCLC的治疗格局更加精准和全面。EGFR Exon 20ins作为最为常见的罕见突变靶点,一直是近几年新药研发的热点方向,在2022年取得的成绩也是可圈可点,除了已经获批上市的双特异性抗体amivantamab和小分子TKI药物mobocertinib的更新数据进一步夯实了在EGFR Exon 20ins患者中的治疗地位以外,舒沃替尼、CLN-081等小分子TKI类药物也有非常令人亮眼的表现,成为EGFR Exon 20ins新药研究领域的希望之星。
新药治疗地位进一步夯实
对比目前已经上市的两个药物amivantamab和mobocertinib,两者具有不同的作用机制和给药方式,均已在含铂化疗失败、EGFR Exon 20ins患者中取得了初步疗效。2022年两个药物更新的数据也给我们带来了更多的启示。
首先,在脑转移病灶控制方面,2022ELCC公布了CHRYSALIS研究中晚期NSCLC患者中amivantamab治疗的进展模式,基线有/无脑转移患者的ORR相当,分别为45%和42%。仅17例(15%)患者治疗后出现颅内进展,其中13例(11.4%)为单发脑转移,研究还发现对脑转移患者继续采用amivantamab+立体定向放疗是可行且易耐受的,这一结果也证实了amivantamab具有较好的颅内活性。相比之下,mobocertinib的颅内活性较为有限。2022ASCO大会上更新的结果显示,在PPP队列接受160 mg qd治疗的64例患者中,21例(33%)的首发疾病累及部位是大脑,11例(17%)首发仅在大脑,上述结果也为存在脑转移患者的临床决策提供了一定参考依据。
其次,用药的安全性也是临床医生非常关注的问题。Amivantamab为靶向EGFR和MET的双抗,为静脉注射给药,其主要的不良反应以皮疹(86%)和甲沟炎(42%)为主,此外输液反应是需要特别关注的TRAE,发生率为67%,主要在用药的第1周期发生,但绝大多数为1~2级,极少影响后续治疗,所以用药前的预处理非常重要。Mobocertinib虽然为小分子TKI,但其不良反应也不容忽视。在2022ESMO大会更新的2年多随访数据中,整体安全性是可控的,但腹泻发生率较高,达到92%,且≥3级腹泻达到23%,需要临床应用时格外注意、及时处理。为了进一步评估药物的疗效及安全性,有研究者使用非锚定匹配调整间接比较(MAIC)分析方法对比了mobocertinib(EXCLAIM研究)和amivantamab( CHRYSALIS研究)的疗效。研究结果分别于2022ASCO及ISPOR大会上公布结果。ASCO大会公布的结果显示,mobocertinib和amivantamab似乎具有总体相似的疗效。而在安全性方面,2022ISPOR大会公布的数据发现,虽然两药在任何级别的TRAE方面发生率相似,但是amivantamab在导致剂量减少的TRAE、≥3级TEAE、≥3级TRAE和SAE的风险显著低于mobocertinib,在临床如何为患者选择合适的方案还值得进一步探索。
最后,在目前公布的针对于amivantamab和mobocertinib研究设计中,均采用多队列设计,缺乏与现有临床治疗策略之间的比较。源于真实世界数据的“外部对照”能够帮助人们进一步评估新药和现有治疗策略的优劣。从2022年ESMO披露的日本数据来看,与真实世界治疗方案相比,amivantamab的获益明显, ORR较对照组提高了近3倍(41.7% vs 14.1%)。欧洲人群[17-19]的真实世界数据也展现出了良好的抗肿瘤活性,在生存获益方面,与接受外部对照治疗患者相比,接受amivantamab治疗的患者OS和PFS更长。安全性方面,amivantamab的TRAEs多为1~2级,耐受性良好。mobocertinib的真实世界数据也证实了该药的疗效,患者用药≥2个疗程后,中位至停药时间(TTD)可延长11个月左右,获益较为明显。因此,这些真实世界研究数据助推了EGFR Exon 20ins突变型NSCLC研究驶入“快车道”,为患者治疗带来了新的希望。
药物研发多点开花
除了amivantamab和mobocertinib以外,CLN-081、舒沃替尼、poziotinib等药物也在EGFR Exon 20ins患者中展现了强劲的抗肿瘤活性。CLN-081治疗既往经治疗的、携带EGFR Exon 20ins突变晚期NSCLC患者的ORR为38.4%,mPFS为10个月,于2022年初获得了FDA授予的突破性疗法认定。舒沃替尼作为我国自主研发的高选择型TKI,在首个中国注册研究WU-KONG6中,患者的ORR高达59.8%,对于基线伴脑转移的患者,ORR达48.4%,成为肺癌领域首个且唯一获得中、美双“突破性疗法认定”的国创新药。
另外一个国产药物伏美替尼在EGFR Exon 20ins人群中开展的FAVOUR研究数据显示,一线治疗的ORR为60%, DCR为100%,该药也在 2022年4 月获得了CDE的“突破性疗法”,用于 EGFR Exon 20ins突变阳性、含铂化疗期间或化疗后进展的局部晚期或转移性NSCLC成人患者的治疗。
目前,全球药企在Exon 20ins突变领域纷纷布局,相关新药如雨后春笋,如MCLA-129(NCT04868877,NCT04930432)、EMB-01(NCT05498389,NCT03797391)、GB263T(NCT05332574)、BLU-451(NCT05241873 )、ORIC-114(NCT05315700)、AP-L1898(NCT04993391)均已进入临床试验阶段。主要包括两大类:(1)抗体类药物:如,MCLA-129和EMB-01均为EGFR/c-MET双特异性抗体。GB263T为EGFR/c-MET/c-MET三特异性抗体,可诱导NSCLC细胞系受体内化和EGFR/c-MET磷酸化,药效呈剂量依赖性。(2)新型口服EGFR TKIs:如BLU-451、ORIC-114、AP-L1898,这些药物各有特点,AP-L1898属于奥希替尼的结构类似物。2022AACR会议中BLU-451和ORIC-114报道的临床前研究结果均表现出了较好大脑渗透性活性,值得进一步探索。
精准检测助力临床药物选择
EGFR Exon 20ins插入形式多样繁杂,导致检出难度加大,临床精准检测仍存在问题。目前已经公布结果的新药临床研究已经发现不同突变位点疗效不同,如amivantamab对于“近环端插入突变”和“远环端插入突变”的ORR差距较大(41% vs 25%),舒沃替尼对于“近环端插入突变”ORR达62%,“远环端插入突变”ORR达50%,提示未来在临床应用中需要考虑患者的突变亚型。
此外,伴随突变的问题在临床上也非常常见,有研究发现EGFR Exon20ins多伴有抑癌基因如TP53的失活或其他旁路基因激活等复合突变,其中以TP53最为常见,发生率高达43.6%~65%。2022ESMO大会[20]报告了159例EGFR Exon 20ins真实世界的数据,TP53阳性和阴性患者的中位OS分别为12.0 vs 20.0个月(P=0.092),在同时发生TP53突变的患者中,与未接受免疫检查点抑制剂的患者相比,接受免疫检查点抑制剂患者的OS更长(16 vs 8个月,P=0.048)。对于这类患者的治疗策略,是采用联合化疗/抗血管生成治疗/免疫治疗等药物,还是开发新的、疗效更优的药物,仍是未来不断探索的方向。
总而言之,道路是曲折的,前途是光明的。新型靶向药物已经为EGFR Exon 20ins患者带来治疗的曙光,但今后谁能更胜一筹,还需要更多研究加以论证,相信EGFR Exon 20ins突变NSCLC患者的精准治疗时代将指日可待,也期待能有更多、更好的中国人群数据结果出炉,尽早推动此类药物在中国落地。
[1] Joshua K, et al. Amivantamab in Post-platinum EGFR Exon 20 Insertion Mutant Non-small Cell Lung Cancer . WCLC 2020, Abs OA04.04
[2] N. Girard, et al. Stable disease (SD) on amivantamab in post-platinum epidermal growth factor receptor (EGFR) exon 20 insertion (Exon20ins) mutated non-small cell lung cancer (NSCLC): A response-based analysis. ELCC 2022, Abs 19P
[3] X. Le, et al. Real-World Case Series on Efficacy and Safety of Amivantamab for EGFR-mutant Non-small Cell Lung Cancer. WCLC 2022, EP08.02-163
[4] J. Trigo, et al. Risk and management of intracranial progression on amivantamab in epidermal growth factor receptor (EGFR) exon 20 insertion (ex20ins)-mutated non-small cell lung cancer (NSCLC). ELCC 2022, Abs 20P
[5] Goto, et al. JCLS 2022. Oral presentation
[6] T.M. Kim, et al. Amivantamab vs real-world (RW) therapy in Japanese patients with advanced non-small cell lung cancer (aNSCLC) epidermal growth factor receptor (EGFR) exon-20 insertion mutation (E20i).ESMO 2022, Abs 1109P
[7] M. Okah, et al. Amivantamab vs real-world (RW) therapies for advanced non-small cell lung cancer (aNSCLC) with epidermal growth factor receptor (EGFR) exon 20 insertion mutation (E20i) in Japan. ESMO 2022.ESMO 2022, Abs 1115P
[8] S.S. Rama, et al. Phase I/II study of mobocertinib in EGFR exon 20 insertion (ex20ins) + metastatic NSCLC (mNSCLC): Updated results from platinum-pretreated patients (PPP). ESMO 2022, Abs 988P
[9] Pasi A. Janne, et al. Mobocertinib (TAK-788) in EGFR exon 20 insertion (ex20ins)+ metastatic non–small cell lung cancer (mNSCLC): Treatment (tx) beyond progressive disease (PD) in platinum-pretreated patients (pts) with and without intracranial PD.ASCO 2022, 9099
[10] P. Christopoulos, et al. Indirect comparison of mobocertinib trial data vs real-world data in patients with EGFR exon 20 insertion (ex20ins)+ nonsmall cell lung cancer (NSCLC) ELCC 2022, Abs 36P
[11] V.H.F. Lee, et al. Real-world treatment duration in patients with non-small cell lung cancer (NSCLC) with EGFR exon 20 insertion (EGFRex20ins) mutations receiving mobocertinib through the global Expanded Access Program (EAP). ESMO 2022, Abs 1111P
[12] Helena Alexandra Yu, et al. Phase (Ph) 1/2a study of CLN-081 in patients (pts) with NSCLC with EGFR exon 20 insertion mutations (Ins20). ASCO 2022, 9099
[13]Xiuning Le, et al. Brain metastases (BM) and next-generation sequencing (NGS) timing: Real-world (RW) outcomes for patients (pts) with advanced non-small cell lung cancer (aNSCLC) and MET exon 14 skipping mutations (METex14). AACR 2022, Abstract 4118
[14] Yasir Y. Elamin, et al. Poziotinib for EGFR exon 20-mutant NSCLC: Clinical efficacy, resistance mechanisms, and impact of insertion location on drug sensitivity. Cancer Cell. 2022 Jul 11;40(7):754-767.e6.
[15] Mengzhao Wang, et al. Sunvozertinib, a selective EGFR inhibitor for previously treated non-small cell lung cancer with EGFR exon 20 insertion mutations. Cancer Discov. 2022 July 06; 12(7): 1676–1689.
[16] M. Wang, et al. Sunvozertinib in NSCLC patients with EGFR exon 20 insertion mutationsESMO 2022, Abs 987P
[17] N. Girard. Amivantamab compared with European, real-world (RW) standard of care (SoC) in adults with advanced non-small cell lung cancer (NSCLC) with activating epidermal growth factor receptor (EGFR) exon 20 insertion mutations (exon20ins), after failure of platinum-based therapy. ESMO 2022, Abs 1117P
[18] C. Chouaid. An adjusted comparison of amivantamab phase II data versus real-world clinical management in France of EGFR exon 20 insertion-mutated (ex20ins)advanced NSCLCpatients. ESMO2022, Abs 1117P
[19] V. Albarrán-Artahona, et al. Spanish Multicenter Retrospective Study of Real-Life Experience of Advanced NSCLC with EGFR Exon 20 Insertions Treated with Amivantamab. WCLC 2022, EP08.02-149[20] A. Kron, et al. EGFR exon 20 insertions in non-small cell lung cancer (NSCLC): Impact of TP53 mutation status and value of immune-checkpoint blockade (ICB). ESMO 2022, Abs 991P
往期回顾
1、破茧成蝶 向森而生 | 2022肺癌年终盘点之EGFR经典突变
2、【2022 ESMO ASIA】破茧成蝶 向森而生 | 王洁教授解读2022 ESMO ASIA:EGFR突变非小细胞肺癌治疗新进展
3、【2022 CSCO】破茧成蝶 向森而生 | 亚洲数据公布!Amivantamab开启晚期肺癌EGFR靶向治疗新纪元!
4、【2022 WCLC】破茧成蝶 向新而生|Amivantamab联合方案一线治疗EGFR敏感突变肺癌患者PFS或超28个月!
5、【2022 ASCO速递】破茧成蝶 向新而生 | 吴一龙教授解读非小细胞肺癌EGFR和MET通路靶向治疗新进展
6、【2022ELCC&AACR】破茧成蝶 向新而生| 赵军教授:EGFR exon 20ins NSCLC靶向治疗新突破
7、【2022 ELCC】破茧成蝶 向新而生| EGFR 20ins非小细胞肺癌治疗前沿进展盘点
8、ESMO2021|囊括EGFR/MET途径,克服奥希替尼耐药,Amivantamab联合Lazertinib研究数据闪耀ESMO
9、【2021 ASCO】陆舜教授分享肺癌靶向治疗最新进展,创新组合疗法有望克服EGFR TKI耐药
10、吴一龙教授谈EGFR 20外显子插入突变NSCLC诊疗现状与进展,Amivantamab(JNJ-61186372)机制独特或可带来突破
11、周彩存教授:WCLC重磅来袭!NSCLC EGFR Exon 20ins难治突变靶向治疗迎来重大突破!EGFR经典突变靶向治疗新组合惊艳全场!

更多精彩内容请扫码关注“杨先森 Mr J”
排版编辑:肿瘤资讯-DND











 苏公网安备32059002004080号
苏公网安备32059002004080号


