黑色素瘤文献月评项目秉承传递最新医学进展的理念,以专业视角多维度关注领域最新进展。继前三期获得业内高度评价后,项目第四期与大家如期而见。本期精选了AACR 2020 (American Association for Cancer Research) 2项重大研究进展和黑色素瘤领域2020年4月最新发表的热点高水平研究,聚焦达拉非尼联合曲美替尼连续用药对比间断用药方案疗效、双靶联合免疫的三联方案研究成果、中国肢端黑色素瘤患者临床病理和生存特征、肿瘤合并突变等内容,特别邀请福建省肿瘤医院陈誉教授为我们带来深入解读。

福建省肿瘤医院特需病房19区行政副主任(主持工作)
福建省肿瘤医院黑色素瘤MDT小组组长
福建省肿瘤医院内科学教研室副主任
福建省五四青年节奖章获得者
CSCO黑色素瘤专家委员会常务委员
CSCO尿路上皮癌专家委员会委员
CSCO肝癌专家委员会委员
CSCO罕见肿瘤专家委员会委员
中华医学会肿瘤学分会肿瘤内科专家委员会 委员
中国抗癌协会第一届青年理事会常务理事
中国抗癌协会科普防治专业委员会委员
CSCO第一届青年委员会委员
福建省肿瘤免疫治疗质控中心委员兼秘书
福建省抗癌协会肿瘤免疫治疗专业委员会 常务委员
福建省医学会肿瘤学分会第六届委员会委员
目 录
1. AACR速递 —— SWOG S1320: 达拉非尼联合曲美替尼的持续给药相对于间断给药能够提高BRAF突变黑色素瘤患者的无进展生存期
2. AACR速递 —— BRAFV600突变阳性晚期黑色素瘤患者接受阿替利珠单抗+考比替尼+维莫非尼方案评估:IMspire 150 III期研究主要研究结果
3. 原发部位不同的肢端黑色素瘤间临床病理和生存特征对比
4. 晚期黑色素瘤中肿瘤CD155表达与抗PD-1免疫治疗的耐药性相关
5. 辅助治疗对于前哨淋巴结活检阳性但未进行淋巴结清扫术的黑色素瘤患者有效
6. TERT启动子突变与MAPK抑制剂治疗的黑色素瘤患者临床预后的不同相关性
1. AACR速递 —— SWOG S1320: 达拉非尼联合曲美替尼的持续给药相对于间断给药能够提高BRAF突变黑色素瘤患者的无进展生存期
背景:BRAF抑制剂联合MEK抑制剂在BRAF V600E/K突变的黑色素瘤患者中具有显著的疗效,但获得性的耐药往往会限制患者的持续缓解时间。临床前数据表明,间断性给药策略似乎能够通过剔除在药物存在下最佳生长的肿瘤细胞,而延迟获得性耐药。 S1320是一项随机的II期临床试验,旨在探索达拉非尼和曲美替尼的间断给药和连续给药是否能够改善晚期BRAF突变黑色素瘤患者的无进展生存期(PFS)。
研究方法:所有患者均接受达拉非尼联合曲美替尼连续治疗8周,随后将无疾病进展的患者随机分为持续用药组和间断用药组(用药5周,停药3周)。两组患者的计划外治疗中断均不得超过14天。使用RECIST v1.1标准每8周评估一次患者对药物的反应,该评估周期与间歇给药组患者的治疗期间一致。 每月使用CTCAE v4标准评估不良事件。 本研究使用Cox模型来评估随机分层因素的数据。
结果:本研究入组242例患者,在接受8周的治疗后,206例无疾病进展的患者随机分组,其中105例为持续给药组,101例为间断给药组。70%的患者既往未接受过免疫检查点抑制剂的治疗。两组患者的基线特征无显著差异。持续给药组的中位PFS为9.0个月,显著高于间断给药组的5.5个月(HR 1.38,80% CI:1.12-1.69,p=0.064)。中位OS在两组患者中无统计学差异,两组均为29.2个月(p=0.93),中位随访时间为2年。77%持续给药组的患者和84%间断给药组的患者因疾病进展中断治疗(p=0.34)。
结论: 持续接受BRAF抑制剂和MEK抑制剂达拉非尼联合曲美替尼的患者,相较于间断给药的方式能够获得更大的PFS获益。
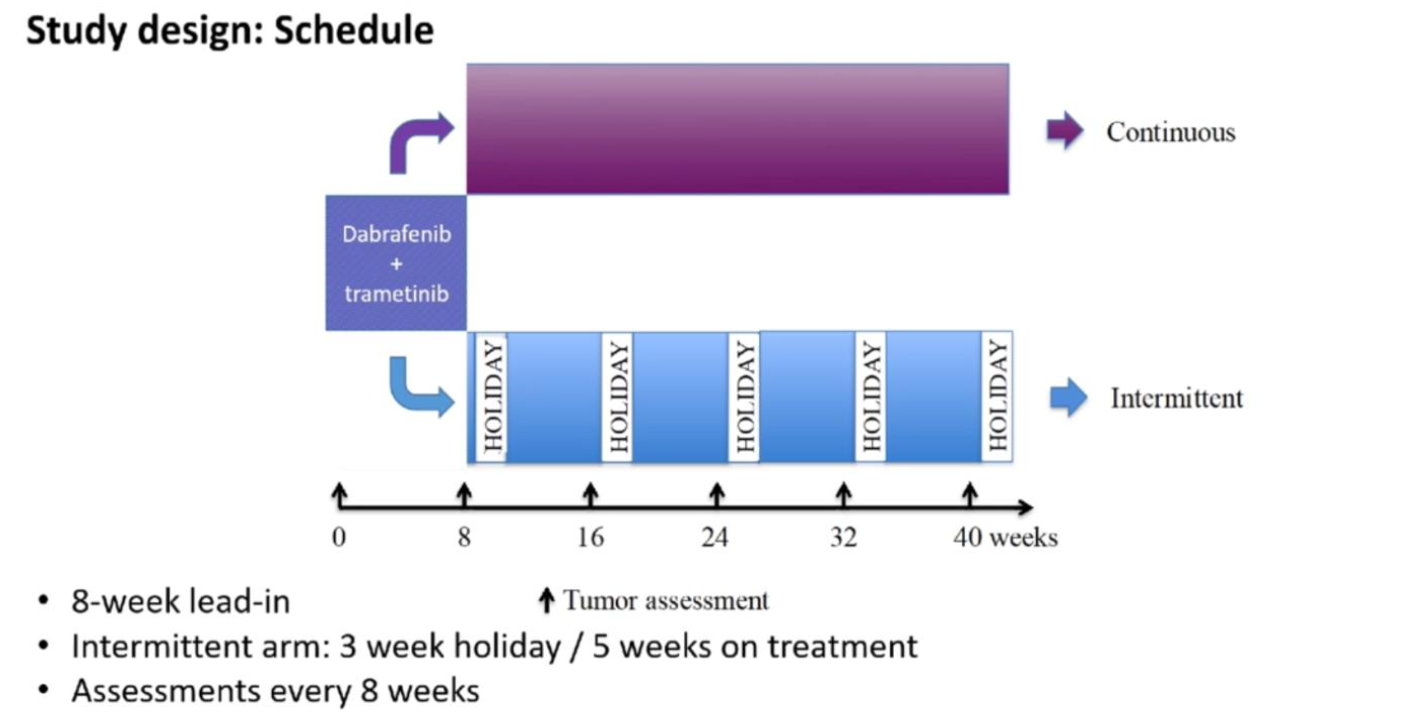
图1.S1320研究设计
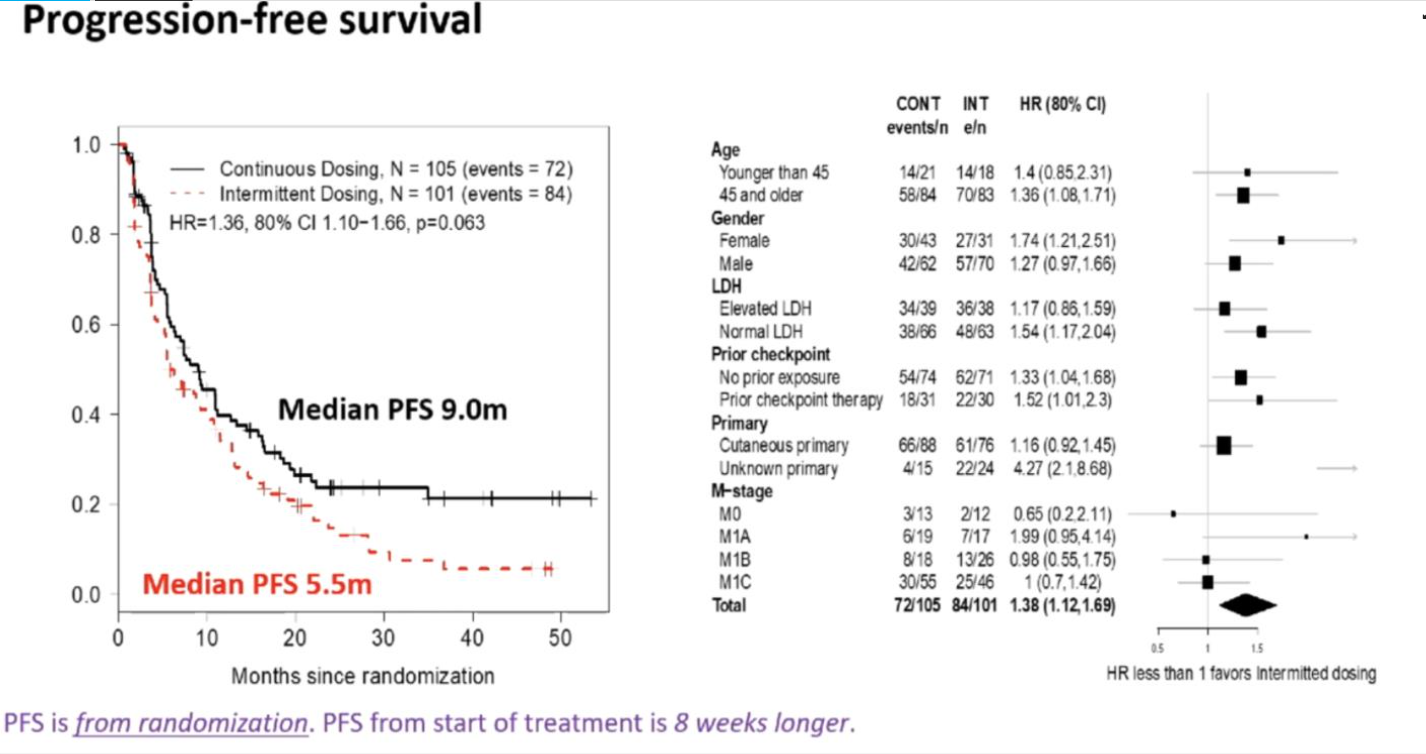
图2.持续给药组的中位PFS为9.0个月,显著高于间断给药组的5.5个月(HR 1.38,80% CI:1.12-1.69,p=0.064)
在既往的研究中,为了逆转或者延缓维莫非尼的耐药,提出间断给药模式,探索是否能让药物敏感细胞和耐药细胞达到某种平衡。早期D+T的体外研究发现2周停药,6周给药似乎也能达到这样的平衡。但法国一研究团队报道了,在体外PDX模型中对比了双靶间断给药以及连续给药的疗效,结果发现无论是单纯使用BRAFi或MEKi,还是两者联合使用,间歇给药与连续给药之间并没有显著的疗效差异。
SWOG研究原本设计思路是间歇给药组的PFS能显著优于连续给药组,但结果大跌眼镜,间歇给药组的ORR和PFS都明显劣于连续给药组。究其原因,可能是达拉非尼的半衰期较短,又属于可逆性抑制剂,但曲美替尼的半衰期相对长又容易在体内蓄积(曲美替尼半衰期相较于考比替尼和Binimetinib更长),故这种间歇方案并未做到完全“间歇”;另外MAPK通路的激活并不是双靶耐药的主要机制,单纯从这条通路上做文章可能也是行不通的。这项研究证实了D+T的这种间歇给药模式(吃5周,歇3周)在临床上行不通,建议要连续给药。
2. AACR速递 —— BRAFV600突变阳性晚期黑色素瘤患者接受阿替利珠单抗(A)+考比替尼(C)+维莫非尼(V)方案评估:IMspire 150 III期研究主要研究结果
背景:晚期黑色素瘤全身治疗已获批方案包括免疫检查点抑制剂治疗(CIT)和针对BRAFV600E/K突变黑色素瘤的BRAF+MEK抑制剂靶向治疗方案。与靶向治疗相比,CITs具有反应率较低和缓解更持久的特点。临床前和临床数据表明,CIT和BRAF + MEK抑制剂之间存在潜在协同作用。因此,我们评估了CIT联合靶向治疗是否比单独靶向治疗疗效更佳。
方法:既往未接受治疗的不可切除IIIc/IV期BRAFV600突变黑色素瘤患者(AJCC第七版,RECIST 1.1评价)随机分组接受A(anti-PD-L1) + C + V或Pbo (安慰剂) + C + V方案。每28天一个周期,在第1天和第15天给药A或Pbo。治疗持续到疾病进展或毒性不可耐受。主要终点是研究者评估无进展生存期(PFS)。
结果: 514例患者入组(A + C + V 256例;Pbo + C + V 258例),中位随访18.9个月。研究者评估的PFS在A + C + V 组较Pbo + C + V组显著延长(分别为15.1 vs 10.6个月; 风险比: 0.78; 95%置信区间: 0.63-0.97; P=0.025),所有预后亚组均可见该趋势。尽管A + C + V组和Pbo + C + V组的客观缓解率相似(66% vs 65%),但A + C + V组(21.0个月)的中位持续缓解时间与Pbo + C + V组(12.6个月)相比有所延长。 IRC评估的中位PFS 为16.1 个月 (95% CI, 11.3-18.5) vs 12.3 个月 (95% CI, 10.8-14.7),P=0.1607,没有统计学差异。总生存数据尚未成熟。A + C + V组和Pbo + C + V组常见治疗相关不良事件(AEs; > 30%)包括:肌酸磷酸激酶(CPK)升高(51.3% vs 44.8%)、腹泻(42.2% vs 46.6%)、皮疹(两组均为40.9%)、关节痛(39.1% vs 28.1%)、发热(38.7% vs 26.0%)、丙氨酸转氨酶(ALT)升高(33.9% vs 22.8%)和脂肪酶升高(32.2% vs 27.4%)。A + C + V组和Pbo + C + V组常见治疗相关的3/4级AEs(>10%)为:脂肪酶升高(20.4% vs 20.6%)、血CPK升高(20.0% vs 14.9%)、ALT升高(13.0% vs 8.9%)和斑疹丘疹(12.6% vs 9.6%)。A + C + V组(33.5%)与Pbo + C + V组(28.8%)治疗相关SAEs发生率相似。A + C + V组(12.6%)和Pbo + C + V组(15.7%)的患者因AEs停止了全部治疗。A + C + V方案的安全性与单个药物的安全性情况基本一致。
结论:A + C + V联合治疗可耐受且可管理,缓解时间持久并且与Pbo + C + V相比显著延长PFS。因此,A + C + V是BRAFV600突变阳性晚期黑色素瘤的可行治疗方案。
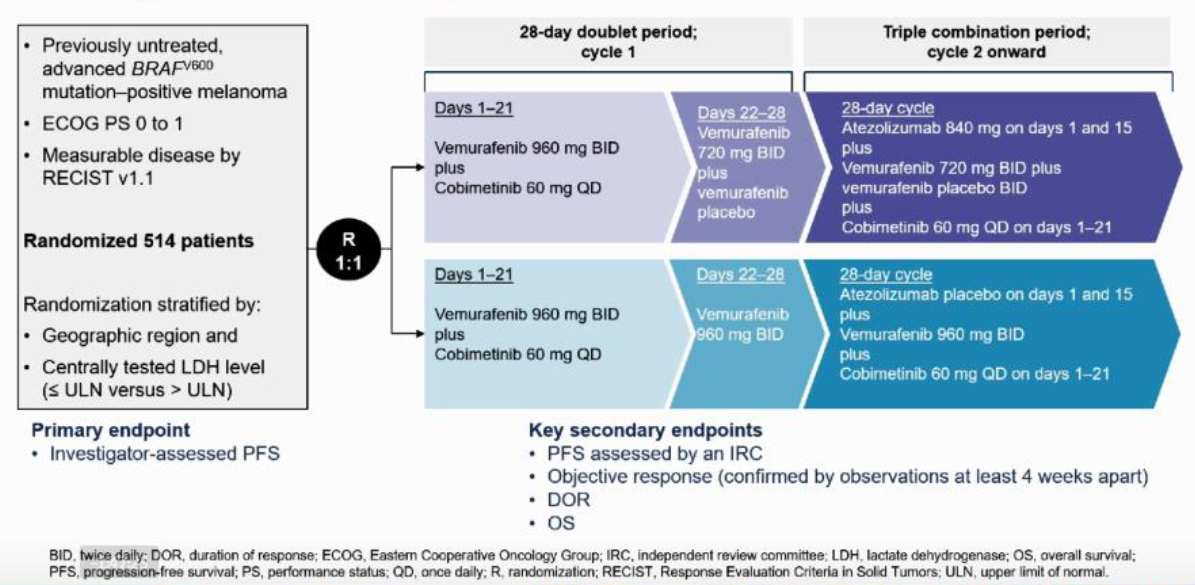
图3.IMspire 150 研究设计
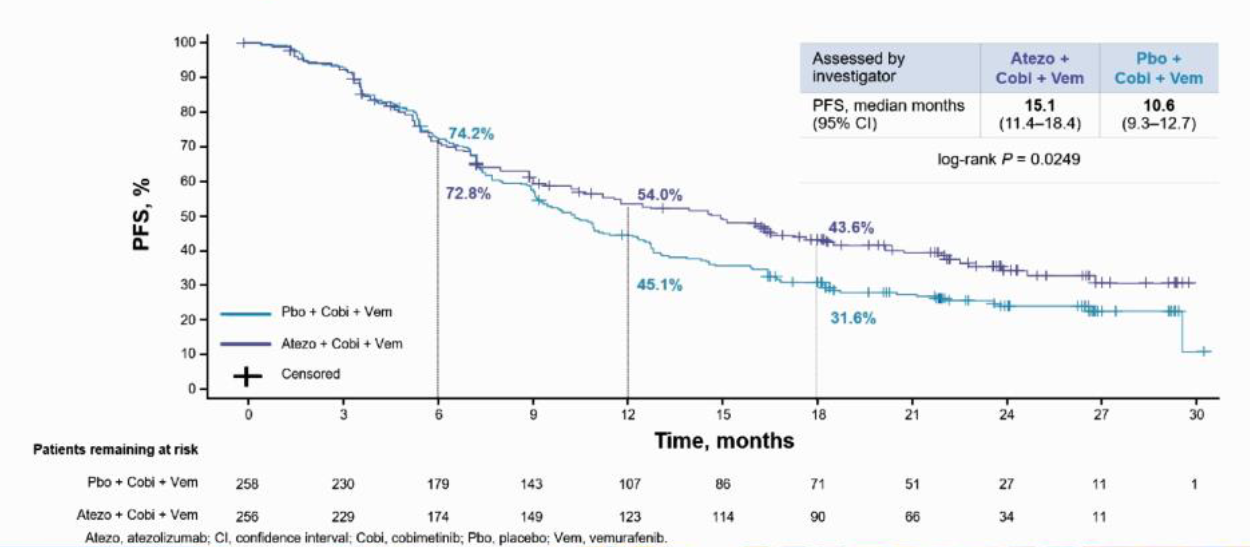
图4.IMspire 150 研究主要研究终点研究者评估的PFS Kaplan-Meier曲线
3. 原发部位不同的肢端黑色素瘤间临床病理和生存特征对比
对于肢端黑色素瘤,不同原发部位患者的临床病理特征和生存情况还不清楚,这项多中心回顾性研究,纳入了从2000年1月1日到2017年12月31日间,来自中国6家高水平医院的肢端黑色素瘤患者数据。比较发生于足底、手掌、甲床等原发部位黑色素瘤的基线特征,患者黑色素瘤疾病特异的生存情况。同时,识别出影响患者黑色素瘤疾病特异生存时间的预测因素。
研究共纳入1157例肢端黑色素瘤患者。其中,原发于足底的患者诊断时临床分期较晚,Breslow厚度更高,复发和远处转移风险更高(所有P值均小于0.05),小于65岁的患者比例和溃疡的发生比例在原发于甲床和手掌的患者中要低于足底组;共有294例患者接受了前哨淋巴结活检,在不同原发部位患者中,前哨淋巴结阳性率无统计学差异。在有基因组学信息的701位患者中,不同原发部位的BRAF,C-KIT和PDGFRA的突变频率相似,NRAS突变频率在不同原发部位组中有差异(足底患者更高,P=0.0102)。原发于足底、甲床和手掌的患者的黑色素瘤疾病特异生存分别为65个月、112个月、未达到(P=0.0053)。在多元回归分析中,原发部位、诊断时临床分期、复发是影响患者黑色素瘤疾病特异生存的预后因素,但不同原发部位患者的差异显著性不同。
结论:在不同原发部位的肢端黑色素瘤患者中,存在显著的临床病理和生存差异,与发生于手掌或甲床的患者相比,足底黑色素瘤的预后更差。
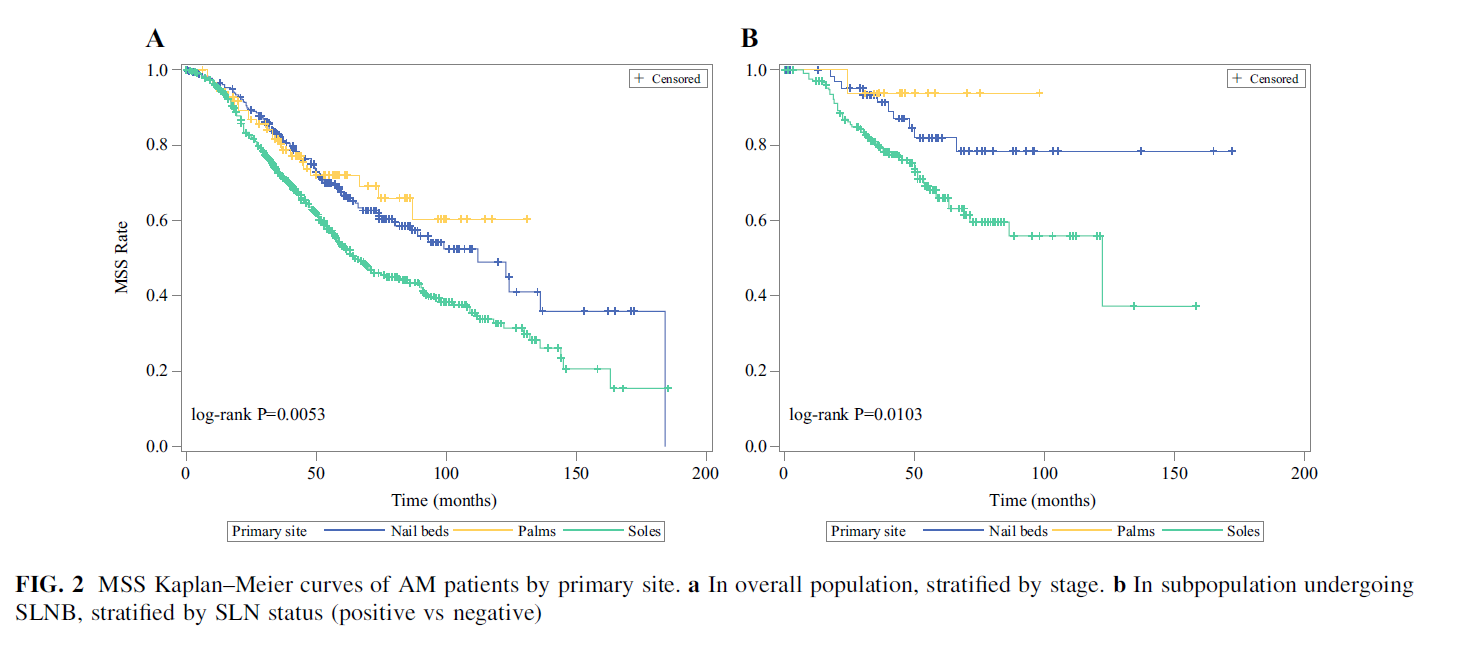
图5.不同原发部位肢端黑色素瘤疾病特异生存曲线
(A)整体人群,根据临床分期分层;(B)根据前哨淋巴结活检结果分层(阳性)
4. 晚期黑色素瘤中肿瘤CD155表达与抗PD-1免疫治疗的耐药性相关
目的:基于抗 PD-1 的免疫检查点阻断 (ICB) 耐药性仍然是治疗转移性黑色素瘤的一个难题。肿瘤细胞以及宿主髓系细胞可以表达免疫检查点配体 CD155 来调节免疫细胞功能。然而,肿瘤 CD155 对人黑色素瘤免疫背景的影响尚未得到很好的描述。这项观察性研究描述了转移性黑色素瘤中 CD155 表达特征,并将结果与免疫细胞特征和对 ICB 反应的差异进行关联性探究。
设计:155 例接受 ICB 治疗的转移性黑色素瘤患者和 50 例接受 BRAF/MEK 定向靶向治疗的患者的治疗前肿瘤标本,通过免疫组织化学评估其 CD155 的表达。使用多重免疫组织化学荧光方法测定CD8、PD-1 和 SOX10 表达以分析肿瘤内 T 细胞特征。针对CD155 肿瘤水平和整体肿瘤 RNA序列结果,以及临床RECIST反应和无进展生存期之间进行相关性分析。
结果:治疗前高 CD155 肿瘤水平与高实质 PD-1+ CD8+/CD8+T 细胞比值 (PD1tR) 和抗 PD1 治疗反应差相关。在 PD-L1 阴性肿瘤中,CD155 肿瘤高表达与抗 PD-1/CTLA-4 联合治疗效果不佳的患者相关。
结论:我们的发现首次提示在抗 PD-1 难治性黑色素瘤研究中,肿瘤 CD155 提示PD-1+ CD8+ T 细胞比值的增加。此外,靶向 CD155 通路可能会改善转移性黑色素瘤患者对抗 PD-1 治疗的反应。
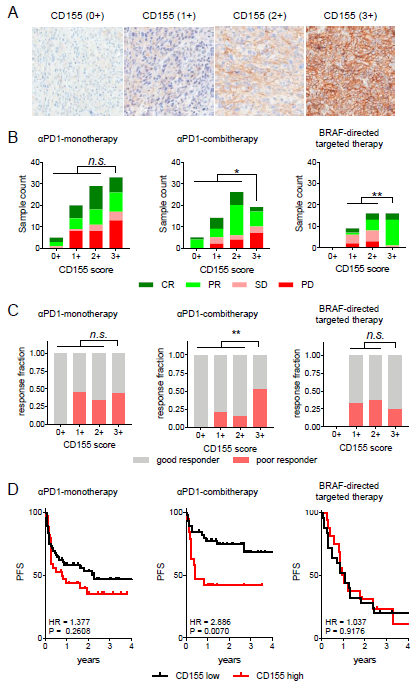
图6.(A)免疫组化染色药物治疗前期恶性黑色素瘤细胞内CD155蛋白表达水平;(B)CD155高表达(3+)对比低表达(0,1+,2+)肿瘤细胞在PD-1联合治疗中客观缓解率更低,但在靶向治疗中缓解率高。(C)CD155高表达(3+)对比低表达(0,1+,2+)肿瘤细胞在PD-1联合治疗中在6个月内更容易进展,其余两个治疗组别中无明显差异。(D)CD155高表达(3+)对比低表达(0,1+,2+)肿瘤细胞在PD-1联合治疗中无进展生存时间更短,在PD-1单药中也有相同趋势,但无统计学差异,在BRAF抑制剂治疗组中无明显差异
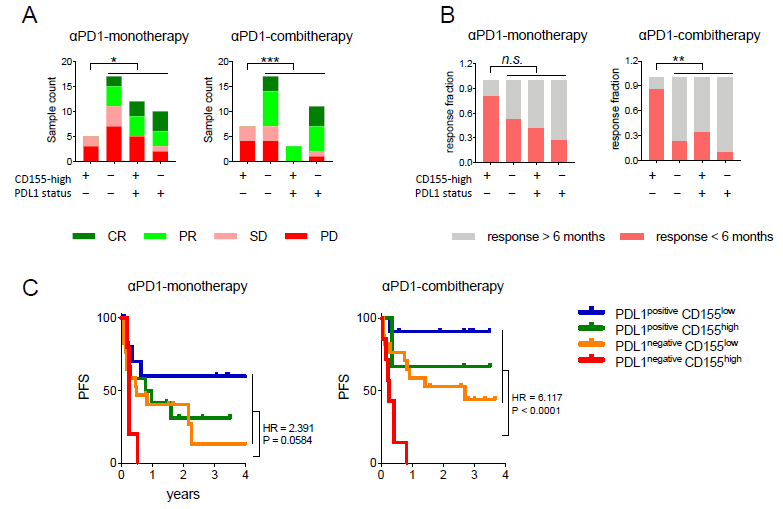
图7.显示PD-L1阴性肿瘤中,CD155肿瘤高表达与抗PD-1/CTLA-4联合治疗效果不佳的患者相关
CD155(也叫PVR 、Necl5或Tage4)是黏附分子家族的成员,在正常组织中不表达或低表达,但在很多肿瘤细胞表面高表达,一旦与NK和T细胞表面的TIGIT结合后(TIGIT是共抑制分子),对肿瘤细胞的杀伤作用就会被抑制。在既往的研究中也证实,使用抗TIGIT单抗后,可逆转动物模型中NK细胞耗竭,并可用于多种肿瘤的免疫治疗。
本研究首次在真实世界中评估了CD155高表达与PD-1单抗治疗疗效的关系,证实了在黑色素瘤免疫治疗中,CD155可能扮演了负性调控免疫的作用,为临床实践提供了指示:1)是否可通过CD155的检测,来预测PD-1单抗的疗效?但是否需要同时检测免疫细胞的其他共抑制分子,如TIGIT、Lag-3,TIM-3等? 2)可在黑色素瘤领域探索此类抗体的疗效,目前已有多家公司针对CD155/TIGIT抗体进行前期临床研究,但是否需要和PD-1单抗、CTLA-4单抗或者其他免疫制剂联合?此外,由于前期的基础和临床研究都是基于皮肤黑色素瘤为研究对象,而对于中国以肢端和黏膜黑色素瘤为主,是否也同样适合?尚需进一步探索。
[1] Gao J, Zheng Q, Xin N, Wang W, et al. CD155, an onco‐immunologic molecule in human tumors. Cancer Science. 2017;108(10):1934-1938.
[2] Manieri NA, Chiang EY, Grogan JL. TIGIT: A Key Inhibitor of the Cancer Immunity Cycle. Trends Immunol. 2017 Jan;38(1):20-28.
5. 辅助治疗对于前哨淋巴结活检阳性但未进行淋巴结清扫术的黑素瘤患者有效
背景:自2015年以来,基于随机试验的多项黑色素瘤辅助治疗已经获批( FDA已批准的辅助治疗靶向和免疫药物包括:达拉非尼+曲美替尼、伊匹木单抗、帕博利珠单抗、纳武单抗;CFDA获批辅助适应证药物为达拉非尼+曲美替尼),试验表明高危患者手术切除后采用辅助治疗可改善无复发生存期(RFS)。 这些试验的纳入标准要求对前哨淋巴结阳性(pSLN)的病例行淋巴结清扫(CLND)。研究旨在阐述目前的治疗方法作为辅助治疗,对于前哨淋巴结阳性但没有进行淋巴结清扫(主动监测[AS])的患者疗效,评估这些患者的复发率。
方法:2016年至2019年间在两个机构中确诊的前哨淋巴结阳性的黑色素瘤患者。 回顾性地分析了人口统计学信息,疾病和治疗特征以及复发细节。通过对患者是否复发进行分层,并分别使用Fisher精确检验和t检验比较患者,治疗和肿瘤相关特征的分类变量和连续变量。
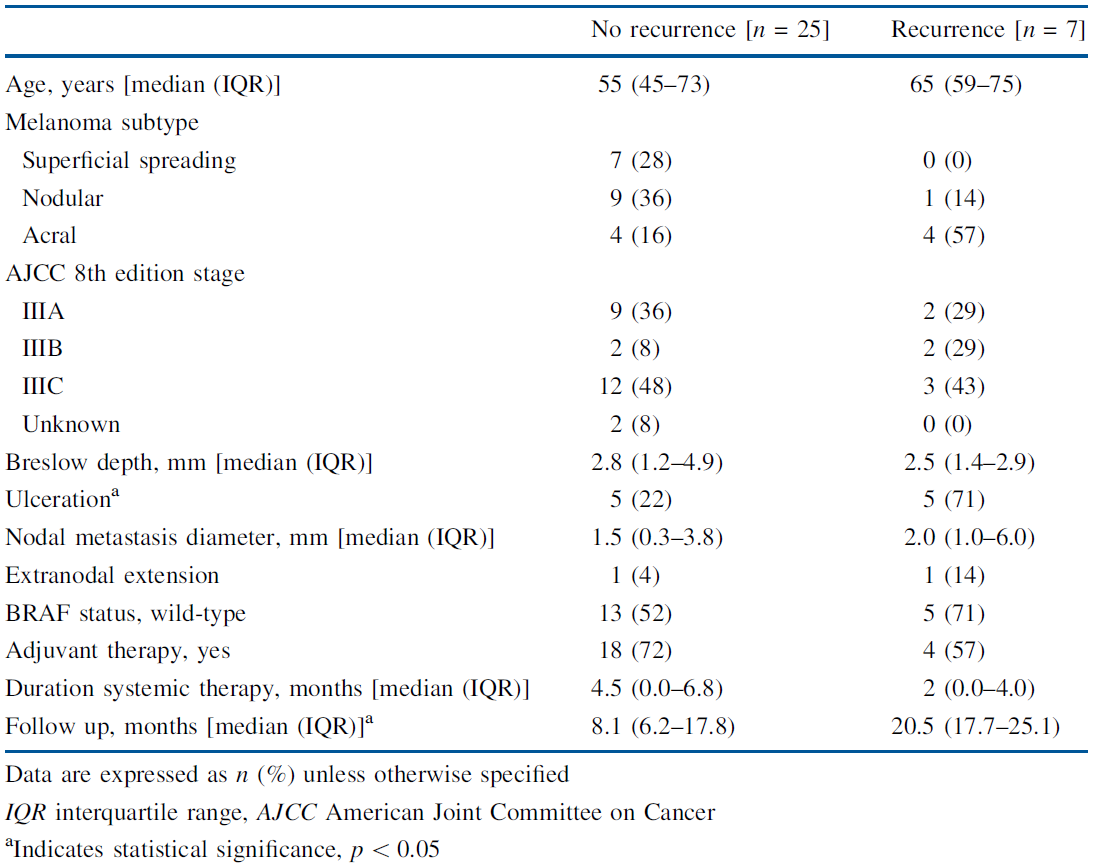
结果:总共纳入了245个前哨淋巴结活检病例,其中36个(14.7%)为pSLN。 在36例pSLN中,有4例接受了CLND,32例接受了AS,其中22例(68.8%)接受了抗程序化死亡1(PD1)抑制剂nivolumab(16/22),抗细胞毒性T淋巴细胞相关蛋白4(CTLA-4)抑制剂ipilimumab(3/22)或BRAF / MEK抑制剂(3/22)。中位随访时间为13.3个月,AS中复发的患者为7/32(21.9%),其中接受辅助治疗的患者为4/22(18.2%),未接受辅助治疗的患者为3/10(30.0%)。 肿瘤溃疡与复发密切相关。 尽管没有显著差异,但在复发患者中,肢端黑色素瘤亚型似乎更为常见。
结论:未经CLND治疗的大多数pSLN患者(68.8%)接受了辅助治疗。未行CLND而接受辅助治疗的患者1年RFS为82%,与当前要求CLND的辅助治疗临床试验的研究结果相似。
表1.采取主动监测的研究患者按照是否复发分层的临床特征
6. TERT启动子突变与MAPK抑制剂治疗的黑色素瘤患者临床预后的不同相关性
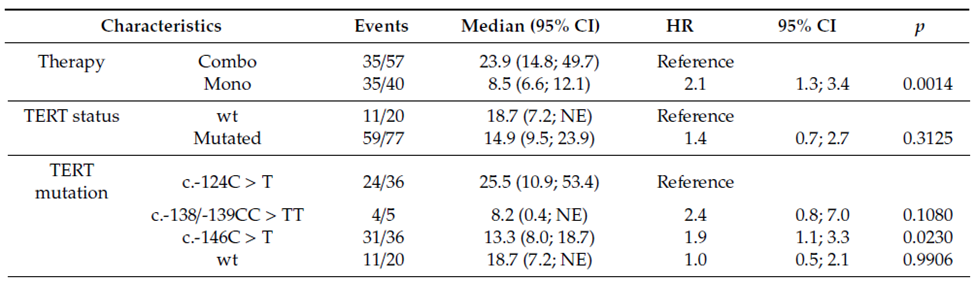
耐药是丝裂原活化蛋白激酶抑制剂(MAPKi)治疗转移性黑色素瘤的主要挑战。肿瘤遗传改变可引起MAPK通路重新激活,导致MAPKi响应率低和预后不良。黑色素瘤患者突变谱的特征对于为患者量身定制治疗方案可能至关重要。端粒酶逆转录酶基因的启动子区域(TERTprom)的突变在BRAFV600突变型黑色素瘤中很常见,可导致端粒酶逆转录酶基因(TERT)表达升高和端粒酶活性增强。据报道,TERTprom和BRAFV600突变共同推动了癌症进展和侵袭。我们评估了TERTprom状态对97例接受MAPKi治疗的黑色素瘤患者临床疗效的影响。我们观察到,与携带c.-124C> T突变的患者相比,具有c.-146C> T突变患者的无进展生存期(PFS)显著更差,并且进展风险增加了两倍(中位数PFS 5.4 vs. 9.5个月;危险比(HR)1.9; 95%置信区间(CI)1.2-3.2; p = 0.013)。对于总生存期(OS)也观察到了这种趋势,与c.-124C> T突变的黑色素瘤患者相比,c.-146C> T突变的患者预后较差(中位OS 13.3 vs. 25.5个月; HR 1.9,95%CI 1.1-3.3,p = 0.023)。我们的结果揭示了这两种TERTprom突变与MAPKi治疗的黑色素瘤患者预后的不同相关性,突显了通路阻断的不同影响。
表2.无进展生存期的单量Cox比例风险模型
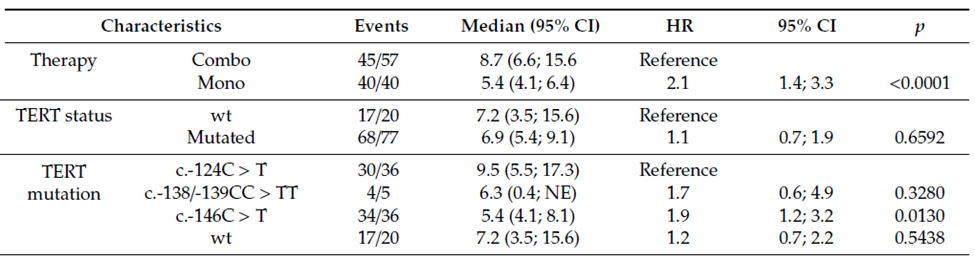
表3.总生存率的变量COX比例风险模型
参考文献
[1]. SWOG S1320: Improved progression-free survival with continuous compared to intermittent dosing with dabrafenib and trametinib in patients with BRAF mutated melanoma. AACR 2020, CT013.
[2]. Evaluation of atezolizumab (A), cobimetinib (C), and vemurafenib (V) in previously untreated patients with BRAF mutation-positive advanced melanoma: Primary results from the phase 3 IMspire150 trial. AACR 2020, CT012.
[3]. The Clinicopathological and Survival Profiles Comparison Across Primary Sites in Acral Melanoma. Ann Surg Oncol. 2020 Apr 6. doi: 10.1245/s10434-020-08418-5. [IF = 4.097]
[4]. Tumor CD155 expression is associated with resistance to anti-PD1 immunotherapy in metastatic melanoma. Clin Cancer Res. 2020 Apr 28. doi: 10.1158/1078-0432.CCR-19-3925. [IF = 8.911]
[5]. Adjuvant Therapy is Effective for Melanoma Patients with a Positive Sentinel Lymph Node Biopsy Who Forego Completion Lymphadenectomy. Ann Surg Oncol. 2020 Apr 20. doi: 10.1245/s10434-020-08478-7. [IF = 3.681]
[6]. TERT Promoter Mutations Differently Correlate with the Clinical Outcome of MAPK Inhibitor-Treated Melanoma Patients. Cancers. 2020, 12(4), 946. [IF = 6.162]
排版编辑:Vincent
精彩回顾
黑色素瘤文献月评 | 第一期 BRAF突变转移性黑色素瘤的最佳治疗方案决策
黑色素瘤文献月评 | 第二期 BRAFi+MEKi调节免疫微环境机制提供双靶治疗长期缓解理论基础
黑色素瘤文献月评 | 第三期 日本真实世界数据验证达拉非尼联合曲美替尼为东亚患者带来显著治疗获益
版权声明















 苏公网安备32059002004080号
苏公网安备32059002004080号


