免疫治疗可提升食管癌5年生存率至少10个百分点。
晚期肺癌和恶性黑色素瘤是免疫治疗率先在临床研究和临床实践中取得成功的两种恶性肿瘤。在美国和日本,2019年的免疫治疗已从恶性黑色素瘤的一线治疗步入术后辅助治疗[1]。同在2019年,PD-1免疫检查点抑制剂帕博利珠单抗在国内获批3个一线治疗晚期非小细胞肺癌的适应证[2],推动我国免疫治疗从二线飞跃至一线。

北京肿瘤医院副院长
北京市肿瘤防治研究所副所长
消化肿瘤内科主任
I期临床病房主任
任中国抗癌协会肿瘤药物临床研究专业委员会主任委员
中国医师协会外科医师分会MDT专委会主任委员
中国抗癌协会胃癌专业委员会秘书长及内科组组长
中国抗癌协会大肠癌专业委员会副主任委员
中国抗癌协会肿瘤精准治疗专委会候任主任委员等职务
一直致力于消化系统肿瘤精准药物治疗、抗肿瘤新药的I-IV期临床试验与基础转化研究,担任科技部国家重点研发计划“胃癌靶向治疗新技术研究”项目首席专家。
消化道肿瘤的免疫治疗虽然相比晚期肺癌和恶性黑色素瘤的免疫治疗起步晚,但在2019年也强势出击,大有厚积薄发,赶超肺癌和恶性黑色素瘤之势。
先有KEYNOTE-240研究结果显示PD-1免疫检查点抑制剂帕博利珠单抗二线单药治疗肝细胞癌相比当前的标准治疗带来具有临床意义的总生存获益[3],后有在ASCO上公布的KEYNOTE-062研究结果显示帕博利珠单抗单药一线治疗PD-L1表达阳性(CPS≥1)的胃癌达到预设终点,带来的总生存(OS)获益非劣效于标准化疗,并在PD-L1 CPS≥10的人群中, 显示OS优效性[4]。
但是最出乎意料之外的,也是最具临床实质意义的进展却产生于食管癌的免疫治疗。
美国FDA基于KEYNOTE-181全球多中心的Ⅲ期临床研究结果,于2019年7月31日批准帕博利珠单抗治疗PD-L1表达阳性(CPS≥10)的复发性局部晚期或转移性食管鳞癌的二线及以上治疗。
更令人兴奋不已的当属在2019年9月的CSCO(中国临床肿瘤学年会)以及在11月的ESMO-ASIA(欧洲肿瘤内科学亚洲大会)上分别公布的KEYNOTE-181研究的亚洲人群和中国人群亚组数据。
相比KEYNOTE-181的整体研究人群的治疗数据,帕博利珠单抗治疗中国人群带来的OS获益更显著,死亡风险降低幅度是整体研究人群数据的3倍:中国人群45%(HR=0.55,95% CI 0.36~0.82)相比整体人群仅有的15% (HR=0.85,95% CI 0.72~1.01;P=0.031)[5]。 而且在PD-L1表达阳性(CPS≥10)的人群中,相比化疗方案,亚洲和中国人群的中位OS分别达到12.5个月[6]和12.0个月[5],都超过了整体人群治疗的数据。
而且在PD-L1表达阳性(CPS≥10)的人群中,相比化疗方案,亚洲和中国人群的中位OS分别达到12.5个月[6]和12.0个月[5],都超过了整体人群治疗的数据。
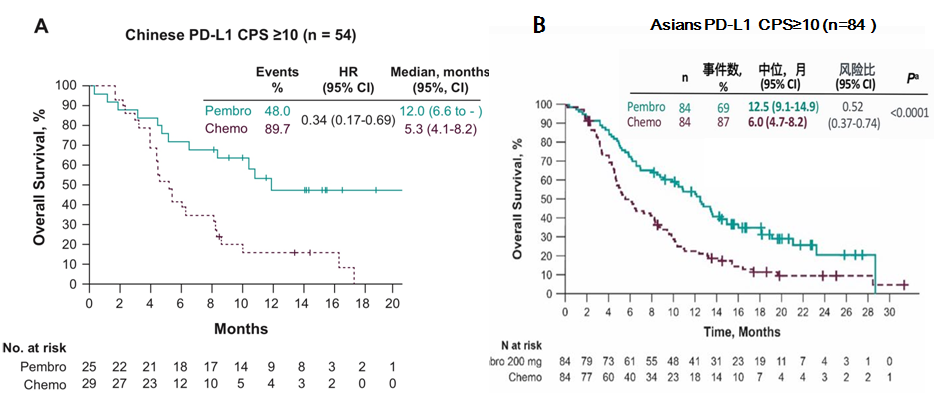
KEYNOTE-181亚洲和中国亚组人群的OS[5,6]
随后,纳武利尤单抗和包括国产PD-1免疫检查点抑制剂卡瑞利珠单抗的Ⅲ期研究结果也分别在2019年的ESMO和世界食管癌大会上公布,结果都显示单药二线治疗,两者都带来显著的OS获益。
食管癌免疫治疗临床研究在2019年的异军突起,以及其药物在国内注册的全速推进,让食管癌治疗成为消化道肿瘤免疫治疗的领航者,PD-1治疗食管癌也有望在2020年全面进入临床实践。
这对于具有中国特色的、死亡率排在所有恶性肿瘤前四位的食管癌治疗来说意味着什么?食管癌免疫治疗在国内的全面爆发还将面临什么挑战? 2020能否见证免疫治疗为国内食管癌治疗带来翻天覆地的变革?
带着这些问题,记者采访了北京大学肿瘤医院副院长、消化科主任沈琳教授。
2020开春,帕博利珠单抗治疗食管癌的适应证可能就会在国内获批。食管癌免疫治疗的临床实践即将开锣,这对于提升食管癌治疗水平,提升5年生存率会有何意义?
沈琳教授:我国70%的食管癌患者在初诊时已发展为局部晚期或转移性。目前我国局部晚期食管癌治疗的疗效仍不尽人意,而晚期食管癌治疗的手段也非常有限。在过去几十年,我们只有5-FU和顺铂这两种化疗一线治疗药物,而且带来的中位OS不到1年,所以有巨大的未被满足的治疗需求。
当前免疫治疗食管癌的研究,包括联合化疗一线治疗的研究,比如,帕博利珠单抗联合化疗一线治疗复发转移性食管癌患者(鳞癌、腺癌和胃食管结合部腺癌)的Ⅲ期临床研究KEYNOTE-590的中国扩展研究已在国内20个中心启动,并于2019年6月完成所有受试者的入组。
另外,在术前新辅助治疗,以及术后联合或序贯放化疗的研究都在陆续开展。
在2020年年底前后,将会有几个大型的Ⅲ期免疫治疗食管癌的临床研究结果发布,而且免疫治疗在围手术期与放化疗结合的研究结果也可能会很快问世。这些研究结果很有可能推动我国食管癌整体治疗的转归发生根本性的改变。
我国食管癌患者的5年生存率很低,仅在20%左右。这些研究结果的出炉,将意味着很多局部晚期或转移性食管癌患者甚至能获得治愈的效果。
未来10年,食管癌治疗的变革会非常大;我不敢说5年生存率翻倍到40%,但是提高10个百分点还是完全可能的,30%以上应该是没有任何问题的。
KEYNOTE-181亚洲和中国人群的数据带来了哪些启示?
沈琳教授:在KEYNOTE-181 这一个临床研究中,既能看到欧美人群,也能看到亚洲国家,如日本、韩国和中国人群的数据结果;既能看到在欧美高发的食管腺癌人群的数据,也能看到在国内高发的食管鳞癌的数据结果; 最后还能看到不同PD-L1表达人群的数据结果。
结果显示不但东西方人群的结果存在差异,而且中国人群的数据与亚洲其他国家人群的数据又不同。这是首次证明虽是同一个疾病,但由于不同地域人群的饮食习惯、不同身体素质、不同发病原因和不同疾病分子特征,免疫治疗带来的疗效和OS是不同的。 虽然从以往针对疾病的基础研究和一些临床研究的结果也已反映出这样的差异,但以前我们拿不出任何一个具有信服力的对比研究结果,呈现给世人说中国的患者和其他亚洲国家的不同,和欧美国家的不同。但在KEYNOTE-181这样一个所有标准都一样的平台上,却呈现出因人种而不同的治疗结果,我们必须重新来审视这种地域和人种之间的差异。未来的研究甚至可能会显示,免疫治疗针对中国食管癌高发和低发地区患者,或在南方和北方患者人群中都会存在疗效差异。
所以我觉得KEYNOTE-181既证实了PD-1单抗对于食管癌,特别是PD-L1高表达人群的疗效,也证实了东西方人种对免疫治疗之间的疗效差异。但最重要的就是它让我们重新客观地来看食管癌在全球地域分布上的差异。我觉得KEYNOTE-181在这一方面的贡献应该比它本身验证一个药物的疗效的意义要更大。
国内的食管癌手术治疗目前面临哪些困境?
沈琳教授:包括食管癌在内的消化道肿瘤目前多还是以手术治疗为主,手术也是一个目前公认的最有可能带来食管癌治愈的一个手段。但是食管癌有特殊性,它的局部的浸润的能力非常强,而食管的周围是包括像大动脉、支气管和肺这样的重要脏器,还有大量的淋巴结等等。食管癌局部浸润这些脏器都是影响手术疗效和/或者不能进行手术的一个重要的原因。
另外,国内食管癌的发病部位可能特别高,有的在食管上段16~18公分,如果手术的话,就相当于切喉癌一样;所以,对于这样的患者只能实施以放疗为主的综合治疗。因此,食管癌的不同部位、不同类型、不同分期都会直接影响到手术的选择和手术的效果。而我国患者70%在发现时已处于局部晚期或发生转移,这类患者还经常容易发生合并症,比如大出血、瘘,感染等等。
所以食管癌治疗很复杂,需要放疗、外科、影像、心理、营养内科的共同参与,缺一不可。
免疫治疗是否为开展食管癌的跨学科综合治疗带来了春天?
沈琳教授:食管癌治疗一直是,目前也仍然是以手术为主要手段。在过去近50年里,食管癌的内科治疗发展缓慢,治疗手段有限,而且疗效不尽人意。所以,在我国所有食管癌专委会里面几乎没有内科医生,也没有内科的声音。但免疫治疗药物的到来可能会带来改变,食管癌内科治疗的重要性有望凸显。
比如说当前的局部晚期食管癌,基本上都是要术前放化疗,或化疗治疗;治疗以后肿瘤缩小、病情改善了,一般状况也好些了,再去做手术;做完手术,再根据对局部复发率和远处转移概率的评估,来选择放疗。
相信帕博利珠单抗等PD-1抑制剂类药物今年在国内获批进入临床应用后,不但会在晚期食管癌治疗领域,而且在术后辅助维持治疗,术前新辅助诱导治疗,甚至在根治性放化疗后的维持治疗领域都会有巨大的临床应用空间。但这需要与外科、放疗科等学科密切合作。
我们最近在北京癌症防治学会下成立了食管癌专业委员会,联合全国高发地区的食管癌治疗专家,以内科和放疗科医生为主,就是为了促进我国食管癌的综合治疗。
[1] http://www.msd.com/newsroom/index.html
[2] http://samr.cfda.gov.cn/WS01/CL0135/
[3] Finn R S, Ryoo B-Y, Merle P et al. Results of KEYNOTE-240: Phase 3 Study of Pembrolizumab versus Best Supportive Care for Second-line Therapy in Advanced Heptocellular Carcinoma. 2019 ASCO, abstract 4004.
[4] Tabernero J, van Cutsem E, Bang Y J, et al. Pembrolizumab with or without Chemotherapy Versus Chemotherapy in Advanced G/GEJ Adenocarcinoma: The Phase 3, KEYNOTE-062 Study. 2019 ASCO, abstract LBA4007
[5] Chen J, Luo S, Qin S, et al. Pembrolizumab versus Chemotherapy in Patients with Advanced/Metastatic Adenocarcinoma or Squamous Cell Carcinoma of the Esophagus as Second-line Therapy: Analysis of the Chinese Sub-group in KEYNOTE-181. 2019 ESMO, abstract 760P.
[6] Shen L et al. 帕博利珠单抗对比化疗二线治疗晚期/转移性食管腺癌或鳞状细胞癌: KEYNOTE-181亚洲亚组分析. 2019 CSCO.
排版编辑:DD















 苏公网安备32059002004080号
苏公网安备32059002004080号


