针对分子分型较为复杂的、HR+/HER2-晚期乳腺癌患者,氟维司群已被临床试验证实疗效优于阿那曲唑,成为晚期HR+乳腺癌单药内分泌治疗的优选方案。并且,氟维司群能够通过与CDK4/6抑制剂的联合应用、进一步延长患者的生存获益。在此介绍一例HR+/HER2-晚期乳腺癌患者在一线化疗接受以后、继续氟维司群联合CDK4/6抑制剂作为维持治疗的病例。

四川省肿瘤医院乳腺外科副主任医师
中国医师协会外科医师分会乳腺外科医师委员会青年委员
中国医药教育协会乳腺癌多学科诊疗学组委员
四川省医促会乳腺肿瘤专委会常委
四川省抗癌协会肿瘤防治科普专业委员会委员
四川省抗癌协会乳腺癌专业委员会青年委员
四川省女医师协会肿瘤学专业委员会委员
JCO中文版乳腺肿瘤专刊青年编委
2015年加拿大McGill University 教学医院Jewish General Hospital进修,在国内外期刊杂志发表学术论文十余篇,参编专著一部。参加多项全国多中心乳腺癌流行病学调查及药物临床试验
基本情况
1. 患者女性,48岁。2012年10月29日因“右乳及右腋窝肿块半年,局切术后15天”入院治疗。
2. 现病史:2012年10月11日在外院行彩超检查,提示右乳包块内上肿块,约2.5 cm×2 cm,BIRADS 4B类;右腋窝淋巴结,皮髓质分界不清,转移可能。2012年10月12日在外院接受右乳及右腋窝肿块切除术。2012年10月21日的外院病理结果为:<右乳房>乳腺腺病;<右腋窝>:浸润性癌。
3. 个人史:G4P3A1,未绝经,末次月经:2012年10月25日。既往史、家族史:无特殊。
诊断过程
1. 2012年10月19日入我院的专科查体:右乳见长约5 cm手术切口,右腋窝见长约7 cm手术切口,均愈合可。右乳未扪及确切肿块,右腋窝未扪及肿大淋巴结,左侧腋窝、双侧锁上 (-)。
2. 2012年11月,我院的病理会诊结果:<右乳肿块>腺病,伴少量上皮不典型增生;<右腋窝肿块>浸润性导管癌(II级) ;免疫组化:ER (+90%) 、PR (+80%) 、CerbB2 (-) 、 Ki-67 (+90%) 、MAMAGLOBIN (+)。
3. 胸部CT、颅脑CT、腹部彩超、骨扫描等全身检查未见转移征象。
4. 初步诊断:右腋浸润性导管癌(cTxN1M0),Luminal B型(HER2阴性型)。
治疗过程
1. 根治性手术:2012年11月7日行右乳肿瘤残腔扩大切除术+右腋窝淋巴结清扫术。
l 术后病理:右乳浸润性导管癌II级,周围见导管内癌成分,右腋淋巴结13/20查见癌转移。各切缘未见癌残留。
l 免疫组化:ER(++)>80%,PR(++)>80%,HER2(0),Ki67 约10%。
l 术后病理诊断:右乳浸润性癌(pTxN3M0 ⅢC期 ),Luminal B型(HER2阴性型)
2. 术后辅助治疗方案:
l 化疗:TEC(多西他赛联合表柔比星、环磷酰胺)×6周期(2012年11月15日至 2013年3月9日 )
l 放疗:2013年开始胸部局部放疗,IMRT 50Gy/25f/5w、瘤床加量。
l 内分泌治疗:2013年放疗后至2017年7月期间,口服托瑞米芬治疗;2017年7月门诊随访时,将方案换成戈舍瑞林+托瑞米芬治疗,3个月后更换托瑞米芬为来曲唑治疗。
3. 一线进展:DFS达到5年10个月。
l 2018年08月25日患者因腰疼就诊我院门诊复查,行MRI检测发现: L1锥体右侧份骨代谢增高灶,考虑骨转移可能。
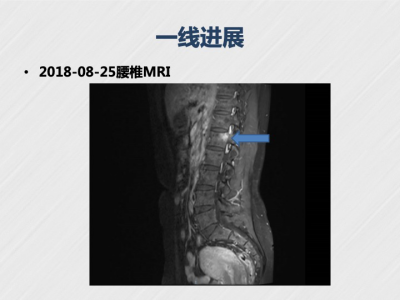
(图1: L1锥体右侧份骨代谢增高灶,考虑骨转移可能)
l 2018年08月28日骨扫描:L1椎体右侧份放射性异常浓聚,左侧髂骨放射性异常浓聚,均较前新增。
l 2018年09月04日腹部增强CT:L1椎体及附件骨质密度欠均匀,考虑转移所致。扫及左侧髂骨后份骨质密度增高影,考虑转移可能大。肝右叶散在数个斑点及低密度结节影,考虑肝转移瘤可能性大,较大者大小约为1.3 cm×1.2 cm。
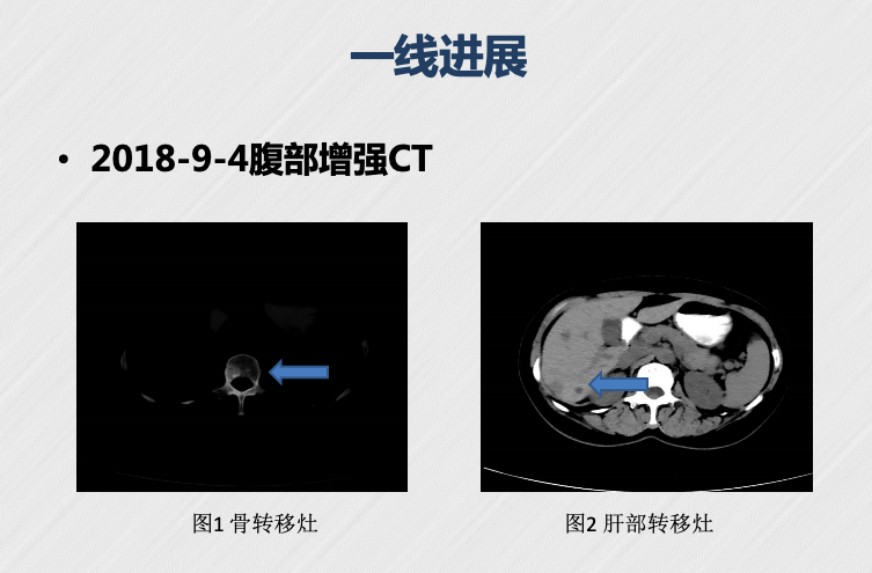
(图2: L1椎体及附件骨质密度欠均匀、肝右叶散在数个斑点及低密度结节影,考虑转移瘤可能性大)
l 其他检查:血常规、生化、胸部CT、颅脑CT未见异常
l 患者拒绝肝脏病灶穿刺活检
4. 一线治疗:
l 解救化疗:TP方案(TXT 120 mg ivgtt d1+卡铂600 mg ivgtt d1/Q21d)×6周期(2018年9月8日—2018年12月22日)
l 维持治疗:患者接受双侧卵巢切除术以后,2019年1月开始、至今接受氟维司群、CDK4/6抑制剂联合治疗。
l 其他治疗:唑来膦酸抗骨转移治疗。
l 为快速缓解症状,同时考虑患者经济原因,经与患者讨论,进行解救化疗。
5. 一线疗效评估:PFS达到13个月
2019年12月04日,增强 CT显示,L1椎体及附件骨质密度欠均匀,较2018.11.29稍明显,扫及左侧髂骨后份骨质密度增高影,均考虑骨转移所致。肝右后叶转移瘤,较前变化不明显。肝内多发小囊肿可能,部分小病灶待排其它,同前相似。疗效评估为SD。
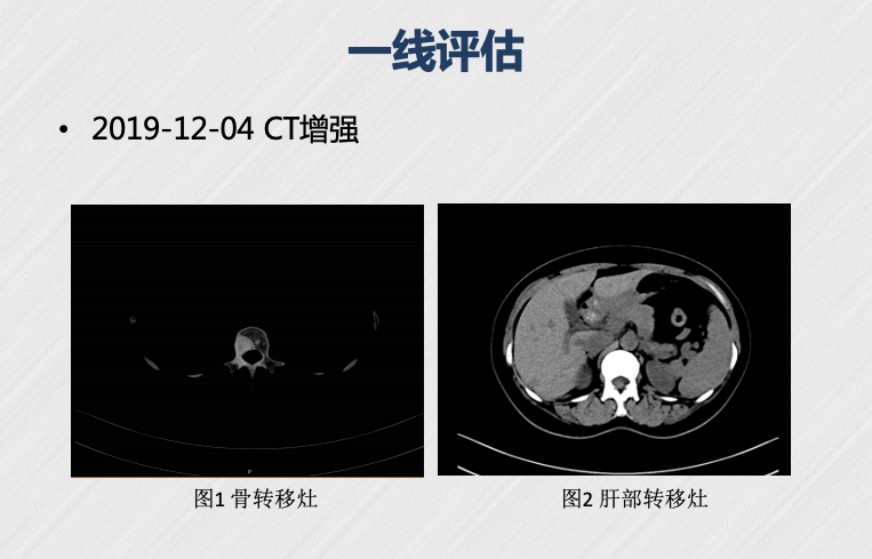
(图3: 2019年12月4日增强CT结果的疗效评估为SD,一线PFS达到13个月)
l 2019年3月15日:增强CT结果显示,L1椎体及附件骨质密度欠均匀,扫及左侧髂骨后份骨质密度增高影,范围较前类似,均考虑骨转移所致。肝右后叶转移瘤,较前变化不明显。肝内多发小囊肿可能,部分小病灶待排其它,同前相似。
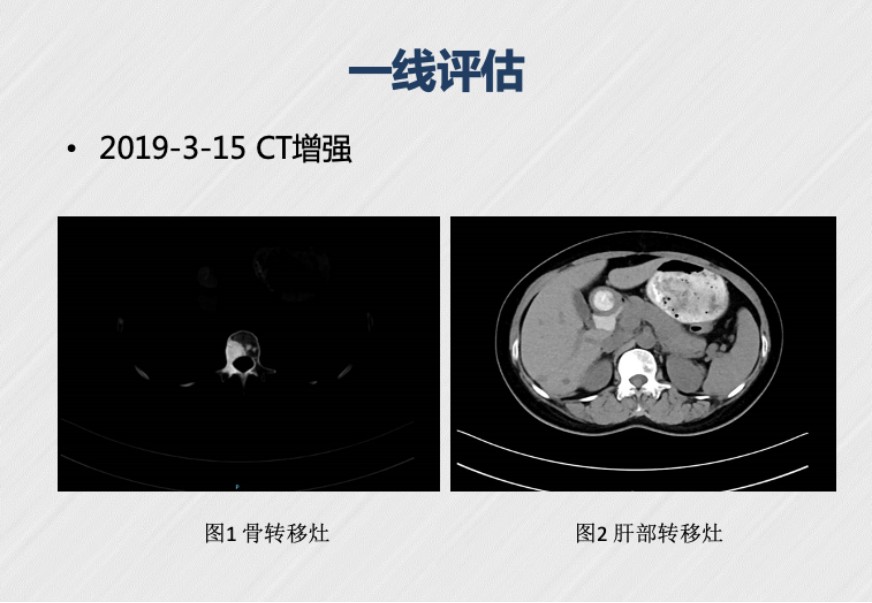
(图4: 2019年3月15日增强CT结果显示,L1椎体、肝右后叶转移瘤,较前变化不明显)
病例小结
该患者为年轻女性,月经规律。初诊为:右乳浸润性导管癌Ⅱ级(pTxN3M0,ⅢC期) Luminal B型,术后病理提示:右乳浸润性导管癌Ⅱ级,免疫组化:ER(++)>80%,PR(++)>80%,CerbB-2(0),Ki67 约10%。患者临床病例特征,包括月经状态、转移部位、病理分型、肿瘤负荷、无病生存期等多方面因素,为患者提供最优方案。

中国抗癌协会乳腺癌专业委员会委员
中国医师协会外科医师分会乳腺外科医师委员会委员
四川省抗癌协会乳腺癌专业委员会主任委四川省预防医学会乳腺癌专业委员会副主任委员
国家肿瘤质控中心乳腺癌专家委员会委员
四川省医学会乳腺病学专业委员会副主任委员
《肿瘤预防与治疗》杂志编委
该病例为未绝经的年轻患者,术前诊断为乳腺浸润性癌 I期,Luminal B(HER2 阴性型)。根治性手术切除、联合术后辅助治疗,DFS达到5年10个月。一线化疗结束后,接受氟维司群联合CDK4/6抑制剂维持治疗,目前疗效评估为SD,一线PFS达到13个月并继续维持。结合美国NCCN 2019 V3乳腺癌指南和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019年版)》分析,针对复发转移的Luminal B(HER2 阴性型)乳腺癌患者,临床医生在诊断治疗过程中需要考虑以下重要因素:
1. 针对复发转移的Luminal B(HER2 阴性型)乳腺癌患者:一线氟维司群的多重角色
根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019)》推荐,对于复发转移型HR阳性乳腺癌患者接受内分泌治疗,对于既往AI治疗失败的复发转移性Luminal B(HER2 阴性型)乳腺癌,I级推荐为氟维司群内分泌治疗或Ⅱ级推荐为氟维司群联合CDK4/6抑制剂的联合方案(均为IA类证据),均可以选择。
结合该例患者在2018年出现肝、骨转移,综合分析患者年龄、身体状况和病理结果,对于年轻且多发转移的HR+/HER2-乳腺癌患者(无内脏危象),2018版 CSCO指南推荐内分泌治疗。但是,一线非甾体类AI治疗失败后,更换甾体类AI的mPFS基本在3个月以内,难以维持较长的生存获益。其II级推荐为内分泌治疗联合CDK4/6抑制剂、或者氟维司群联合CDK4/6抑制剂治疗(均为IA类证据)。但因为患者考虑到经济压力过大,经治医生与患者结合实际与经治医生商议后,考虑先行化疗,后续行解救内分泌维持治疗。
首先,氟维司群能够作为晚期复发型乳腺癌患者的一线治疗。既往的FIRST研究显示,氟维司群500 mg能够比阿那曲唑、更能延长晚期乳腺癌患者的总生存期[1]。FIRST研究纳入既往未经治疗的绝经后激素受体阳性、局部晚期或转移性乳腺癌患者,接受氟维司群500 mg(第0,14,28天,此后每28天一次)或阿那曲唑1 mg/日。氟维司群500 mg对比阿那曲唑OS风险比为0.70(P = 0.04),中位OS分别为54.1个月和48.4个月。
其次,氟维司群能够作为晚期乳腺癌患者在一线治疗后的维持治疗方案。在2017年的ASCO会议上,来自中山大学肿瘤防治中心的王树森教授作为PI、汇报了FANCY研究的结果[2]。FANCY研究结果显示,适合化疗的HR+/HER2-晚期乳腺癌患者,在一线化疗结束后后、继续氟维司群维持治疗,其临床获益率达到76%,中位PFS为16.1个月,而若从化疗算起,中位PFS为19.5个月,最长PFS近60个月。
由此可见,氟维司群在HR阳性的晚期乳腺癌患者的不同治疗过程中、均扮演着重要的角色。
2. 氟维司群联合 CDK4/6抑制剂:多重作用机制协同抗肿瘤,可显著提高生存获益
通过协同不同药物的作用机制,新型靶向内分泌药物CDK4/6抑制剂联合氟维司群方案、在理论上也能显著提高患者的生存获益。在这一方面,PALOMA-3 研究最先证明了该联合方案对于晚期HR+/HER2-转移性乳腺癌的有效性。PALOMA-3研究纳入了针对既往内分泌治疗失败的、激素受体阳性、HER2 阴性的晚期乳腺癌患者,对比了氟维司群联合CDK4/6抑制剂、或者氟维司群联合安慰剂的疗效与安全性。其中期分析结果、总生存数据分别于2015年[3] 、2018年[4]发表于《新英格兰医学杂志》(NEJM)。中期分析显示,较单用氟维司群相比,氟维司群联合CDK4/6抑制剂、能够显著延长中位PFS (分别为9.2 个月、3.8 个月)(风险比0.42; 95% CI, 0.32 ~ 0.56; P < 0.001);研究组和对照组的中位OS分别为34.9 个月(95% CI 28.8 ~ 40.0)、28.0个月 (95% CI, 23.6 ~ 34.6)(风险比 0.81; 95% CI, 0.64 ~ 1.03; P = 0.09)。并且,2019年发表在《柳叶刀》(The Lancet)上的荟萃分析显示,对于HR+/HER2-晚期乳腺癌患者,CDK4/6抑制剂联合内分泌治疗能够带来的PFS获益明显优于传统内分泌治疗,优于任何方案化疗,因此成为该类患者的首选一线或二线治疗方案。
对于绝经后和绝经前这两种不同状态,氟维司群联合 CDK4/6抑制剂的疗效也分别在MONALEESA-3研究[5]、MONALEESA-7[6]研究中得到证实。MONALEESA-3研究的亚组分析显示,氟维司群单药治疗组达到了18.3个月的无进展生存期,印证了此前在FIRST和FALCON等研究中的结果;更为重要的是,氟维司群联合 CDK4/6抑制剂方案显著延长患者的中位PFS达到20.5个月(对照氟维司群单药组为12.8个月)(风险比0.593; 95% CI, 0.480 ~ 0.732; P < 0.001)。
因此,氟维司群是目前治疗HR阳性乳腺癌的首选内分泌单药,其更大价值在于能够通过联合CDK4/6抑制剂、进一步显著延长患者的生存获益。结合该患者,一线治疗PFS已经达到13个月,期待患者通过氟维司群联合CDK4/6抑制剂继续获益。
[1] Ellis MJ, Llombart-Cussac A, Feltl D et al. Fulvestrant 500 mg Versus Anastrozole 1 mg for the First-Line Treatment of Advanced Breast Cancer: Overall Survival Analysis From the Phase II FIRST Study. JCO 2015; 33(32):3781–3787.
[2] Wang S, Zheng Q, Xu F et al. Fulvestrant as maintenance therapy after first-line chemotherapy in patients with hormone receptor-positive, HER2-negative advanced breast cancer (FANCY), a prospective, multicenter, single arm phase 2 study. JCO 2017; 35(15_suppl):1066–1066.
[3] Turner NC, Ro J, André F et al. Palbociclib in Hormone-Receptor–Positive Advanced Breast Cancer. New England Journal of Medicine 2015; 373(3):209–219.
[4] Turner NC, Slamon DJ, Ro J et al. Overall Survival with Palbociclib and Fulvestrant in Advanced Breast Cancer. New England Journal of Medicine 2018; 379(20):1926–1936.
[5] Slamon DJ, Neven P, Chia S et al. Phase III Randomized Study of Ribociclib and Fulvestrant in Hormone Receptor–Positive, Human Epidermal Growth Factor Receptor 2–Negative Advanced Breast Cancer: MONALEESA-3. JCO 2018; 36(24):2465–2472.
[6] Im S-A, Lu Y-S, Bardia A et al. Overall Survival with Ribociclib plus Endocrine Therapy in Breast Cancer. New England Journal of Medicine 2019; 381(4):307–316.
排版编辑:肿瘤资讯-frank















 苏公网安备32059002004080号
苏公网安备32059002004080号


