徐峥的新作“我不是药神”可谓是国产片的佳作,点映期间就好评如潮,此处为他的电影默默打call。这本影片让人们了解了慢性粒细胞性白血病(CML)这一类人群,剧中治疗CML的神药“格列宁”,其实就是临床被广泛应用的伊马替尼(商品名:格列卫)。
伊马替尼在血液科的丰功伟绩不必多说,但请注意,伊马替尼并不是血液科的专利,它同样是胃肠道间质瘤(gastrointestinal stromal tumor,GIST)的特效药。本期,就让Frank蹭着电影的热度,带你看电影,长知识,说说伊马替尼拯救GIST的故事,揭开GIST的神秘面纱。
潜伏水底的大白鲨
GIST是胃肠道最常见的间叶源性肿瘤
2017版中国胃肠间质瘤诊断治疗共识对GIST的定义如下:GIST 是胃肠道最常见的间叶源性肿瘤,在生物学行为上可从良性至恶性,免疫组化检测通常表达CD117 和DOG1 阳性,显示卡哈尔细胞(Cajal cell)分化,大多数病例具有c-kit 或血小板源性生长因子受体α多肽(platelet derived growth factorreceptor alpha,PDGFRA)基因活化突变。
针对定义的关键词,作如下解读:
什么是间叶源性肿瘤?
胃肠道间叶细胞又称间充质细胞,源于中胚层,广泛存在于胃肠道管壁的各层组织中,包括粘膜层、粘膜下层、肌层、浆膜层及其系膜。间叶源性的肿瘤有良恶性之分,恶性的间叶源性肿瘤,又称为肉瘤。它不同于我们平时熟知的癌,癌在病理学上的定义为,起源于上皮组织的恶性肿瘤。
什么是Cajal细胞?
Cajal细胞呈网状结构分布于胃肠道的肌层之间,是胃肠道慢波活动(基本电节律)的起搏点,调节内脏的运动,参与胃肠道肿瘤的发病机制。该细胞是胃肠道中惟一表达c-Kit和CD34的细胞,而胃肠道间质瘤也同时表达上述表型,因此,GIST的细胞起源考虑起源于Cajal细胞。
免疫组化是诊断GIST的重要标准
KIT(CD117)是c-kit基因的产物,在GIST中表达率约为85%。CD117除在CD34阳性GIST中表达外,在一些CD34阴性GIST中也有表达,而在真正的平滑肌瘤和神经鞘瘤的胃肠道及外周均不表达,因此CD117的表达也可以将GIST同真正的平滑肌瘤和神经鞘瘤分开。
DOG1的功能是为钙离子激活的离子通道,在形成胃肠道基本电节律过程中发挥着重要作用。文献报道DOG1在GIST中的表达率可达90%~95%,且表达不依赖于KIT或PDGFRA基因的突变状态。不同的DOG1抗体将在整个胃肠道的Cajal细胞一致染色,帮助围绕肠神经丛的神经节细胞延伸的众多薄胞质突起显影,它们还染色增生的Cajal 细胞。与此相反,在其他正常的间充质细胞中未检测到 DOG1的表达。因此,有助于鉴别GIST。
c-kit 或PDGFRA突变是伊马替尼治疗GIST的理论基础
GIST发生的中心事件是 C-kit和 PDGFRa获得功能性突变,所以基因检测是诊断GIST的重要依据,同时也是靶向药物伊马替尼治疗GIST的理论依据。大部分患者往往存在c-kit 或PDGFRA突变。
c-kit是一种跨膜生长因子,属于酪氨酸激酶受体TKR家族的成员,通过诱导细胞外区的分子构象发生变化激活下游的信号传导通路,最终导致基因突变,包括缺失、插入、错义、点突变等,最终引起细胞的癌变。
PDGFRA基因定位与c-Kit极为相近,同属Ⅲ型酪氨酸蛋白激酶家族,当PDGFRα与配体PDGF结合后可激发酪氨酸残基磷酸化,从而调节细胞的生长、增殖、黏附、转移、分化和凋亡,最终引起细胞的癌变。
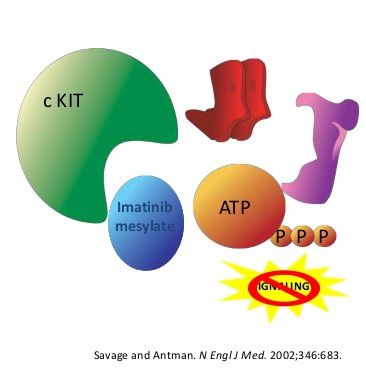 伊马替尼(imatinib)作为酪氨酸激酶抑制剂,抑制其酪氨酸激酶活性,使酪氨酸残基不能磷酸化,从而抑制其细胞信号传导途径,进一步抑制c-kit和PDGFRA,使其一跃成为了治疗GIST的特效药物。
伊马替尼(imatinib)作为酪氨酸激酶抑制剂,抑制其酪氨酸激酶活性,使酪氨酸残基不能磷酸化,从而抑制其细胞信号传导途径,进一步抑制c-kit和PDGFRA,使其一跃成为了治疗GIST的特效药物。
争做临床的夏洛克——GIST的诊断
临床表现缺乏特异性
GIST在临床表现上缺乏特异性,症状与肿瘤的部位、大小和生长方式有关,最常见的症状是腹部隐痛不适,50%-70%的患者腹部可触及包块,浸润到消化腔道内表现为溃疡或出血,大约1/3的患者可出现胃肠道出血。
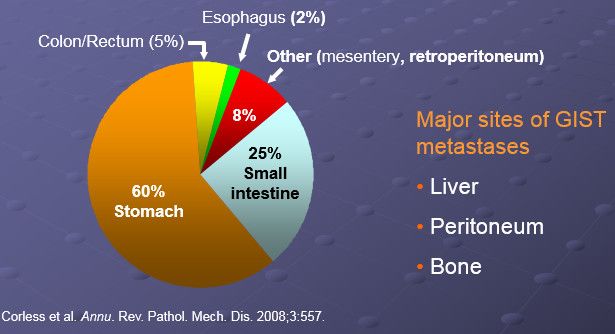
早期发现,对后期诊疗至关重要。GIST好发于40岁以上中老年患者,发生率与性别无关。原发于胃壁者占绝大多数(约60-70%),小肠次之(约20%-30%)。
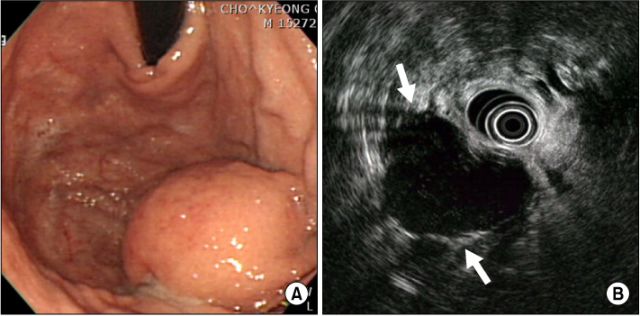
如虎添翼——“双镜组合”胃镜+超声内镜诊断粘膜下隆起病变
胃镜是重要的筛查手段,因为GIST是潜伏在粘膜下的大白鲨,内镜下只是单纯表现为粘膜下隆起,此时,需要结合患者特点,重点排除粘膜下肿瘤(submucosal tumor,SMT),而GIST属于SMT中发病率最高的类型,内镜下特征性病变主要包括:①伴有桥样皱襞形成的粘膜隆起型病变;②伴有顶端小凹陷(delle);③顶端伴有溃疡形成。
近年来兴起的超声内镜,犹如为胃镜装上了透视眼,是诊断SMT最重要手段,可仔细观察粘膜下病变,测量大小,甚至在超声导引下穿刺活检,明确诊断。
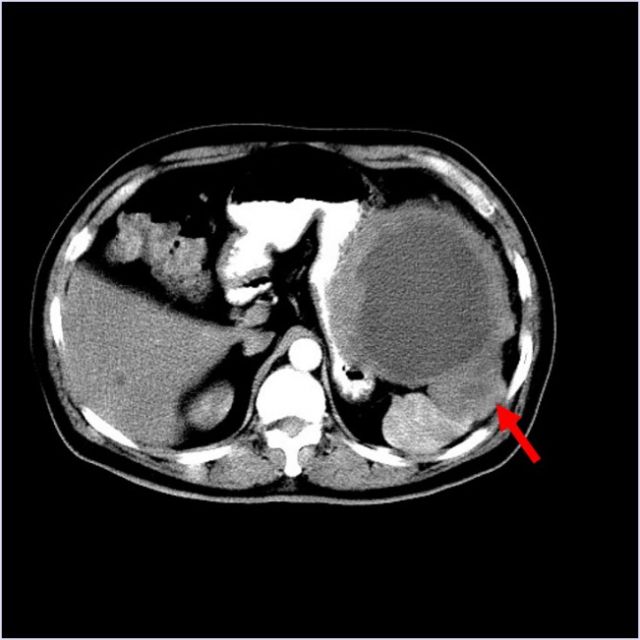
 同时,腹部增强CT对了解患者胃外及腹腔情况,了解是否有远处转移,至关重要。
同时,腹部增强CT对了解患者胃外及腹腔情况,了解是否有远处转移,至关重要。
金标准——“双子星”病理+免疫组化
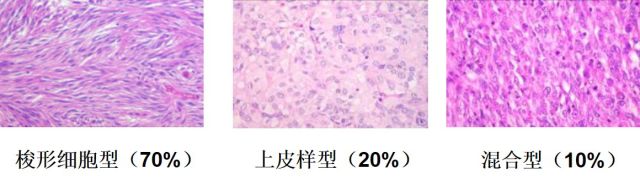
组织学上,依据瘤细胞的形态可将GIST 分为3 大类:梭形细胞型(70%)、上皮样细胞型(20%)及梭形细胞—上皮样细胞混合型(10%)。
 前面提及的CD117、DOG1免疫组化标记是GIST重要的诊断依据。关于病理诊断思路,指南给出了如下流程,由此可见“双子星”的重要地位。
前面提及的CD117、DOG1免疫组化标记是GIST重要的诊断依据。关于病理诊断思路,指南给出了如下流程,由此可见“双子星”的重要地位。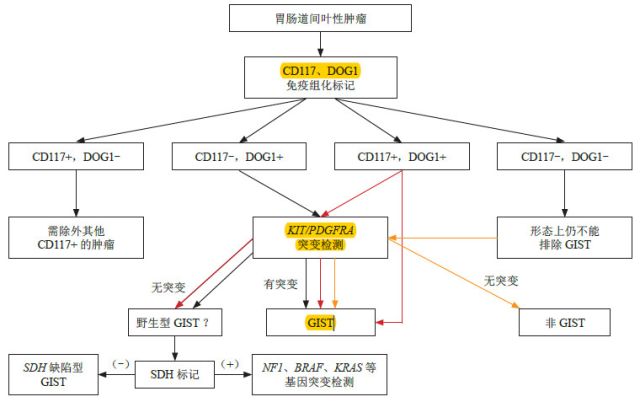
因基因检测费用相对昂贵,而大部分GIST患者都存在c-kit 或PDGFRA突变,因此伊马替尼是其治疗的特效药物。然而对下列患者,指南推荐其行基因检测:

双管齐下
手术治疗+术后危险程度评估至关重要
外科手术治疗是GIST的唯一根治手段,也是无转移病灶时的标准首选治疗。手术原则为要求完整切除、保证切缘阴性和避免肿瘤破裂溢出,其中肿瘤是否完全切除是独立的预后指标,GIST以血行转移为主,淋巴转移<5%,不需要常规进行淋巴清扫。对于无法切除或转移病灶,靶向治疗为一线治疗。指南推荐的具体治疗流程如下:
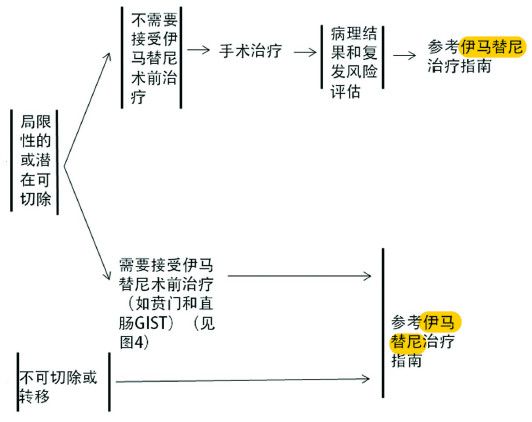
内镜下治疗尚存争议,由于多数GIST起源于固有肌层,生长方式多种多样,瘤体与周围肌层组织界限并不十分清晰,内镜下不易根治性切除,且操作并发症的发生率高(主要为出血、穿孔、瘤细胞种植等),目前尚缺乏内镜下切除GIST 的中长期安全性的对比研究,故不作为常规推荐。
原发GIST 切除术后建议常规进行危险度分级,指南给出了如下推荐意见:
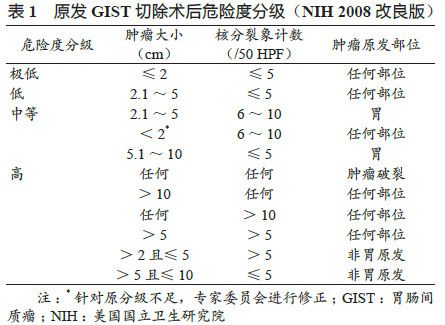 从危险度分级来看,肿瘤大小及核分裂率是评估GIST的恶性风险的重要依据,也是预测患者远期预后的重要依据。
从危险度分级来看,肿瘤大小及核分裂率是评估GIST的恶性风险的重要依据,也是预测患者远期预后的重要依据。
黑暗中的曙光
伊马替尼是GIST患者的特效救星
伊马替尼是GIST术后中高危患者的优选辅助治疗药物
针对有条件进行手术且术后病理提示为中高危的患者,指南推荐伊马替尼为首选治疗治疗药物,具体推荐意见如下:
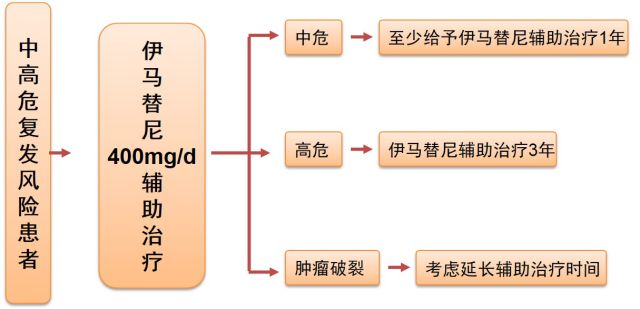
(2) 伊马替尼是转移复发/不可切除GIST患者的一线治疗药物
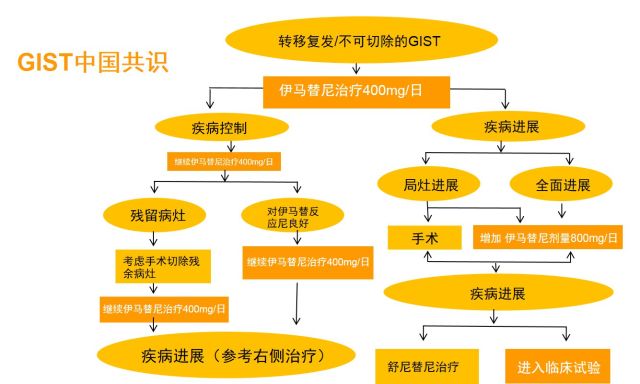
在伊马替尼没有问世之前,晚期GIST患者中位生存时间只有19个月,对常规放化疗基本无效。而伊马替尼的问世,彻底打破这一僵局,改写了指南。对于转移复发/不可切除GIST,指南推荐意见如下,靶向治疗贯穿始终,伊马替尼成为了不可替代的一线治疗药物。
B2222试验结果提示:伊马替尼可将晚期GIST患者中位总生存时间提高到57个月。
因此,伊马替尼在GIST的治疗中,特别是针对转移复发/不可切除GIST患者,是黑暗中的一束曙光,它彻底改变了GIST的常规诊疗模式,它是开启靶向治疗模式的先驱。中国意见共识针对伊马替尼的具体用法,推荐如下:
 综上所述,GIST是一条潜伏在水底的大白鲨,是胃肠道常见的间叶源性肿瘤。临床缺乏特异性表现,胃镜及超声内镜的双镜组合有助于诊断粘膜下肿瘤,腹部增强CT是评估胃外及腹腔脏器转移情况的重要手段。手术治疗是GIST的优选一线治疗,术后危险度的评级至关重要。伊马替尼的问世,彻底打破GIST治疗僵局,一跃成为GIST术后中高危患者的优选辅助治疗药物,同样也是转移复发/不可切除GIST患者的一线治疗药物。
综上所述,GIST是一条潜伏在水底的大白鲨,是胃肠道常见的间叶源性肿瘤。临床缺乏特异性表现,胃镜及超声内镜的双镜组合有助于诊断粘膜下肿瘤,腹部增强CT是评估胃外及腹腔脏器转移情况的重要手段。手术治疗是GIST的优选一线治疗,术后危险度的评级至关重要。伊马替尼的问世,彻底打破GIST治疗僵局,一跃成为GIST术后中高危患者的优选辅助治疗药物,同样也是转移复发/不可切除GIST患者的一线治疗药物。
[1] 中国临床肿瘤学会胃肠间质瘤专家委员会. 中国胃肠间质瘤诊断治疗共识(2017年版)[J]. 中国循证指南共识, 2018, 4(1):31-43.
[2] 中国胃肠道间质瘤病理专家组. 中国胃肠道间质瘤病理共识意见[J]. 中华病理学杂志, 2007, 36(10):704-707.
[3] Von Mehren, M., et al. Follow-up results after 9 years of the ongoing, phase II B2222 trial of imatinib mesylate in patients with metastatic or unresectable KIT+ gastrointestinal stromal tumors (GIST) [J]. Journal of Clinical Oncology, 2011, 29(15): 10016-10016.
[4] 郁雷, 梁小波. 胃肠道间质瘤诊治指南解读[J]. 中华结直肠疾病电子杂志, 2015(1):8-14.














 苏公网安备32059002004080号
苏公网安备32059002004080号


