肿瘤骨转移是许多晚期恶性肿瘤患者面临的严峻挑战,它不仅会引发病理性骨折等一系列骨相关事件(SREs),严重影响患者的生活质量,还常常预示着不良的预后。深入理解肿瘤骨转移的复杂生物学机制,对于开发有效的治疗与预防策略至关重要。为此,我们特别邀请到北京积水潭医院骨肿瘤科徐海荣教授,系统性地探讨肿瘤骨转移的核心机制、关键的分子通路,以及由此衍生的靶向治疗策略和免疫增效等后续研究方向。
北京积水潭医院主任医师
北京积水潭医院聊城医院执行院长
中国抗癌协会(CACA)肉瘤专业委员会
副主任委员
中国临床肿瘤学会(CSCO)肉瘤专家委员会
常务委员兼秘书长
中国抗癌协会骨与软组织肿瘤整合康复专委会副主任委员
中国医药教育协会转化医学专委会常务委员
国家卫健委能力建设和继续教育肿瘤学专家委员会委员
中国临床肿瘤学会(CSCO)理事
国际保肢学会(ISOLS)Education Committee委员
《中国骨与关节杂志》编委
《中国药物警戒》青年编委
点击观看完整视频
骨转移的流行病学与危害
谈及肿瘤骨转移,一个绕不开的经典理论便是“种子与土壤”学说。这一理论由Paget在1889年首次提出,距今已有一百多年的历史。肿瘤细胞可比作蒲公英的种子,需要离开母体,漂泊到其他地方,并且必须找到一块合适的、肥沃的“土壤”,才能生根发芽、茁壮成长。这个看似简单的比喻,精准地描述了肿瘤转移过程中肿瘤细胞(种子)与远端器官微环境(土壤)之间的选择性亲和关系。
尽管在过去的一个多世纪里,科学家们发现了众多与肿瘤转移相关的复杂机制,但“种子与土壤”学说至今仍是理解这一过程的基石理论。我们通过一个经典的动物模型实验可以直观地理解这一过程。该研究将前列腺癌的肿瘤细胞注射到实验小鼠体内,三分钟后通过影像学检查可以看到肿瘤细胞已扩散至全身,但15分钟后大部分细胞便已消失。经过20天的观察,最终只有一到两个部位(如骨盆)会形成稳定的转移灶。这表明,骨骼,尤其是像骨盆这样的部位,对于某些肿瘤细胞而言是一片特别适宜生长的“土壤”。
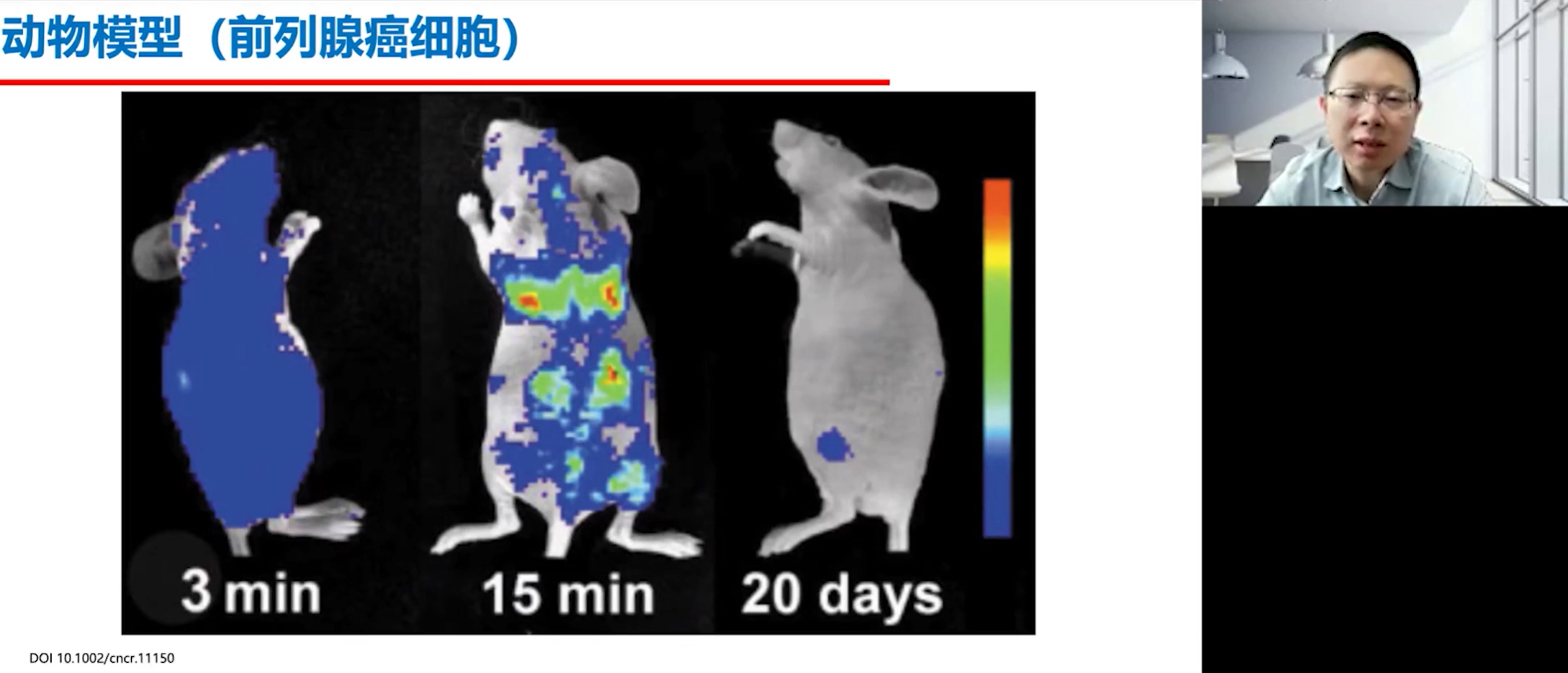
然而,肿瘤细胞的“迁徙”之旅历经千辛万苦。以肺癌为例,肿瘤细胞首先要脱离原发灶,进入血液循环,在此过程中,它必须成功逃脱免疫细胞的监视和杀伤。幸存下来的肿瘤细胞抵达骨骼这片“土壤”后,开始进行增殖。在这个过程中,肿瘤细胞与骨骼微环境发生了复杂的相互作用,特别是激活了破骨细胞并影响了成骨细胞的活动,从而开启骨破坏的进程。
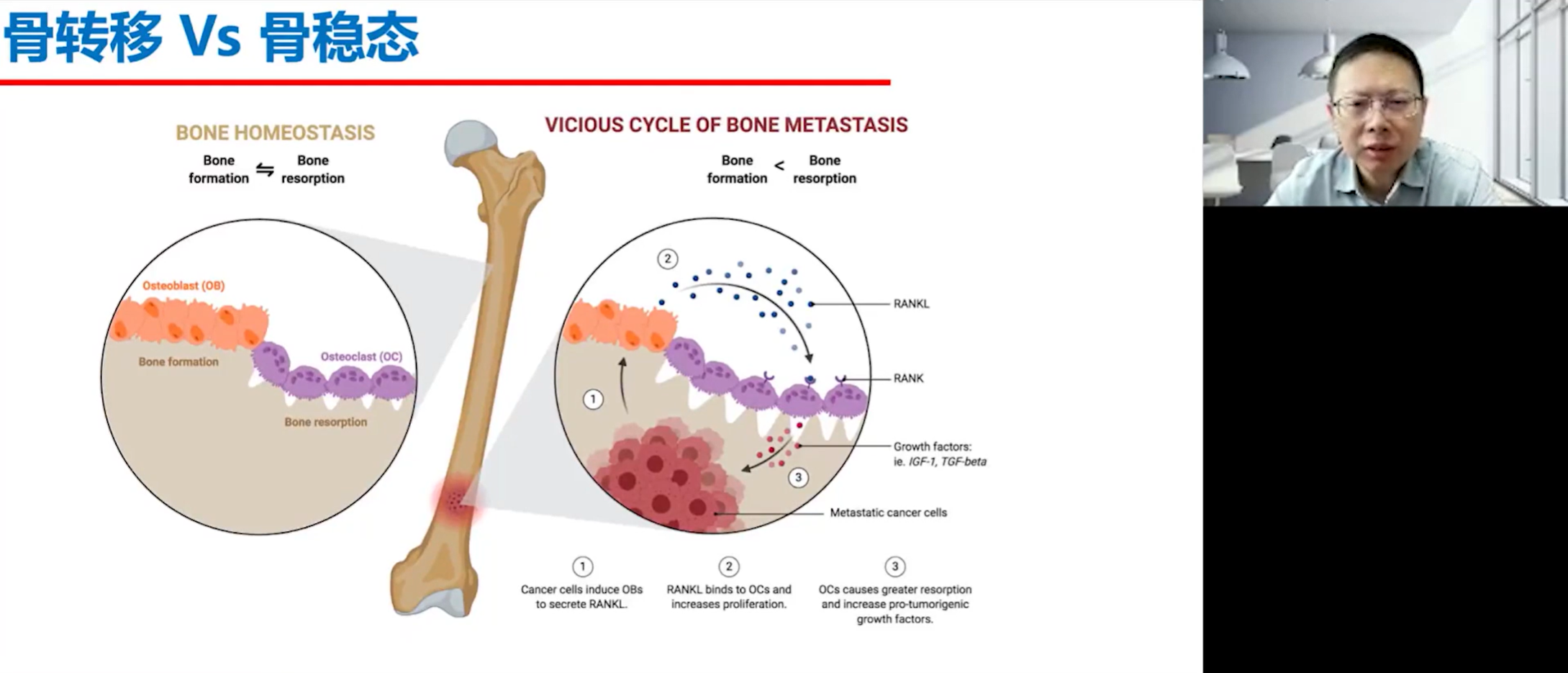
骨转移的微观核心:成骨细胞与破骨细胞的失衡
要理解肿瘤如何破坏骨骼,首先需要了解骨骼本身。从骨科医生的视角来看,骨骼的宏观结构之下,是微观层面的持续动态平衡,其核心是两种关键细胞:成骨细胞与破骨细胞。成骨细胞负责骨骼的形成与修复,而破骨细胞负责骨质的吸收与分解。正常情况下,这两种细胞的功能处于一个精密的平衡状态,维持着骨骼的健康和稳定。例如,人体的松质骨大约每三到四年会完全更新一次,而皮质骨的更新周期则更长,大约为十年。
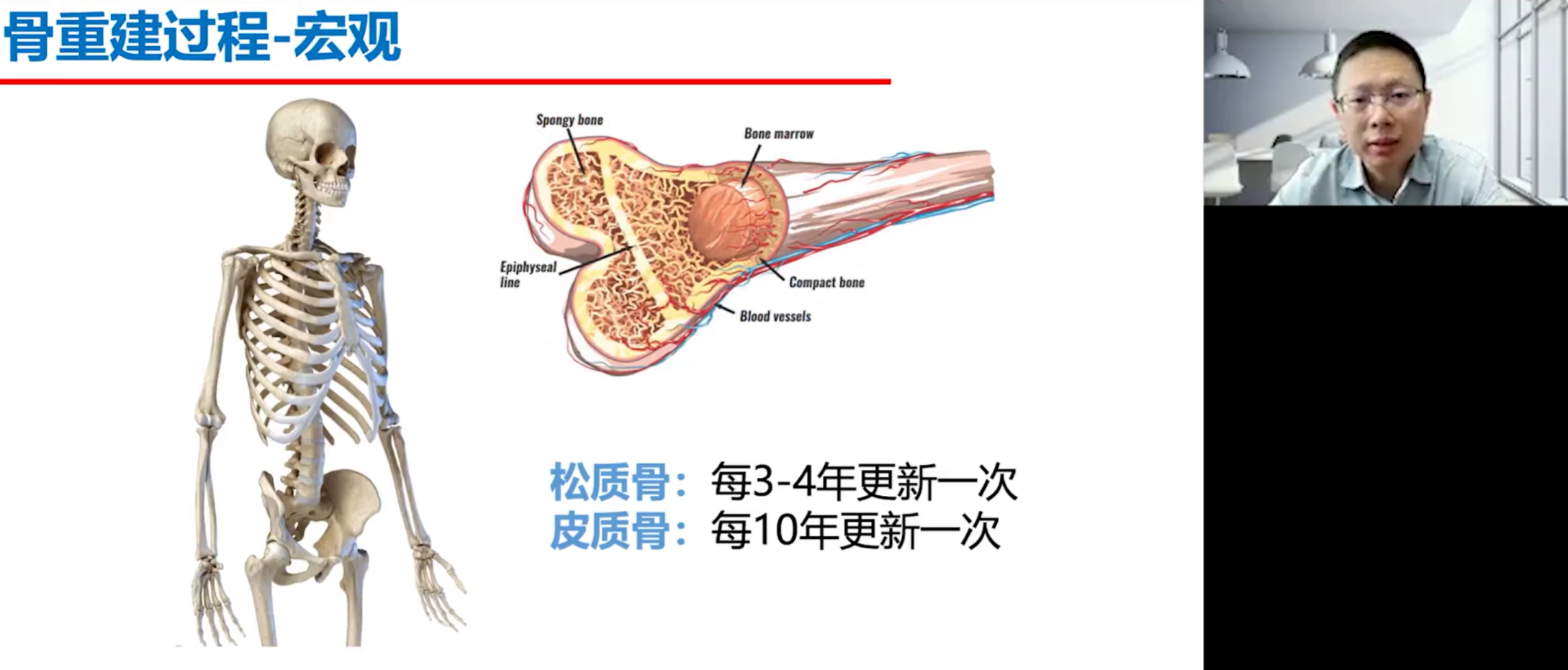
骨骼具有强大的再生能力,这得益于其微观层面的修复机制。当骨骼受到损伤时,破骨细胞会首先被招募到损伤部位,清除掉受损的组织;随后,成骨细胞会迁移过来,分泌骨样基质并最终矿化形成新的骨组织。这个过程周而复始,保障了骨骼的完整性。民间常说的“伤筋动骨一百天”,也从侧面反映了骨骼修复的周期性:破骨细胞清除骨屑的过程较快,大约需要30到40天,而成骨细胞修复重建骨骼则需要更长的时间,大约120天。
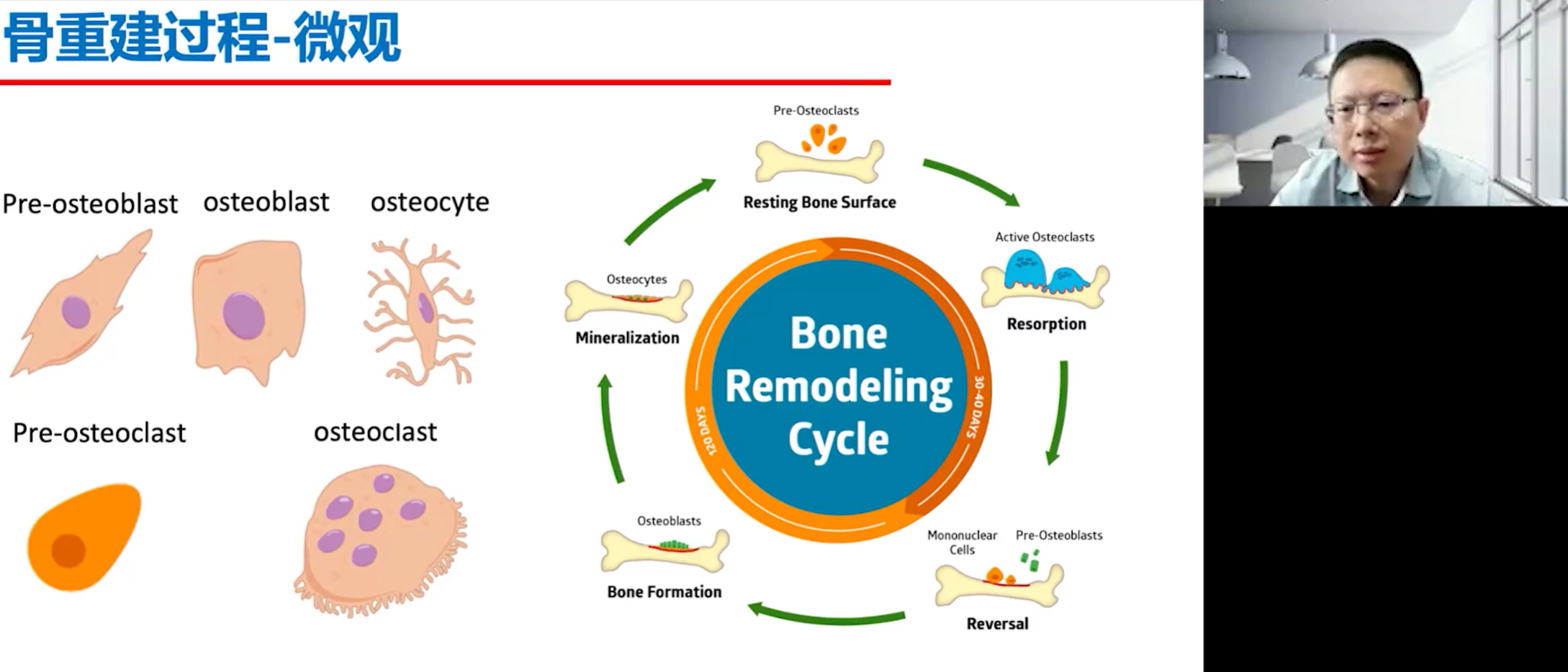
然而,当肿瘤细胞侵入骨骼后,这种精妙的平衡被彻底打破。肿瘤细胞本身并不直接破坏骨质,而是通过“劫持”并操纵成骨细胞和破骨细胞,参与到骨重塑的过程中。肿瘤细胞会分泌多种细胞因子,极大地改变骨骼的微环境,导致破骨细胞功能异常亢进,而成骨细胞的功能则相对不足或异常,最终造成骨质的溶解性破坏或成骨性病变。因此,骨转移的本质,是肿瘤细胞介导下的成骨细胞与破骨细胞功能严重失衡。
关键调控通路:RANK/RANKL/OPG的发现与功能
对骨转移机制的理解,在RANK/RANKL/OPG信号通路的发现之后取得了突破性进展。骨保护素(OPG)的发现颇具偶然性。研究人员在筛选抗肿瘤药物的过程中,从一个人类cDNA文库中发现了一种特殊的蛋白质,它在体外扩增后注射到小鼠体内,可以使小鼠的骨骼密度显著增加(影像上从黑变白),因此将其命名为骨保护素。
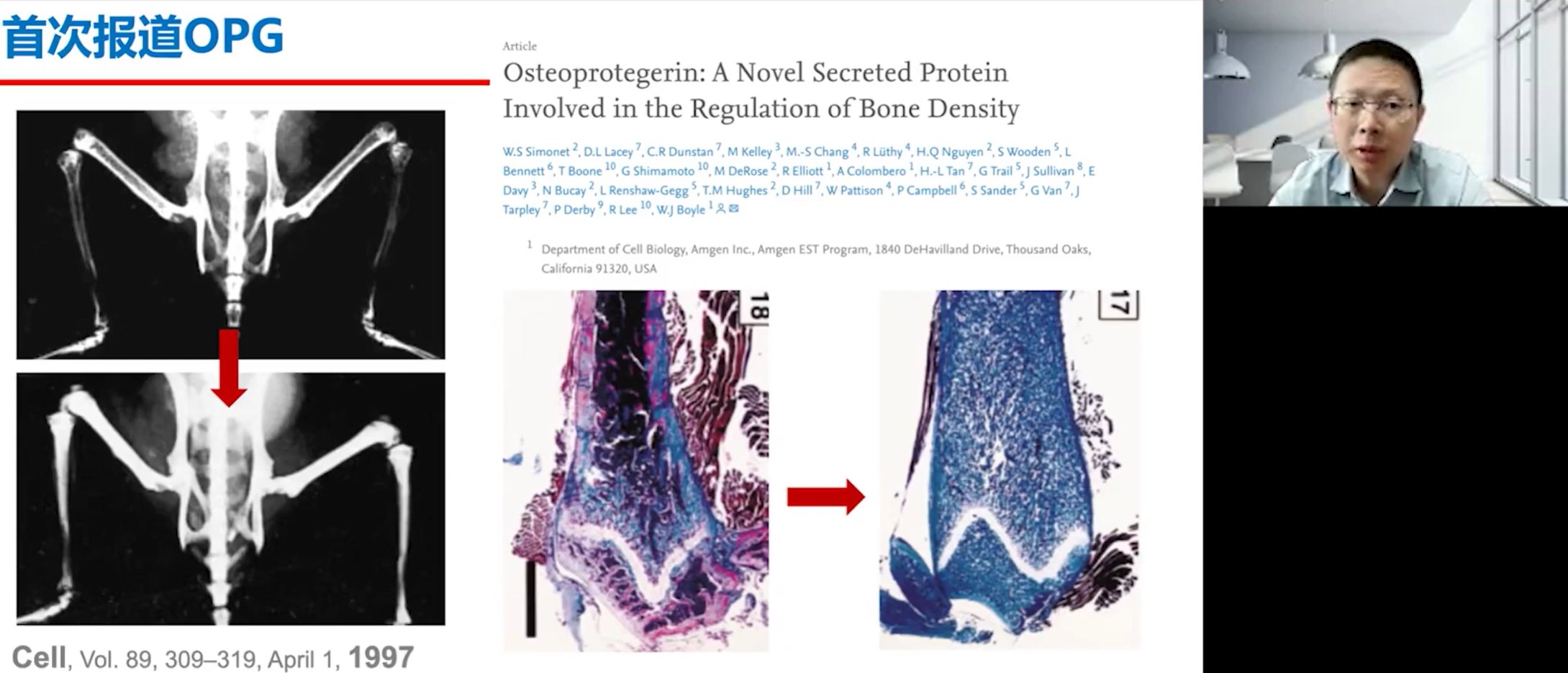
在OPG被发现之前,科学家们对成骨细胞和破骨细胞的研究已经相当深入,并基于这些研究开发了一些药物,其中最为关键的两大类是双膦酸盐和后来的单克隆抗体抑制剂。而OPG/RANK/RANKL通路的阐明,则清晰地揭示了骨重塑的精密调控机制。
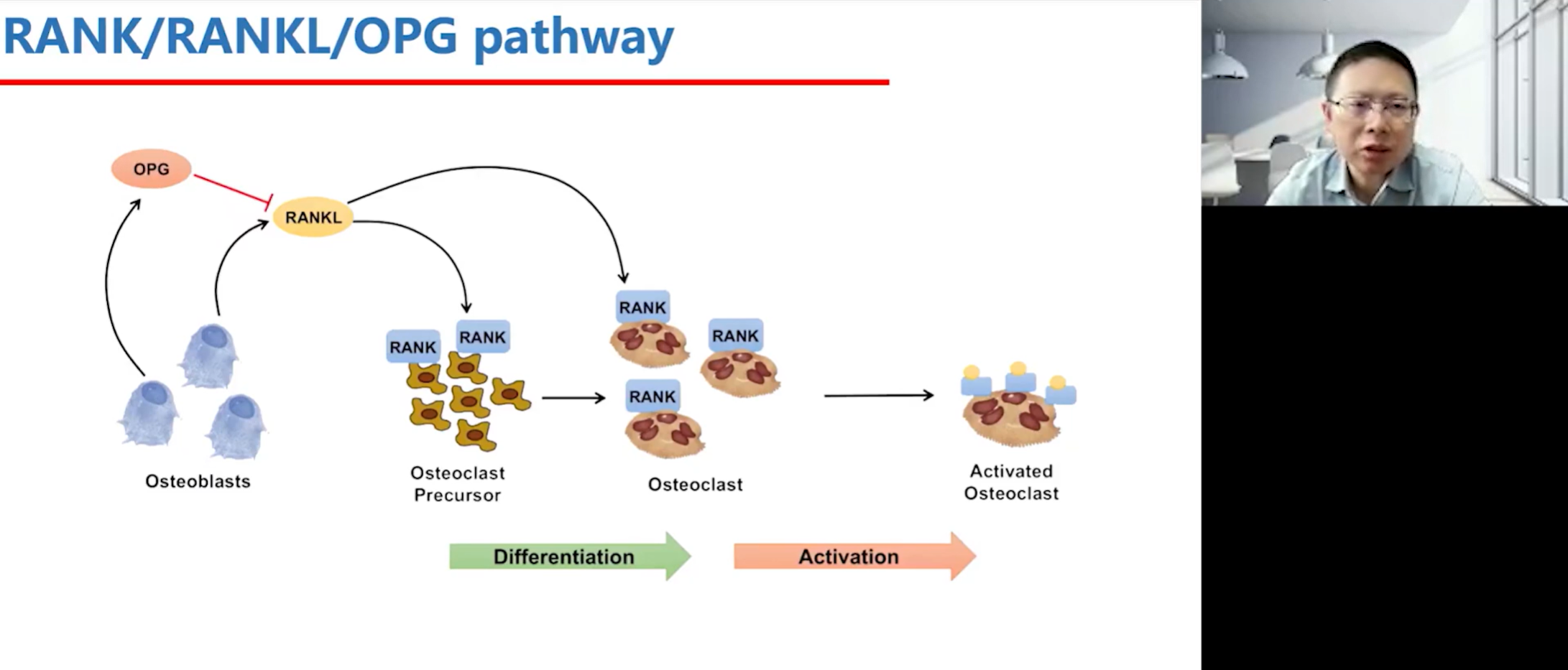
成骨细胞在骨重塑过程中扮演着“指挥官”的角色。它分泌一种名为核因子κB受体活化因子配体(RANKL)的蛋白质(可比作“油门”),RANKL会与破骨前体细胞表面的RANK受体结合,促进其分化、活化为成熟的破骨细胞,从而启动骨吸收。这是一个促进破骨细胞功能的核心信号。然而,为了防止骨吸收过程失控,成骨细胞同时也会分泌OPG(可比作“刹车”)。OPG是一种可溶性的诱骗受体,它能与RANKL结合,阻止RANKL与破骨细胞上的RANK结合,从而抑制破骨细胞的活化。因此,骨吸收的速率和程度,精确地由成骨细胞分泌的“油门”(RANKL)和“刹车”(OPG)之间的比例来决定。
肿瘤对RANKL通路的“劫持”与临床意义
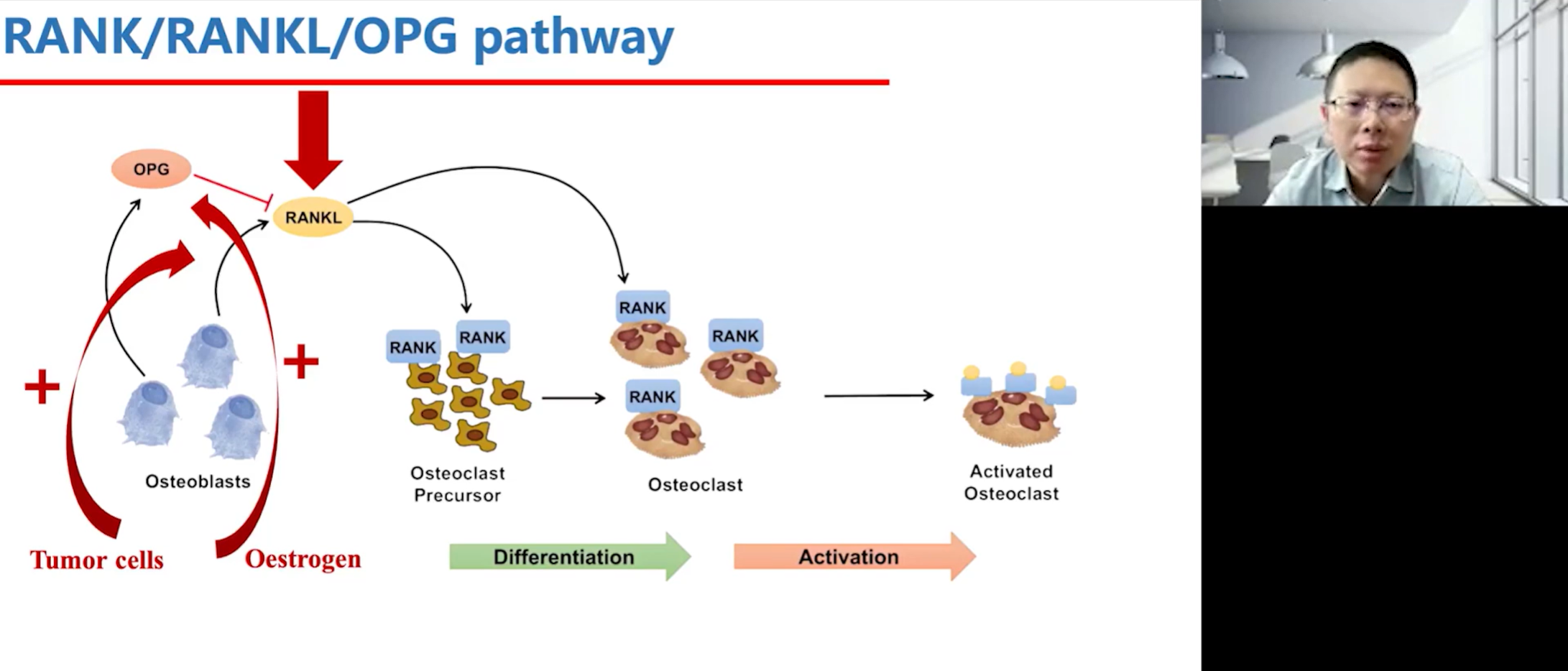
在肿瘤骨转移的病理状态下,肿瘤细胞巧妙地“劫持”了这一生理调控系统。研究发现,无论是肿瘤细胞自身,还是在肿瘤细胞诱导下的成骨细胞,都会大量分泌RANKL。这打破了原有的OPG/RANKL平衡,导致RANKL水平远超OPG,持续激活破骨细胞,引发了恶性循环式的骨破坏。此外,女性在绝经后,由于雌激素水平下降,OPG的生成会减少,RANKL的作用相对增强,这也是导致骨质疏松的原因之一,其背后的机制与肿瘤骨转移有共通之处。
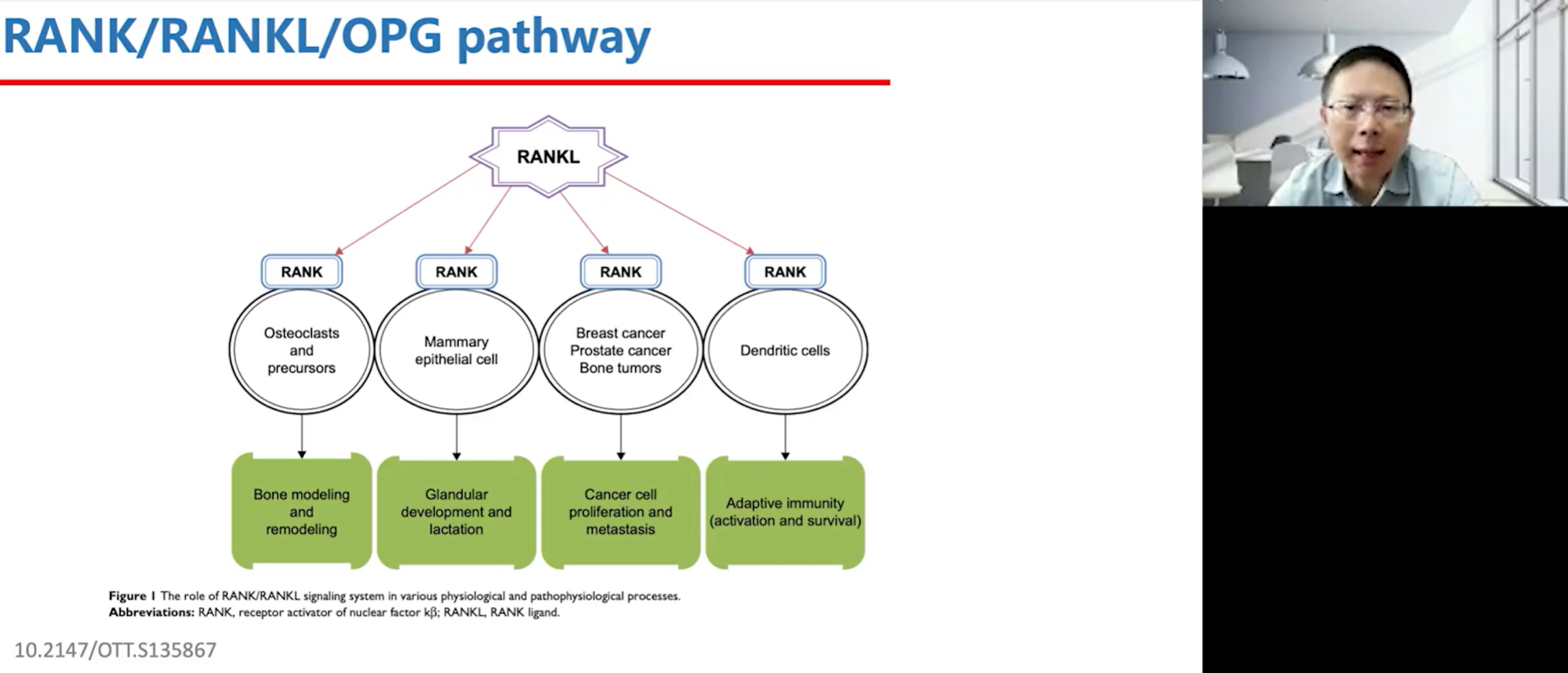
值得注意的是,RANKL通路不仅在骨骼系统中发挥作用,也与免疫系统密切相关。进一步的研究发现,许多恶性肿瘤细胞,如前列腺癌、黑色素瘤、骨肉瘤、肾癌、乳腺癌和肝癌等,其细胞表面本身就高表达RANK受体。这意味着,这些肿瘤细胞天生就带有“骨亲和性”,因为它们可以直接被骨微环境中由成骨细胞等分泌的RANKL所吸引,这为“种子与土壤”学说提供了有力的分子层面的解释。
此外,RANKL-RANK的结合不仅促进肿瘤细胞向骨骼迁移,还能通过激活下游的AKT等信号通路,促进血管生成和肿瘤细胞的迁移能力,这在划痕实验等体外研究中得到了证实。临床研究也发现,肿瘤组织中RANK表达水平高的患者,发生骨转移的时间更早,且预后也更差。在一个经典的动物实验中,研究者发现,给予小鼠OPG进行治疗,可以显著改善荷瘤小鼠的生存预后,这篇文章发表在了顶尖期刊Nature上。
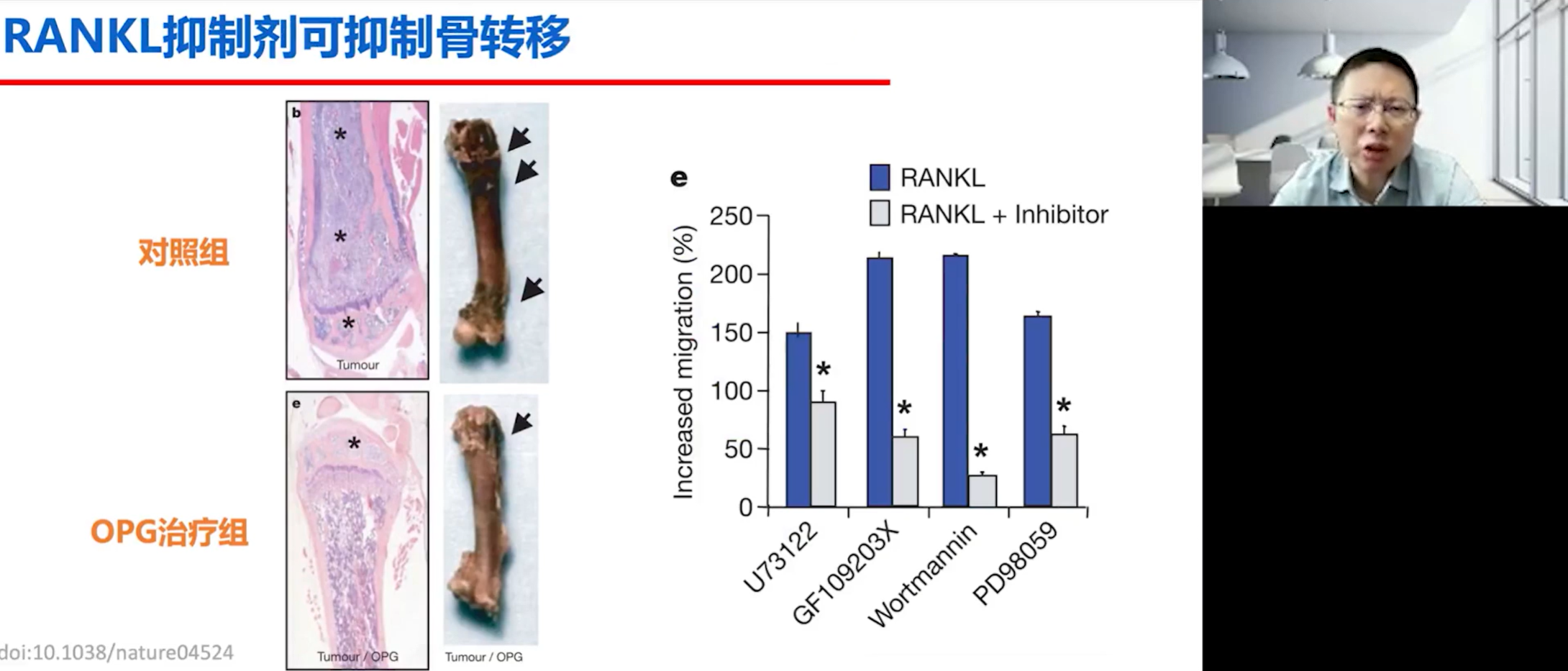
肿瘤细胞的休眠、再激活与骨靶向治疗
肿瘤细胞到达骨骼后,并非立即开始增殖,很多时候会进入一个“休眠”(arrest)状态。这也是有些患者在原发肿瘤治愈后数年甚至数十年才出现骨转移的原因。肿瘤细胞的休眠与再激活之间存在一个动态平衡。有实验表明,为骨转移动物模型注射甲状旁腺激素(PTH),可以打破这种休眠,导致肿瘤细胞疯狂增殖,骨转移迅速进展。
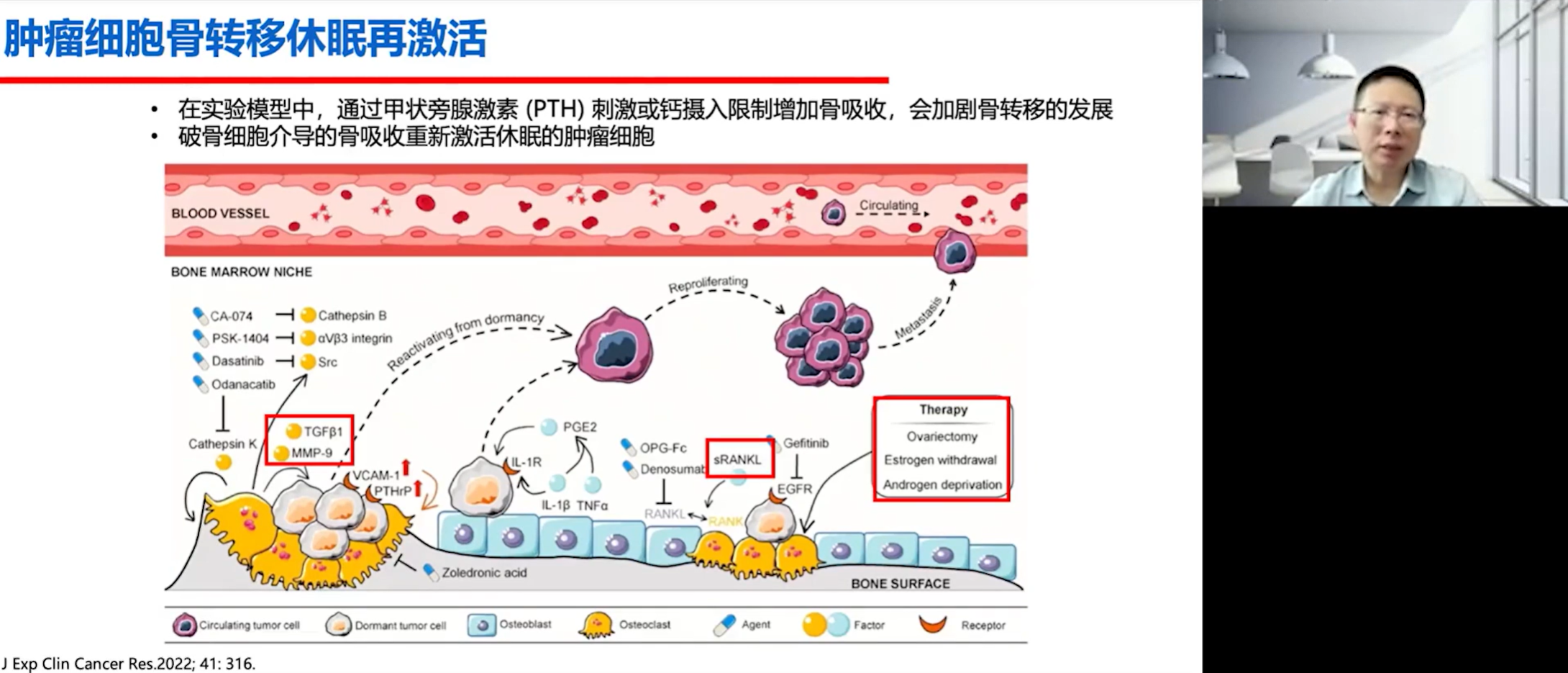
在骨转移的治疗上,一旦诊断明确,无论患者是否有疼痛等症状,都应立即启动骨靶向治疗。这是国内外所有治疗指南的共识。骨靶向药物的发展经历了从上世纪80年代开始的双膦酸盐时代,到2000年以后的地舒单抗时代。地舒单抗的III期临床研究采用随机双盲、非劣效性设计,结果显示,与双膦酸盐相比,地舒单抗能将发生SREs的风险进一步降低18%。
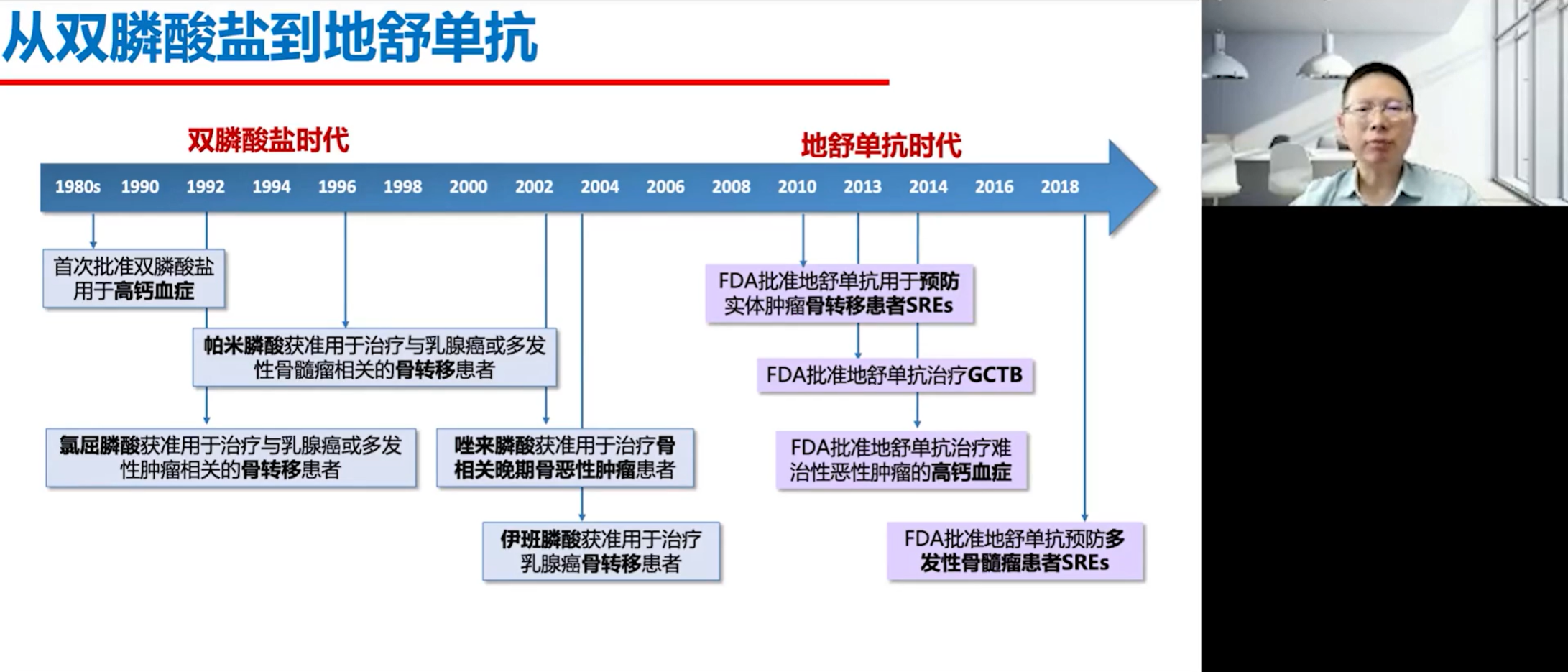
在治疗某些富含破骨细胞的肿瘤(如骨巨细胞瘤)时,地舒单抗的应用带来了革命性的变化。用药前,这类肿瘤血供极其丰富,手术极具挑战性;用药后,肿瘤组织会发生骨化,坚硬如石头,血管急剧减少,使得手术变得非常简单和安全,能够完整地切除肿瘤,并保留周围重要的神经血管。这清晰地展示了靶向抑制破骨细胞所带来的强大疗效。
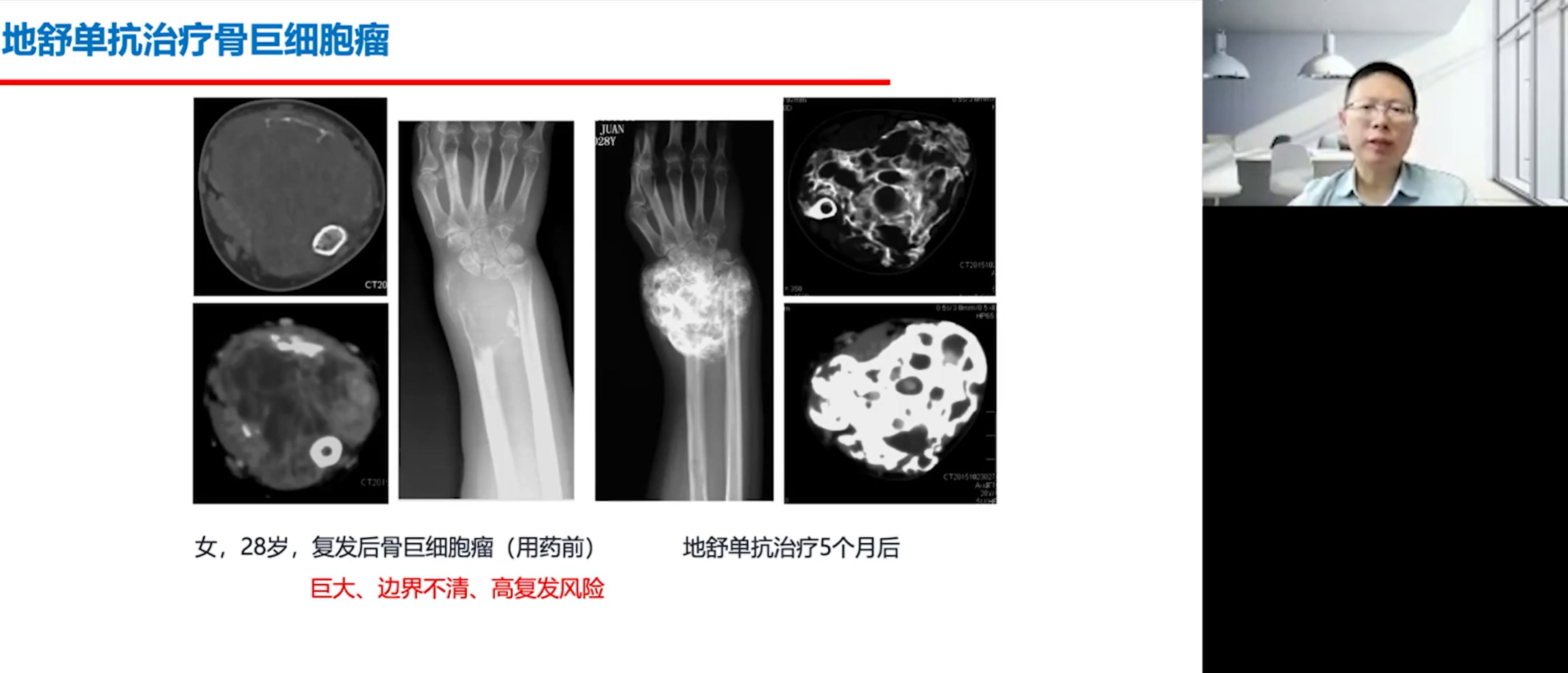
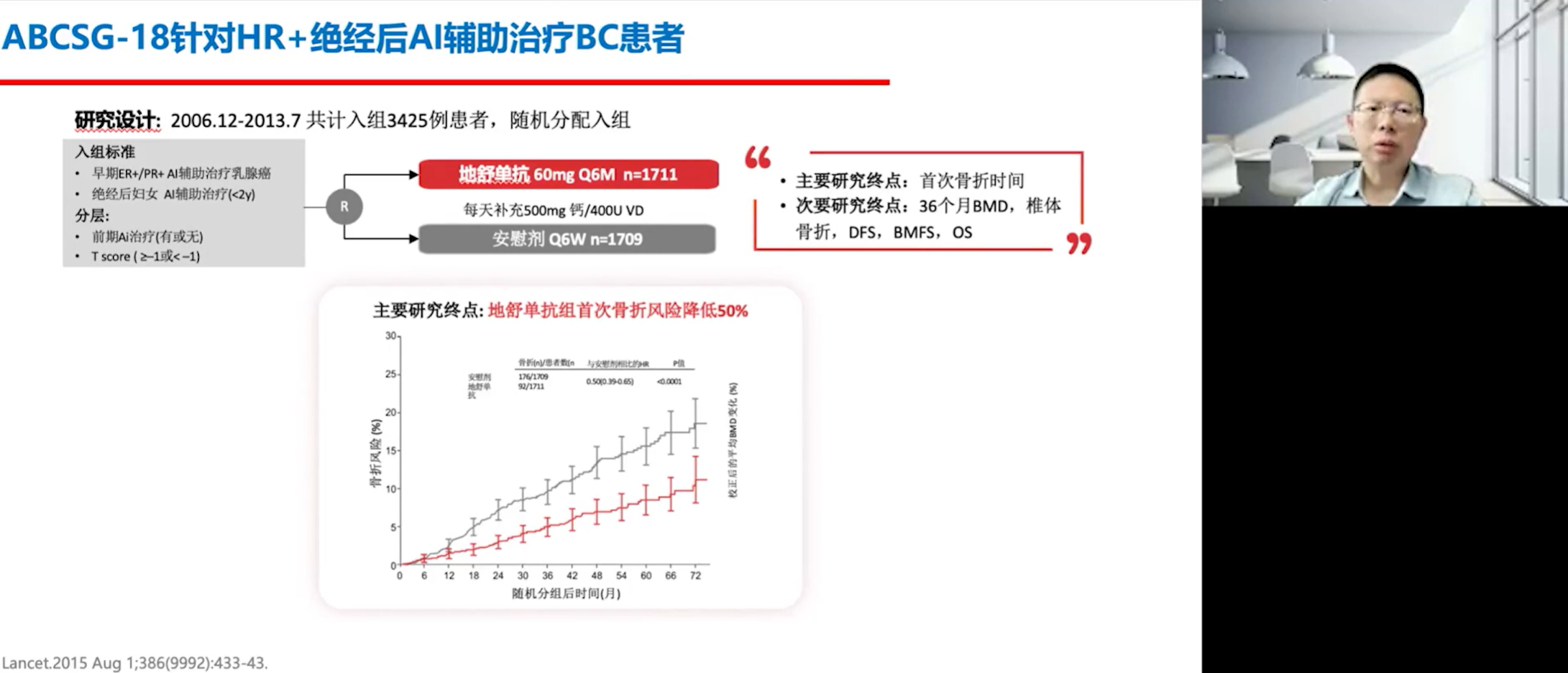
既然骨靶向药物能有效治疗骨转移,那么它能否用于预防骨转移呢?研究者们对此进行了大量探索。一项针对去势抵抗性前列腺癌患者的研究显示,地舒单抗能将骨转移生存期延长4.3个月,首次骨转移时间推迟3.7个月,结果达到了边缘显著的阳性。另一项在乳腺癌患者中开展的研究,使用了治疗骨质疏松的60毫克剂量的地舒单抗,结果发现地舒单抗组首次骨折风险降低50%。
前沿展望:骨转移微环境与免疫治疗的协同作用
在免疫治疗时代,一个严峻的临床现象日益凸显:伴有骨转移的肿瘤患者往往无法从免疫检查点抑制剂(ICI)中获得理想的生存获益,其总生存期和肿瘤缓解率均显著低于无骨转移的患者,这使得骨转移成为ICI疗效的“阿喀琉斯之踵”。近期以Cancer Cell发表的突破性研究为代表的证据链揭示了其背后的核心机制。

研究证实,骨转移病灶并非孤立的局部问题,而是一个活跃的“免疫抑制器官”。它通过RANKL信号通路过度激活破骨细胞,使其大量分泌骨桥蛋白(OPN)并释放入血。这种循环OPN能“远程遥控”,系统性地抑制骨外病灶的免疫微环境,特别是削弱了对ICI疗效至关重要的关键免疫细胞——前体耗竭性CD8+ T细胞的增殖与功能,从而导致免疫治疗的全局性失败。

这一深刻的机制阐明直接催生了精准的协同增效策略。既然RANKL是免疫抑制信号的源头,那么通过使用其特异性抑制剂地舒单抗,即可从上游阻断OPN的产生,从而逆转全身性的免疫抑制。
多项临床研究数据已初步证实了这一策略的巨大潜力:与单纯使用ICI或联合传统双膦酸盐相比,地舒单抗与ICI的联合应用能显著提升骨转移患者的无进展生存期(PFS)、总生存期(OS)和客观缓解率(ORR)。这标志着一次重要的“认知跃迁”:地舒单抗的角色已从单纯预防SREs的“骨保护剂”,转变为能够改善全身免疫微环境、与ICI协同增效的“免疫调节剂”。因此,对于接受ICI治疗的骨转移患者,起始同步联合地舒单抗有望成为新的标准治疗模式,以最大化免疫治疗的临床获益。研究发现,如果在使用免疫治疗的同时,联合使用骨转移的抑制剂(如骨靶向药物),就能够很好地抑制肿瘤在骨骼内的“作恶”,从而恢复甚至增强免疫治疗的效果。
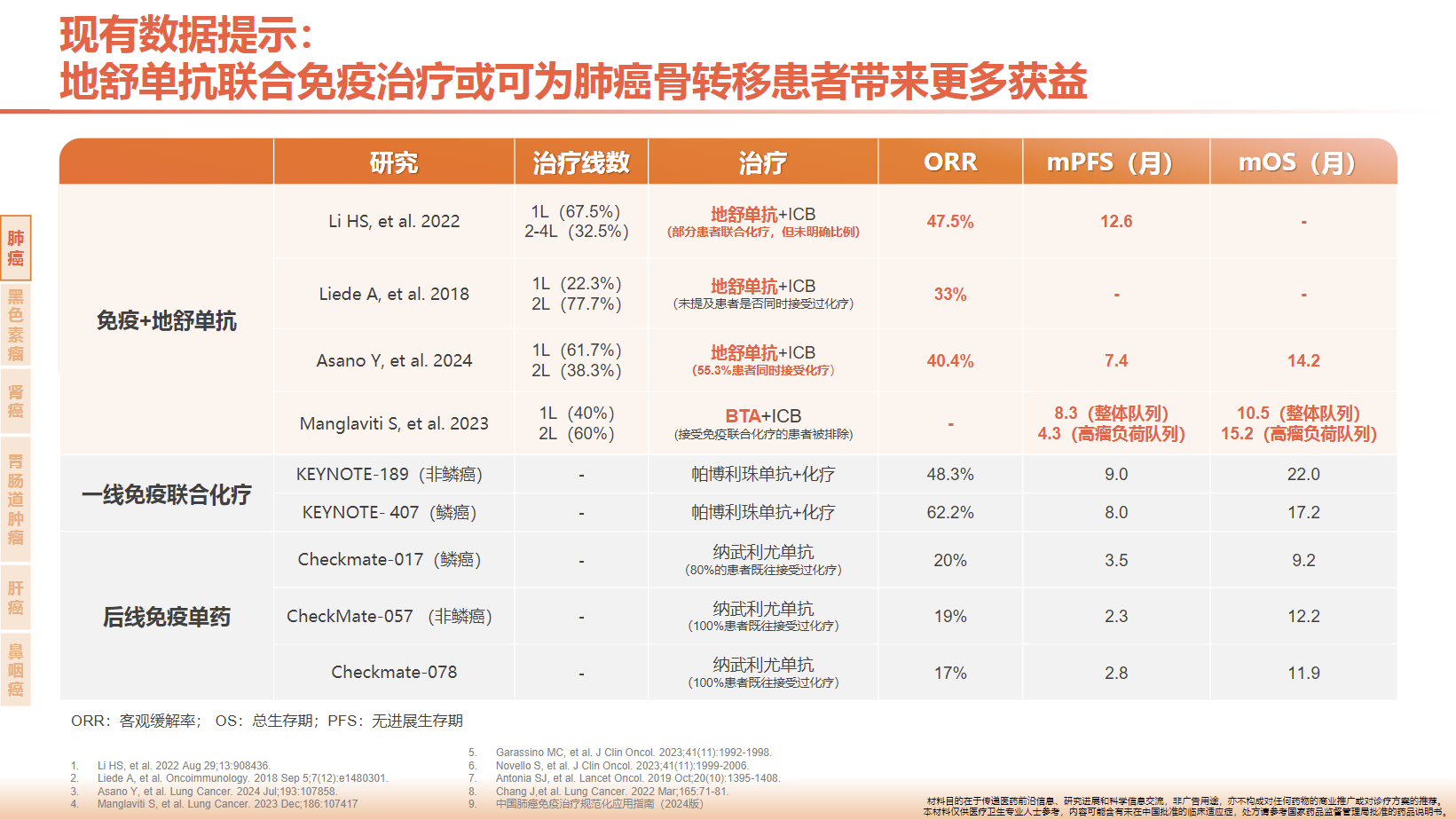
总而言之,对骨转移的研究已经从控制SREs,扩展到了与免疫治疗等前沿疗法的联合应用。这预示着未来针对肿瘤骨转移的患者,通过合理的联合治疗策略,有望带来更多的生存获益。
讨论
1. 关于地舒单抗与血钙水平的探讨:尽管临床上部分老年骨转移患者使用该药物后未出现明显的血钙紊乱,但理论上低钙血症的风险依然存在。为确保用药安全和规避风险,尤其考虑到儿童患者停药后可能出现反弹性高钙血症,规范操作上仍建议在使用该药物时常规为患者补充钙剂。
2. 地舒单抗的临床应用价值与优势:地舒单抗在治疗前列腺癌骨转移方面效果显著,尤其是在快速缓解骨痛方面作用突出,其余优点包括给药更方便(皮下注射)、对肾功能影响小以及临床疗效更优。
3. 对骨转移微环境与免疫治疗的新认知:骨转移本身可能会削弱免疫检查点抑制剂的疗效。先行使用地舒单抗等骨改良药物来修复和改善骨髓微环境,这可能为后续的免疫治疗创造更有利的条件,从而有潜力提升其整体抗肿瘤效果。
4. 跨学科协作(MDT)在骨转移治疗中的重要性:泌尿外科、骨科、肿瘤科等多学科的交流形式能带来重要收获。在处理骨相关不良事件时,应积极采用MDT模式。加强与骨外科的合作,采取综合治疗手段,对于改善患者的最终疗效和生活质量至关重要。
排版编辑:肿瘤资讯-IRIS











 苏公网安备32059002004080号
苏公网安备32059002004080号


