早期乳腺癌(EBC)患者中,手术切除后、系统治疗前的循环肿瘤DNA(ctDNA)是否和复发风险及无复发生存(RFS)相关还不清楚。近日发表一项回顾性研究,探索了系统治疗前ctDNA和EBC患者预后的相关性,发现术后单次时间点ctDNA阴性和无远处复发生存(DRFS)相关,为此类患者的系统治疗策略提供依据[1]。【肿瘤资讯】整理文章内容如下,以飨读者。

研究背景
尽管乳腺癌诊断和治疗已经取得极大进展,依旧需要更好的工具来进行局部治疗后风险分层。理想的工具应可指导个体化辅助治疗选择。目前根治性治疗后的乳腺癌随访包括体格检查和乳腺成像。目前ctDNA已经成为发现分子残留病(MRD)的无创工具,具有指导辅助治疗和监测复发的潜力。结肠癌中一项研究发现初始治疗后检出ctDNA有助于发现疾病进展高危人群[2]。提示术后ctDNA分析可能可发现需要强化治疗的高危患者。因此开展研究,评估术后ctDNA检出和RFS及DRFS的相关性,为术后MRD阳性与更差结局的相关性提供证据。
研究方法
这项回顾性原理证实研究中,行手术切除治疗乳腺癌的EBC患者(n=48)入组PlasmaDNA和ITH样本收集研究。收集手术或首诊乳腺癌时的组织标本,术前(n=31)、术后1~14周开始辅助治疗前(n=48)和完成辅助治疗后随访中(n=17)收集全血标本进行ctDNA检测,行个体化肿瘤知情多重聚合酶链式反应(mPCR)二代测序(NGS)检测,评估术后ctDNA和RFS及DRFS的相关性。
研究结果
在48例浸润性导管癌(n=39)、浸润性小叶癌(n=8)和转移性乳腺癌(n=1)患者中收集115例血浆样本。患者中位年龄50.5岁,术后中位随访60个月。
术前ctDNA检出率及相关因素
20/31例患者(65%)术前单次时间点检测到ctDNA,较高的检出率见于HER2+(100%,2/2)和三阴性乳腺癌(TNBC)(88%,7/8)疾病,其次是激素受体(HR)+/HER2-(52%,11/21)亚型(图1A)。
最高中位MTM/ml水平见于TNBC(67.3),其次是HER2+(2)和HR+/HER2-(3.5)患者(图1B)。4例接受新辅助治疗的患者中,3例术前依旧可检测到ctDNA。
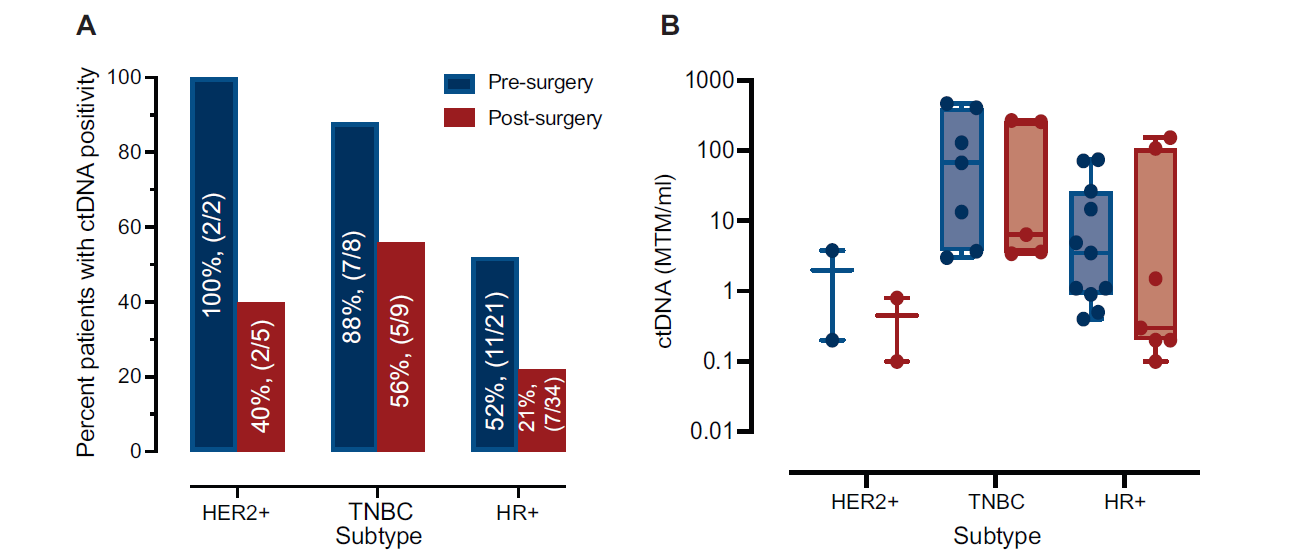
单变量分析显示术前ctDNA检出和肿瘤级别(P=0.019)相关。ctDNA检出和组织学,亚型,或淋巴结受累不相关。多变量分析中,术前ctDNA检出和亚型(P=0.01)相关,更具侵袭性的亚型如TNBC具有更高的ctDNA检出率(88%,7/8),而HR+/HER2-患者为52%(11/21)。
术后ctDNA阳性和更差生存结局相关
所有亚型术后ctDNA检出率下降(HER2+:40%[2/5],TNBC:56%[5/9],HR+:21%[7/34])(图1A)。术后(中位0.5个月)ctDNA浓度同样降低,HER2+为0.45 MTM/ml,TNBC为6.4 MTM/ml,HR+/HER2-疾病为0.3 MTM/ml(图1B)。术后ctDNA检出和组织学,肿瘤级别或淋巴结受累无相关性。术后单次时间点发现复发的阳性预测价值(PPV)是35.7%,阴性预测价值(NPV)是91.2%。
术后检出ctDNA的患者RFS劣于未检出患者,尽管未达到统计学显著性(HR 3.7,95%CI 0.9-15.7,P=0.073)(图2A)。ctDNA检出和更差的DRFS显著相关(HR 5.5,,95%CI 1-28.5,P=0.043)(图2B)。术后ctDNA检出和未检出患者的4年DRFS率分别是78% vs 97%。
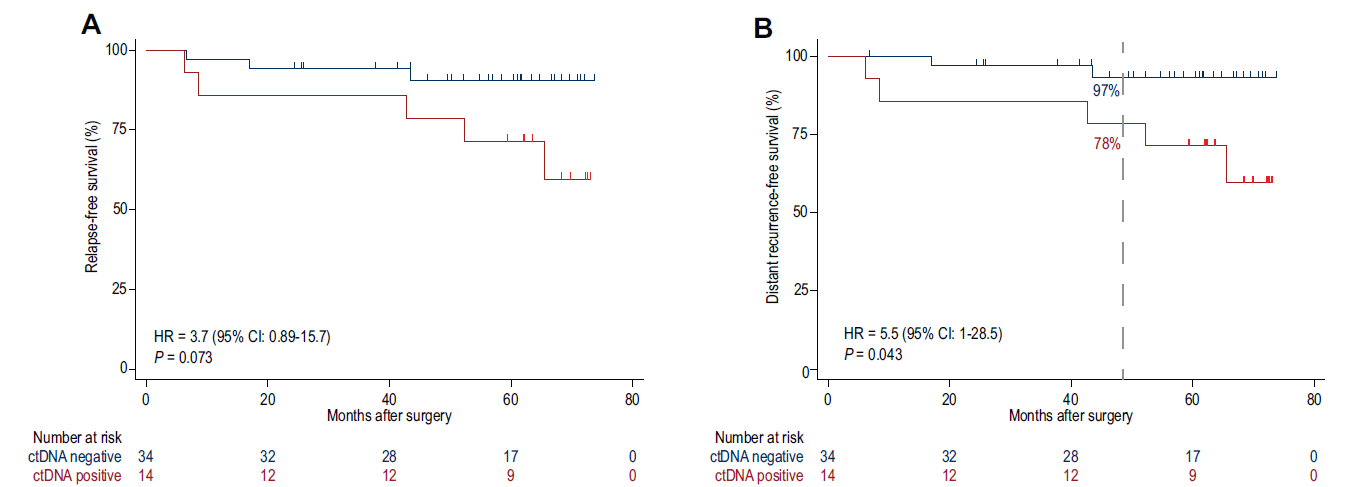
之后探索术前术后联合ctDNA状态和复发风险的相关性,观察到任一时间点检出ctDNA的患者具有更差RFS(HR 7.8,95%CI 0.95-63.77,P=0.05)(图3A)和DRFS(HR 6.8,95%CI 0.8-57,P=0.07)(图3B)。

随访中ctDNA检出可预测复发
35%的患者具有完成辅助化疗后的随访血浆标本。其中76%(13/17)为HR+疾病,除了1例患者外均接受辅助内分泌治疗伴或不伴放疗。3例为HER2+疾病,行抗HER2治疗(伴或不伴放疗),1例为TNBC。17例患者中,4例(24%)可检出ctDNA。没有患者疾病进展,3例患者为HR+疾病,ctDNA检测后持续接受辅助内分泌治疗(伴或不伴放疗)。1例患者(HER2+)接受抗HER2治疗。ctDNA检出较临床复发的中位领先时间是16个月。
术后ctDNA或可预测辅助化疗反应
术后存在ctDNA和辅助化疗反应相关。34例ctDNA未检出的患者中,仅7%(2/29)接受辅助化疗的患者发生DRFS(图4),5例未接受辅助化疗的患者无事件。ctDNA检出患者(n=14)具有更高的复发率,未行辅助化疗的患者为75%(3/4),行辅助化疗的患者为20%(2/10)(图4)。
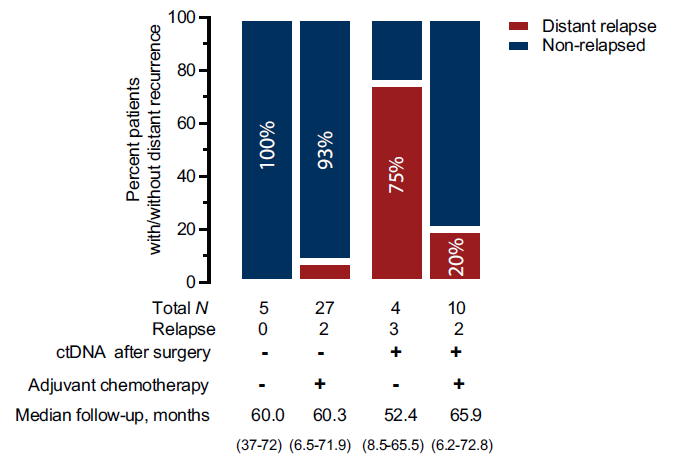
研究讨论
临床中亟需术后可检测MRD和预测疾病复发的生物标志物,以改善EBC患者的辅助治疗决策。当前行手术切除的EBC患者队列中,使用ctDNA分析可发现切除后MRD状态,并发现术后ctDNA检出和复发相关。
研究评估ctDNA检出和生存的相关性,发现和未检出ctDNA的患者相比,术后单次时间点检出ctDNA的患者具有更差RFS(HR 3.7,95%CI 0.9-15.6,P=0.07)和DRFS(HR 5.5,95%CI 1.1-28.5,P=0.04)。尽管和RFS的相关性不显著(可能是由于样本量小),结果也和EBC患者中另一小样本研究数据类似[3]。相似非乳腺癌研究也发现术后单次ctDNA检出和更差的RFS相关[2,4]。
既往多项研究显示术后单次ctDNA检出和更差RFS相关[5,6]。因此术后单次ctDNA检出可准确预测早期疾病复发。但是纵向监测有助于提高发现复发的敏感性,特别是对于复发风险持续的HR+/HER2-疾病。
研究结果提示术后ctDNA检出可发现更能从辅助化疗中获益的患者,而未检出ctDNA的患者可能从辅助化疗中无额外获益。结论有必要在大型前瞻性研究中进行验证。
研究结论
术后ctDNA检出可EBC患者更差的RFS及DRFS相关,并可早期预测复发。术后ctDNA检查或可发现可从辅助化疗中获益的患者。
[1] Cutts R, et al. Association of post-operative ctDNA detection with outcomes of patients with early breast cancers. ESMO Open. 2024;9(9):103687.
[2] Kotani D, et al. Molecular residual disease and efficacy of adjuvant chemotherapy in patients with colorectal cancer. Nat Med. 2023;29(1):127-134.
[3] Coombes RC, et al. Personalized Detection of Circulating Tumor DNA Antedates Breast Cancer Metastatic Recurrence. Clin Cancer Res. 2019;25(14):4255-4263.
[4] Yamaguchi T, et al. Clinical Implications of Pre- and Postoperative Circulating Tumor DNA in Patients with Resected Pancreatic Ductal Adenocarcinoma. Ann Surg Oncol. 2021;28(6):3135-3144.
[5] Garcia-Murillas I, et al. Mutation tracking in circulating tumor DNA predicts relapse in early breast cancer. Sci Transl Med. 2015;7(302):302ra133.
[6] Garcia-Murillas I, et al. Assessment of Molecular Relapse Detection in Early-Stage Breast Cancer. JAMA Oncol. 2019;5(10):1473-1478.
声明:材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批编号:CN-147397
过期日期:2025-11-18
责任编辑:肿瘤资讯-Kelly
排版编辑:肿瘤资讯-yu











 苏公网安备32059002004080号
苏公网安备32059002004080号


