根据2024年国家癌症中心最新发布的《2022年中国恶性肿瘤流行情况分析》,肺癌是目前中国发病率和死亡率最高的恶性肿瘤,造成了巨大的疾病负担。中国肺癌患者基数庞大,其中非小细胞肺癌(NSCLC)约占~85%,且存在多种类型的驱动基因突变。MET14外显子跳跃突变(METex14跳突)是明确的致癌驱动变异,在NSCLC患者中的突变比例约为1-3%。过往这部分患者的治疗方案仅能参考驱动基因阴性的化疗和免疫治疗,直到2020年FDA批准首个特异性MET抑制剂卡马替尼上市后,精准的靶向治疗才成为这部分患者的治疗选择。不过由于METex14跳突整体发生率较低,且患者年龄偏大,因此要开展大型随机对照研究去对比不同治疗方案极具挑战性。在这种情况下,真实世界研究就是一种极为有效的证据补充方式,一方面可以回答临床研究尚未回答的问题,一方面也可以验证临床研究结果的可靠性。
大样本真实世界研究再次证明卡马替尼靶向先行
近日在 Future Oncology 杂志上发表了一篇关于METex14跳突的真实世界研究,标题为Effectiveness of standard treatments in non-small-cell lung cancer with METexon14 skipping mutation: a real-world study。该研究回顾性收集了来自全美国医疗网络自2017年1月开始一线治疗(1L)的287例METex14跳突晚期NSCLC患者,对比一线接受卡马替尼、免疫单药(IO)、免疫联合化疗(IO+CT)、单纯化疗(CT)的临床结局。该研究为目前METex14跳突NSCLC领域对比不同治疗模式的样本量最大的真实世界研究,其中一线接受卡马替尼的患者为146名。
研究发现,卡马替尼一线治疗的客观缓解率(rwORR)达73.4%,疾病控制率(rwDCR)达95%,至治疗终止时间(mTTD)为19.1月,中位无进展生存(rwPFS)和中位总生存 (mOS)暂未达到,但18个月PFS率和OS率分别达68%和92.6%。其他治疗组无论在短期缓解或长期生存上均低于卡马替尼,且组间差异具有统计学意义。Cox PH回归分析进一步显示,在控制了人口统计学和基线临床特征后,接受IO、CT和IO+CT的患者治疗终止率、疾病进展率、死亡率均显著高于接受卡马替尼(HR>1)(表1),且CT、IO+CT组与卡马替尼组的差异具有统计学意义(p<0.05)。
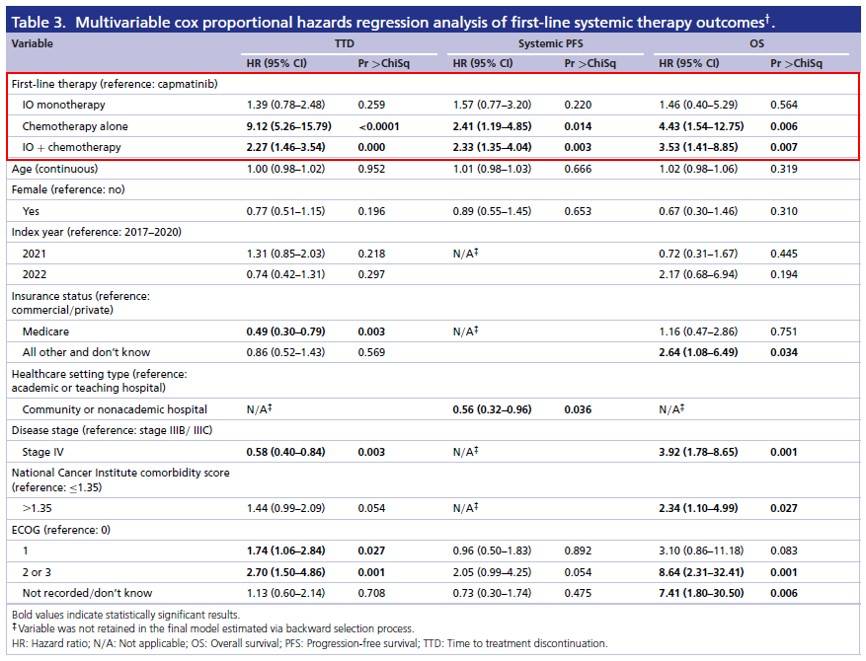
表1 一线系统性治疗临床结局的多因素COX比例风险回归分析
这项研究证明,相比较以化疗和免疫治疗为基础的方案,卡马替尼作为METex14跳突NSCLC一线治疗肿瘤缓解更优,疾病进展的风险更低,生存期更长。这项研究提供了支持在一线治疗中使用卡马替尼的真实世界证据,并为医生的临床决策提供重要参考信息。
此外,在通常情况下,真实世界研究相较于RCT研究,在研究设计上因其控制因素较少、涉及人群较为广泛且入组患者基线情况更差等特点,其报告的药物疗效数据结果大多劣于RCT研究。然而卡马替尼以其卓越的抗肿瘤活性,不仅在各项多中心临床研究中数据表现亮眼,且在全球范围内的多项大样本真实世界中取得了高度一致的疗效获益。
卡马替尼为FDA首个获批的特异性MET抑制剂,被NCCN指南一线优先推荐
卡马替尼是一种口服生物利用度高、强效、高选择性的特异性MET受体酪氨酸激酶抑制剂,可有效抑制MET及MET介导的下游信号蛋白的磷酸化,从而抑制c-MET依赖性肿瘤细胞的增殖和迁移,并有效诱导细胞凋亡,展现出抗肿瘤活性。与其他MET抑制剂相比,卡马替尼的IC50值同类最低(0.13nM),对c-MET的抑制力更高,且能高效透过血脑屏障,具有良好的脑部抑瘤活性。
2020年5月美国FDA基于GeoMETry mono-1研究加速批准了卡马替尼治疗METex14跳突转移性NSCLC患者的治疗,成为欧美首个获批上市的特异性MET抑制剂。随着验证性队列和长随访研究数据的公布,2022年8月卡马替尼又获FDA常规批准,再次成为首个获得常规批准的MET抑制剂。目前卡马替尼已在全球包括中国香港在内的多个国家和地区获批上市。在国内,卡马替尼作为国际创新药物已落地中国海南博鳌及粤港澳大湾区。
此外,基于充足明确的临床证据和可及性,目前国际权威指南如NCCN指南和ASCO指南均将卡马替尼列为METex14跳突NSCLC的一线优先推荐(图1)。虽然卡马替尼在中国大陆尚未获批上市,但目前CSCO非小细胞肺癌指南也将卡马替尼列为一线治疗的III级推荐。
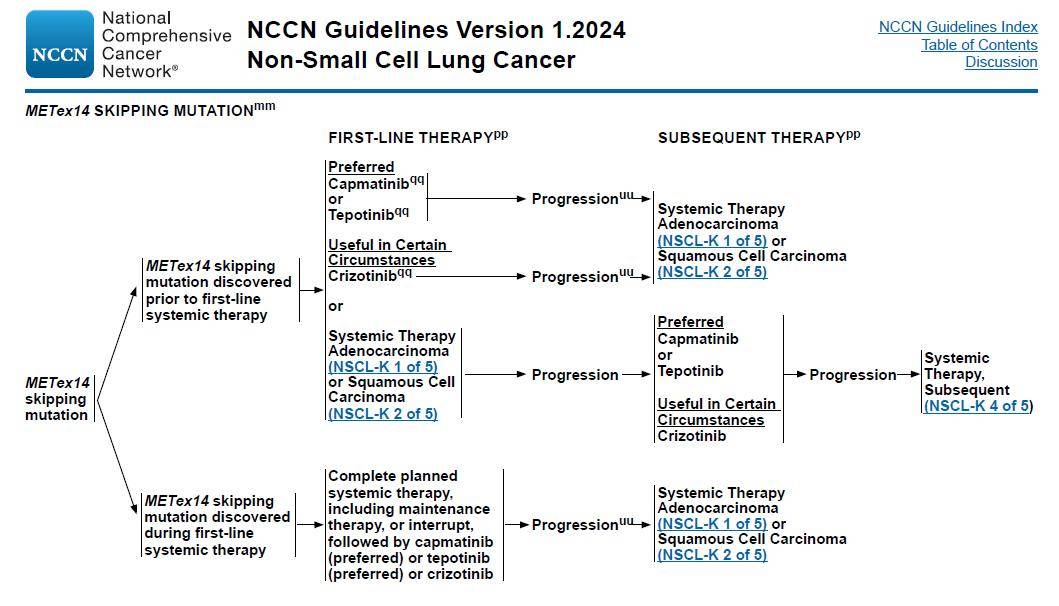
图1 非小细胞肺癌NCCN指南2024v1版对于METex14跳突阳性患者的治疗推荐
临床研究显示卡马替尼一线治疗METex14跳突疗效优异,DCR近100%,中位OS超2年
卡马替尼在全球范围内的获批依据的是一项国际多中心II期临床研究GeoMETry mono-1。该研究纳入了不同MET变异类型的NSCLC,其中队列4、5b、6、7分别纳入了经治及初治的METex14跳突患者。研究结果显示MET ex14跳突初治患者(队列5b和7,n=60)接受卡马替尼治疗ORR为68.3%,DCR为98.3%,中位PFS达12.5个月,中位OS达25.5个月(表2)。无论从短期病灶缓解到长期生存获益,卡马替尼都展现出了令人惊艳的疗效。
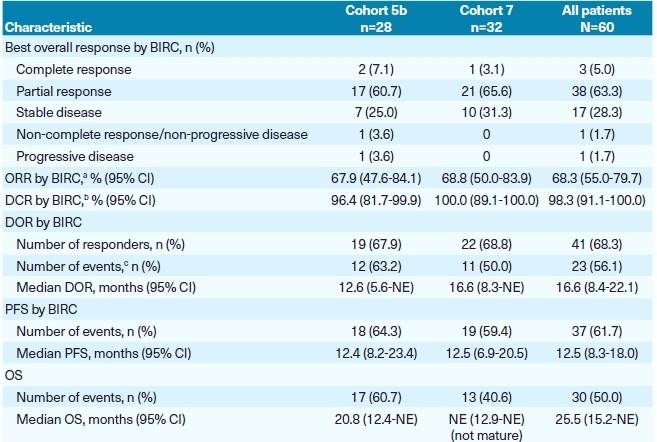
表2 GeoMETry mono-1研究中卡马替尼一线治疗队列5和队列7的疗效
在中国人群中,卡马替尼同样开展了一项多中心单臂II期临床研究GeoMETry-C。在400mg BID给药剂量下,初治队列可评估集的ORR达69.2%,DCR达86.7%,且大部分患者出现了深度缓解。PFS和OS数据尚未成熟。卡马替尼在中国人群中展现出了与全球人群相似的疗效,进一步提示对于中国人群的强效获益。
卡马替尼在临床研究和真实世界中均显示出强大的颅内疗效
约1/3的METex14跳突晚期NSCLC患者在疾病发展全周期中会出现脑部转移。伴随脑转移的患者生存预后明显更差,因此对于脑转移患者的治疗一直是临床关注的重点。卡马替尼作为一款能高效透过血脑屏障,具有良好的脑部抑瘤活性的小分子抑制剂,其在临床研究及真实世界中也展现出了对颅内病灶的优异疗效。
GeoMETry mono-1研究中纳入了13例基线有可测量颅内病灶的METex14跳突脑转移患者,其基于BIRC评估的颅内病灶缓解率iORR达54%,颅内病灶控制率iDCR达92.3%。在7例颅内病灶应答者中有4 例患者的所有脑部病灶完全消退,iCR率达到31%。全部7例应答患者在首次评价时(治疗开始后6周)即有颅内缓解,提示卡马替尼不仅能强效抑瘤,且颅内应答迅速。在中国注册临床研究GeoMETry-C中同样观察到了卡马替尼突出的颅内疗效,一线初治队列中脑转移患者颅内病灶完全缓解率iCR高达50%,iDCR为100%。这意味着有一半的患者颅内病灶完全消失,而全部患者的颅内病灶均未进展。
在一项较大样本的真实世界回顾性研究中,55例METex14跳突阳性的脑转移患者接受一线卡马替尼治疗后全身病灶rwORR 为90.9%,rwDCR为96.4%,颅内病灶iORR达87.3%;iDCR达96.4%。如此惊艳的数据,再次验证了卡马替尼与临床研究一致的对脑转移患者颅内病灶和全身病灶的强大控制。从生存获益上看,脑转移患者接受一线卡马替尼的中位系统PFS为14.1个月,中位颅内PFS暂未达到,12个月的颅内未进展生存率为83.5%,意味着对于颅内病灶的控制可有效的转化成长期的生存获益。此外,该项研究还发现无论患者先前是否接受过脑部放疗、脑转移有无症状,卡马替尼都能保持其优异的疗效。以上所有证据都再次提示卡马替尼应成为METex14跳突患者的一线首选治疗。
卡马替尼安全低毒,降低临床管理负担,提高患者生活质量
METex14跳突患者多为老年患者,平均年龄为65-76岁,因此对于药物使用的便捷性和安全性有着更高的需求。临床研究显示,卡马替尼在体内的吸收代谢不受空腹或进食状态影响。因此卡马替尼的服用方式灵活,与食物同服或不同服均可,有助于提高患者的用药依从性。
来自临床研究的安全性数据显示卡马替尼整体安全性良好,不良反应发生率低,严重程度低,且消退快。在亚洲人群中3/4级治疗相关不良事件(TRAEs)的发生率仅为20%,且无致死性TRAE。没有因不良事件导致患者停药。对于目前MET抑制剂常见的不良反应,卡马替尼的水肿发生率显著低于其他MET抑制剂,亚洲人群中治疗相关所有级别水肿发生率仅为26.7%,且无3/4级发生。卡马替尼的肝毒性也较低,是目前唯一一个有证据支持可在重度肝损患者中使用的MET抑制剂。轻、中、重度肝损患者使用卡马替尼的初始剂量均无需调整。其他一些特殊不良反应如血液毒性(贫血)、心脏毒性(QT间期延长)等,卡马替尼也无报道发生。
汇总卡马替尼治疗METex14跳突晚期NSCLC所有研究证据,均证实了卡马替尼是一款优效且安全的特异性MET抑制剂。对于部分年龄较大、基础情况较差、预后不良的METex14跳突患者,应尽可能的好药先用,通过靶向治疗精准发力,延长患者的长期生存获益。期待卡马替尼能够早日在中国获批,造福更多的中国患者!
1. 郑荣寿, 陈茹 等. 2022年中国恶性肿瘤流行情况分析. 中华肿瘤杂志, 2024, 46(3):221-231.
2. Tan AC, et al. Targeted Therapies for Lung Cancer Patients With Oncogenic Driver Molecular Alterations. J Clin Oncol. 2022 Feb 20;40(6):611-625.
3. Liu SY, et al. The Unique Characteristics of MET Exon 14 Mutation in Chinese Patients with NSCLC. J Thorac Oncol. 2016 Sep;11(9):1503-10.
4. Furqan M, et al. Effectiveness of standard treatments in non-small-cell lung cancer with METexon14 skipping mutation: a real-world study. Future Oncol. 2024 Apr 17. Epub ahead of print
5. Liu X, et al. A novel kinase inhibitor, INCB28060, blocks c-MET-dependent signaling, neoplastic activities, and cross-talk with EGFR and HER-3. Clin Cancer Res. 2011 Nov 15;17(22):7127-38.
6. Fujino T, et al. Presented at WCLC 2018; abstract P1.13-41.
7. U.S. Food and Drug Administration. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-capmatinib-metastatic-non-small-cell-lung-cancer
8. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®). Non-Small Cell Lung Cancer. Version 1.2024
9. Navneet Singh et al. Therapy for Stage IV Non–Small-Cell Lung Cancer Without Driver Alterations: ASCO Living Guideline, Version 2023.1. JCO 41, e51-e62(2023).
10. 2023 CSCO非小细胞肺癌诊疗指南.
11. Yi-Long Wu, et al. Presented at ESMO Asia 2022, Poster 388.
12. Jurgen W, et al. Presented at ELCC 2022, Poster 26.
13. Michael Offin et al. CNS Metastases in Patients With MET Exon 14–Altered Lung Cancers and Outcomes With Crizotinib. JCO Precis Oncol 4, 871-876(2020).
14. Paik PK, et al. Real-world outcomes in non-small-cell lung cancer patients with MET Exon 14 skipping mutation and brain metastases treated with capmatinib. Future Oncol. 2023 Jan;19(3):217-228.
15. Capmatinib (TABRECTA®). FULL PRESCRIBING INFORMATION. https://www.accessdata.fda.gov/drugsatfda_docs/label/2022/213591s004lbl.pdf
排版编辑:肿瘤资讯-Raffle











 苏公网安备32059002004080号
苏公网安备32059002004080号


