
徐州医科大学附属医院乳腺甲状腺外科
中国抗癌协会会员
江苏省抗癌协会会员
癌症筛查与早诊早治专业委员会会员
乳腺癌专业委员会委员
甲状腺癌专业委员会会员
徐州市甲状腺疾病研究学会委员
擅长甲状腺、乳腺良恶性疾病的规范化综合诊治。长期从事甲状腺癌、乳腺癌根治术,乳腺癌保乳术,前哨淋巴结活检术,乳腺微创旋切术,静脉输液港植入术
病史简介
患者:刘某,女,44岁。初诊日期:2021-07-20。
主诉:发现右乳肿块一月。
现病史:患者一月前无意中发现右侧乳房下方核桃大小肿块,无疼痛不适,无乳头溢液。门诊就诊,超声提示:右乳低回声团块伴钙化,BI-RADS:5类。右腋窝多发肿大淋巴结声像。收治入院。
既往史:糖尿病4年,胰岛素治疗,血糖控制良好。
家族史:否认乳腺癌和其他恶性肿瘤家族史。
月经婚育史:未绝经,已婚,孕1产1。
查体:双乳基本对称,轮廓无畸形,未见橘皮样征,皮肤无红肿、破溃,无乳头溢液。右乳下方可及大小约2.5*3.5cm肿块,质地硬,边界不清,活动度差。右侧腋窝可及肿大淋巴结,最大约2*2.5cm。左侧乳房及腋窝未及明显异常。
影像学检查
乳腺彩超示(2021-07-13,图1):右乳房7:00距离乳头约3cm,距离皮肤约1.4cm探及低回声团块,大小约3.7*1.8*1.8cm,形态不规则,内示多枚强回声,纵横比<1,内示血流信号,超声弹性成像质地偏硬(4分)。右侧腋窝多发低回声结节,最大约2.5*1.7cm,内示血流信号。
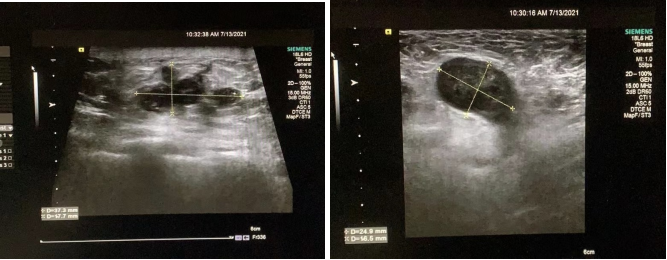
图1.乳腺彩超示图
钼靶(2021-07-20,图2):右乳房下象限肿块影,形态不规则,边界不清,边缘可见分叶,病灶内多发点状、粗点状钙化灶,病灶大小约38*17mm。右腋前份显示增大淋巴结。
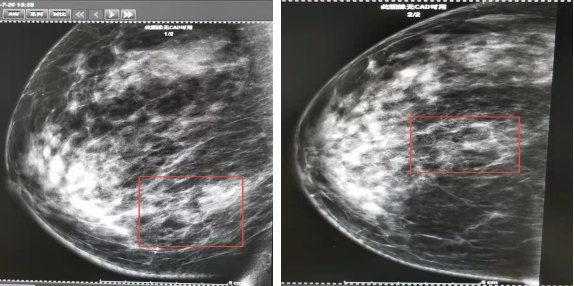
图2.右乳钼靶影像
乳腺MR(2021-08-06,图3):右乳下象限见多发结节、肿块影,呈集簇状分布,T2WI呈高信号,较大病灶大小约19*32*13mm,形态不规则,边缘可见分叶,内部强化不均匀,时间-信号强度曲线平台型,DWI呈高信号,ADC值为0.865-0.932*10-3mm2/s。右侧腋窝多发增大淋巴结,最大者短径约21mm;胸骨右旁示稍大淋巴结,短径约5mm,DWI呈高信号。
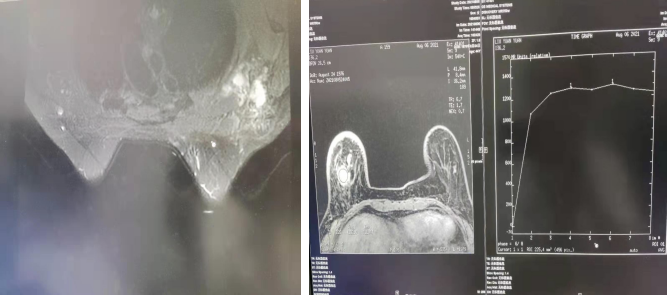
图3.乳腺核磁共振图
胸部CT平扫(2021-07-21):显示右肺上叶小结节,直径约2mm。右乳下象限肿块影,大小约25*21mm,右侧腋窝多发增大淋巴结,建议结合钼靶及超声。
头颅CT,消化系彩超,骨扫描等未见癌转移。
病理结果:
乳房肿块和腋窝淋巴结穿刺病理(2021-07-22):
乳房肿块病理示:右乳浸润性癌;腋窝淋巴结见异形细胞巢,伴坏死。
免疫组化示(2021-07-28):
右乳肿块: Ki-67(+70%),P53(弥漫+),ER(-),PR(1+,5%),HER2(3+),EGFR(部分+),CK5/6(-),AR(+),E-cadherin(膜+),P120(膜+),CK5/6(-),P63(散+),Calponin(-),GATA(+)。符合浸润性导管癌。
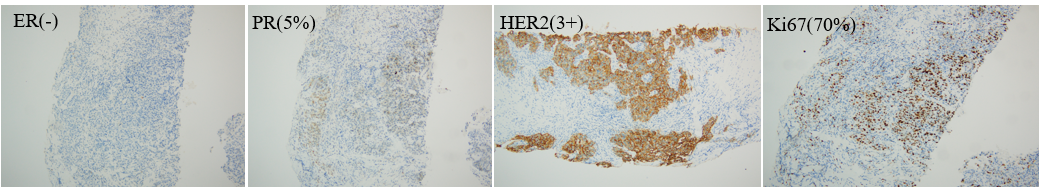
图4.右乳免疫组化结果
右腋窝淋巴结:Ki-67(+,热点区60%),ER(-),PR(1+,<1%),HER2(3+),CKp(+),GCDFP-15(-),Mammaglobin(部分+),GATA3(部分+)。
初步诊断
右乳浸润性癌 T2N1M0 IIB 期(HER-2阳性乳腺癌)。
治疗方案和疗效评估
新辅助治疗:
结合各大指南推荐,选择新辅助化疗联合靶向治疗
新辅助化疗方案选择:TCbHP。
患者2022-08-06开始行新辅助化疗联合靶向治疗,具体用药:紫杉醇(白蛋白结合型)+卡铂+曲妥珠单抗(汉曲优,首次600mg/后续450mg)+帕妥珠单抗(首次840mg,后续420mg)。6个周期,3周一个疗程。
疗效评估:
患者2021-08-27行第2周期化疗。行化疗后疗效评估。
乳腺彩超示(2021-08-27):右乳房7:00距离乳头约4.8cm,距离皮肤约0.9cm探及低回声团块,大小约1.7*1.0*1.3cm,形态不规则,内示多枚强回声,纵横比<1,内血流信号不明显,超声弹性成像质地偏硬(4分)。右侧腋窝多发低回声结节,最大约2.4*1.5cm,内示血流信号。提示右乳肿瘤缩小明显,治疗方案疗效确切,疗效评估PR。继续按既定方案执行6周期化疗。
患者2021-11-20行第6周期化疗和靶向治疗。术前影像检查评估疗效。
彩超示(2021-12-15):右乳房7:00距离乳头约5.2cm,距离皮肤约1.4cm探及低回声团块,大小约0.5*0.7*0.5cm,形态不规则,边界不清晰,纵横比<1,血流信号不明显。右侧腋窝探及淋巴结声像,淋巴门存在,皮髓质分界清,大小约1.1*0.6cm,皮质稍厚。
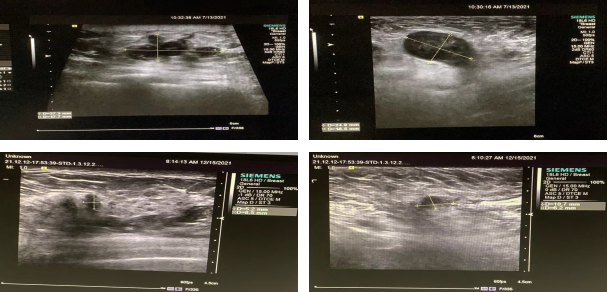
图5.2021-07-20彩超图(上)vs2021-12-15彩超图(下)
钼靶(2021-12-15):右乳房下象限肿局部腺体稍紊乱,可见条片状稍高密度影,伴多发点状,粗点状钙化灶。双腋窝未示明显肿大淋巴结影。
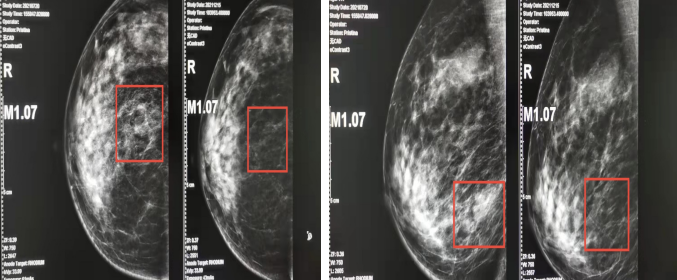
图6.2021-07-20钼靶图(左)vs2021-12-15钼靶图(右)
乳腺MR(2021-11-03):右乳ca治疗后,右乳腺体T2W1信号不均,DWI呈高信号,ADC值为2.01*10-3mm2/s。外下象限可见斑片影,边界不清,增强后强化不明显。双腋窝未示明显肿大淋巴结。胸骨右旁示DWI呈高信号小结节样影。
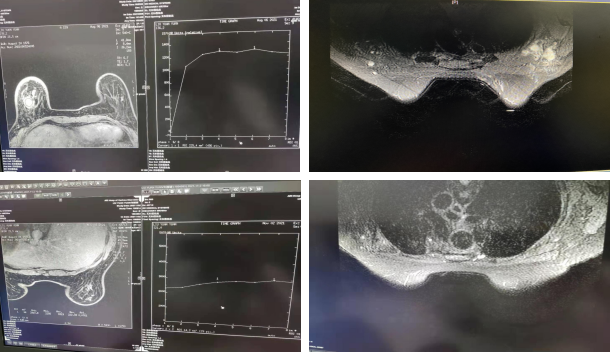
图7.2021-08-06MR结果(上)vs2021-11-03MR结果(下)
手术方式:
患者2021-12-16行右乳癌保乳术+右腋窝淋巴结清扫术。
术后病理示:
新辅助化疗后右侧乳房保乳术标本:(右乳)乳腺间质硬化,局灶泡沫细胞,淋巴细胞浸润。保乳切缘:上,下,内,外,基底切缘(-)。
RCB系统:0。
腋窝淋巴结:21枚,无癌状态,伴治疗后改变。
新辅助治疗后疗效评估:PCR。
术后病理分期ypT0N0M0。
后续治疗方案
1.继续双靶治疗一年,汉曲优6mg/kg+帕妥珠单抗420mg q3w。
2.放疗治疗。
病例小结
该患者为年轻、绝经前的HER2阳性乳腺癌,临床诊断为右乳浸润性癌 T2N1M0,ⅡB期,按照指南要求给予TCbHP双靶治疗。患者在新辅助治疗6个周期后,术前影像学疗效评估为PR。结合患者意愿和治疗效果,决定行右乳癌保乳+腋窝淋巴结清扫术。术后病理显示PCR, 术后继续双靶抗HER2治疗。
曲妥珠单抗一直以来是乳腺癌抗HER2治疗的首选药物。曲妥珠单抗作用于HER2受体胞外结构域Ⅳ,阻断二聚体的形成,从胞外阻断信号传导。帕妥珠单抗作用于HER2受体胞外结构Ⅱ,阻止HER2与其他HER2受体形成异源二聚体,从而阻断信号传导。研究发现曲妥珠单抗和帕妥珠单抗机制互补,能够使得ADCC效应叠加,从而增强抗肿瘤的活性1-2。目前,各项研究也证实曲帕双靶在新辅阶段的应用可以是患者获得较好的长期生存获益3-4。
根据《CSCO中国生物类似药专家共识》:生物类似药与参照药疗效等同、安全性相似,临床上可以替代使用。作为曲妥珠单抗生物类似药,本次病例中,患者在使用汉曲优联合帕妥珠单抗新辅助治疗后,达到PCR,证明生物类似药同样可以患者带来了显著的疗效获益。
乳腺癌的分子分型主要包括Luminal A型、Luminal B型、HER2阳性和三阴性乳腺癌,其中,HER2阳性乳腺癌占比约20%-25%5。在临床上,HER2阳性乳腺癌通常表现出侵袭性强、易复发转移、预后差的特点,各指南共识更推荐采用新辅助治疗的模式5, 6。
随着精准医学时代的到来,乳腺癌患者可以通过分子检测,结合组织学病理进行分子分型,更准确评估患者预后。对于特定分子变异的乳腺癌患者,如HER2表达阳性、BRCA1/2突变、PD-L1表达阳性或PIK3CA突变等,可以更精准从靶向或免疫药物中获益,提高患者生存期5,7,8。
[1]Scheuer W , Friess T , Burtscher H , et al. Strongly Enhanced Antitumor Activity of Trastuzumab and Pertuzumab Combination Treatment on HER2-Positive Human Xenograft Tumor Models[J]. Cancer Research, 2009, 69(24):9330.
[2]Rita, Nahta, Mien-Chie, et al. The HER-2-targeting antibodies trastuzumab and pertuzumab synergistically inhibit the survival of breast cancer cells.[J]. Cancer research, 2004.
[3]Plg A, Ptp B , Yhi C , et al. 5-year analysis of neoadjuvant pertuzumab and trastuzumab in patients with locally advanced, inflammatory, or early-stage HER2-positive breast cancer (NeoSphere): a multicentre, open-label, phase 2 randomised trial. 2016.
[4]Efficacy, Safety, and Tolerability of Pertuzumab, Trastuzumab, and Docetaxel for Patients With Early or Locally Advanced ERBB2-Positive Breast Cancer in AsiaThe PEONY Phase 3 Randomized Clinical Trial[J]. JAMA Oncology, 2020.
[5]Exman P, Tolaney SM. HER2-positive metastatic breast cancer: a comprehensive review. Clin Adv Hematol Oncol. 2021;19(1):40-50.
[6]黄香, 蒋梦萍, 包胜南,等. 2021年CSCO《乳腺癌诊疗指南》更新要点解读[J]. 中国肿瘤外科杂志, 2021, 13(3):7.
[7]André F, Ciruelos E, Rubovszky G, et al. Alpelisib for PIK3CA-Mutated, Hormone Receptor-Positive Advanced Breast Cancer. N Engl J Med. 2019;380(20):1929-1940. doi:10.1056/NEJMoa1813904
[8]Cortes J, Cescon DW, Rugo HS, Nowecki Z, Im S-A, Yusof MM, et al.Pembrolizumab plus chemotherapy versus placebo plus chemotherapy for previously untreated locally recurrent inoperable or mTNBC (KEYNOTE355): a randomized, placebo-controlled, double-blind, phase 3 clinical trial. Lancet 2020;396:1817-28.














 苏公网安备32059002004080号
苏公网安备32059002004080号


