2020年3月20日,“赫赫有声——HER2云间谈”会议顺利召开。会议邀请到浙江省肿瘤医院杨红健教授、空军军医大学西京医院张聚良教授、福建医科大学附属协和医院傅芳萌教授、复旦大学附属肿瘤医院黄亮教授、上海交通大学附属瑞金医院孙慧平教授、江苏省肿瘤医院秦建伟教授聚焦HER2阳性乳腺癌治疗策略,探寻ADC药物内在机制。
Less is More:从关注“病”到关注“人”
在会议开场,来自空军军医大学西京医院的张聚良教授,结合2016年“健康中国2030纲要”中把以治病为中心转变为关注人民健康为中心的指示,指出从关注“病”到更关注“人”将是乳腺癌外科治疗的未来趋势。
在乳腺癌的手术治疗模式中,Less is More(少即是多)的理念已经逐步得到认同,在最早Halsted确立乳腺癌根治术标准后,扩大根治术随即登上舞台。然而,该理论很快受到了挑战,有学者发现照此进行手术后,并未改善患者生存,反而增加了并发症。因此,改良根治术慢慢出现,即缩小手术范围,保留功能性结构,再后来逐渐开展了保乳手术。即便如此,我国保乳手术比例不足20%,城市间差距巨大,而在欧美该比例可达40%~50%。不过,总体而言,对保乳理念的认同在近年来呈逐步提升趋势,越来越多的患者采取该种方式进行治疗。
针对保乳治疗的研究,开展的极早,不论是米兰的EORTC10801研究抑或NSABP B-06研究,随访时间均超过20年。在如此长的随访时间中,已能充分表明保乳手术的安全性。早期乳腺癌协作组(EBTCG)亦进行过相关的荟萃分析,指出保乳联合放疗相比乳腺全切,两者的复发指标没有显著差异。EORTC10801研究所得出的结论,也与早期研究相似,即保乳手术与乳腺全切患者的远处转移和总生存无差别。系列研究奠定了保乳手术的可行性,安全性。
在此基础上,有学者对腋窝手术的省略提出了思考。系列研究证实,若患者的前哨淋巴结只有1~2枚阳性,属于T1~T2期,保乳手术时,进行腋窝淋巴结清扫和未进行但予以放疗的患者预后相同。如今,在初诊时对于病理阳性的患者,亦有证据支持在新辅助化疗之后进行前哨淋巴结活检,若活检显示阳性淋巴结超过3枚,采取标记夹亦可行。这些现代的保乳手术进展,均充分体现了Less is More的理念。
基于此,中国抗癌协会乳腺癌诊疗指南与规范明确指出保乳的适应证,将乳腺癌分类而治。对于临床Ⅲ期的患者推荐进行新辅助治疗,在新辅助治疗后约81%的患者肿瘤显著缩小,达到降期目的,从而实现保乳。
T-DM1:No One, Only One(非单一,唯独一)
乳腺癌中约有20%的为HER2过表达,而HER2阳性的晚期乳腺癌,约有78%是由HER2阳性的早期乳腺癌复发所致。尽管如此,依旧有75%的HER2阳性乳腺癌有望获得治愈,因此,福建医科大学附属协和医院傅芳萌教授指出尽早地给予最有效的治疗方案将有利于把握住患者仅有一次的治愈机会。
如今,新辅助治疗是乳腺癌系统治疗的重要组成部分,然而HER2阳性的早期乳腺癌新辅助治疗后仍有30%~60%患者被评估为非病理完全缓解(non-pCR),而根据CTNeoBC荟萃研究显示,这类患者不仅长期生存劣于病理完全缓解患者(pCR),且不论激素状态,长期预后较差。多项研究治疗方案显示non-pCR患者辅助治疗使用了抗HER2靶向治疗或联合化疗,但仍然无法满足该类患者的治疗需求。
鉴于此,T-DM1(恩美曲妥珠单抗)横空出世。该药为抗体药物偶联物(ADC),是一种新型抗肿瘤大分子药物。其中,DM1为微管蛋白抑制药物,提供强效细胞毒作用,根据既往的研究显示DM1的抗肿瘤强度是紫杉醇的百倍,实现杀伤强效;硫醚键连接体用于保持DM1的惰性状态,结构稳定、靶外毒性小;曲妥珠单抗,为经典的乳腺癌抗HER2靶向药物,可以抑制信号传导,介导ADCC,因此,T-DM1的结构决定了其具有靶向、强效和稳定的特点。
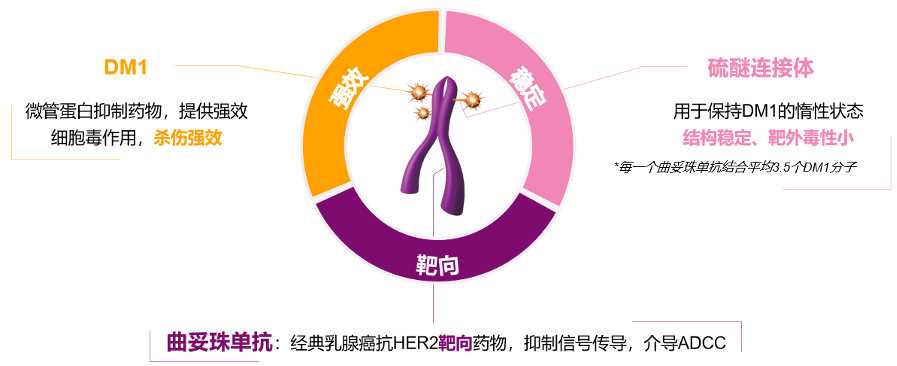
图1.T-DM1通过硫醚键共价连接了曲妥珠单抗和微管抑制药物DM1,具有靶向、强效和稳定的特点
在T-DM1的优势中,最为瞩目的是安全性,根据CA012研究和KATHERINE研究的对比显示,由于DM1通过硫醚键连接体,经过内吞、裂解后,才被释放入肿瘤细胞中,胞外毒性小,因此,相比纳米白蛋白紫杉醇和溶剂型紫杉醇,T-DM1发生3级以上的不良反应少,疗效更好。
综上,T-DM1不仅仅是一种单克隆抗体的靶向药物,也不是单纯的化疗药物,而是巧妙的将靶向药物和化疗药物偶联起来,形成选择性的生物导弹。
现今,学者已对T-DM1展开临床研究,其中KATHERINE研究是目前唯一一项针对HER2阳性早期乳腺癌新辅助治疗后non-pCR患者强化辅助治疗显示出生存获益的Ⅲ期随机对照研究,旨在评估HER2阳性早期乳腺癌新辅助治疗后non-pCR患者,接受T-DM1治疗后的有效性和安全性。研究结果显示,无论激素受体、淋巴结状态、新辅助抗HER2方案如何,甚至是仅有少量残存病灶的淋巴结阴性患者,T-DM1各亚组3年无侵袭性疾病生存期均显示获益,其中,无论既往新辅助化疗是单靶或者双靶,改善的幅度是一样的(分别为11.8%、10.5%)。而仅有少量残存病灶的淋巴结阴性患者,改善幅度也达到4.7%。总之,与对照组曲妥珠单抗相比,T-DM1治疗组有效提升约11.3%的3年iDFS率。同时,中国人群的主要终点与全球结果一致(3年iDFS率提升13.4%)。在强有力的疗效和安全性数据的支持下,美国综合癌症网络(NCCN)指南将T-DM1列为HER2阳性新辅助治疗后non-pCR乳腺癌患者强化辅助治疗的标准治疗方案,T-DM1让non-pCR患者获得治愈可能。
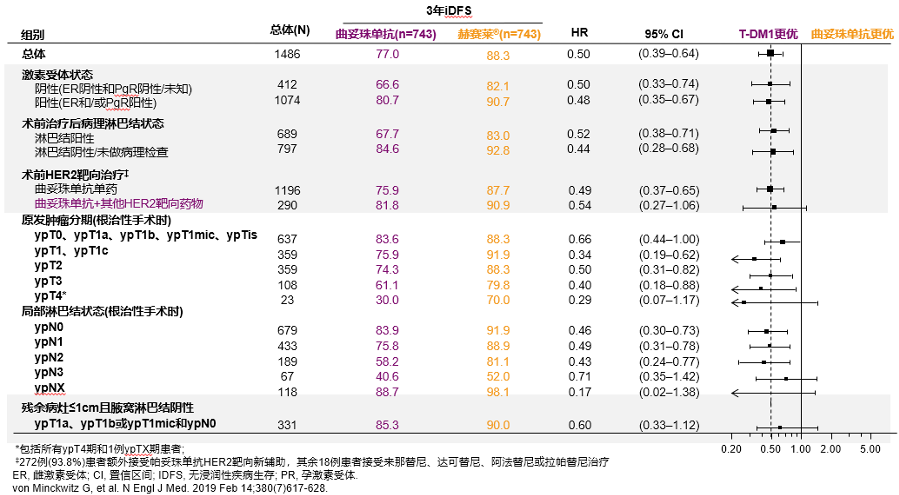
图2. T-DM1组和对照组3年iDFS
T-DM1的不良反应,程度轻且可控
在病例讨论环节,专家们针对T-DM1以及KATHERINE研究各抒己见。其中上海交通大学附属瑞金医院孙慧平教授对T-DM1的血液学毒性进行了分享,她指出不论临床实践抑或研究,安全性是非常重要的考量方面。T-DM1和化疗药物在结构上存在较大区别,既有化疗药物的成分,又具备靶向引导的功能。从理论而言,T-DM1是一个非常特异性的药物,只有在具有特异抗原的HER2过表达细胞中,才会释放细胞毒成分。从该角度分析,T-DM1和传统化疗不同,其血液学毒性较低,安全性较高。
此外,在临床实践中还存在少数血小板减少情况。其实,包括化疗药在内的各种药物都可能出现药物相关血小板减少的情况。由于DM1是抗微管的细胞毒药物,尽管在与曲妥珠单抗偶联后具备靶向性,然而亦具备髓类毒性,特别是会导致血小板下降。因此,需要定期监测血象,关注血小板变化。一般而言,80%的患者使用T-DM1都能平稳的渡过治疗期,所出现的不良反应大多为一、二级,根据KATHERINE研究显示,T-DM1三级以上不良反应的发生率与安全性较高的靶向药曲妥珠单抗相似,均为小概率事件。不过仍需要进行随访观察,根据趋势及时减量甚至停药,同时使用辅助药物提升血小板。所以,只要做好监测,及时处理,就可以使得患者平稳渡过治疗阶段,达到安全又有效的治疗目的。
作为本场学术分享的主持,来自浙江省肿瘤医院杨红健教授亦对孙慧平教授的观点表示了认同,表示对于T-DM1所导致的血小板减少,在战略上要藐视它,因为其发生比例较低,可能为一过性,而在战术上要重视它,应该充分和患者进行交代,嘱患者尽量减少碰撞,以保障患者安全的完成治疗。
往期文章精粹:
赫赫有声:规范化病理评估为乳腺癌治疗提供可靠依据,助力患者走向治愈
赫赫有声:改善non-pCR患者预后,强化辅助治疗让新辅助治疗更有意义!
赫赫有声:“生物导弹”助力早期乳腺癌治愈之路,化疗药与靶向药合为一体,疗效显著!
赫赫有声,共赢未莱:比靶向更强效,比化疗耐受性更好,ADC药物是如何做到的?
排版编辑:Mice













 苏公网安备32059002004080号
苏公网安备32059002004080号


