2019年欧洲肿瘤内科学会(ESMO)年会已成功举行,然而大会期间公布的众多研究结果在业内所引起的震动依旧余波未平。为了及时向中国学者传递ESMO最新研究进展,2019年10月27日-11月20日,正大天晴医学事务部在全国多地主办“安之有道--2019年 ESMO会后会热点速递”,跨时1个月,安之有道系列会议圆满落下帷幕。本文着重记录了结直肠癌(CRC)、肝细胞癌(HCC)、胰腺癌和胆管癌的相关内容,与【肿瘤资讯】的读者共同分享。
席卷全国,大咖云集,速递ESMO学术强音
为更好地将ESMO最新进展呈现给未能直接参会的中国学者,更好地将研究结果转化为临床实践,更好地指导未来研究,此次系列会议邀请众多领域内大咖现场解读ESMO最新进展,系统梳理热点内容,为医务工作者搭建最便利的学习与交流的平台。会议覆盖了西安、金华、南昌、南宁、广州、济南、太原、北京、沈阳、南京、乌鲁木齐、成都、河南、福州等14个城市和地区;云集国内肿瘤学领域数位大咖,主席团阵容强大,包括李恩孝、丁克峰、杜金林、熊建萍、彭志刚、黄昌杰、赵明、程玉峰、江浩、邱文生、牛作兴、杨牡丹、毋永娟、周爱萍、曲秀娟、束永前、柳江、李秋、张涛、樊青霞、余祖江、王耀东、石铮等多位教授(按会议召开时间顺序);此外,会议还邀请到全国消化道肿瘤领域的诸多知名专家,针对2019年ESMO会议热点进行梳理盘点,共同交流探讨2019年ESMO年会最新研究进展,速递ESMO学术强音。现场大咖云集,高朋满座,会议隆重热烈而富有生气,为国内的临床医生带来了高质量的学术盛宴。
百花齐放的结直肠癌研究
回顾结直肠癌治疗领域,早先公布的CALGB/SWOG 80405、IDEA等研究的结果令人振奋,给CRC的治疗带来了启发,但近期此类大规模的、影响力较大的结果公布地较少。随着CRC领域规范化治疗和精准医疗时代的开启,研究者们对CRC诊疗的探索更加充满热情和希望,尤其在靶向治疗、免疫治疗以及生物标志物方面的探索尤为突出。
1.循环肿瘤DNA(ctDNA)在I-III期结肠癌辅助化疗中的应用
随着CRC术后辅助化疗观念被广泛认可,患者群的选择逐渐成为被关注的问题,一直以来都是根据TNM分期以及临床病理风险因素来决定患者是否需要术后辅助化疗。一般认为辅助化疗疗程为6个月,但随着IDEA研究结果的公布和领域对其认可度的提升,不同病理危险因素患者的化疗时长也有了不同的选择。尽管如此,仍有部分患者存在过度治疗或治疗不足的问题,将真正需要足疗程化疗的、有不良预后风险患者鉴别出来的需求,一直未能得到充分满足。
LBA30报告了IDEA-FRANCE研究中患者的ctDNA对辅助治疗的预测和预后作用,共805例患者有符合要求的化疗前和化疗后的连续ctDNA检测结果,其中109例(13.54%)患者术后化疗前的ctDNA为阳性,696例为阴性(86.46%),结果显示ctDNA阳性患者更多存在T4分期、分化差与合并肿瘤穿孔的情况,ctDNA阳性与阴性患者的2年无病生存率(DFS)分别为64.12%和82.39%,多元分析证实ctDNA是独立预后因素,IDEA-FRANCE研究中无论ctDNA阳性还是阴性,均是6个月的辅助治疗更优,ctDNA阳性患者3个月的治疗结果最差(图1)。
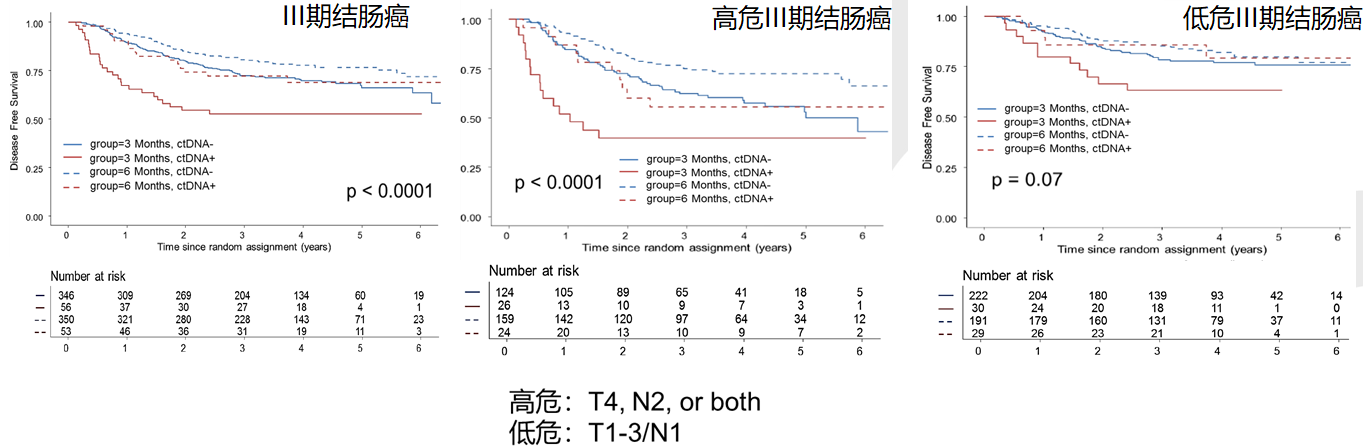
图1. ctDNA与III期结肠癌不同辅助治疗时程的预后相关
522O报告的研究则是通过ctDNA突变检测到的微小残留疾病根据肿瘤分期、CMS亚型和CDX-2的表达情况来预测局限期CRC的高复发人群。该研究建立了29个突变基因的组合,研究结果显示:①手术时血样中ctDNA的含量与预测预后无关;②术后ctDNA含量能够预测DFS,这与其他研究的结果一致;③术后连续ctDNA检测能更好的检测到复发,且早于CT检查11.5月;④ctDNA是独立的高危复发风险指标。
既往多项研究结果提示ctDNA在CRC中可能可作为预后指标,但对ctDNA的含量阈值、突变基因的组合、甲基化水平等方面的选择都值得进一步探索,是ctDNA在CRC领域中的热点。目前开展的“CIRCULATE IDEA”研究旨在探讨如何根据ctDNA的含量指导II/III期CRC术后辅助化疗,届时将更好地区分患者(无需辅助治疗、常规辅助治疗和强化辅助治疗患者群),达到术后精准辅助化疗。
2.免疫治疗在MSS型mCRC患者中的探索
免疫检查点抑制剂在高度微卫星不稳定(MSI-H)型转移性CRC(mCRC)患者中的治疗作用已得到公认,但在微卫星稳定(MSS)型mCRC 治疗中却连番遇挫,如何让免疫检查点抑制剂攻破MSS型mCRC是当前免疫治疗领域的热点。今年ASCO会议上公布的REGONIVO研究结果令人眼前一亮,该研究采用瑞戈非尼联合纳武利尤单抗在24例MSS型 mCRC中后线治疗的总客观缓解率(ORR)达33%,为免疫检查点抑制剂在MSS型mCRC中的应用注入了一针强心剂。本次ESMO会议上也有多项相关研究,现将其中较为重要的4项研究汇总如下。
533PD是一项II期随机、双盲、多中心、安慰剂对照研究,采用卡培他滨/贝伐珠单抗联合阿特珠单抗(治疗组)对比卡培他滨/贝伐珠单抗联合安慰剂(安慰剂组)治疗难治mCRC。研究结果显示,治疗组和安慰剂组的中位无进展生存(mPFS)分别为4.4和3.3个月,两组的中位总生存期(mOS)和12月OS率均相似。MSS型患者的亚组分析中,治疗组有5例获部分缓解(PR),安慰剂组仅有1例。这项研究结果提示MSS型患者可能从卡培他滨/贝伐珠单抗联合阿特珠单抗治疗中获益,但需要鉴定能够预测治疗疗效的标志物以更好的筛选潜在获益患者。
608P报道的是KEYNOTE-651研究中队列B和D的结果,患者均为非MSI-H/错配修复基因完整(pMMR)mCRC,队列B为一线治疗队列,入组15例患者采用帕博利珠单抗联合FOLFOX方案,队列D为二线治疗队列,入组了一线接受FOLFOX后进展的16例患者,采用帕博利珠单抗联合FOLFIRI方案。队列B和D的ORR分别为60.0%和12.5%,疾病控制率(DCR)分别为93%和69%,两组各有12例和4例患者肿瘤缩小≥30%,不良反应多为化疗相关,且不良反应可控。
1201P报告的是一项Ib期研究,前期剂量爬坡确定了Monalizumab最佳剂量,Monalizumab是NKG2A抗体,也属于免疫检查点抑制剂,机制为阻断NKG2A后可促进自然杀伤(NK)细胞和T细胞的免疫反应,进而促进细胞因子释放。扩展队列中纳入的是一线治疗进展的MSS型mCRC,采用四类药物联合方案(即Durvalumab+Monalizumab+FOLFOX+贝伐珠单抗)。治疗16周时,17例可评估患者中7例达到已确证PR,ORR为41.2%,另有2例为未确认PR,6例为疾病稳定(SD)(图2)。
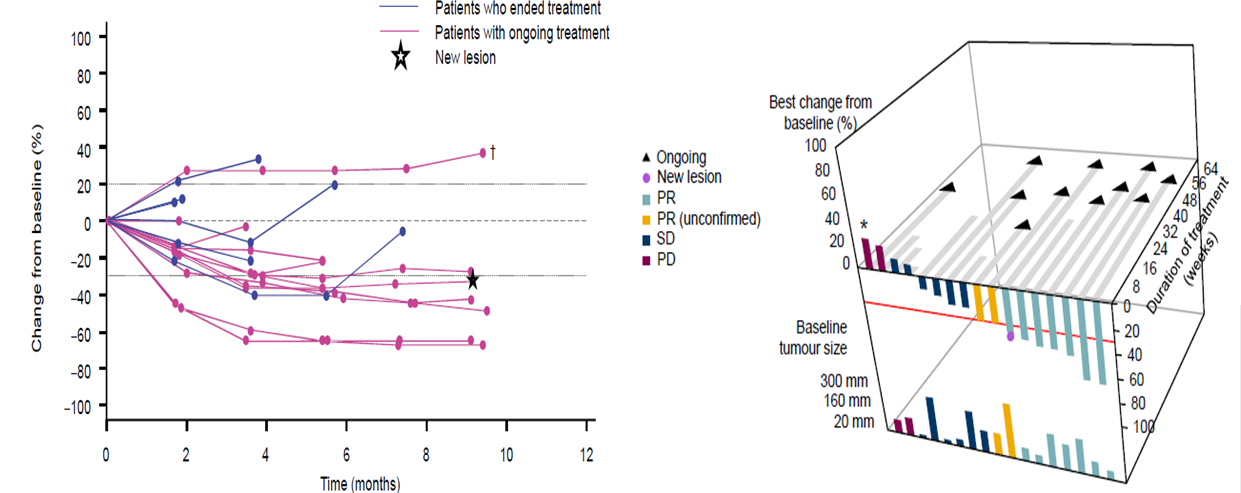
图2. Durvalumab+Monalizumab+FOLFOX+贝伐珠单抗治疗MSS型mCRC结果
528PD报告了CCTG CO.26 研究的进一步分析,拟明确基因克隆性和DNA修复突变对血浆肿瘤突变负荷(pTMB)的影响及其与MSS型mCRC接受免疫治疗疗效间的关系。今年ASCO会议中公布的结果说明:TMB≥28 mts/Mb是单独最佳支持治疗(BSC)的不良预后指标,且TMB≥28mts/Mb的患者接受Durvalumab + Tremelimumab + BSC治疗相比只接受BSC治疗的患者可取得更好的OS获益(5.5月 vs 3.0月),因此TMB≥28mts/Mb可考虑作为预测预后的指标。本次ESMO大会报道的结果根据基因克隆性将TMB分为了亚克隆TMB(突变频率小于最大突变频率10%的TMB)和克隆TMB,结果显示克隆TMB≥10.6mts/Mb,亚克隆TMB≥26mts/Mb均与Durvalumab + Tremelimumab + BSC治疗的OS获益相关,研究者还对抗表皮生长因子受体(EGFR)单抗前线治疗对TMB的影响进行了分析,提示抗EGFR单抗治疗可能使TMB升高,并且可能改变了克隆TMB和亚克隆TMB的构成比,这可能是其他MSS型mCRC进行免疫治疗失败的原因。
上述研究提示免疫治疗在MSS型mCRC中仍有大作为的可能,但仍处于探索阶段,患者数量少、缺少明确的预测预后标志物,因此MSS型mCRC的免疫治疗之路仍需要更多、更大的临床研究数据来支持。
3.驱动基因阳性mCRC患者的靶向治疗
mCRC患者中人类表皮生长因子受体2(HER-2)阳性患者占比约5%,在RAS野生型患者中HER-2阳性患者的比例会更高,因此RAS野生型且HER-2阳性患者的治疗也逐渐成为结直肠癌治疗领域中的关注问题。在我国部分地区,HER-2的基因检测已成为mCRC的必检项目,NCCN指南推荐HER-2阳性者二线可采用曲妥珠单抗联合帕妥珠单抗或曲妥珠单抗联合拉帕替尼的治疗。现将本次ESMO大会中关于HER-2靶向治疗的结果进行汇总分析。
LBA35报告了帕妥珠单抗联合曲妥珠单抗-美坦新(T-DM1)治疗HER-2阳性/RAS野生型mCRC 的HERACLES研究(B队列)。HERACLES研究的A队列结果早前已经公布:曲妥珠单抗联合拉帕替尼治疗mCRC,带来30%的ORR,且达到PR的患者中88%为HER-2评分≥3分的患者。本次大会报道的B队列纳入了30例既往接受过曲妥珠单抗联合拉帕替尼治疗的患者,其中HER-2 强阳性(免疫组化检测IHC 3+)者占比80%,阳性(IHC 2+)者占比20%。结果显示ORR为10%,DCR为80%,mPFS为4.8个月,亚组分析后发现,HER-2 强阳性患者的mPFS为5.7个月,阳性患者的仅为1.9个月,统计有显著差异(图3)。但由于患者数量少,强阳性患者是否可从HER-2靶向治疗联合化疗中获益仍需要进一步探索。
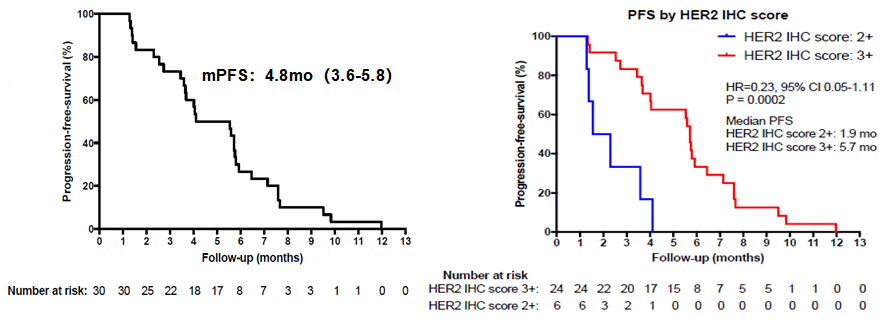
图3. 帕妥珠单抗+T-DM1联用在HER-2强阳性患者中PFS获益更显著
527PD则报告了另一个HER-2靶向治疗的结果,研究采用HER-2靶向小分子和单抗类药物联用的方案,探索了Tucatinib联合曲妥珠单抗在HER-2阳性/RAS野生型mCRC中后线治疗的疗效,结果显示三线治疗的ORR为46.2%,mPFS为8.1个月,mOS为18.7个月(图4),亚组分析结果提示ORR获益集中于原发灶位于左半结肠和直肠患者中,这部分患者的ORR达到64.7%,mPFS为11.7个月;而右半结肠患者的ORR为0。
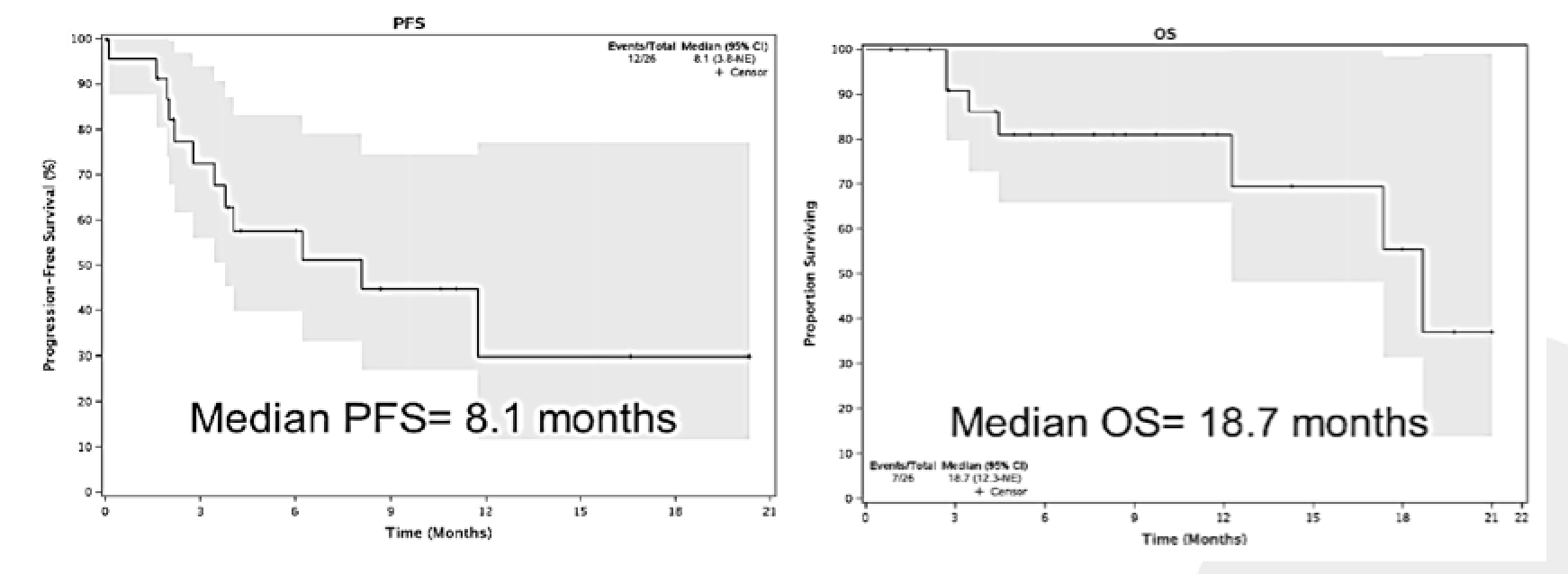
图4. Tucatinib联合曲妥珠单抗治疗mPFS为8.1月,mOS为18.7月
LBA32的BEACON 研究报告了BRAF V600E患者的相关进展,该研究探索了Encorafenib+西妥昔单抗±Binimetinib在二线以上治疗BRAF V600E mCRC中两药联合以及三药联合的疗效和安全性。
既往已经公布了研究主要终点,即两药组和三药组分别与对照组进行比较,研究达到主要终点,三药组(Encorafenib+西妥昔单抗+Binimetinib)与对照组相比,患者的OS和PFS均显著获益。本次大会公布的结果对两药组(Encorafenib+西妥昔单抗)和三药组进行了比较,在中位随访7.8个月时,三药组与两药组相比,OS无显著差异,mOS分别分9.0 vs. 8.4个月(HR 0.79;95%CI:0.59-1.06);进一步延长随访时间至12.5个月,三药组OS有获益的趋势,两组的mOS分别分9.5 vs. 8.3个月(HR 0.74;95%CI:0.53-1.04,图5)。BRAF突变是指南中最早推荐必检基因内容之一,携带BRAF突变的患者生存期短,单独西妥昔单抗治疗无效,美国国家综合癌症网络(NCCN)指南中有多个针对BRAF V600E的治疗组合,Encorafenib+西妥昔单抗+Binimetinib位列其中。
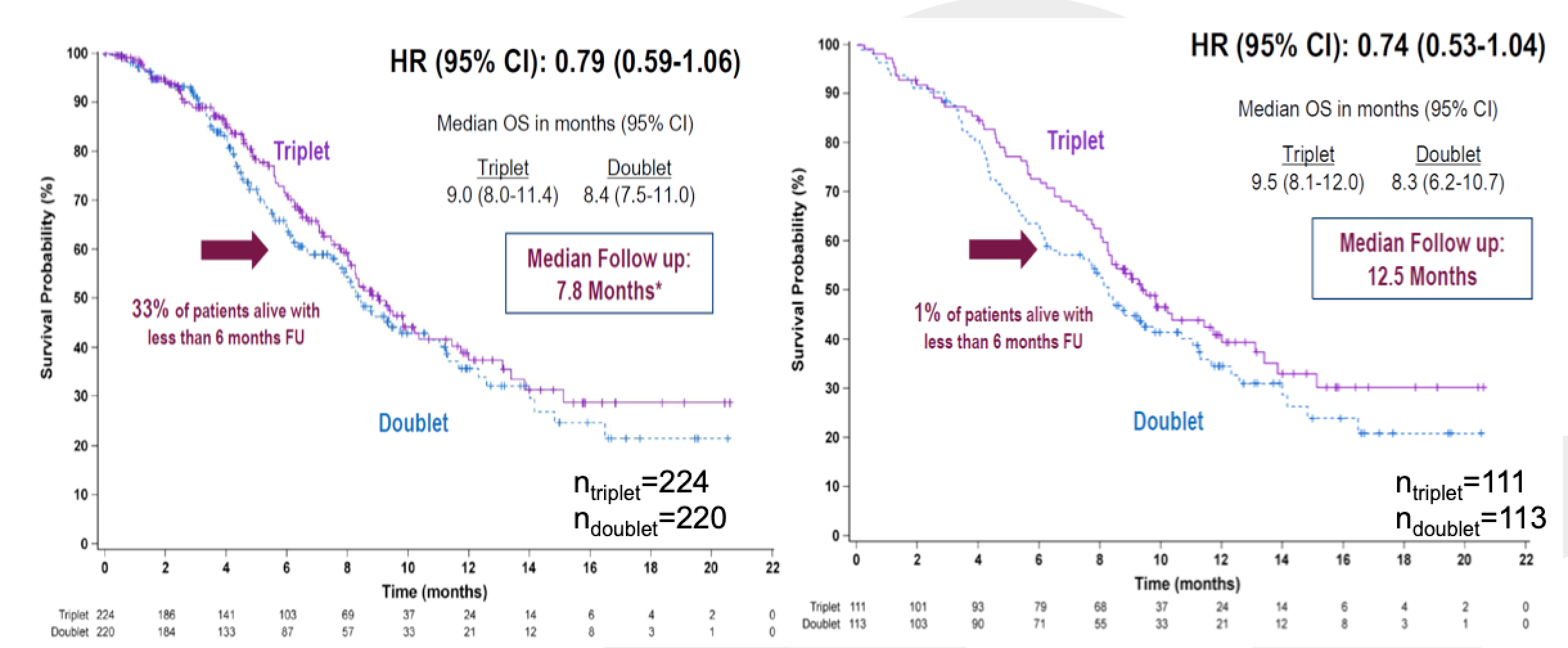
图5. 三药组与两药组中位随访时间的mOS对比
4.靶向联合化疗治疗新进展
肝转移是mCRC的常见转移部位,通过转化治疗,提高肝转移的切除率,有望改善这类患者的预后。本次ESMO上LBA31是来自中国许剑民教授牵头进行的BECOME研究,该研究以切实的临床研究结果证实了临床实践中一直在做的事,即贝伐珠单抗联合FOLFOX转化治疗不可切除、仅肝转移且RAS突变的mCRC,可显著提高R0切除率,PFS和OS获益显著(图6)。
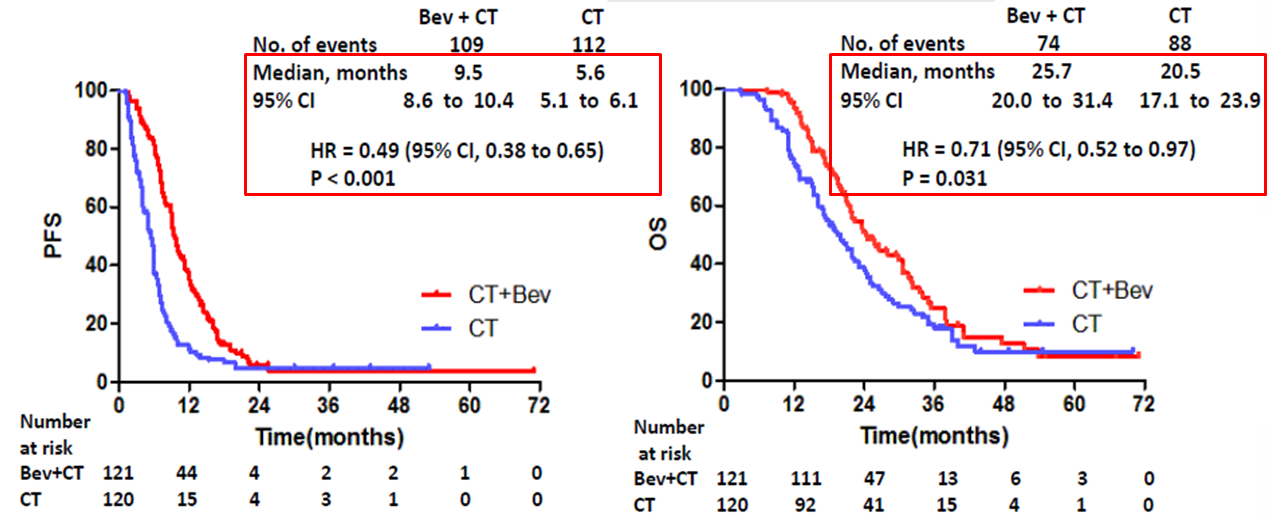
图6. 贝伐珠单抗联合FOLFOX治疗的PFS和OS获益显著
本次会议还对TAS-102联合贝伐珠单抗在mCRC领域中的应用进行了分享。620P的研究显示TAS-102联合贝伐珠单抗一线治疗老年mCRC,mPFS为8.0月,OS尚未达到,ORR为40.5%,且无论有无RAS突变,患者获益相似。619P则探讨的是TAS-102联合贝伐珠单抗二线以上治疗mCRC,mPFS为3.7个月,OS为9.1个月,ORR为3.1%,RAS野生型和突变型的获益无差异。621P则是专注于TAS-102联合贝伐珠单抗三线治疗mCRC,mPFS为4.3个月,OS为13.3个月,ORR为4.4%。上述研究结果表明,TAS-102联合贝伐珠单抗全线治疗mCRC均可获益,且获益不受RAS突变状态影响。
在新的治疗时代,结直肠癌的循证医学领域正以精准治疗为手段,以提高患者生存质量为目的地开展相关研究。在辅助治疗阶段,合理利用分子标志物精准筛选患者群,减少部分患者的过度用药,筛查易复发人群,为其制定精准治疗方案以提高生存质量。在晚期结直肠癌的精准治疗中,根据驱动基因细分患者已逐渐被认可,如HER-2阳性、BRAF V600E、NTRK、MSI-H/MSS等,但相应的治疗方案仍需更有力的循证医学证据来支持,更大程度为患者带来增效减毒的生存获益。
锐意进取的肝细胞癌治疗
1. 单药治疗晚期肝细胞癌新选择
近年,沉寂多年的肝细胞癌治疗因靶向治疗和免疫治疗的到来而取得了一些新的进展。本次ESMO会议上有关晚期HCC比较受瞩目的研究是Checkmate 459研究,头对头对比纳武利尤单抗与索拉非尼一线治疗晚期HCC,主要研究终点为OS,次要研究终点包括ORR、PFS、PD-L1与疗效的相关性、健康相关生存质量(HRQoL)。结果显示两组的OS分别为16.4和14.7个月,mPFS分别为3.7和3.8个月,并无显著统计学差异;但亚组分析显示,肿瘤细胞的PD-L1表达阳性患者较阴性患者有获益趋势(图7)。该研究同时显示,纳武利尤单抗在一线治疗晚期HCC上较索拉非尼有更好的安全性。
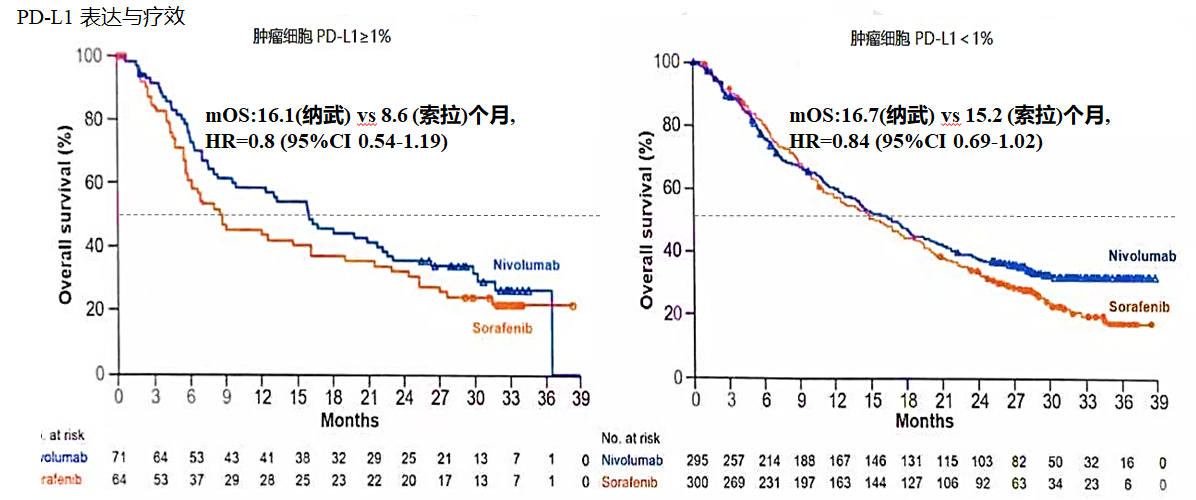
图7. 肿瘤细胞PD-L1表达≥1% 有更多获益趋势
676PD报告的是KEYNOTE 240研究,分析帕博利珠单抗对比最佳支持治疗二线治疗晚期HCC对于生活质量影响,结果显示两组对于生活质量的影响并无显著差别,提示帕博利珠单抗在二线治疗晚期HCC上有着较好的风险获益平衡。
751P则报道的是另一引人关注的研究ALTER 0802,安罗替尼单药一线和二线治疗晚期不可切除HCC的中期分析。其中队列1为一线治疗组,队列2为二线治疗组,分别有26例及17例纳入此次中期分析。研究结果显示,一线治疗组和二线治疗组的DCR分别为84.6%和76.5%,疾病进展时间(TTP)分别为5.5和4.01个月,OS为10.8个月和尚未达到(图8)。上述结果提示,安罗替尼单药在治疗晚期肝癌上有着持续良好的疗效,特别是二线治疗上有着潜在的优势,且安全性良好,患者耐受性好。
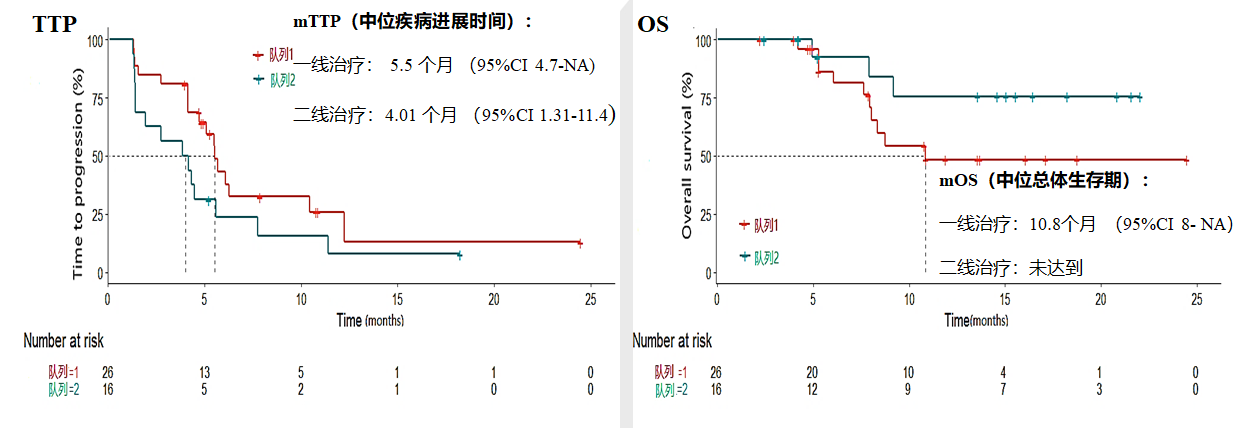
图8.安罗替尼单药一线和二线治疗晚期不可切除HCC探索的中期分析
总体而言,晚期HCC的单药免疫治疗的安全性已较多得到证实,但单药免疫治疗的疗效仍需更多探索,靶向治疗中以安罗替尼为代表的小分子、多靶点酪氨酸激酶抑制剂的单药治疗有效性前景可期。
2.抗血管生成联合免疫治疗晚期肝细胞癌不断在突破
免疫联合免疫、免疫联合抗血管生成、免疫联合化疗在各个瘤种的研究层出不穷,晚期HCC领域也不例外。LBA39为GO30140研究,报告了阿特珠单抗联合贝伐珠单抗一线治疗不可切除HCC的研究结果,研究中A臂为阿特珠单抗联合贝伐珠单抗单臂的临床试验,2019年ESMO报道时入组104例,ORR 36%, DCR 71%, mPFS 7.3个月;F臂为阿特珠单抗联合贝伐珠单抗对比单药阿特珠单抗随机对照临床试验,mPFS分别为5.6和3.4个月(图9)。上述结果表明阿特珠单抗联合贝伐珠单抗有望成为晚期HCC一线治疗新选择。
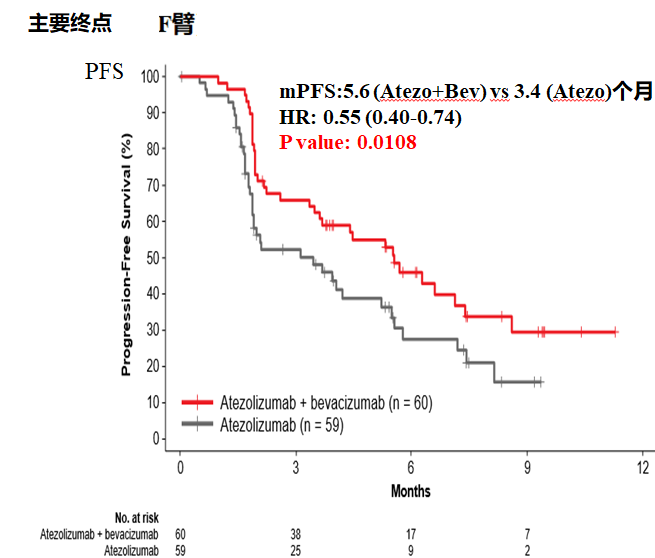
图9. 联合治疗组mPFS明显长于阿特珠单抗单药治疗组
747P报告的则是KEYNOTE 524研究,仑伐替尼联合帕博利珠单抗治疗不可切除HCC研究更新结果,主要终点为ORR,无论是研究者还是独立影像评估,mRECIST或RECIST 1.1 标准评估,ORR均达到了史无前例的40%以上,DCR超过80%,OS达20.4个月(图10),显示出该组合在一线治疗晚期HCC上良好及持久的疗效,2019年7月该组合获得FDA突破性药物资格。
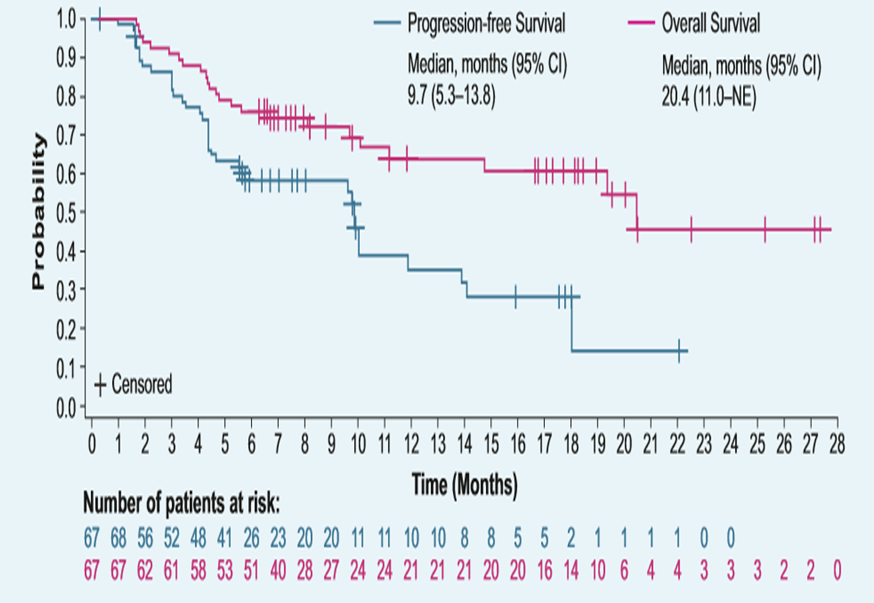
图10. 仑伐替尼联合帕博利珠单抗治疗不可切除HCC结果
3.生物标志物的研究前路漫漫
虽然免疫治疗与靶向治疗在晚期HCC治疗上取得了不菲战绩,但实现更精准的治疗一直是人们追求的更高目标。678PD探索了卡博替尼在CELESTIAL研究中基于血清生物标志物的疗效分析,但遗憾的是,未能发现与卡博替尼治疗获益相关的预测标志物。755P报告的是甲胎蛋白(AFP)在RESORCE研究中对于瑞戈非尼治疗反应的探索,与安慰剂治疗患者相比,瑞戈非尼治疗患者AFP反应的比例更高(46%和11%),且AFP反应与更长的OS相关,因此AFP反应作为HCC患者治疗结局预测指标值得进一步探究。744P报告的是中性粒细胞和淋巴细胞比值(NLR)、血小板和淋巴细胞比值(PLR)在纳武利尤单抗治疗HCC中的预测价值,结果显示不论治疗前后,低水平的NLR和PLR与长的OS相关,因此PLR和NLR有可能成为潜在纳武利尤单抗治疗HCC的OS预测指标,为其他免疫治疗标志物的探索提供参考。
胰腺癌与胆管癌治疗的不断尝试
胰腺癌侵袭性强,预后极差,尽管近年靶向治疗与免疫治疗风头无限,但在胰腺癌治疗上均折戟沉舟,除针对乳腺癌易感基因(BRCA)靶点治疗外,胰腺癌治疗目前仍以手术和化疗治疗为主。671O报告了NEOLAP研究结果,该研究比较了白蛋白结合型紫杉醇联合吉西他滨或基于FOLFIRINOX方案的诱导化疗对于局部进展期胰腺癌(LAPC)转化率的影响,673PD则报告的是GISCAD研究结果,白蛋白结合型紫杉醇联合吉西他滨对比吉西他滨治疗局部进展期不可切除胰腺癌,两项研究同时显示白蛋白结合型紫杉醇联合吉西他滨治疗不可切除局部进展期胰腺癌的良好疗效。
胆管癌作为发病率相对较低的瘤种,一直以来未能得到更多关注,患者愈后极差,但以基因筛查为基础的靶向治疗似乎为晚期胆管癌治疗注入新的活力。LBA10报告的是全球III期AG120-C005研究结果,采用Ivosidenib对比安慰剂治疗IDH1突变晚期胆管癌,Ivosidenib明显提高IDH1突变晚期经治胆管癌患者的PFS(图11)和OS(校正后),安全性亦较好。
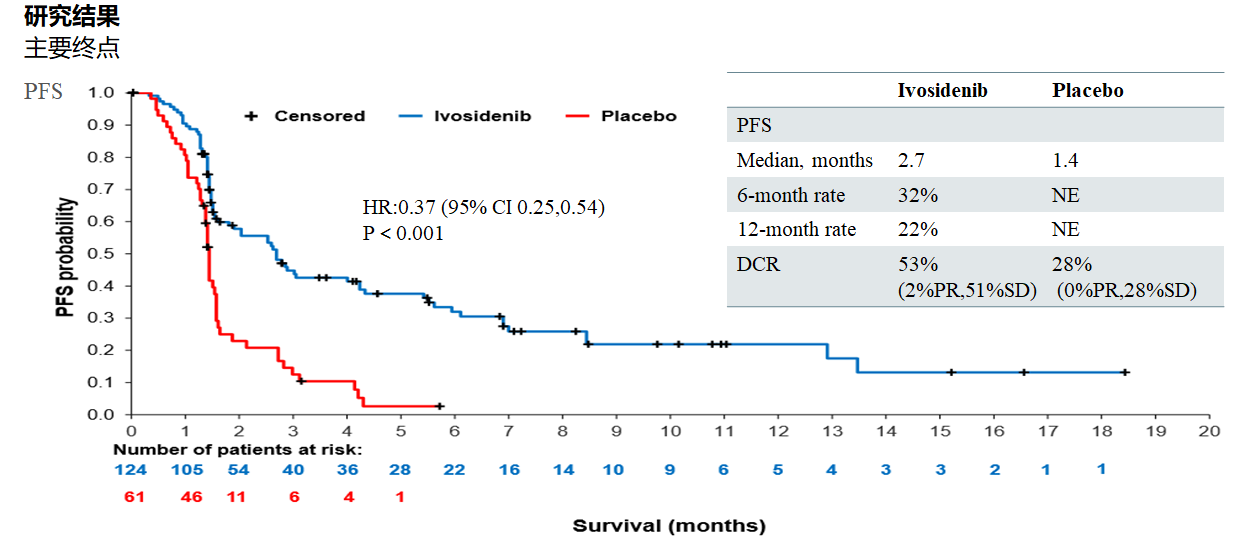
图11. Ivosidenib明显提高IDH1突变晚期经治胆管癌患者的PFS
LBA40报告的是II期临床研究FIGHT-202结果,采用Pemigatinib 治疗既往经治的局部晚期或者转移性胆管癌,携带成纤维细胞生长因子受体2(FGFR2)基因融合/重排患者有潜在的生存获益,安全性良好。评估Pemigatinib 对比吉西他滨+顺铂一线治疗FGFR2融合/重排胆管癌的III期研究正在进行中。
结束语——聚焦当下,绽放未来,不忘使命,砥砺前行
ESMO的大幕已落下,但ESMO带来的学术冲击远未结束。从上述研究可以看出,精准治疗是未来研究的主导,标志物鉴定、靶点基因检测、有针对性的靶向治疗与免疫治疗势必占据肿瘤治疗的主战场,大瘤种的研究愈发精细化,小瘤种的研究更有针对性,不断提高有效率,改善患者生存,甚至达到治愈的同时,尽最大努力保证患者生活质量,将会一直是我们追求的目标。
安罗替尼是由正大天晴药业集团股份有限公司自主研发的是一种新型小分子多靶点酪氨酸激酶抑制剂,能有效抑制血管内皮生长因子受体(VEGFR)、血小板衍生生长因子受体(PDGFR)、成纤维细胞生长因子受体(FGFR)、干细胞生长因子受体(c-Kit)等激酶活性,具有抗肿瘤血管生成和抑制肿瘤生长的双重作用。从2007年开始申请化合物专利到正式上市,正大天晴和广大的医护人员、肿瘤患者一起见证了肿瘤药物研发的辉煌历程。目前,安罗替尼相关的临床研究正在多个瘤种中同时进行。
除了专注于肿瘤药物的研发和临床研究,正大天晴还致力于学术传播。在今年的ESMO大会后,在全国范围内开展的“安之有道--2019年 ESMO会后会热点速递”系列大会,得到全国消化道肿瘤工作者的大力肯定;未来,正大天晴将继续在学术和研究上进一步努力,期待造福更多肿瘤患者。
部分会议现场掠影:


















 苏公网安备32059002004080号
苏公网安备32059002004080号


