2019年ASCO盛会于5月31日至6月4日在美国芝加哥召开。今年大会主题:Caring for Every Patient, Learning from Every Patient。值此盛会之际,《新见》栏目特邀乳腺癌领域专家学者共同推出六期ASCO-BC特刊,报道与点评乳腺癌领域热点。特刊第二期特邀中国科学院大学附属肿瘤医院(浙江省肿瘤医院)郑亚兵教授:就“Genomic markers in the PALOMA-3 trial”展开精彩回顾与点评。

中国科学院大学附属肿瘤医院(浙江省肿瘤医院)乳腺肿瘤内科 病区副主任、主任医师
中华医学会肿瘤学分会乳腺肿瘤青年学组委员
中国医药教育协会乳腺疾病专业委员会委员
浙江省医师协会乳腺肿瘤专业委员会常委
中国医药教育协会乳腺疾病专业委员会浙江分会常委
中国抗癌协会乳腺癌专业委员会青年委员
浙江省抗癌协会乳腺癌专业委员会青年委员会常委
浙江省康复医学会青年理事会理事
浙江省转化医学学会精准医学分会副会长
浙江省抗癌协会肿瘤内科专业委员会青年委员

《新见》是由中华医学会肿瘤分会乳腺肿瘤青年学组主办的国际会议期刊文献解读与点评专栏。
背景
既往研究表明,内分泌治疗(氟维司群)联合CDK4/6抑制剂方案治疗内分泌治疗耐药ER+晚期乳腺癌 (ABC)患者相比氟维司群单药取得更好的疗效,但是治疗中仍有部分患者发生早期进展(early relapse),目前对这些治疗方案中提示早期进展的相关标记物的认识仍有限。
本研究通过对基线血浆中循环肿瘤 DNA 的分析探讨了 PALOMA-3 试验中氟维司群±哌柏西利经治患者的基因组突变情况。
方法
PALOMA-3 Ⅲ期试验将 521 名 ER+HER2-ABC 患者按 2:1 随机分配至哌柏西利+氟维司群组(P+F)和安慰剂+氟维司群组(F)。收集了459(88.1%的ITT人群)例患者血浆用于检测基线ctDNA水平,基线ctDNA检测采用商业化的测序panels,主要包括检测17个靶向驱动基因全外显子或者热点突变检测,评估827个常见SNPs的肿瘤基因片段以及对11个基因扩增拷贝数的分析。一共有310例标本可进行全ctDNA的分析,其中331例做了突变检测,401例标本分析了循环肿瘤基因片段(circulating tumor fraction CTF)和基因拷贝数,CTF预设的cut-off值是10%。单因素和多因素Cox比例风险模型分析这些结果与临床因素及 PFS 的相关性。用一个 17 基因组分析基线血浆样本中的体细胞突变情况。同时用一个包括8个常见突变位点中~800SNPs的14基因组标记拷贝数变异(CNA),以此估算肿瘤纯度,血浆中来源于肿瘤细胞DNA 比例。可从 310 名患者(P+F 组 n=203,F 组 n=107)中获得突变和 CNAs 结果,并通过单因素和多因素Cox比例风险模型分析这些结果与临床因素及 PFS 的相关性,其中变量包括肿瘤纯度和治疗方案。
结果
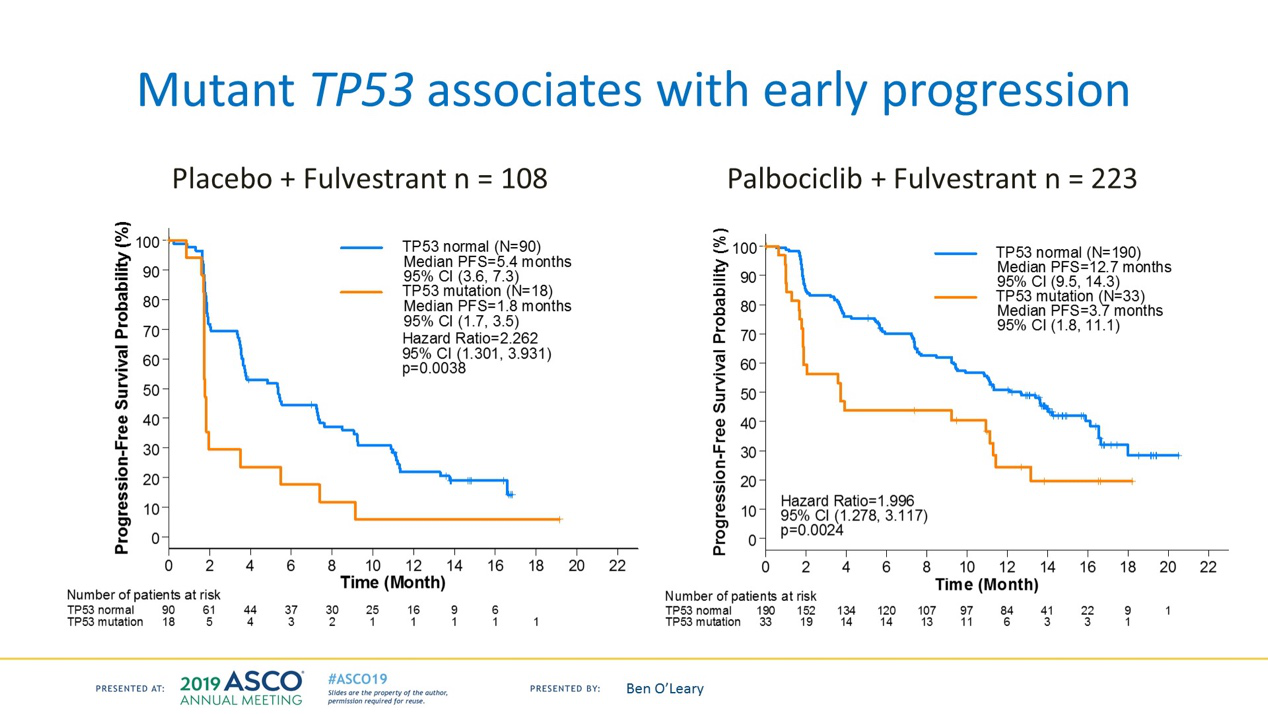
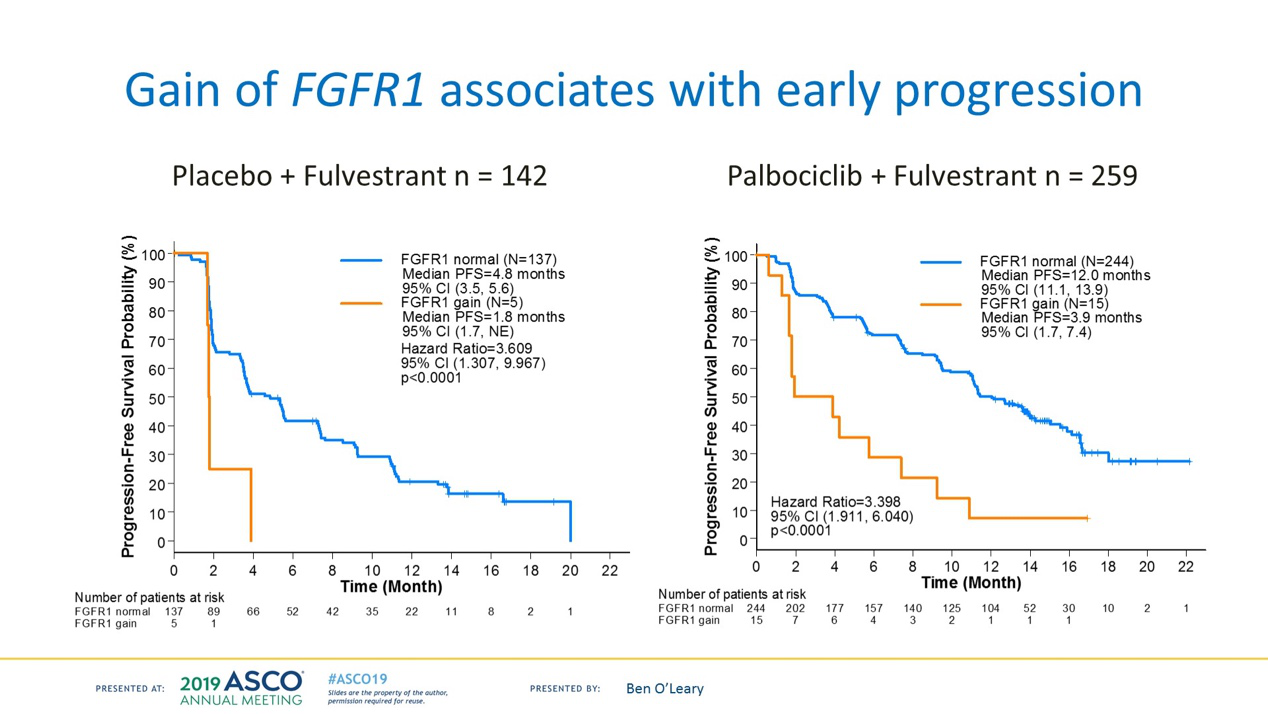
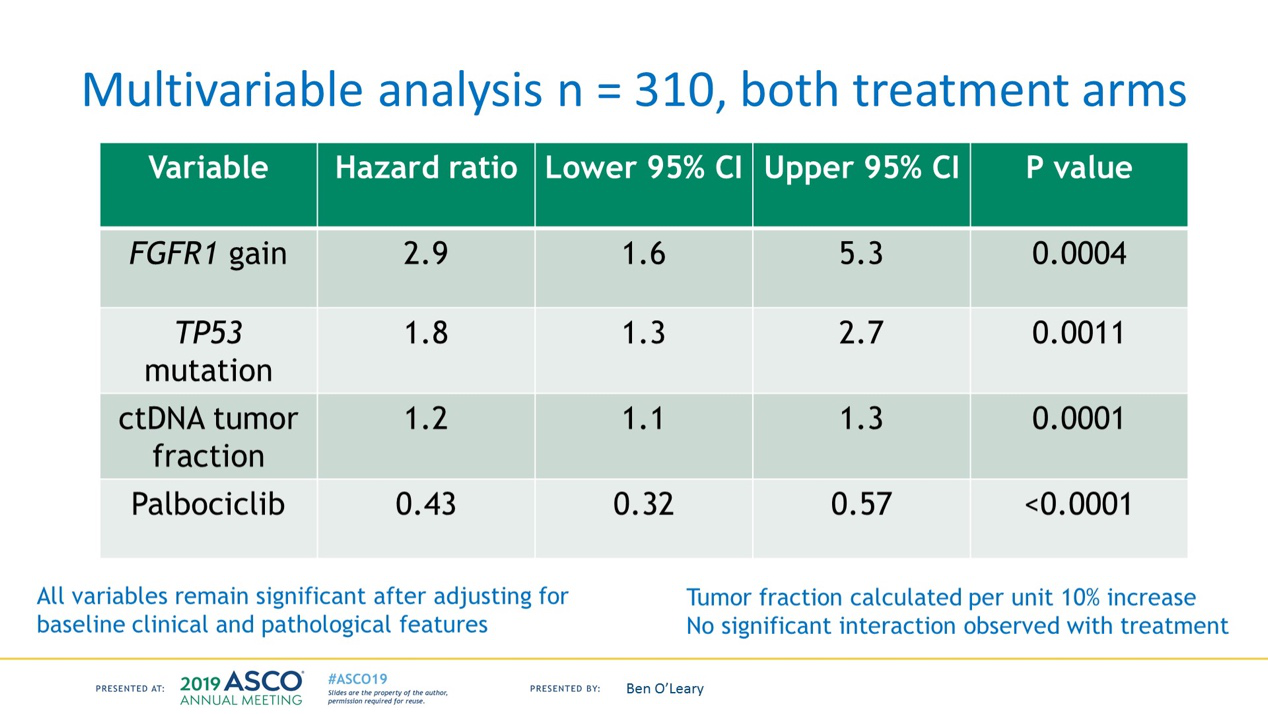
整体队列的多因素分析中,血浆基线循环肿瘤基因片段>10% (HR 1.20, 95% CI 1.09~1.32, P= 0.0001, HR per 10% increase in purity)、TP53 突变(HR 1.84, 95%CI 1.27~2.65, P= 0.0011)及 FGFR1 扩增(HR 2.91, 95%CI 1.61~5.25, P= 0.0004)均提示 PFS 较差。 多因素分析未显示 PI3KCA 和 ESR1 突变与 PFS 相关。与总体试验结果一致,哌柏西利可显著改善 PFS(HR 0.43, 95%CI 0.32~0.57, P< 0.0001)。通过多次检验矫正后发现 TP53 突变与内脏转移(q = 0.046)、软组织/淋巴结转移(q = 0.042)以及病灶部位的数目(q = 0.0086)显著相关。
结论
血浆中 TP53 突变、 FGFR1 扩增及循环肿瘤基因片段>10%可甄别出 PALOMA-3 试验中具有早期进展风险的人群。当然这需要进一步的临床试验验证,对这部分高风险的人群未来的临床治疗可能需要更强的治疗方案。一经验证,这些结果可以为未来开展 CDK4/6 抑制剂联合方案的相关临床试验提供信息。
专家点评
随着新的内分泌药物和靶向药物的不断研发上市,内分泌治疗在ER+晚期乳腺癌中的地位不断提升,其中,CDK4/6抑制剂更是近几年来的明星药物。三个不同的CDK4/6抑制剂联合AI在ER+晚期乳腺癌一线治疗中都取得了PFS时间超过2年的好成绩,联合氟维司群在二线治疗中PFS也明显优于单药氟维司群,PALOMA-3研究中,哌柏西利+氟维司群的PFS时间为11.2月,安慰剂+单药氟维司群PFS时间仅为4.6月,而在MONARCH-2研究和MONALEESA-3研究中观察不同的CDK4/6抑制剂联合氟维司群,同样看到患者PFS延长获益。可以看到,CDK4/6抑制剂联合氟维司群已经成为内分泌治疗进展的转移性乳腺癌患者的标准治疗选择。
有没有明确的生物标志物来预测CDK4/6抑制剂的优势人群?目前为止仍缺乏循证医学证据,从PALOMA-1到PALOMA-2研究,都试图去寻找这样的预测指标,包括RB1、CCND1、p16、PIK3CA、CCNE1、ESR1等,但都无功而返。同样,对于CDK4/6抑制剂使用后再进展的耐药机制仍不是很清楚,尽管临床前研究表明多个基因如RB缺失、CCNE1扩增、FAT1缺失等机制可能与耐药相关,但仍缺乏有效的临床预测指标。部分患者即使使用了CDK4/6抑制剂,仍会发生早期进展,其具体机制及预测指标仍不明确。该项研究通过对PALOMA-3入组病人检测其血浆中ctDNA的水平来预测肿瘤的早期进展,并探索哌柏西利联合氟维司群治疗可能的预测指标。结果证明所有患者基线ctDNA中,具有TP53突变、 FGFR1 扩增及循环肿瘤基因片段>10%的患者早期进展风险较大,这些因素反映的是此类人群本身的特点,即初次内分泌治疗耐药后并携带这些因素的患者后续治疗整体疗效不佳。其中较高ctDNA纯度可能意味着较高的肿瘤负荷或更活跃的肿瘤细胞,引起患者治疗或预后不良不能算意外;而TP53突变在乳腺癌中是经典的预后不良因素。同时也提示对这类病人未来的临床治疗可能要采取更强的治疗方案,当然也需要更多前瞻性临床试验来验证这一结果。
本研究中也并未发现CDK4/6抑制剂本身相关的疗效预测指标。哌柏西利作为针对基因靶点的靶向治疗,理论上旁路或者本通路基因的激活可能作为这类药物的耐药机制,本研究中检测的基因并不多或许限制了这个方向的探索。但是这个研究结果依然提供了重要的信息,即在今后的药物临床试验中或许要把这些这些早期进展相关的因素考虑在内。
敬请关注《新见》ASCO-BC特刊
第一期:
复旦大学肿瘤医院余科达教授:NSABP clinical trials in early breast cancer: A 60-year odyssey
第二期:
北京大学肿瘤医院邵彬教授:Biomarker analysis of the APHINITY trial
浙江省肿瘤医院郑亚兵教授:Genomic markers in the PALOMA-3 trial
第三期:
广东省中医院大学城医院陈前军教授:Adjuvant Targeted Therapy: When Is More Better?
中山大学肿瘤防治中心史艳侠教授:TALA in Breast Cancer
第四期:
福建省立医院叶松青教授: GeparOLA: A randomized phase II trial
吉林大学第一医院宋东教授:Biomarkers in BC: BRCA/HRD/PD-L1
第五期:
武汉同济医院李兴睿教授:What is the role of surgery in metastatic breast cancer?
天津肿瘤医院王忱:CDK4/6 inhibitors:Optimizing Care in ER-positive Breast Cancer
第六期:
中国医科大学附属第一医院徐莹莹教授:Breast Cancer: 40 years of Research and Progress &Emerging system therapies:What’s new in 2019?
精彩回顾
【新见】徐莹莹教授&邢鹏教授:剂量密集型化疗在靶向治疗时代的价值
【新见ASCO特刊】余科达教授:NSABP乳腺癌研究60年奥德赛之旅













 苏公网安备32059002004080号
苏公网安备32059002004080号


