随着手术、放疗及系统治疗的进步,部分类型乳腺癌已获得较高生存,但三阴性乳腺癌(TNBC)由于缺乏靶点,仅有的化疗疗效有限,患者生存期短。近年免疫治疗在肿瘤治疗中取得重大突破,IMpassion130研究首次证明免疫治疗对TNBC有治疗作用,此外还有大量乳腺癌免疫治疗研究正在进行。中国医学科学院的徐兵河教授座客【肿瘤资讯】,为乳腺癌医师详解乳腺癌免疫治疗的前世今生,并提出乳腺癌免疫治疗的未来发展方向。

中国医学科学院、北京协和医学院肿瘤医院内科主任
中国抗癌协会乳腺癌专业委员会第七届主任委员
中国抗癌协会肿瘤药物临床研究专业委员会候任主任委员
国家肿瘤质控中心乳腺癌专家委员会主任委员
中国老年医学学会肿瘤分会副会长
北京乳腺病防治学会理事长
北京乳腺病防治学会内科专业委员会主任委员
北京肿瘤学会副理事长
St.Gallen早期乳腺癌治疗国际专家共识团成员
国际局部晚期和转移性乳腺癌共识(ABC consensus)专家团成员
现代乳腺癌概况
▎ 流行病学
徐兵河教授:乳腺癌是女性最常见的恶性肿瘤,全球每年新发乳腺癌病例数超过160万,中国每年新发病例数超过27万。总体来说,乳腺癌发病率呈快速上升趋势,增速每年3%-4%,位居女性恶性肿瘤第一位。虽然乳腺癌发病率较高,但死亡率相对低于肺癌、胃肠道肿瘤等,这主要得利于乳腺癌的早期诊断和综合治疗,只要认真进行筛查就可以提高乳腺癌的早期诊断率。
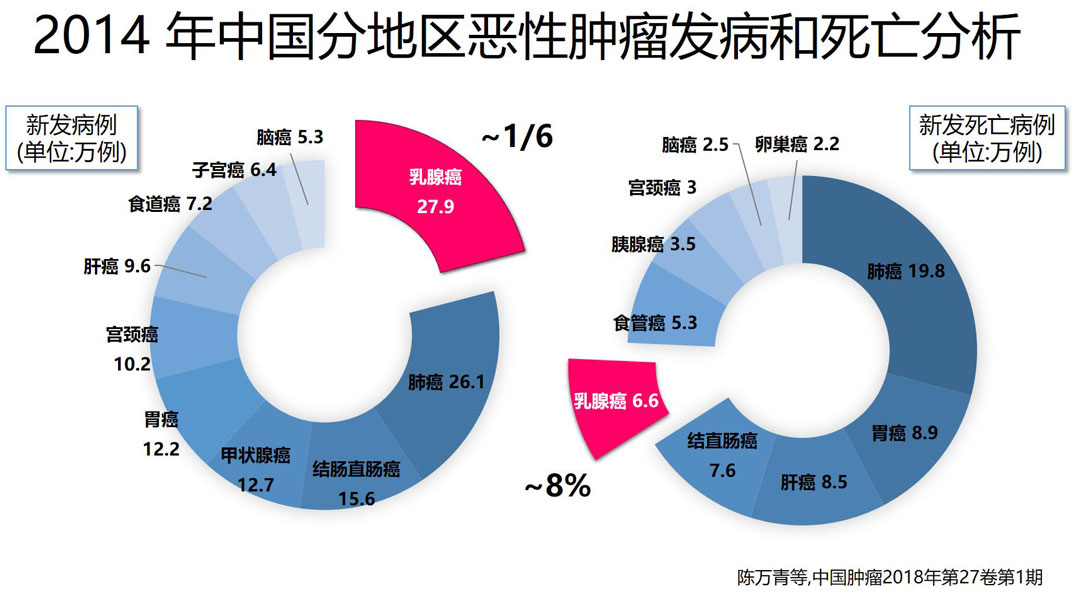
▎治疗现状
治疗方面现在强调的是分子分型指导的治疗。对于可手术的乳腺癌以手术治疗为主,术后根据分子分型、分期等多项指标决定其他治疗手段的选择,包括化疗、靶向治疗、内分泌治疗、放疗等。对一些局部晚期患者,还需要新辅助治疗。
分子分型对全身治疗手段选择的影响较大,2011年St.Gallen早期乳腺癌共识里[1],首次提出应根据乳腺癌分子分型指导全身治疗,这种理念在实体肿瘤治疗中提出较早。乳腺癌的分子分型主要基于ER、PR、HER2和Ki67分型,不同亚型的治疗手段并不一样,主要包括四种亚型:Luminal A、Luminal B、三阴性(TNBC)和HER2阳性乳腺癌。Luminal A型以内分泌治疗为主;Luminal B型也是以内分泌治疗为主,并根据不同情况加用化疗,对一部分HER2阳性者要抗HER2治疗;在没有抗Her2治疗前HER2阳性乳腺癌患者预后非常差,但抗HER2治疗使这类患者的预后与Luminal 型患者预后区别不再显著;TNBC治疗手段有限,除了化疗以外,缺少更多有效治疗。
▎TNBC治疗进展
最近几年TNBC的诊疗取得一定进步,最主要的就是将TNBC进一步分型,包括了BRAC基因阳性和雄激素受体表达型等,基于此可进行不同的治疗选择,但主要治疗手段仍是化疗,其中铂类药物和艾日布林对TNBC疗效较好,铂类对有BRAC突变的TNBC疗效更好。今年ASCO会议上我们报道了UTD1联合卡培他滨较单药卡培他滨能够显著延长HER2阴性晚期乳腺癌患者的无病生存和总生存的研究结果,亚组分析也显示联合组对TNBC的效果比单药组要好(图1)[2]。

图1 徐兵河教授ASCO大会作报告
除化疗药以外,靶向药如AKT抑制剂[3]、雄激素受体拮抗剂[4]等也都在研究中。获批的靶向药物PARP抑制剂主要用于TNBC BRCA基因突变亚型,2017年ASCO会议上报道了OlympiAD研究[5],结果显示PARP抑制剂奥拉帕尼较医师选择的单药化疗方案,能够显著延长患者的无进展生存,亚组分析显示对TNBC疗效更好。这是首个证实对BRAC阳性TNBC有效的靶向药物,无进展生存可延长3个月。但BRAC基因突变乳腺癌只占所有乳腺癌的5%-10%,TNBC和家族性乳腺癌中比例略高一些,对大部分TNBC而言,还需要寻找新的治疗手段与策略以进一步改善预后。
乳腺癌的免疫治疗
▎乳腺癌免疫治疗现状
徐兵河教授:免疫治疗实际上经历了几十年起起伏伏,最近几年热度高涨,2018年随着诺贝尔生理学/医学奖揭晓,免疫治疗再次达到高峰,美国免疫学家詹姆斯·艾利森和日本生物学家本庶佑在免疫检查点的发现中做出了突出贡献[6]。现在国内外批准上市的PD-1/PD-L1抗体已经超过6种,获得的适应症包括黑色素瘤、肺癌、淋巴瘤和头颈部肿瘤等多个瘤种,还有多个瘤种正在做临床研究[7],疗效令人鼓舞。虽然免疫治疗在其他瘤种取得巨大突破,但乳腺癌免疫治疗进展相对落后,既往公布的数据均是I/II期结果,这些研究发现PD-1/PD-L1抑制剂单药治疗乳腺癌疗效有限,客观缓解率在0%-20%(图2)[8],同时发现在TNBC和PD-L1表达患者中疗效相对较好。
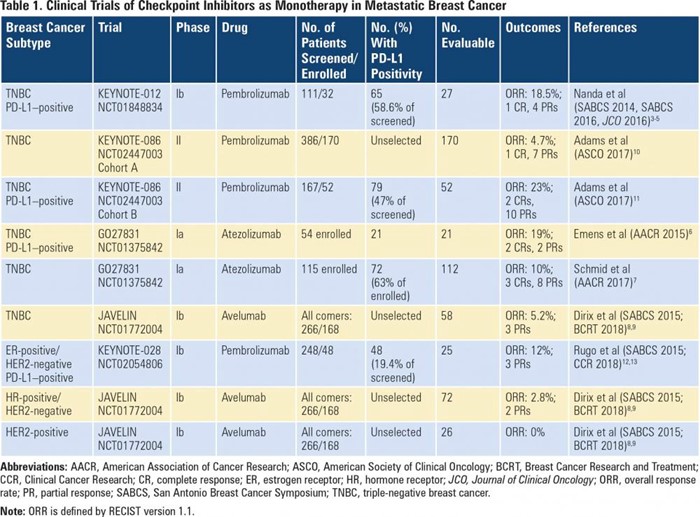
图2 免疫检查点抑制剂单药治疗转移性乳腺癌临床研究结果
▎IMpassion130研究开启乳腺癌免疫治疗新篇章
徐兵河教授:PD-1/PD-L1抑制剂单药治疗效果并不理想,我个人认为原因在于乳腺癌是冷肿瘤,如何将它变成热肿瘤以便免疫治疗产生疗效,这可能就需要联合其他治疗手段,通过增加肿瘤突变负荷、产生更多抗原等,来增加药物疗效。今年ESMO大会上公布的IMpassion130研究结果正式开启了乳腺癌免疫治疗之门,该研究入组晚期TNBC患者,随机接受一线阿替利珠单抗联合白蛋白紫杉醇和安慰剂联合白蛋白紫杉醇治疗,主要终点包括ITT人群和PD-L1+人群的PFS和OS。结果显示(图3),PFS在ITT和PD-L1阳性人群均为阳性结果,PD-L1+人群获益更好;虽然OS数据尚不成熟,但现有结果显示PD-L1+人群实验组的中位OS从对照组的15.5个月延长到25.0个月,延长了9.5个月[9]。这样的数据对于TNBC而言令人振奋,可以说IMpassion130是乳腺癌进入免疫治疗时代的第一步。这个研究同时也提示,对TNBC或是对乳腺癌而言,单用免疫治疗的效果并不好,如何将免疫治疗与其他治疗手段联合产生更好的疗效,这可能是今后的主要研究方向。
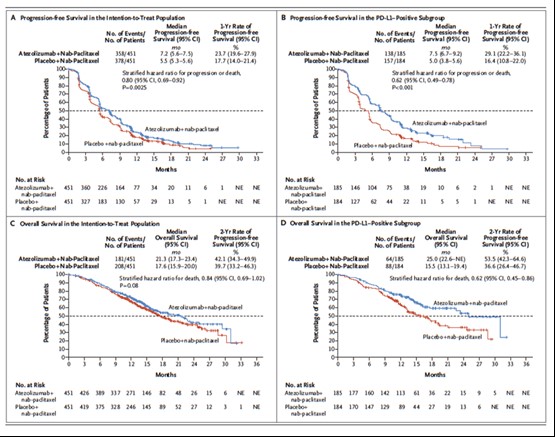
图3 ITT和PD-L1+人群的OS和PFS结果
▎正在进行的乳腺癌免疫治疗研究
徐兵河教授:除了IMpassion130研究之外,还有大量正在进行的乳腺癌免疫治疗研究,大部分为I/II期研究, III期TNBC的研究包括IMpassion131、IMpassion132、IMpassion030、KEYNOTE-355、KEYNOTE-522等[10],HER2+乳腺癌有KATE-2研究[11],ER+HER2-乳腺癌有KEYNOTE-756研究等[12]。以上研究均是免疫治疗与其他治疗手段的联合治疗,这是很好的研究方向。
除了PD-1/PD-L1抑制剂外,其他免疫治疗手段也在乳腺癌中进行探索,今年ESMO大会公布了一项乳腺癌疫苗NeuVax的II期结果,显示其可以预防HER2低表达TNBC的复发[13]。虽然细胞免疫疗法对实体瘤疗效有限,但今年Nautre Medicine上发表了一篇TIL细胞治疗HR+MBC的文章[14],患者达到长期完全缓解,虽然个案报道不能作为证据,但也给出一些启示,这种TIL细胞或其他免疫治疗手段,可能会对乳腺癌有一定治疗效果。

▎乳腺癌免疫治疗发展方向
徐兵河教授:乳腺癌的免疫治疗已经取得一定突破,但仅限于TNBC中证实PD-1/PD-L1抑制剂联合白蛋白紫杉醇优于安慰剂联合白蛋白紫杉醇,对HER2阳性或是HR阳性乳腺癌疗效如何,PD-1/PD-L1抑制剂联合其他化疗药物的疗效如何仍不清楚,也就是说仍有大量问题悬而未决,我个人认为如下几个方面在近期是需要着重进行探讨的内容。
第一,探索免疫治疗生物标记物,基于IMpassion130研究,PD-L1状态已证实为分子标记物,但其检测手段和界值在不同研究中并不统一,需要进一步探索;
第二,需要继续探索免疫治疗的联合治疗策略[15],IMpassion130研究中阿替利珠单抗联合白蛋白紫杉醇具有很好的疗效,那么免疫治疗联合其他化疗方案、抗HER2治疗、内分泌治疗、CDK4/6抑制剂和PARP抑制剂治疗的疗效或是不同免疫治疗间联合的疗效又是如何呢(图4)?这些联合方案如果能够成功,将会进一步提高疗效、扩大治疗人群;
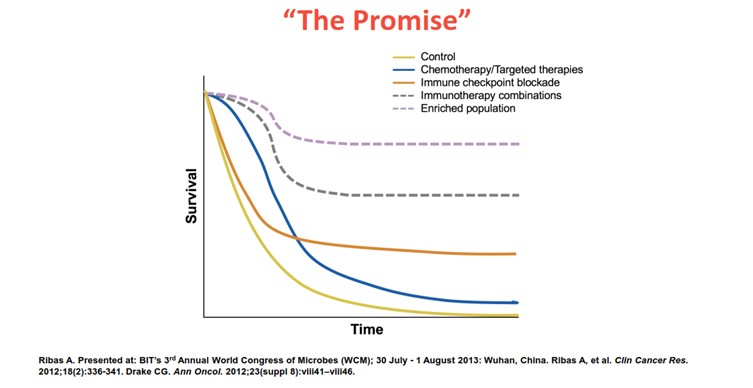
图4 值得继续探索的免疫治疗联合治疗
第三,重视免疫治疗的安全管理问题[16],免疫治疗与传统抗肿瘤药物的特点不同,因过度免疫可造成全身损害,如甲状腺功能异常、肝炎、心肌炎和肺的改变等,如何更好的预防和管理不良反应是临床试验和临床工作中应该关注的方向;
第四,明确疗效评价判断标准也非常重要,传统治疗的疗效评估标准应用于免疫治疗时可能会产生一些问题,如假性进展的情况,所以临床怎样判断假性进展和真进展非常关键,有必要研究新疗效评价工具。现在有探讨采用iRECIST标准指导临床[17],我个人认为这个标准仍有待进一步评估是否可以更好的判断免疫治疗疗效;
第五,肿瘤机制(图5)研究为新药研发提供了基础[18],目前已经批准的PD-1/PD-L1抑制剂、CAR-T细胞等药物,开启了肿瘤免疫治疗时代。但是放眼未来,仍需更多的基础研究和转化研究,发现肿瘤发生发展和转移的机制以及免疫治疗机制,从而开发更多的新药用于临床,提高肿瘤治疗效果,这是肿瘤研究最重要的内容,更是最终目标。
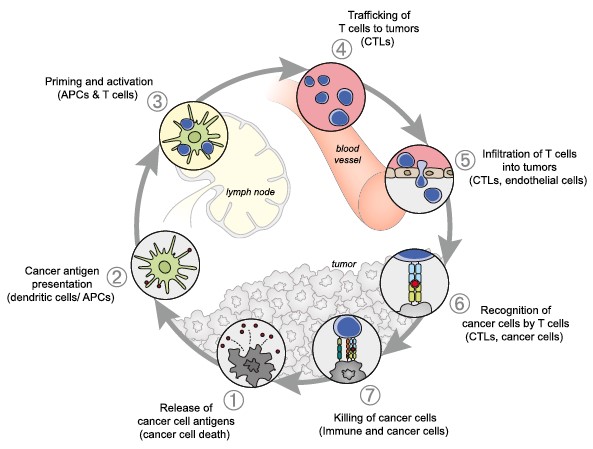
图5 肿瘤免疫机制
▎IMpassion131研究
徐兵河教授:肿瘤的免疫治疗之门已经开启,为肿瘤患者带来更多生的希望,所以患者也特别关注免疫治疗。国内总体而言,乳腺癌免疫治疗的临床研究数据比较缺乏,治疗药物在中国多不可及,而且价格普遍比较昂贵。鉴于IMpassion130研究的阳性结果,而中国患者未能参加该研究,目前国内正在开展IMpassion131临床研究,它是一项国际多中心随机安慰剂对照三期临床研究,该研究也是比较阿替利珠单抗联合紫杉醇和安慰剂联合紫杉醇一线治疗晚期TNBC的疗效和安全性,与IMpassion130研究不同的是采用了2:1的随机设计,患者有更多机会进入实验组。中国目前有20家医院参与该研究,我是该研究的中国首席研究者和全球专家委员会委员,中国大陆患者虽然没有机会参与IMpassion130研究,但可以参与IMpassion131研究,获得获益机会,因此鼓励TNBC患者复发后积极参加研究。
结语
徐兵河教授:免疫治疗是乳腺癌的重要治疗手段之一,免疫治疗开启了乳腺癌治疗的新篇章,希望免疫治疗之路的开启为乳腺癌患者带来更多生的希望。现有研究只是乳腺癌免疫治疗的冰山一角,期待更多研究结果公布,也希望开展更多研究,解决现有问题,期待这些研究结果造福乳腺癌患者。
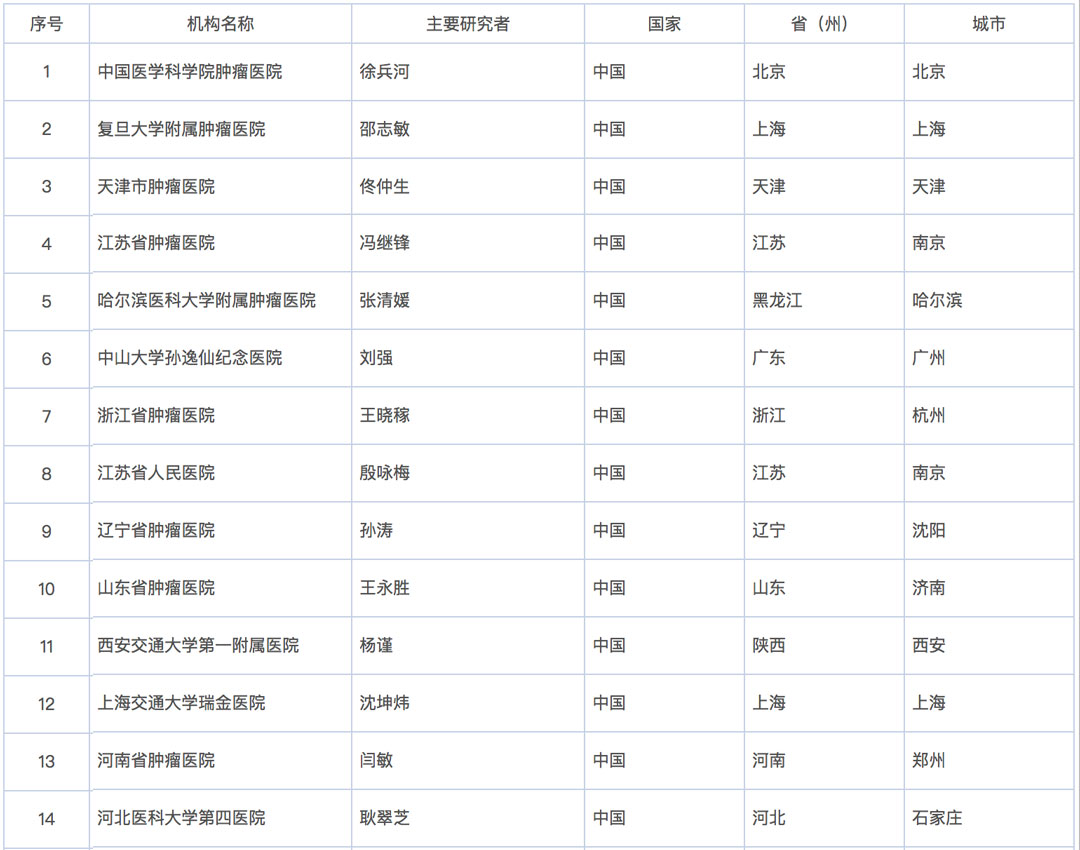
附目前已启动IMpassion 131研究的医院名单
1. Michael Gnant, et al. Breast Care (Basel). 2011 Apr; 6(2): 136–141.
2. Xu BH, et al. ASCO 2018
3. Peter Schmid, et al. ASCO 2018
4.Ayca Gucalp, et al. Clin Cancer Res. 2013 October 1; 19(19): 5505–5512.
5. Mark Robson, et al. ASCO 2017
6. https://www.nobelprize.org/nobel-prizes-2018/
7. https://www.cancer.org/treatment/treatments-and-side-effects/treatment-types/immunotherapy/immune-checkpoint-inhibitors.html
8. http://am.asco.org/checkpoint-inhibitors-breast-cancer-changing-therapeutic-landscape
9. Schmid P, et al. IMpassion130 ESMO 2018 (LBA1_PR)
10. CLINICALTRIALS.GOV: NCT03125902/ NCT03371017/ NCT03498716/ NCT02819518/ NCT03036488
11. CLINICALTRIALS.GOV: NCT02924883
12.CLINICALTRIALS.GOV: NCT03725059
13. DF Hale, et al. ESMO 2018
14. Nikolaos Zacharakis, et al. Nature Medicine 2018
15. Giuseppe Curigliano. ESMO 2018 LBA1_discussion
16. Chapimat S, et al. Ann Oncol.2016;27:559-574
17. Lesley Seymour, et al. Lancet Oncol 2017; 18: e143–52
18. Miguel F. Sanmamed, et al. Cell 2018
想与全国乳腺癌医生同道一起交流,沟通,分享吗?请您发工作牌或者医师证等可以证明医生身份的照片给小明,验明医生身份后邀请入群。更有获得国内线下会议参会机会哦!
















 苏公网安备32059002004080号
苏公网安备32059002004080号


