胃癌(GC)是全球范围内发病率高、致死性强的恶性实体肿瘤之一,对人类健康构成严重威胁。尽管在诊断和治疗上取得了进步,但针对晚期胃癌的选择仍然有限,预后往往较差。代谢重编程是癌症的一个关键特征,其中葡萄糖代谢重塑(GMS)在肿瘤进展和免疫逃避中发挥核心作用。本研究旨在阐明GMS的调控机制,为开发基于GMS的个性化诊断、预后和治疗提供潜在的生物标志物和理论基础。【肿瘤资讯】特整理研究内容,以飨读者。
研究背景
尽管“瓦博格效应”已被公认为癌症的关键特征,并证实其与肿瘤细胞的快速增殖、恶性进展、免疫逃逸以及对化疗的耐受性密切相关,但传统的批量转录组分析往往将整个肿瘤组织视为同质的整体,这种分析方法难以捕捉到肿瘤内部细胞群体的高度异质性以及肿瘤微环境(TME)中不同细胞类型(如肿瘤细胞、免疫细胞、基质细胞)之间在GMS状态上的显著差异。这种对GMS复杂性的认知不足,直接限制了我们理解代谢重塑在GC进展中的作用机制,也成为了开发基于GMS的靶向精准治疗药物和伴随诊断工具的重大挑战。
近年来,以单细胞测序(scRNA-seq)和空间转录组测序为代表的高分辨率组学技术得到了广泛应用,极大地革新了癌症异质性研究。这些技术使得研究者能够以前所未有的分辨率,在单细胞和组织空间位置层面,精准描绘肿瘤细胞亚型的代谢特征、干性状态、恶性程度,并解析细胞间的通讯网络。利用多组学数据(如mRNA、甲基化、突变、lncRNA)进行整合分析,已成为系统性识别关键驱动因素、进行分子分型以及构建稳健预后模型的科学趋势。
本研究正是在弥补传统分析不足和利用高分辨组学优势的背景下展开。研究旨在通过整合单细胞、空间和批量转录组等多层次数据,系统性地描绘胃癌中GM的异质性及其临床相关性。通过鉴定具有高GMS评分的特定上皮细胞亚型(如TOP2A+细胞),揭示其在肿瘤干性、恶性潜能和免疫微环境重塑中的作用,并构建基于GMS相关基因特征的精准预后模型[1]。本研究的最终目标是为胃癌的分子分型、预后风险分层以及开发靶向葡萄糖代谢的个体化治疗策略提供新的生物标志物和理论基础。
研究方法
数据来源与预处理
本研究通过整合多来源、多层次的组学数据,系统性地探究GC中GMS的异质性。核心数据包括来源于GEO数据库GSE163558数据集的scRNA-seq,该数据集经过严格的质量控制和处理,最终纳入了来自GC、转移性GC(MGC)和正常对照样本的细胞进行分析,并使用Seurat、CSS和Harmony方法进行了批次校正。空间转录组数据(stRNAseq)则来源于GSM6177607和GSM6177609两个样本,其中肿瘤边界的识别通过SpaCET工具包完成。此外,批量转录组数据(Bulk-RNA seq)以TCGA-STAD作为训练集(348个样本),并纳入了来自GSE84437、GSE84433等多个GEO数据库的验证集,所有这些数据集均含有生存信息;对这些数据,研究采用了TPM格式或进行了归一化和批次效应去除(通过Limma和SVA工具包),以确保多数据集间分析的可比性。
异质性解析与分子分型
在解析异质性方面,本研究首先对GC样本中的肿瘤上皮细胞进行重新聚类,随后利用CytoTRACE2数据包对肿瘤细胞进行了轨迹和拟时序分析,以评估其干性特征和分化潜能。同时,通过CellChat和NicheNet数据包分析了不同细胞类型间的通讯网络。在分子分型层面,研究基于GMS差异基因集,并联合考虑与预后相关的miRNA、lncRNA、甲基化和突变基因,使用MOVICS数据包对TCGA-STAD样本进行了多组学联合聚类,以确定最终亚型。
预后模型构建与评估
基于CS2亚型高表达且TOP2A肿瘤细胞特异的基因特征,本研究利用Mimel数据包建立了GMS相关的预后风险评分(RS)模型。该建模过程整合了包括RSF、GBM等在内的117种机器学习算法组合,并选择在多个队列中平均C-index最高的RSF + GBM组合作为最终候选模型。模型的性能和稳健性通过C-index、时间依赖性ROC曲线(time-dependent ROC)、DCA等多种指标在TCGA训练集和多个独立验证集上进行了严格评估,并且与已发表的14个胃癌预后模型进行了比较,结果显示本模型具有相对稳健和优秀的预测性能。此外,研究还从免疫角度对模型进行了深入分析,评估了高/低 RS 组之间的免疫细胞浸润差异,发现高风险评分与T细胞、NK细胞、B细胞等浸润水平低以及“冷肿瘤”状态密切相关,并分析了RS与免疫检查点分子、EMT/基质/ESTIMATE 评分等免疫特征的关联性。
核心基因分析与验证
作为模型中的核心基因,本研究对SH3BP1进行了多组学层面的功能探索和初步临床验证。通过GSEA功能富集分析,研究探索了SH3BP1高表达与细胞周期、葡萄糖代谢及免疫激活通路之间的关系。同时,单细胞和空间转录组分析揭示了SH3BP1在CD8+T细胞和恶性肿瘤区域的表达定位,并发现其表达水平与 CD8+T细胞的细胞毒活性和浸润呈正相关。最后,为了对核心发现进行初步验证,研究采集了来自武汉新洲区人民医院的18对胃癌组织及其配对癌旁组织样本,并通过RT-qPCR实验对SH3BP1基因的表达差异进行了验证。
研究结果
GMS在肿瘤中高度富集且与预后不良相关
研究首先通过多组学分析揭示了GMS特征在胃癌中的富集情况。在单细胞层面,经过质量控制、降维和聚类后,细胞类型得到了清晰区分,并且发现成纤维细胞、内皮细胞和上皮细胞在高GMS组中的比例较高。在空间转录组层面,GMS的表达在肿瘤区域显著增加,其次是交界区和基质区。进一步利用六种基因集富集分析方法发现,与正常对照(NT)和MGC组相比,GMS在GC组中表达显著上调。在批量转录组水平,GMS特征在肿瘤组织中显著高表达,并且与患者的不良预后密切相关,通过GSEA分析进一步证实GMS特征显著富集。这些结果共同提示GMS是肿瘤细胞的一个关键特征,并在胃癌的发生发展中发挥重要作用。
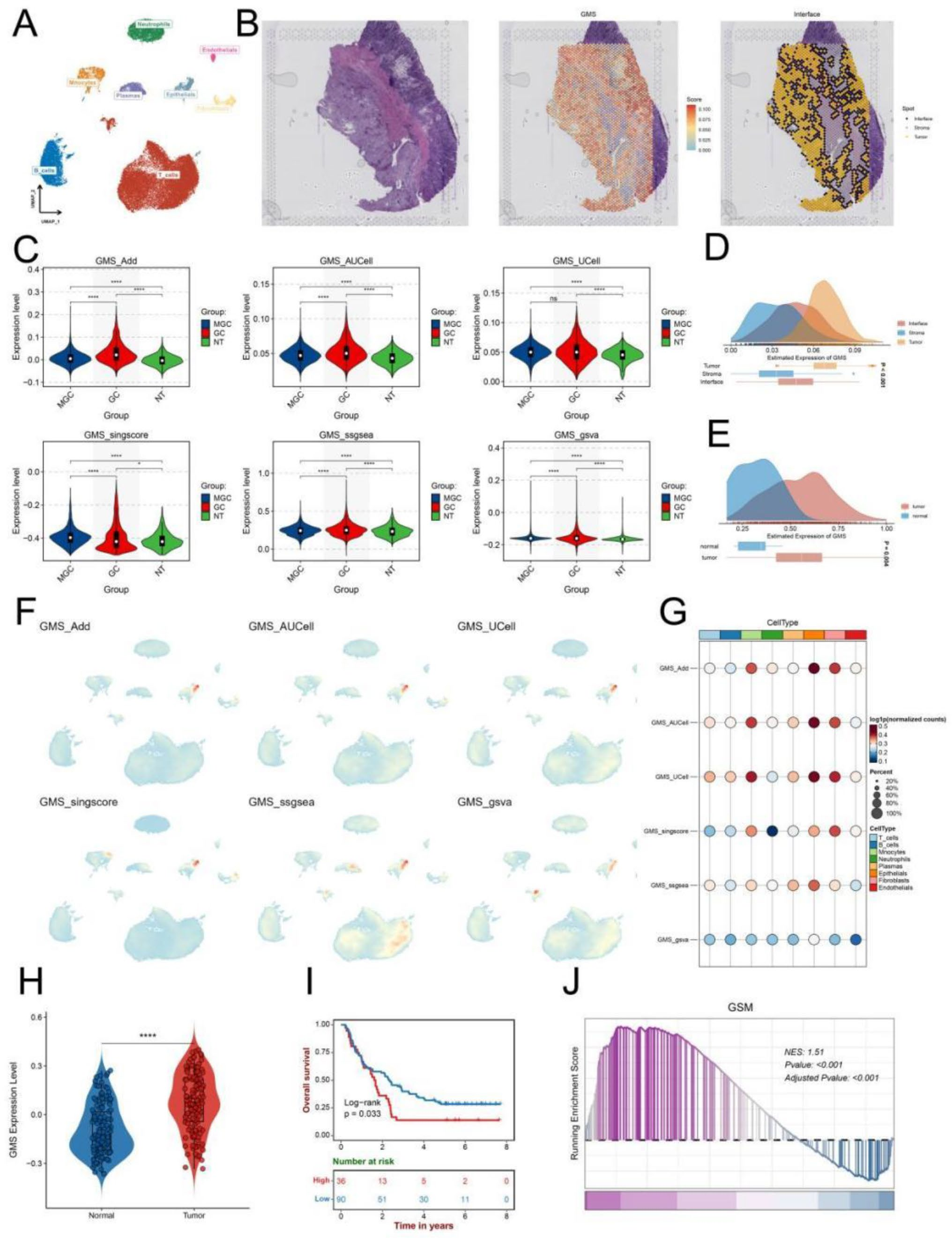
TOP2A+亚型具有高GMS特征、高干性和不良预后
通过对恶性上皮细胞进行重新聚类,研究共鉴定出三种具有显著差异的细胞群体,即TOP2A亚型、GABRP亚型和OLFM4亚型 。值得注意的是,TOP2A亚型显示出最高的GMS表型,并且与患者的不良预后显著相关,而GABRP亚型预示着较好的预后水平。通路富集分析表明,TOP2A亚型细胞高度上调了与细胞周期和糖酵解相关的通路。轨迹分析(Slingshot)和拟时序分析(CytoTRACE2)进一步证实,TOP2A亚型细胞具有更高的干性特征和高分化潜能,细胞周期推断结果也验证了TOP2A亚型细胞在S期和G2M期评分最高。在细胞通讯方面,TOP2A亚型与GABRP亚型之间存在明显的通讯。NicheNet分析和scMLnet推断表明,GABRP亚型高表达配体EFNB2,而TOP2A亚型高表达受体EPHB2,这条信号通路可能通过CKLF等配体激活细胞周期相关通路,从而调控TOP2A亚型的恶性表型。
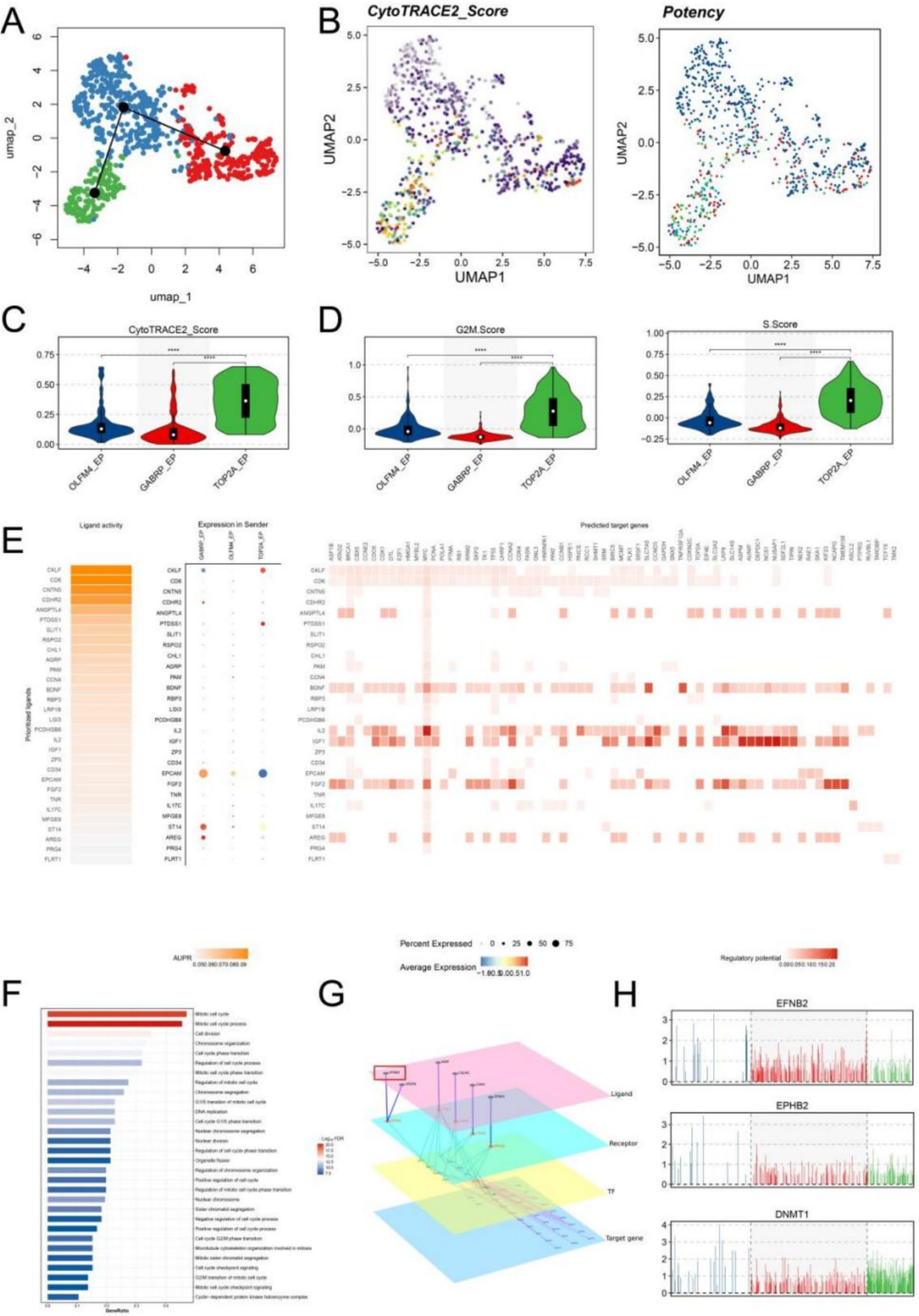
多组学聚类定义了具有高GMS和不良预后的CS2亚型
研究进一步基于GMS差异基因和与预后相关的miRNA、lncRNA、甲基化和突变基因,使用MOVICS软件对TCGA-STAD样本进行了多组学联合分类。聚类分析将样本稳定地分为了CS1和CS2两个亚型。结果显示,CS2亚型具有更高的GMS特征,并与患者的不良预后密切相关。在四个独立的外部数据集中(GSE84433、GSE26253、GSE62254和GSE84437)对这一分类结果的验证显示出良好的稳健性和一致性,即CS2分类均表现出较差的预后。功能富集分析(ORA和GSEA)结果揭示了CS2亚型与CS1亚型之间在功能上的明显差异,其中CS2亚型在不同数据库中均高度富集于细胞周期和糖代谢相关的通路,这与单细胞分析中TOP2A亚型的特征一致。
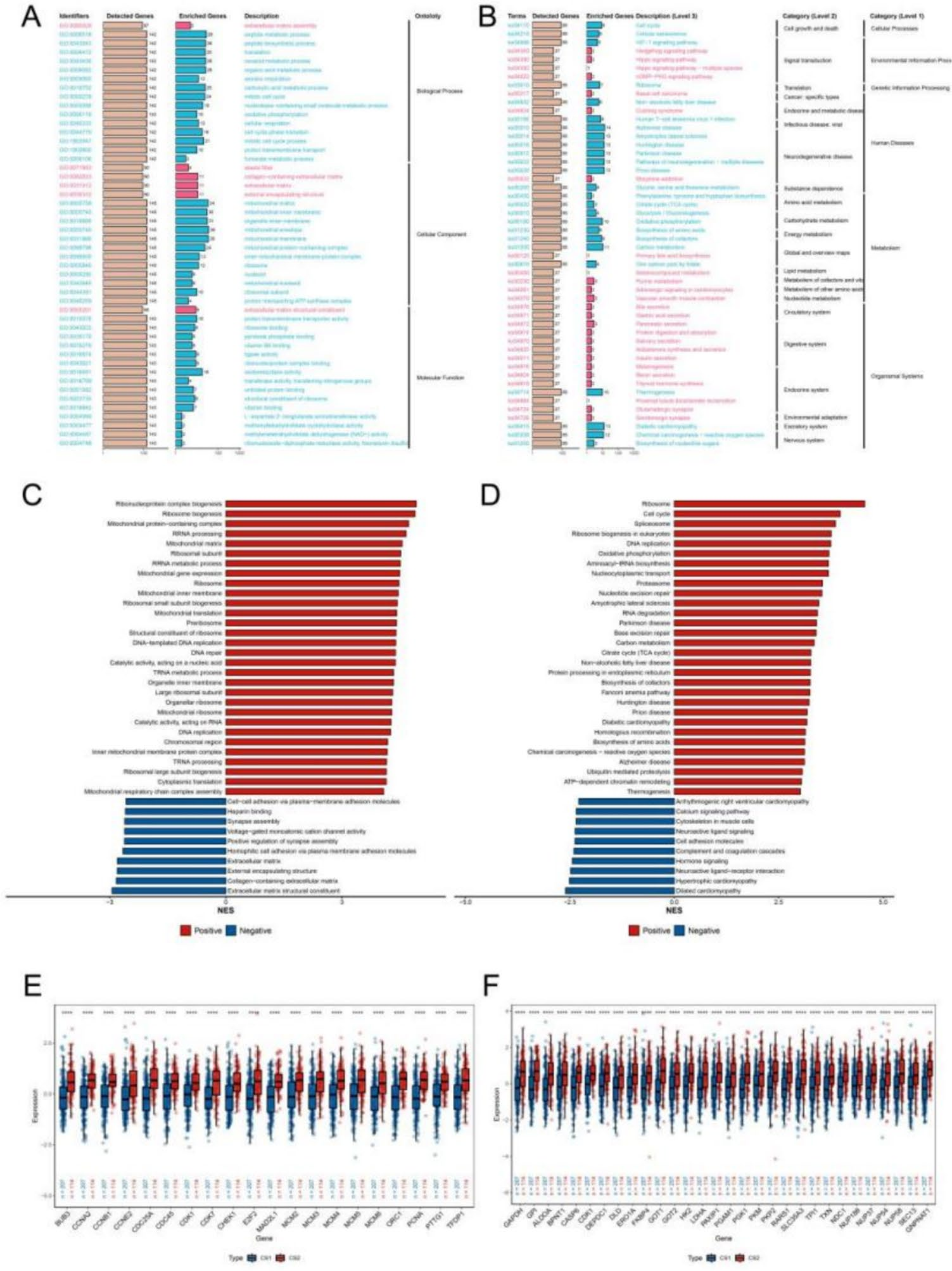
稳健的8个基因预后模型与核心抑癌基因SH3BP1
研究利用Mimel数据包,基于CS2特异性差异基因和TOP2A特异性基因,构建了一个由八个基因(SH3BP1, FEN1, SNORC, E2F2, SLC1A5, CHAFIA, EZH2, LMNB2)组成的GMS相关预后模型。该模型在TCGA训练集和多个独立验证集上均表现出稳健的预测性能(C-index约为0.6),并且在与14个已发表模型的比较中,显示出相对更优的稳健性。免疫学分析显示,高风险评分患者与“冷肿瘤”状态密切相关,表现为T细胞、NK细胞、B细胞等免疫细胞浸润水平较低,且与EMT/基质/ESTIMATE评分呈显著正相关,预示预后不良。核心基因SH3BP1被鉴定为一个潜在的肿瘤抑制因子(风险比HR=0.87),其高表达与较低的肿瘤分期和增强的CD8+T细胞杀伤和浸润相关。RT-qPCR验证结果初步证实SH3BP1在肿瘤样本中的表达高于癌旁组织。
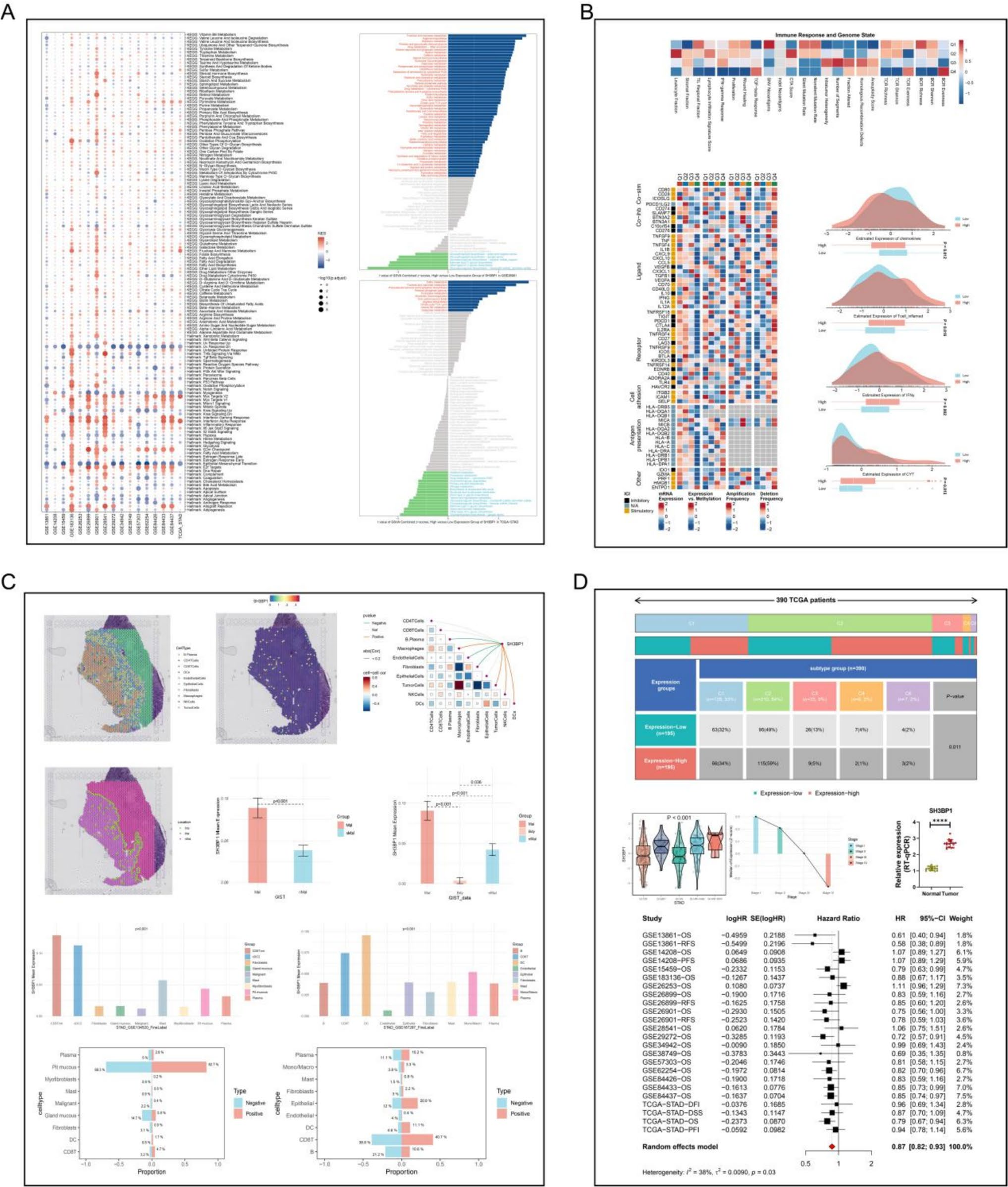
结论
本研究利用多组学数据,系统地揭示了GC中GMS的显著异质性及其临床意义。研究成果成功鉴定了具有高GMS特征和不良预后的TOP2A+肿瘤上皮细胞亚型以及相应的CS2分子分型。基于这些特征构建的GMS风险评分模型,在多个队列中展现出稳健的预后预测能力,并提示高风险患者可能处于免疫抑制的“冷肿瘤”微环境。特别值得关注的是,核心抑癌基因SH3BP1被发现其高表达与增强的CD8+T细胞活性和较好的预后相关,表明其是GMS-免疫调控轴上的关键节点。这些发现不仅为胃癌的精准分子分型和预后评估提供了新的生物标志物和风险分层工具,更为未来开发靶向葡萄糖代谢与免疫互作的个性化治疗策略奠定了理论基础。
[1]Liu L, Cao J, Qi X, Lu J. Multi-omics unravel heterogeneity of glucose metabolism reprogramming in gastric cancer. Clin Exp Med. Published online 18 November 2025 . doi:10.1007/s10238-025-01921-7.
审批编号:CN-174154 有效期:2027-4-12
声明:本材料由阿斯利康提供,仅供医疗卫生专业人士进行医学科学交流,不用于推广目的。
排版编辑:肿瘤资讯-Alex











 苏公网安备32059002004080号
苏公网安备32059002004080号


