【35 under 35】风采展示第二轮已经开始啦!本轮正经名叫“病例实战分析”,不正经名叫“互相伤害”,哈哈哈~100位入围选手每人提交一个有意思的病例,并就病例提出一个问题,形成一个病例库!然后100位入围选手从病例库中任意选择一个非自己提供的病例进行解读并回答问题!最后,我们将呈现病例+别人的点评+病例提供者自己的点评,同步展示!
 100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
患者病史摘要
性别:女
年龄:38
主述:左乳癌术后1年半,发现双肺结节5天
体能状态评分:0
既往史:无特殊
家族史:无特殊
入院查体:双乳未扪及明显肿块,左乳硅胶未移位,双腋窝及双侧锁骨上未扪及肿大淋巴结。余体查未见明显异常。
入院实验室检查:
1) 血常规检查:无异常
2) 尿常规:无异常
3) 便常规:无异常
4) 肝、肾功能:无异常
5) 肿瘤标志物:CEA、CA153、CA125均在正常范围内
6) BRCA1/2基因检测:N/A(患者拒绝)
影像学检查
入院时胸、腹、盆腔等影像学检查及CT/MRI片子
双肺CT见多发结节,考虑转移,余检查无异常。
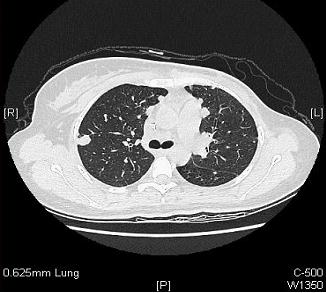
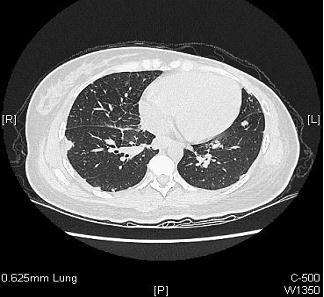
入院前治疗史
此前是否经过手术?术式?术后病理,淋巴结转移情况
2015.6外院行左乳癌保留乳头乳晕的皮下全切+扩张囊植入+左腋窝淋巴结清扫术,术后病理:左乳浸润性导管癌,III级,最大径2.7cm,ER2%+、PR-、HER2-,Ki67 50%+, AR-,CK5/6+,LVI+, LN 5/21转移,分期T2N2M0 (III期)
是否曾接受术前或术后放疗?时间、方式、总量?(常规放疗/伽马刀?)
术后常规放疗
是否曾接受术前或术后化疗(是否同步放疗?是否放疗后辅助?化疗的方案、剂量,疗程?)
未接受术前化疗,术后行ECT*6次化疗,化疗后放疗,放疗后法乐通内分泌治疗。
PFS:1.5年
五、入院诊断
患者入院诊断
左乳癌术后双肺转移
问题一:一线治疗方案是什么呢?
开始时间:2016年12月
治疗周期数:8程
疗效评估情况:PD
方案是否调整,如何调整:否
六、一线治疗疗效评估—影像学检查
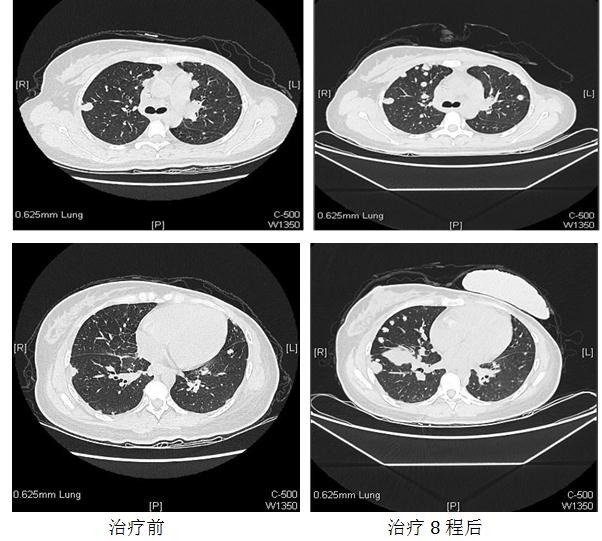
七、一线治疗疗效评估——概述
治疗两个周期后:PR
治疗四个周期后:PR
治疗六个周期后:SD
治疗八个周期后:PD
一线PFS:6个月
此时患者同意BRCA1/2基因检测,结果示BRCA1突变
问题二:一线治疗失败后的下一步治疗策略?
--------------------------------------
此病例共有1位入围选手点评:55-王静姝 ;病例提供作者为:39-刘洁琼。详情如下:
点评医生简介:55-王静姝
 点评内容分享:
点评内容分享:
一、手术后复发乳腺癌的一线治疗的选择
关于晚期乳腺癌的一线治疗,需要复核原发灶的病理类型及分子分型,另一方面,近年来临床实践发现,部分患者乳腺癌转移灶与原发灶分子分型不一致。EMSO和NCCN指南指出,乳腺癌出现转移后,应对复发转移灶予重新活检,从而更好地指导治疗。而我国今年的CSCO乳腺癌诊疗指南也推荐对晚期乳腺癌进行转移灶的病理活检以明确病理类型和分子分型来指导治疗决策。
转移灶活检后如果Her2高表达,需要行抗Her2治疗联合化疗。H0648g研究表明Her-2高表达的转移性乳腺癌化疗联合Herceptin(赫赛汀)治疗较单独化疗组缓解率提高23%-32%,中位疾病无进展时间延长了3个月,两年总生存率也有显著提高。依据最新的CSCO临床指南,转移性Her2阳性乳腺癌一线治疗可使用曲妥珠单抗为基础加化疗,化疗可采用紫杉类、长春瑞滨、希罗达等。
该患者术后病理为左乳浸润性导管癌,ER 2%+、PR-、HER2-,如果转移灶激素受体表达亦低于10%+,则属于激素受体低表达,对内分泌治疗不敏感,可参照三阴乳腺癌来进行下一步治疗 [1-3])。对于转移性三阴性乳腺癌的一线治疗,来自中国胡夕春教授的III期临床试验(CBCSG 006),对比了GP方案与紫杉醇+吉西他滨(GT)方案一线治疗转移性TNBC的疗效,主要终点PFS 在GP 和GT 组分别达到了7.73个月和6.47个月,结果发现转移性三阴乳腺癌一线治疗 GP优于GT。该研究进一步确定了顺铂联合吉西他滨(GP)是一种有效治疗转移性三阴乳腺癌的非蒽环、非紫杉方案[4]。此外,去年的tnAcityⅡ期临床研究结果显示,白蛋白紫杉醇+卡铂方案的双药化疗对比吉西他滨+卡铂的传统方案可以降低40%的复发和死亡风险,两组的有效率分别为92% vs 40%。白蛋白紫杉醇组较吉西他滨组的无进展生存期(PFS)延长1.4个月。因此白蛋白紫杉醇+卡铂也可以作为很好的mTNBC化疗一线方案之一[5]。
二、一线治疗失败以后下一步治疗策略
该患者一线治疗8个周期后疾病进展,行BRCA1基因检测,为突变阳性型。乳腺癌中BRCA1/2胚系突变是基底样型乳腺癌的特征之一,在三阴性乳腺癌中检出率约为10%,但BRCA1/2胚系突变并非只发生在三阴性乳腺癌中。BRCA1突变细胞由于存在DNA损伤修复障碍,因此对铂类药物有较高的敏感性。TNT是研究比较卡铂或多西他赛治疗晚期三阴性乳腺癌的随机III期研究,结果发现两组的客观缓解率相似,然而BRCA1/2突变者,卡铂客观缓解率高。TB-CRC009研究显示,与整体人群相比,铂类单药对BRCA1/2胚系突变的患者具有更高的有效性[6]。因此该患者一线治疗后进展,如果一线治疗时没使用过铂类,二线治疗可考虑含铂为基础的化疗。如果一线治疗已经使用铂类,二线治疗可使用非含铂的方案化疗,如长春瑞滨联合希罗达等方案化疗。
近年来PARP抑制剂在BRCA突变肿瘤如卵巢癌、乳腺癌中的治疗地位得到广泛重视。研究发现BRCA突变肿瘤由于损伤修复障碍,PARP抑制剂显示对肿瘤细胞的杀伤作用。NCT00494234等研究发现BRCA1/2突变的转移性乳腺癌中单药PARP抑制剂奥拉帕尼(olaparib)的客观缓解率为12.9-41.0%[7,8]。今年ASCO年会报道的NCT02000622研究表明,在BRCA1突变的Her2阴性的转移性乳腺癌中,奥拉帕尼组对比标准化疗组(卡培他滨或长春瑞滨或艾瑞布林)PFS更长(7.0 vs 4.2个月,HR 0.58;P=0.0009),客观缓解率更高(59.9% VS 28.8%),因此使用奥拉帕尼对比标准化疗获益更大[9]。但是由于奥拉帕尼中国未上市,因此可以推荐患者参加奥拉帕尼临床实验。
总之,转移性乳腺癌的治疗是一门艺术,治疗要兼顾生存质量和生存期,需要综合考虑肿瘤的分子分型、疾病负荷、治疗药物的可及性、患者的治疗愿望等,推荐行多学科会诊,以明确治疗方案。
--------------------------------------
病例提供作者简介:39-刘洁琼
 病例提供作者自评:
病例提供作者自评:
此患者复发转移前的乳腺癌病理是左乳浸润性导管癌,III级,ER2%+、PR-、HER2-,Ki67 50%+, AR-,CK5/6+,可以看做类似三阴乳腺癌。2011 年,Lehmann 等通过基因分析首次将三阴乳腺癌再细分为7 个亚型:基底细胞样1(BL1)、基底细胞样2(BL2)、免疫调节(IM)、间充质样细胞(M)、间充质样干细胞(MSL)和管样雄激素受体(LAR)、和不稳定亚型(UNS)。针对不同细分亚型的特点可以选择相应的治疗方案,目前有一些探索性研究结果,如BL1 和BL2 亚型存在DNA 损伤修复缺陷,可以优先选择铂类药物或PARP 抑制剂治疗。依据此患者的IHC结果可大致判断其可能是BL1 或BL2 亚型。对于该患者在复发转移前的外院治疗方案,我觉得稍有不妥,2017年St Gallen共识绝大多数专家支持肿瘤超过2cm的三阴乳腺癌首选术前化疗。因此该患者可先进行新辅助化疗,肿瘤降期后再手术。
该患者是蒽环联合紫杉方案化疗后托瑞米芬内分泌治疗(基于ER 2%+)期间发生的双肺转移,复发转移后的一线治疗方案,我们选择的是吉西他滨联合顺铂(GP)化疗。Winner教授牵头的一项III期临床试验(NCT00938652)比较GC(吉西他滨联合卡铂) + Iniparib 与单纯GC 治疗晚期三阴乳腺癌的疗效。尽管该研究未能证实Iniparib 在转移性三阴乳腺癌 中的地位,但单纯GC 组的中位PFS 和OS 分别达到了4.1个月和11.1个月。此项试验的结果证明GC 双药联合方案是一个安全有效的的方案,此方案因而被2015 年NCCN 指南推荐用于晚期三阴患者。铂类治疗晚期三阴乳腺癌到底选择顺铂还是卡铂? TBCRC009研究提示顺铂可能比卡铂更高效。此外,中国上海的胡夕春教授主持了一项III期临床试验(CBCSG 006),进一步确定了顺铂联合吉西他滨(GP)是一种有效治疗转移性三阴乳腺癌的非蒽环、非紫杉方案。该试验对比了GP方案与紫杉醇+吉西他滨(GT)方案一线治疗转移性TNBC的疗效,主要终点PFS 在GP 和GT 组分别达到了7.73个月和6.47个月,非劣效检验和优效性检验均显示有统计学的差异,亚组分析显示40 岁以下的女性患者从GP 的治疗中获益更为明显。回到我们的病例,该患者是对铂类敏感的BL1 或BL2 亚型三阴患者,年龄小于40岁,因此我们一线治疗方案选择PFS较长的GP化疗方案。
该患者一线方案的PFS为6个月。一线治疗失败后患者同意进行BRCA1/2基因检测,结果是BRCA1突变。二线治疗我们选择的是Olaparib PARP 抑制剂靶向治疗。此患者为BRCA1突变的转移性三阴患者,复发转移后GP化疗失败,选择单药Olaparib是基于2017年ASCO年会上报道的最新的NCT02000622研究结果。该研究入组302例BRCA1/2突变的转移性三阴患者,后线2:1随机接受Olaparib靶向治疗或标准化疗(卡培他滨、长春瑞滨或艾日布林),Olaparib组的PFS显著优于化疗组(7月 vs 4.2月),且副作用更少。
--------------------------------------
以上为【35 under 35】的观点,您怎么看?欢迎广大肿瘤医生在下方留言发表您的观点!
以上所有点评参考文献略。














 苏公网安备32059002004080号
苏公网安备32059002004080号


