乳腺癌是全球女性中发病率最高的癌症之一,也是癌症相关死亡的重要原因。目前临床常用的预后评估工具包括乳腺X线摄影(钼靶)、超声、磁共振成像(MRI)和组织活检。然而,这些方法存在明显局限,例如在致密型乳腺组织中的敏感性较低、对操作者依赖性强、费用较高以及具有侵入性等。
肌动蛋白结合蛋白(ABP)的异常表达或调控会增强细胞迁移能力、侵袭性和耐药性。本文聚焦于肌动蛋白及ABP在乳腺癌中的预后价值。通过梳理其作用机制及体内外研究证据,旨在挖掘潜在生物标志物,以改善早期预后评估、风险分层和个体化治疗策略。大量体外和体内研究一致表明,Fascin、Cofilin和Mena等ABP,以及Rho GTP酶、PI3K和MAPK/ERK等信号通路,在介导肌动蛋白骨架重构、促进乳腺癌进展方面具有关键作用。

根据GLOBOCAN数据,2022年全球新增乳腺癌病例近230万例,死亡人数超过65万。尽管筛查和治疗手段不断进步,但转移和治疗耐药等问题仍严重影响临床疗效。由遗传和表观遗传改变所塑造的肿瘤异质性,导致患者对治疗反应和疾病进展存在显著差异。此外,浸润性乳腺癌还可逃避免疫监视,并适应肿瘤微环境以支持其生存和扩散。因此,肿瘤异质性、治疗耐药和免疫逃逸会延误疾病进展的发现,使预后评估更加困难,也影响及时干预。延迟检测可能导致死亡率上升、治疗启动延后,并可能降低患者生存率。开发靶向治疗依赖于准确、及时的诊断,这对改善患者结局和总体生存率至关重要。
肌动蛋白丝在细胞迁移中发挥关键作用,其动态重塑过程由肌动蛋白结合蛋白(ABP)精密调控。在癌症中,ABP的异常表达或调控会增强细胞迁移能力、侵袭性和耐药性。ABP还在上皮-间质转化(EMT)过程中发挥关键作用。此外,富含肌动蛋白的结构,如片状伪足、丝状伪足和侵袭足,可帮助细胞穿越细胞外基质,实现定向迁移和侵袭,是肿瘤转移的重要基础。因此,ABP的突变或失调会增强细胞运动性、侵袭性和转移潜能,从而加速癌症进展。
鉴于肌动蛋白及ABP在癌细胞迁移、侵袭和细胞骨架重塑中的核心作用,它们在乳腺癌中具有成为预后生物标志物的巨大潜力。已有多项研究将特定ABP与肿瘤侵袭性行为及治疗结局联系起来,但其临床应用价值仍有待深入探索。
Breast Cancer: Targets and Therapy发表的一篇综述纳入176篇文献进行分析。其中,167项研究采用体外乳腺癌模型进行实验,且其中59项进一步结合体内验证;另有9项研究仅采用体内模型,如小鼠异种移植模型或基因工程小鼠模型。
对肌动蛋白调控通路的实验性干预一致表明,乳腺癌细胞迁移并非单纯由肌动蛋白含量决定,而是受协调的信号网络调控,这些网络控制细胞骨架的可塑性。其中,Rho家族小GTP酶——包括RhoA、Rac1和Cdc42——作为核心信号枢纽,将细胞外刺激转化为肌动蛋白重组信号。在多种乳腺癌模型中,通过抑制或表达显性负突变形式,可观察到细胞迁移行为显著改变。Rac1和Cdc42在细胞前缘动力学中尤为关键,驱动片状伪足和丝状伪足形成,促进持续的定向迁移;而RhoA主要调控肌动蛋白-肌球蛋白收缩性及应力纤维组装,其对迁移的影响更具情境依赖性,既维持细胞骨架完整性,又提供后端收缩力,因此其功能受损可能根据细胞环境不同而增强或抑制细胞运动。
除上游信号外,直接调控肌动蛋白丝周转的蛋白也是迁移效率的关键决定因素。Profilin-1通过维持ATP-肌动蛋白单体库促进肌动蛋白聚合,其在侵袭性中的作用具有情境依赖性;而cofilin介导的肌动蛋白丝切割对于维持细胞运动所需的动态重塑至关重要。相比之下,fascin作为主要的促迁移肌动蛋白束集蛋白,通过稳定丝状伪足和侵袭足结构增强细胞迁移。在多种乳腺癌模型中,抑制fascin与肌动蛋白的相互作用可显著降低迁移和侵袭能力,提示其是最具潜力的抗转移细胞骨架治疗靶点之一。
激素及转录调控程序同样影响乳腺癌中的肌动蛋白重塑。类固醇激素(如雌激素、孕激素和雄激素)在激素受体阳性肿瘤中显著影响细胞骨架组织,显示核受体信号在赋予细胞迁移能力中的作用。类似地,TGF-β通路激活可促进EMT,这一过程伴随显著的肌动蛋白骨架重编程;抑制该通路则可逆转转移相关表型。
此外,肌动蛋白细胞骨架还作为整合多种环境信号的平台。代谢因素(如葡萄糖供应)、细胞外基质的机械信号、药物及天然化合物,以及微小RNA(miRNA)的转录后调控,均可精细调节肌动蛋白动态。值得注意的是,多种miRNA可同时靶向多个肌动蛋白调控因子,作为内源性抑制因子抑制侵袭性细胞骨架程序。调控性miRNA的丧失可能促进转移,而其恢复则可能通过多层次调控肌动蛋白网络抑制癌细胞迁移。
大多数体外研究使用乳腺癌细胞系评估基因修饰或新型化合物对肌动蛋白骨架动态及ABP的影响,尤其关注细胞迁移和侵袭能力。部分研究进一步通过动物模型进行体内验证,主要观察指标为肿瘤体积和肺转移情况。最早探讨ABP与乳腺癌关系的体外研究发表于1998年,首个体内研究发表于2001年,此后相关研究持续开展,表明该领域长期受到关注。
常用的体外乳腺癌细胞系包括MDA-MB-231、MCF-7、T47D、4T1和BT549,涵盖从Luminal A到三阴性乳腺癌等不同分子亚型。实验设计包括基因沉默(如RNA干扰/短发夹RNA敲低)、过表达系统及靶向肌动蛋白聚合或ABP功能的药物干预。除表型观察外,迁移、侵袭、细胞形态及EMT标志物检测也是常用功能实验。尽管研究设计多样,但普遍发现多种ABP表达水平与迁移、侵袭及转移能力增加呈正相关。相反,抑制或缺失特定ABP通常会降低细胞运动性和侵袭潜能,显示其作用具有复杂且情境依赖的特点。
在所有研究中,fascin、α-actinin、Arp2/3复合体、cofilin和filamin A等ABP被反复证实为乳腺癌细胞运动和骨架重塑的重要调控因子。F-肌动蛋白聚合状态常作为细胞骨架重塑的指标。常用功能检测方法包括Boyden小室实验和Matrigel侵袭实验。总体而言,抑制ABP或其上游调控因子通常会降低癌细胞迁移和侵袭能力;而过表达则常伴随迁移增强、EMT表型形成及转移扩散增加。然而,进一步分析表明,不同ABP作用并不完全一致。例如,在多个模型中,下调Filamin A会削弱迁移能力;而Profilin-1的作用则更为复杂。Profilin-1表达降低常与迁移能力增强相关,而其过表达通常抑制迁移。这些结果强调,尽管Profilin-1和Filamin A均为肌动蛋白结合蛋白,但在不同细胞环境下对癌细胞行为的影响可能存在差异,甚至相反。
体内研究为在复杂生理环境中调控肌动蛋白或ABP对肿瘤进展的影响提供了具有转化意义的见解。在纳入动物模型的68项研究中(其中59项同时包含体外与体内实验,9项仅为体内研究),大多数采用原位小鼠模型,即将人源或小鼠乳腺癌细胞注入乳腺脂肪垫中。干预方式多样,最常见的是基因敲除或过表达策略,以及应用此前未在乳腺癌模型中测试过的新型化合物。这些体内研究通常建立在先前使用相同干预措施的体外实验基础之上。在体内模型中最常使用的乳腺癌细胞系包括MDA-MB-231、4T1、MCF-7和MTLn3。
此外,最常用的动物模型为SCID小鼠。研究中最常评估的生物标志物是丝状肌动蛋白(F-actin),而Mena则是研究最为频繁的肌动蛋白结合蛋白。大多数研究主要关注乳腺癌向肺部的转移情况,较少研究同时评估肿瘤体积变化。
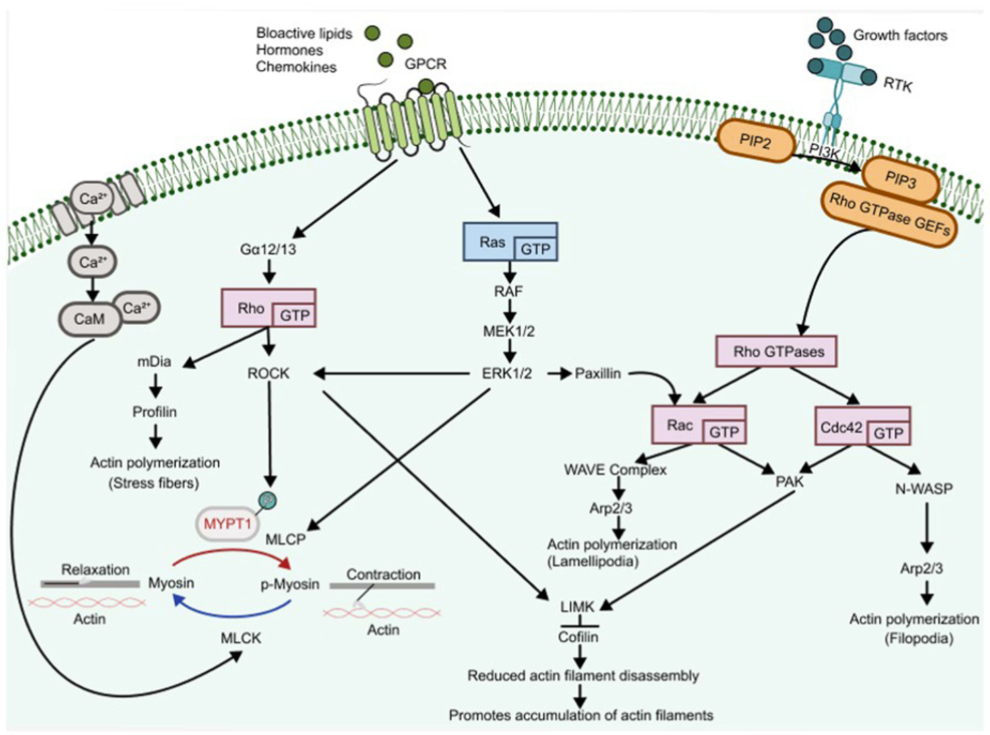
整体来看,这些研究结果共同强调了肌动蛋白动态变化及ABP调控在乳腺癌进展关键细胞行为中的核心作用。不同模型和信号通路中结果的一致性,也进一步凸显其作为潜在预后指标和治疗靶点的价值。
Fascin、Cofilin、Mena、MenaINV、Ezrin和Cortactin是研究中最常被关注的ABP。在信号通路方面,尽管涉及多种途径,但只有少数几条通路在不同研究中反复出现,包括Rho GTP酶通路、PI3K通路、MAPK/ERK通路以及LIMK/Cofilin通路,不过各研究对这些通路的关注时间点并不一致。
总体而言,尽管已有多种ABP及其相关信号通路在乳腺癌背景下被广泛研究,但仍难以明确哪一种ABP在各项研究中始终处于最核心或最优先的位置。多数ABP(如Fascin、Cofilin、Mena、MenaINV、Ezrin和Cortactin)在过表达时通常会促进癌细胞迁移与侵袭;然而,也存在相反情况,例如Profilin-1,其表达升高反而与迁移能力下降相关。这种差异表明,并非所有ABP都会一致性地增强肿瘤转移潜能。
Alfarafisa, N. M., Herriyanto, R. I., Alhaq, K. F., Fauzi, M. B., & Khairani, A. F. (2026). The Role of Actin-Binding Proteins in Breast Cancer Progression. Breast Cancer: Targets and Therapy, 566309.
排版编辑:肿瘤资讯-slb











 苏公网安备32059002004080号
苏公网安备32059002004080号


