本文由复旦大学附属肿瘤医院陈洁教授多学科团队分享一例胸腺神经内分泌肿瘤合并MEN1综合征病例,详细介绍了病例诊疗过程,并探讨神经内分泌肿瘤合并MEN1综合征的诊疗要点,剖析治疗过程中的经验,强调了神经内分泌肿瘤多学科管理的重要性,旨在为临床医生提供参考。
病例介绍
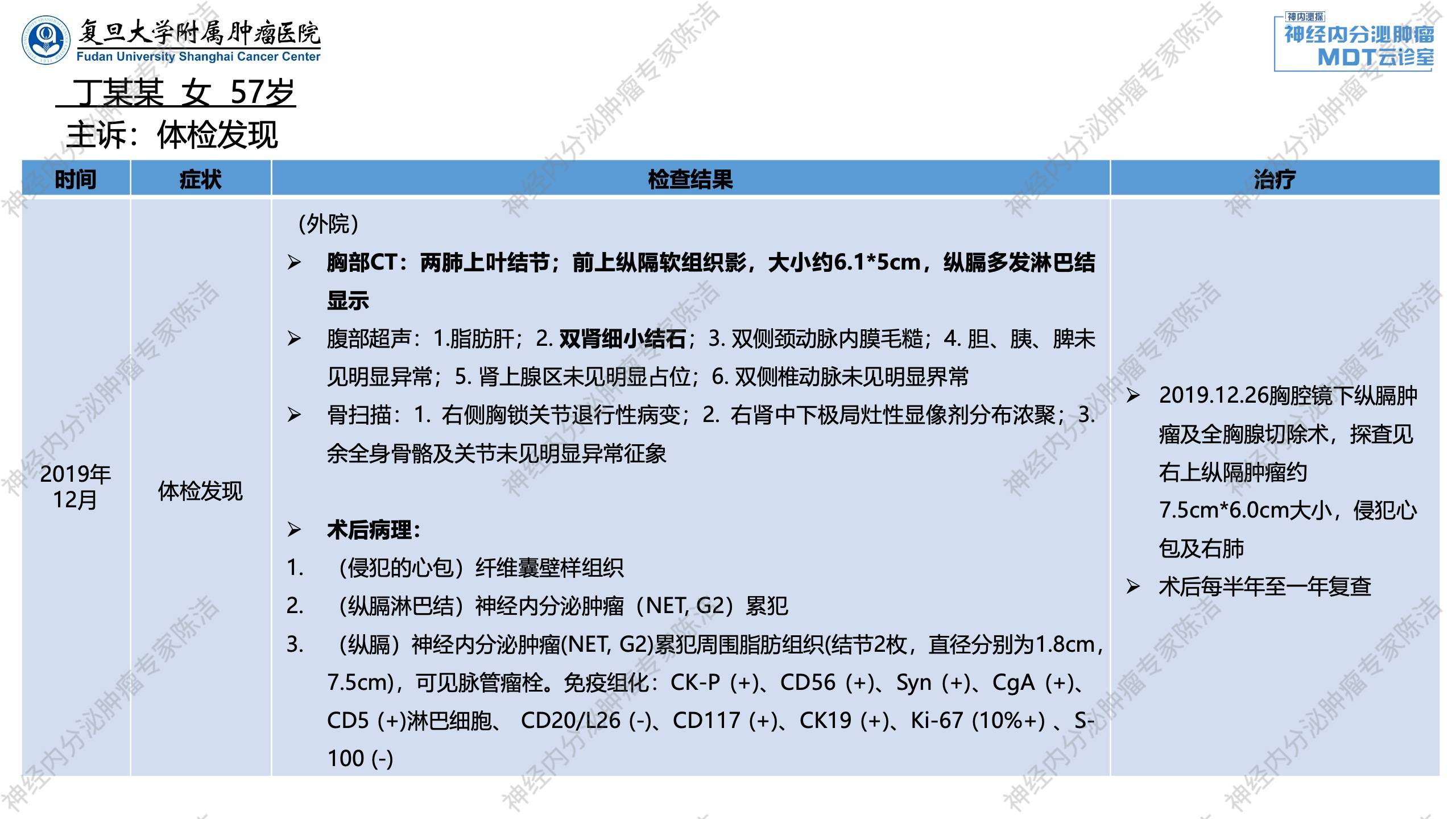
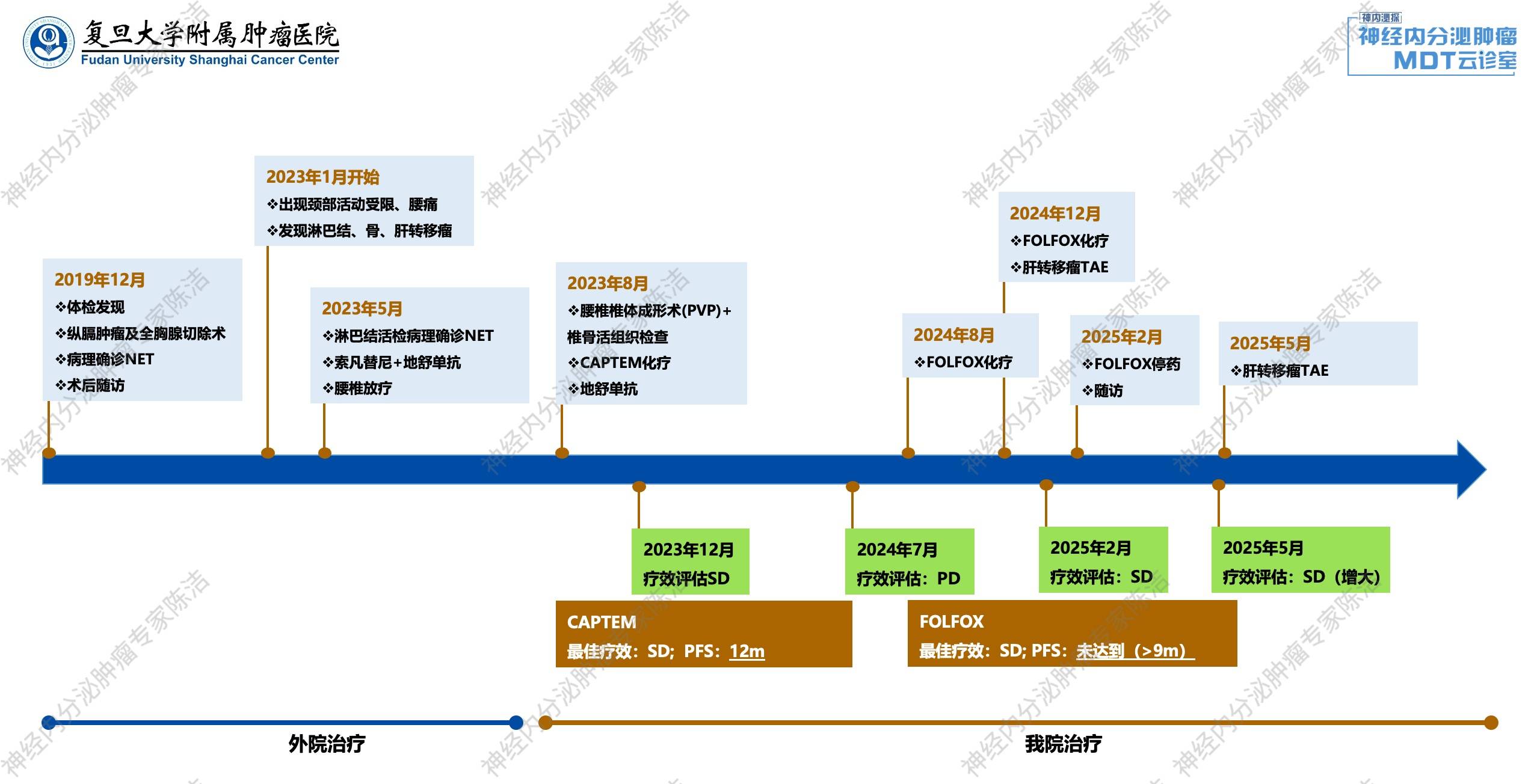
外院初诊及治疗:患者为57岁女性,于2019年12月外院体检胸部CT提示前上纵隔软组织影,大小约6.1*5cm,纵隔多发淋巴结。腹部超声提示双肾细小结石。进一步行骨扫描:1.右侧胸锁关节退行性病变;2.右肾中下极局灶性显像剂分布浓聚;3.余全身骨骼及关节未见明显异常征象。
2019年12月26日于外院接受“胸腔镜下纵隔肿瘤及全胸腺切除术”,探查见右上纵隔肿瘤大小约7.5cm*6.0cm,侵犯心包及右肺。术后病理提示:1.(侵犯的心包)纤维囊壁样组织;2.(纵隔淋巴结)神经内分泌肿瘤(NET,G2)累犯;3.(纵隔)神经内分泌肿瘤(NET,G2)累犯周围脂肪组织(结节2枚,直径分别为1.8cm,7.5cm),可见脉管瘤栓。免疫组化:CK-P(+)、CD56(+)、Syn(+)、CgA(+)、CD5(+)淋巴细胞、CD20/L26(-)、CD117(+)、CK19(+)、Ki-67(10%+)、S-100(-)。术后患者每半年至一年进行复查。
疾病进展:
2023年1月,患者出现颈部及双肩活动受限。外院胸腹CT平扫:前上纵隔术后表现,两肺上叶小结节,纵隔及左侧颈根部多发淋巴结显示;肝内稍低密度灶,双肾低密度灶。但当时未进行特殊处理。
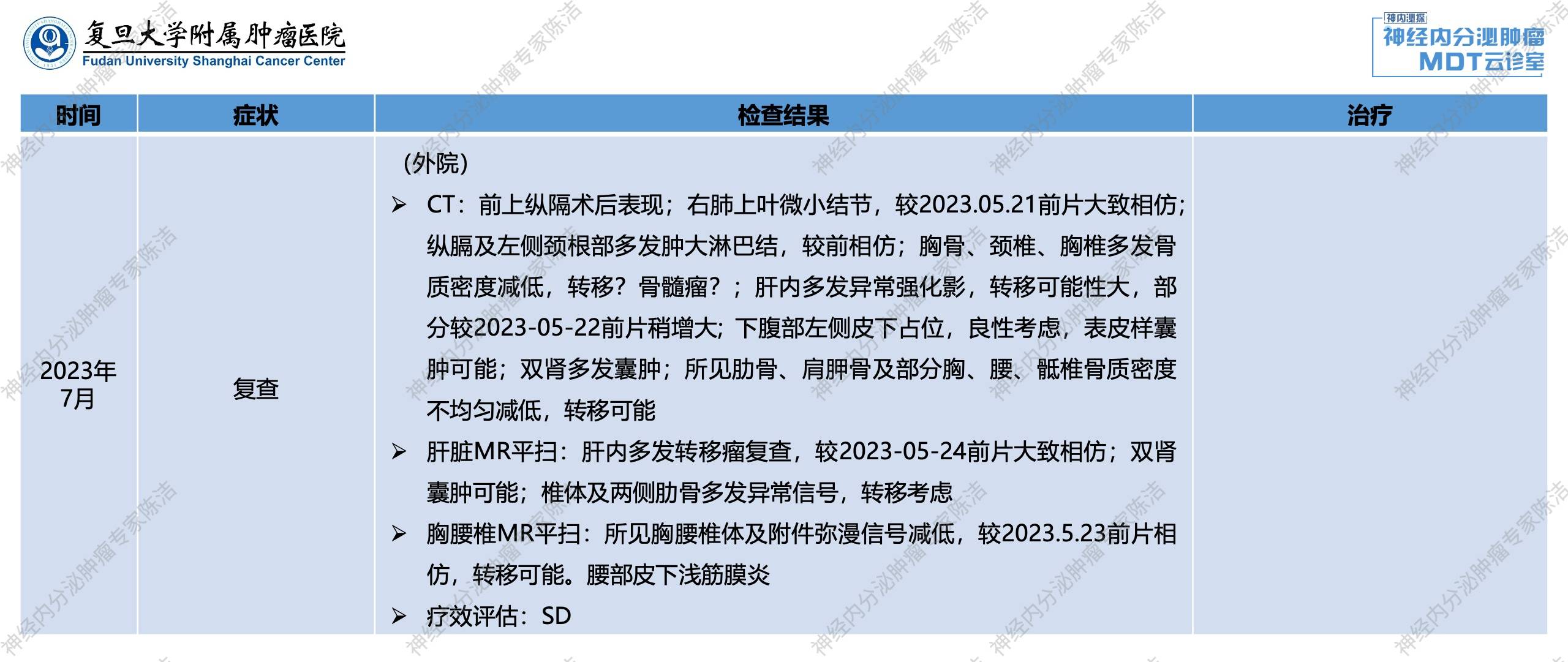
2023年5月,患者出现较明显的腰痛。外院复查胸腹CT提示:前上纵隔术后表现;右肺上叶微小结节,较前片大致相仿;纵隔及左侧颈根部多发肿大淋巴结,较前增多、增大,较大者约1.8*1.6cm;肝内多发异常强化影,转移?右肾占位;左肾多发小囊肿;所见胸骨、颈椎、胸椎、肋骨、腰、骶椎骨质密度减低。
骨扫描提示:全身多发骨转移可能,颅骨、右侧肩胛骨、两侧多发肋骨、脊柱、骨盆骨、股骨等多处显像剂异常浓聚灶。椎体MR平扫:胸椎体及附件弥漫信号减低,转移可能。肝脏MR平扫:肝内多发结节,较大约1.9*1.8cm,转移瘤首先考虑;双肾囊肿可能;椎体及两侧肋骨多发异常信号。外院行颈部淋巴结细针穿刺活检,病理:见散在及成团异形小圆细胞性细胞,形态结合病史,符合神经内分泌肿瘤。
外院给予地舒单抗(120mg Q4W)联合索凡替尼(300mg/日)治疗,并对腰椎骨转移灶行姑息性放疗10次。

2023年7月,外院CT、肝脏MR及胸腰椎MR检查均提示肿瘤病灶较前相仿,疗效评估为疾病稳定(SD)。
我院诊疗经过:
2023年8月,患者为求进一步诊治来到我院。
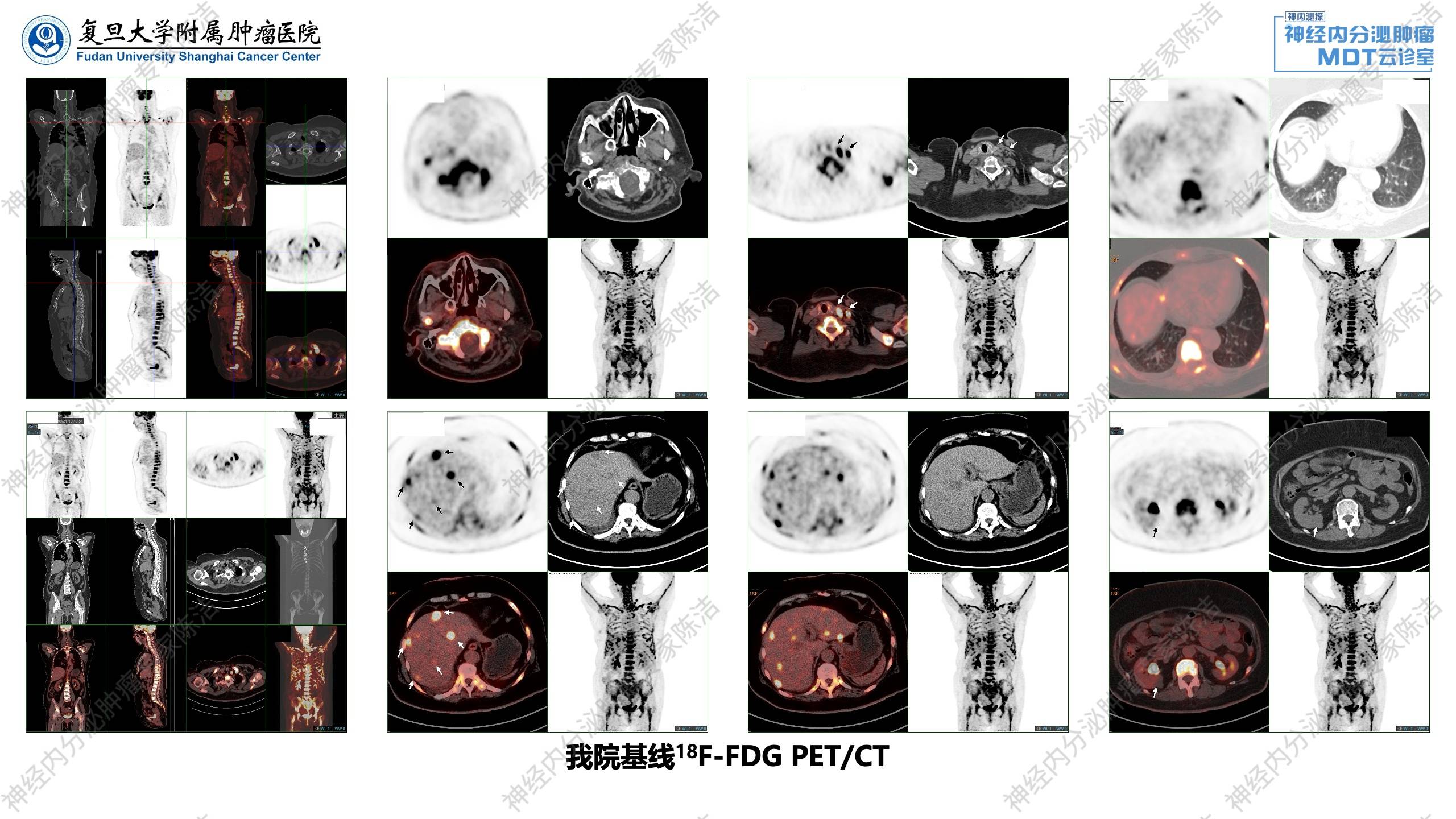
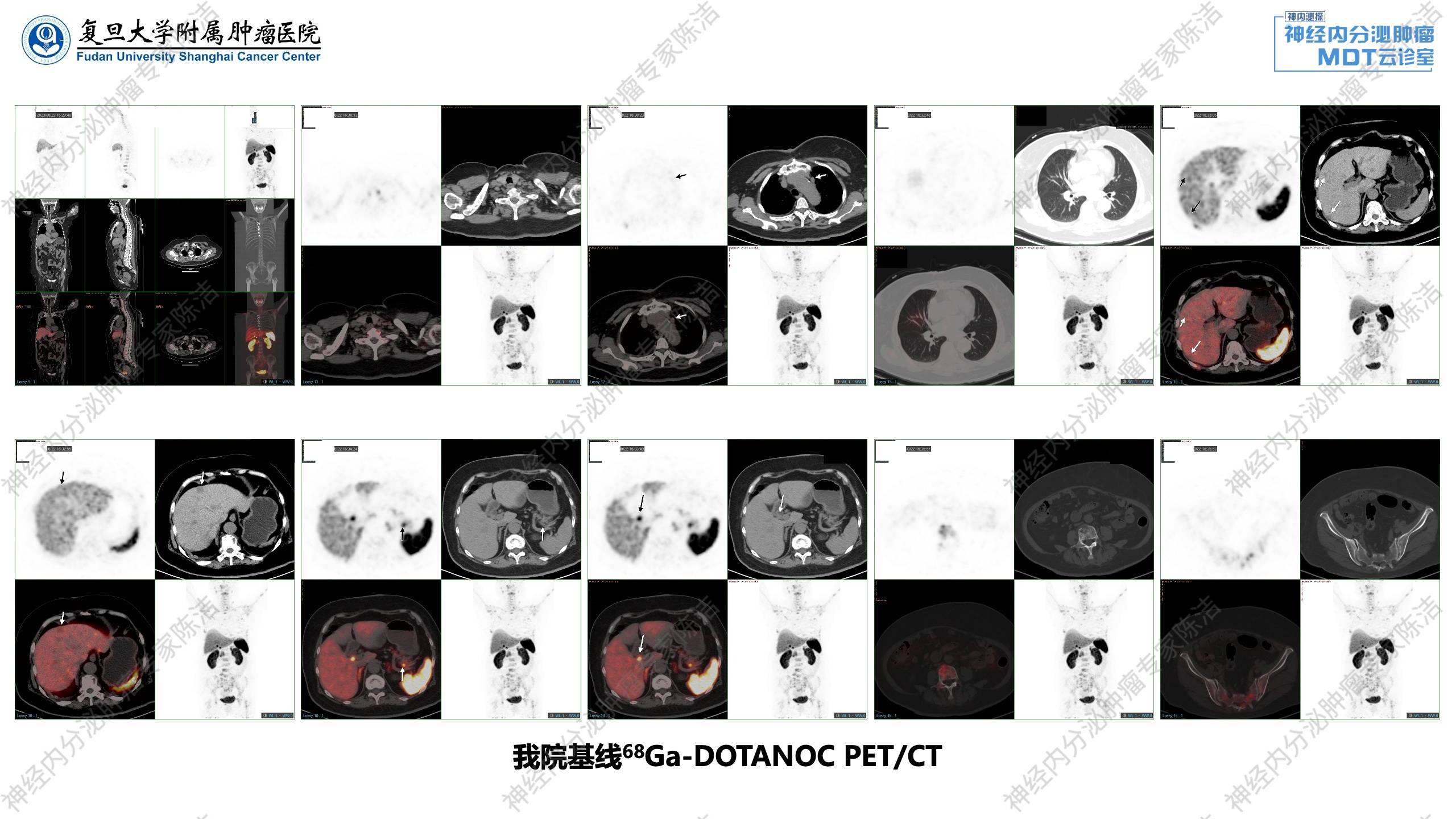
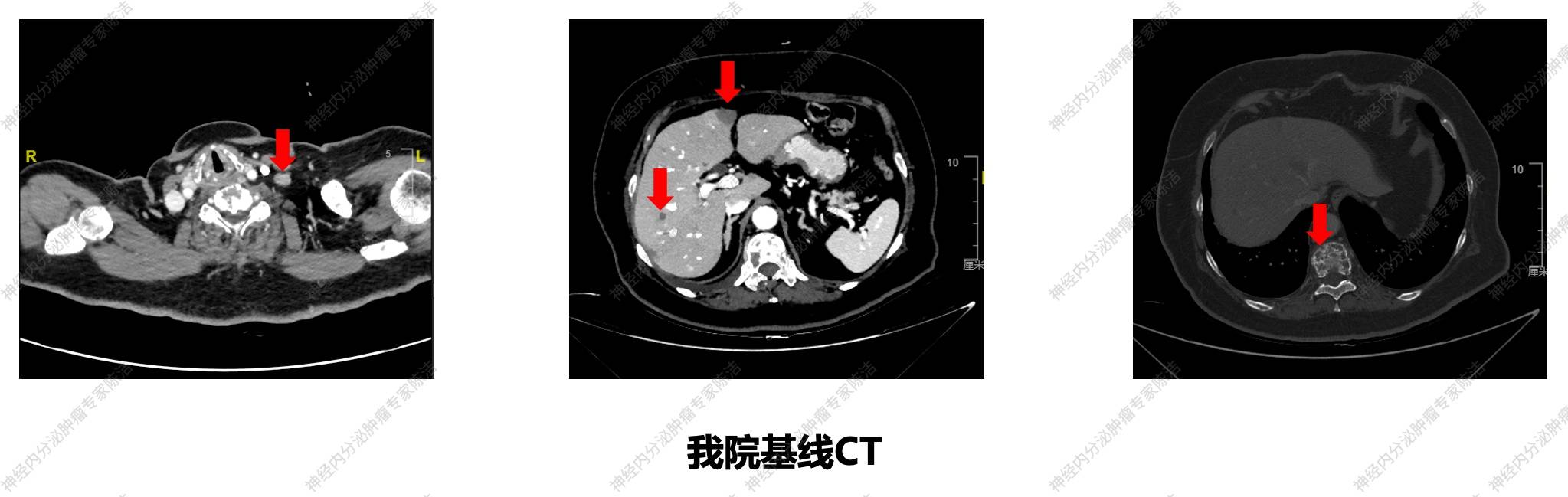
FDG-PET/CT提示:纵隔神经内分泌肿瘤治疗后,全身多发淋巴结转移;骨骼广泛转移;肝脏多发转移;双侧肾上腺转移可能。68Ga-SSA-PET/CT:与FDG-PET/CT相比较,1.胸腺NET术后,左下颈、锁骨上、前纵隔、腹膜后多发淋巴结转移,肝脏多发转移,生长抑素受体不表达,SSTR-RADS 3D;全身广泛混合性骨转移,生长抑素受体表达轻度增高,SSTR-RADS 3A,以上病灶FDG代谢均异常增高。2.胰尾局灶性NOC摄取增高,考虑为NET(第二原发),肝门部淋巴结转移,生长抑素受体高表达,SSTR-RADS 5,FDG低代谢。3.两侧胸腔积液;右肾复杂囊肿,右肾盂扩张、积水。
腰椎MRI:所示各腰椎、骨盆信号及强化不均,骶骨右侧局部骨质破坏,考虑转移可能。L5椎体下缘、S1椎体上缘异常信号,终板炎可能。L3-4/L4-5椎间盘轻度膨出。
激素及相应效应指标检测发现:甲状旁腺素19.4pmol/L,血钙2.64mmol/L,余无特殊。
基因检测:MEN1基因胚系突变。
2023年9月6日予经皮腰椎椎体成形术(PVP)+椎体活组织检查。术后病理:(腰椎,活检)骨小梁间见异形上皮样和短梭形细胞巢团,结合病史和免疫组化结果,符合纵隔神经内分泌肿瘤(NET,G2)转移。免疫组化:AE1/AE3(+),Syn(+),CgA(+),CD56(+),INSM1(+),TTF-1(-),PAX8(-),S-100(-),ERG(-),Ki-67(+,5%)。
术后采取CAPTEM方案(卡培他滨+替莫唑胺)化疗,并继续地舒单抗治疗。

疗效评估:
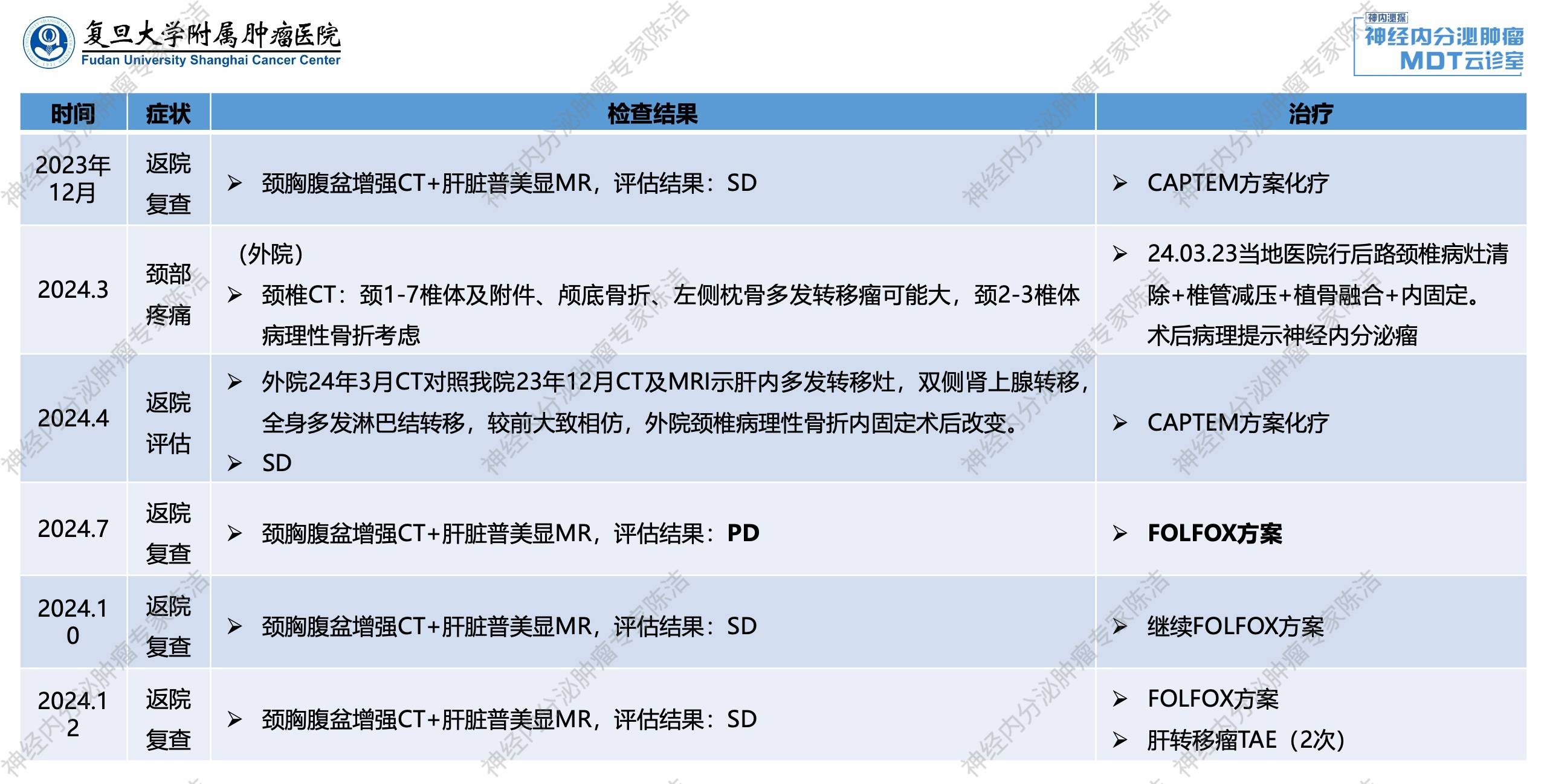
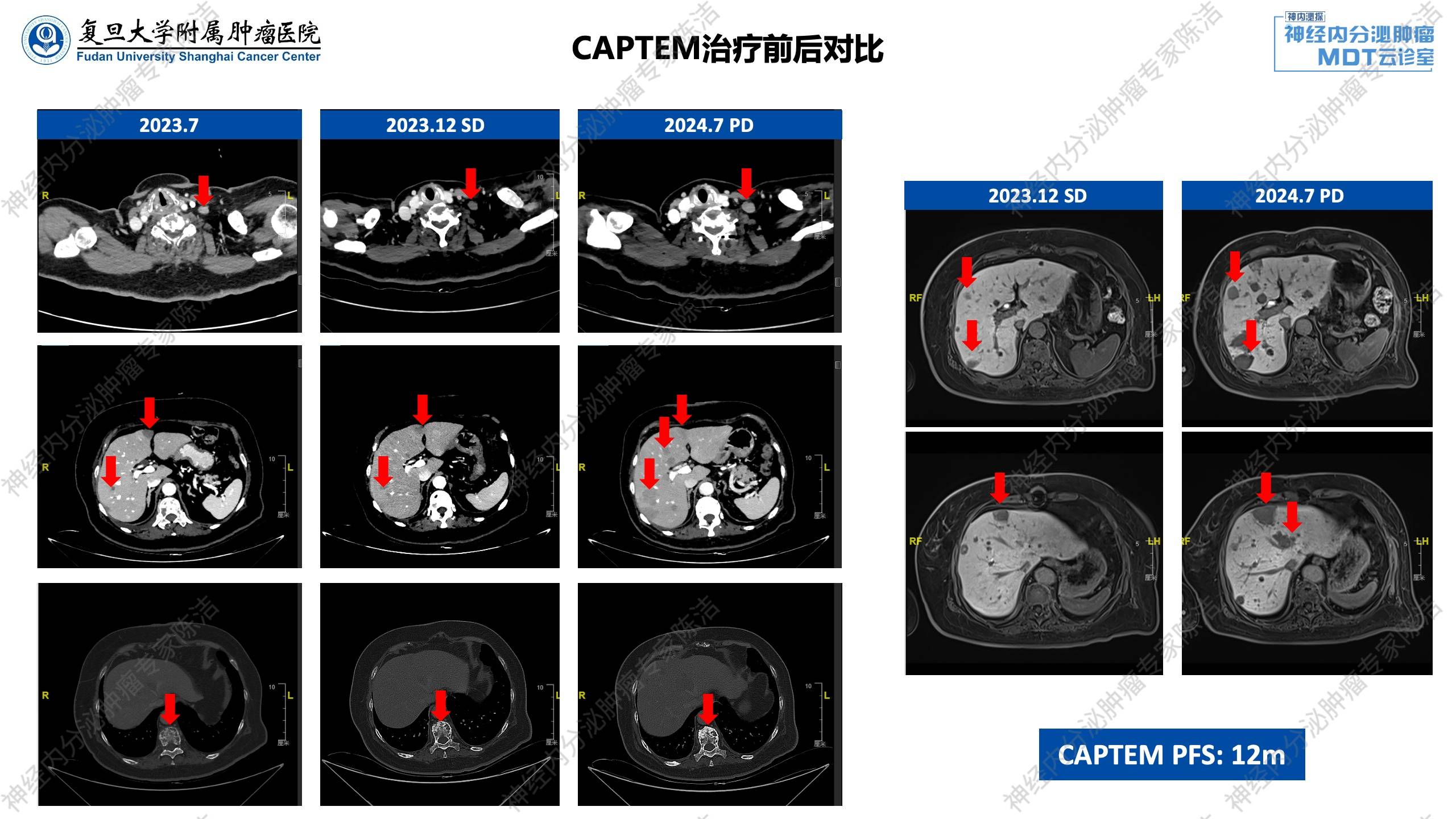
2023年12月复查颈胸腹盆增强CT+肝脏普美显MR,疗效评估为SD,继续CAPTEM方案化疗。
2024年3月,因颈部疼痛,患者于外院行CT检查,提示颈1-7椎体及附件、颅底骨折、左侧枕骨多发转移瘤可能大,颈2-3椎体病理性骨折考虑。于当地医院行后路颈椎病灶清除+椎管减压+植骨融合+内固定,术后病理提示神经内分泌瘤。
2024年4月患者返我院多学科门诊评估:外院2024年3月CT对照我院2023年12月CT及MRI,提示肝内多发转移灶,双侧肾上腺转移,全身多发淋巴结转移,较前大致相仿,外院颈椎病理性骨折内固定术后改变,疗效评估为SD。遂继续CAPTEM方案化疗。
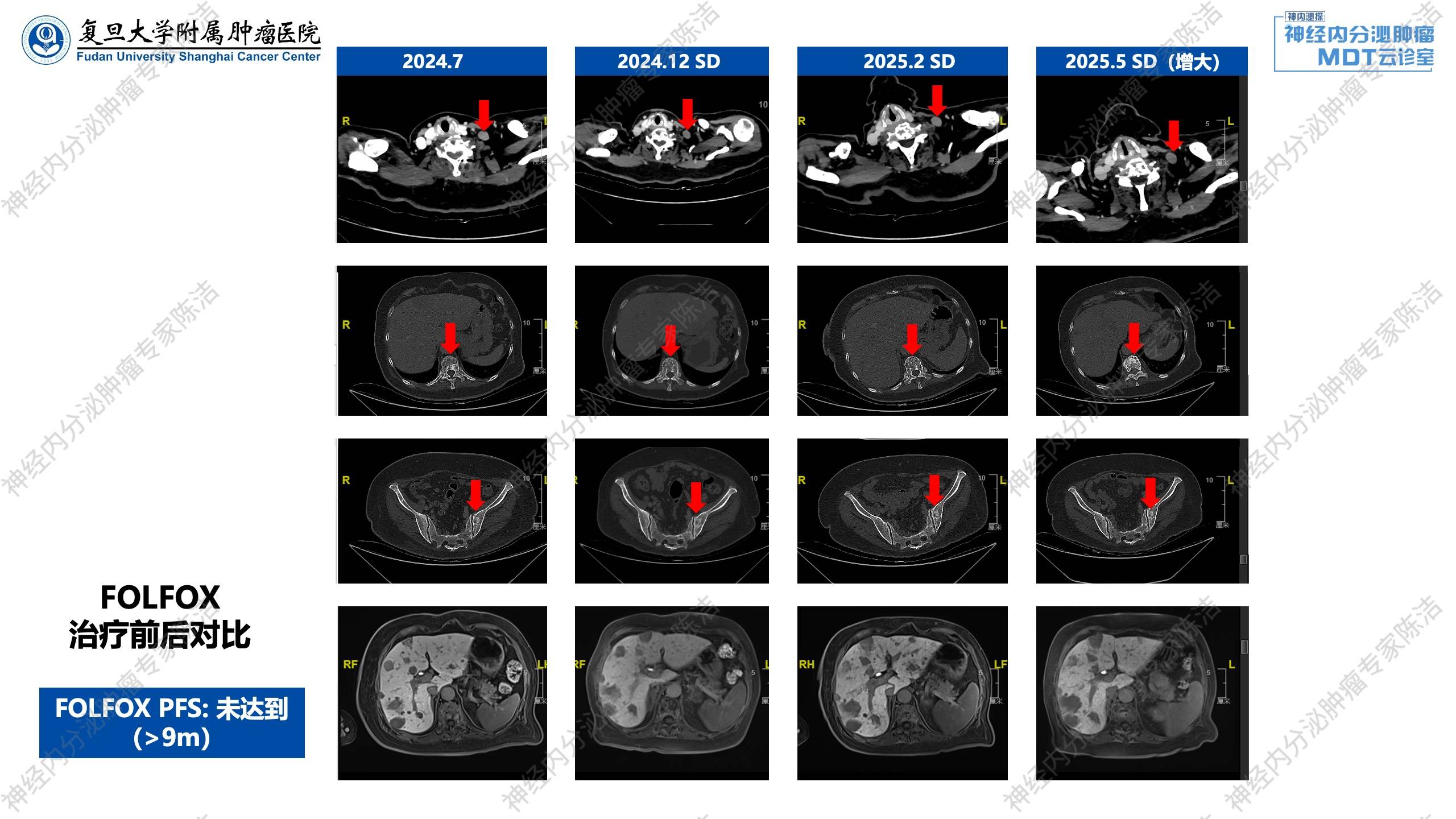
2024年7月复查颈胸腹盆增强CT+肝脏普美显MR,疗效评估为疾病进展(PD),换用FOLFOX方案化疗。
2024年10月复查颈胸腹盆增强CT+肝脏普美显MR,疗效评估为SD,继续FOLFOX方案治疗。
2024年12月复查颈胸腹盆增强CT+肝脏普美显MR,疗效评估为SD,继续FOLFOX方案治疗,并联合2次肝转移瘤经动脉栓塞(TAE)。
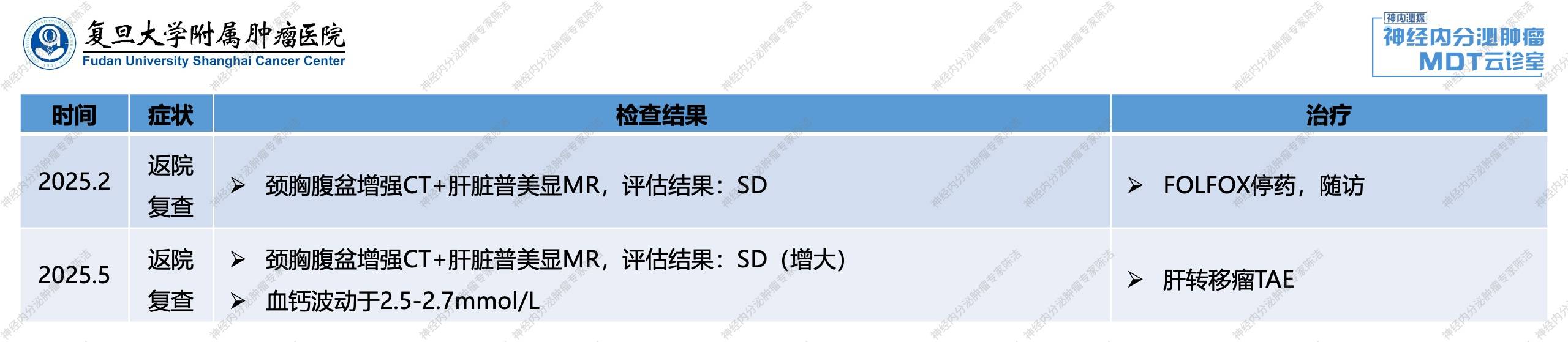
2025年2月,复查颈胸腹盆增强CT+肝脏普美显MR,疗效评估为SD。因FOLFOX方案已使用12周期,停用FOLFOX,并定期随访。
2025年5月,复查颈胸腹盆增强CT+肝脏普美显MR,总体病情稳定,但肝内肿瘤有轻微增大,疗效评估为SD(增大),化疗期间多次复查血钙波动于2.5~2.7mmol/L。于2025.5再次行肝转移瘤TAE治疗。
多学科团队(MDT)讨论
李媛教授:回顾患者两次的病理标本,2019年首次手术的胸腺原发灶,形态学为上皮样肿瘤,免疫组化CgA、Syn、CD56均为阳性,Ki-67为10%,诊断为NET G2级。2023年腰椎转移灶的活检标本,形态学与原发灶一致,Ki-67为5%,仍为G2级。两次Ki-67指数虽有差异(10% vs 5%),但仍在同一级别内,可认为肿瘤分级在四年间没有发生本质变化,差异可能源于肿瘤异质性或取材差异。

徐俊彦教授:该病例的PET/CT双核素扫描非常有价值。FDG-PET/CT图像显示,患者存在广泛的骨转移(颅骨、脊柱、肋骨、盆骨等)、多处淋巴结转移及肝转移,这些病灶均表现为FDG高代谢。
68Ga-DOTATATE PET/CT结果显示出明显的肿瘤异质性。上述FDG高代谢的骨、肝、淋巴结转移灶,其生长抑素受体(SSTR)表达均为阴性或低表达。
然而,在胰腺的头部和尾部,可清晰地看到多个SSTR高表达的小结节病灶,这些病灶在FDG-PET上不显影。
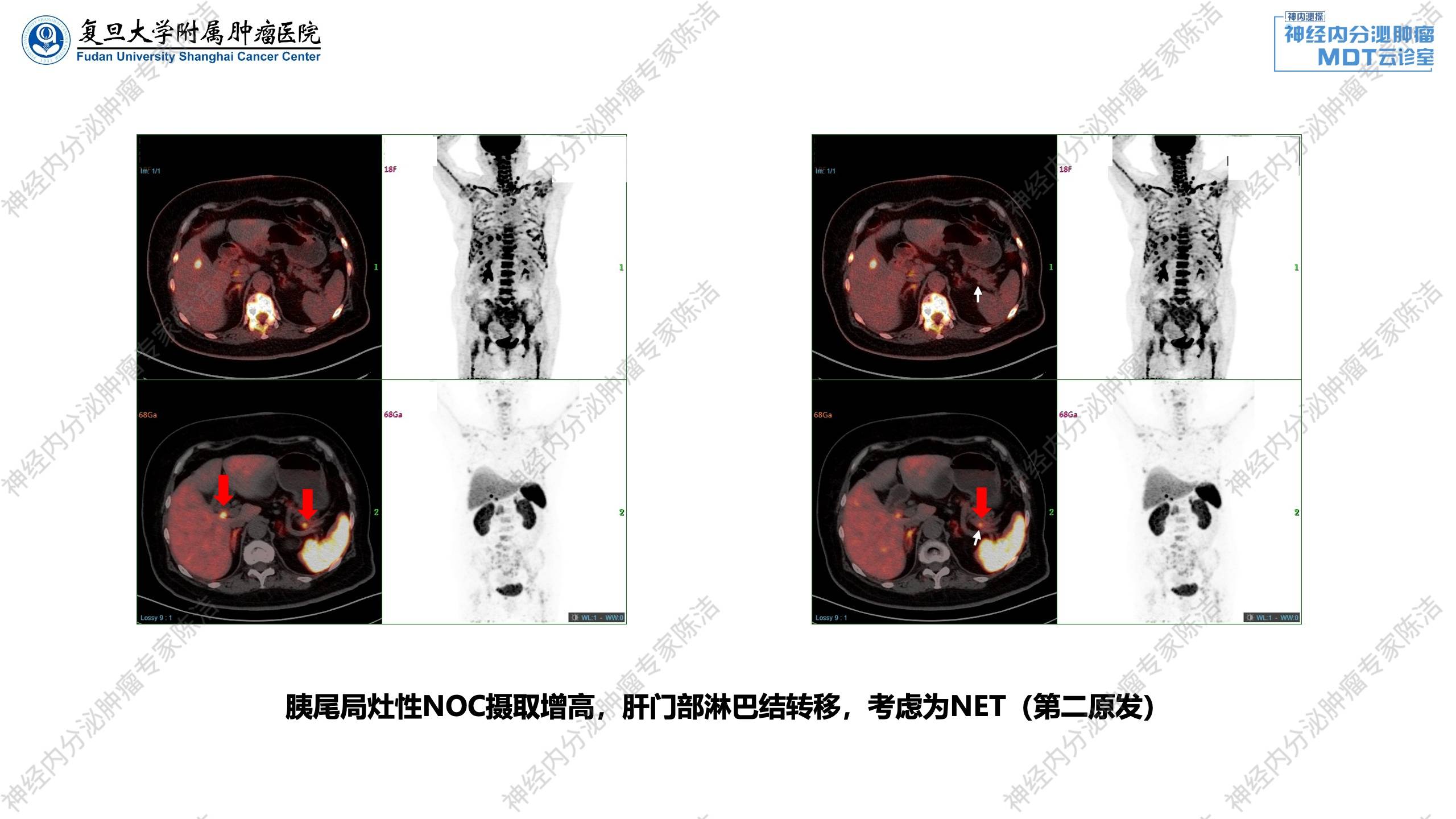
这一发现强烈提示患者为MEN1综合征,存在多原发神经内分泌肿瘤(胸腺NET和胰腺NET)。其广泛转移的病灶来源于SSTR阴性、FDG阳性的胸腺NET,生物学行为更具侵袭性。而SSTR阳性的胰腺病灶是独立的、分化可能更好的原发灶。双核素扫描对于明确诊断、揭示肿瘤异质性及指导后续治疗(如是否适用PRRT)至关重要。
汤伟教授:从系列影像学来看,该患者的转移特点是“散”,多发、散在分布于淋巴结、肝脏和全身骨骼。对比2023年7月(治疗前)和12月(治疗后)的影像,可见淋巴结和肝脏病灶保持稳定,证实了CAPTEM方案的有效性。到2024年7月,可见锁骨上淋巴结较前饱满,肝脏转移灶增大增多,明确为PD,为更换治疗方案提供了依据。在FOLFOX治疗后,对比2024年12月及2025年2月的影像,可见淋巴结和骨转移病灶持续稳定,肝脏病灶也基本稳定,显示FOLFOX方案再次控制了病情。
宋丽杰教授:肺与胸腺神经内分泌肿瘤常被误作小细胞神经内分泌癌处理,而该病例证明,遵循神经内分泌肿瘤的规范化阶梯治疗能为患者带来长期的生存获益,远优于小细胞神经内分泌癌的治疗模式。其次,该病例强调了在肺与纵隔NET中检测MEN1基因的重要性,尤其是当患者出现血钙异常等提示性体征时,应积极进行相关基因检测。同时,该病例也印证了这类肿瘤骨转移发生率远高于胃肠胰NET的临床特征。宋教授还提出疑问,对于这种Ki-67指数较低的患者,依维莫司是否可纳入用药考量范围?如果纳入,何时使用最佳?
陈洁教授总结
该病例患者病程已达五年,符合NET惰性与恶性并存的特点。胸腺NET一个非常显著的特征就是易于发生广泛骨转移,本例患者的弥漫性骨转移是其典型表现。通过双核素PET/CT扫描,我们不仅明确了转移范围,更重要的是发现了胰腺的SSTR高表达病灶,并结合基因检测最终确诊为MEN1综合征。这提示我们,对于看似散发的NET,尤其是多器官受累或年轻患者,应有遗传综合征的鉴别诊断意识。
对于治疗策略的选择,患者在外院使用了索凡替尼,但考虑到其肿瘤负荷高、骨转移广泛且症状明显,我们评估认为需要更强的全身治疗。CAPTEM方案是晚期分化良好NET(G2/G3)的标准一线化疗方案,该患者获得了长达12个月的PFS,疗效显著。在CAPTEM进展后,我们选择了FOLFOX方案,目前已帮助患者稳定病情超过9个月,并显示出持续的获益。
在全身治疗的同时,积极运用局部手段。针对疼痛和有病理性骨折风险的腰椎,进行了放疗和椎体成形术;针对进展的肝脏病灶,适时介入TAE治疗。这种全身与局部相结合的模式,是晚期NET综合管理的核心。
针对没有选择依维莫司原因,一是考虑依维莫司在如此高肿瘤负荷的患者中可能疗效有限;其次,依维莫司的不良反应不容忽视,如口腔炎、感染风险增加、高血糖、高血脂等。尤其重要的是间质性肺炎的风险,对于胸腺原发、肺部情况复杂的患者,使用时需格外谨慎。此外,对于需要进行手术的患者,依维莫司会增加感染和并发症的风险。因此,针对这例患者,倾向于将化疗(如CAPTEM)或其它靶向药(如TKI)置于依维莫司之前,依维莫司可作为后线或特定情况下的选择。
该病例充分展示了对于晚期胸腺神经内分泌肿瘤,如何通过精准诊断、MDT、以及规范化全身与局部治疗相结合的策略,为患者争取到长期的生存和良好的生活质量,这对临床实践具有重要的指导意义。
更多精彩病例,可点击或复制以下链接,粘贴到浏览器查看神经内分泌肿瘤MDT云诊室-胸腺类癌/不典型类癌专场回放:
https://doctor.liangyihui.net/#/doc/150698

本文仅供健康科普使用,不能作为诊断、治疗的依据,请谨慎参阅。











 苏公网安备32059002004080号
苏公网安备32059002004080号


