由北京健康促进会发起的“希愈纪”2024血液肿瘤临床思维菁英show项目自2024年6月启动以来,踊跃出许多血液肿瘤领域优秀的病例,本系列旨在通过摘取出该项目突出病例,使更多的临床医师更快、更便捷的学习血液疾病诊疗相关知识,促进血液疾病个体化和全程规范治疗,帮助更多血液肿瘤患者获得获得创新前沿的诊疗方案,造福更多患者。本文邀请分享一例MM诊疗病例,详情如下。
病例简介
患者信息
一般资料:患者男,55岁;
现病史:2018年1月24日因“突发双下肢无力,伴大小便失禁3天”入住亳州市人民医院。患者于无明显诱因下出现双下肢无力,不能行走,背部有轻度疼痛,伴大小便失禁,无外伤史。2018年1月23日,上海市第六人民医院行PET/CT提示:全身弥漫性骨质疏松、骨质破坏,以T7、T9为著,考虑多发性骨髓瘤可能性。患者为求进一步治疗,随来亳州市人民医院,拟“多发性骨髓瘤”收住,病程中神志清楚,精神欠佳,体重无明显变化,睡眠可,进食少。
既往史:既往无高血压、冠心病、糖尿病等慢性病史,无乙肝、结核病史,无药物、毒物接触史,无药物、食物过敏史,无吸烟、饮酒史,无家族遗传史。
阳性体征:神清,精神一般,推入病房。腹壁以下深浅反射消失,双下肢无力,肌力0级。
辅助检查
血常规:WBC 10.02×109/L,N 7.02×109/L,HB 104g/L,PLT 307×109/L;
生化:TP 95.5g/L,GLO 64.2g/L,CREA 144.4μmol/L ,LDH 21U/L,血钙2.21 mmol/L;
免疫球蛋白:IgG 5.42g/L,IgA 53.7 g/L,IgM < 0.169 g/L,IgE 43.1 IU/mL;
β2-微球蛋白:3.89mg/L;
骨髓细胞形态学:浆细胞明显增多占21%;
骨髓免疫分型:骨髓中可见单克隆增生的浆细胞,约占有核细胞的10.58%,考虑为浆细胞骨髓瘤(CD38强阳性、CD56阳性,Lambda阳性);
免疫固定电泳:IgA阳性、λ链阳性;
血清蛋白电泳:M蛋白46g/L;
骨髓活检:浆细胞及浆样细胞比例增高,考虑浆细胞骨髓瘤;
骨髓染色体:46,XY;
FISH检测(经CD38磁珠富集分选):del(17p),t(4;14),t(14;16),t(14;20),1q21,t(11;14)均未见信号异常
临床诊断
多发性骨髓瘤(IgA-λ型 DS III期A组,ISS II期, R-ISS II期,mSMART3.0:标危
患者转入北京大学第一医院行胸椎7,9椎体病灶清除+椎管减压内固定术。
术后病理回报:(胸9肿物)破碎软骨、纤维及骨髓组织,骨髓结构破坏,见大量浆细胞一致弥漫性浸润,部分形态幼稚,部分形态成熟(图1)。
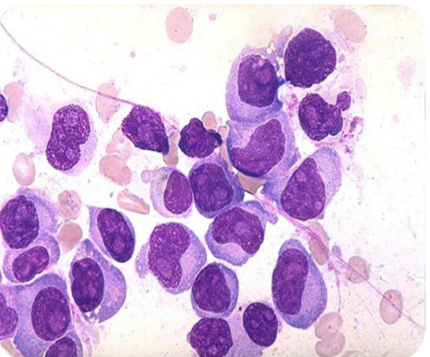
术后大小便失禁、四肢无力症状明显好转。
治疗经过
第一个治疗阶段(诱导治疗阶段)

2018年5月26日,行4周期PAD方案(硼替佐米:2.2mg ih d1、d4、d8、d11,DEX:20mg d1-2、d4-5、d8-9、d11-12,表柔比星:26mg d1-4)治疗后,疗效评估为VGPR,建议患者行自体造血干细胞移植,但患者因经济原因拒绝。

2018年11月14日,行9周期PAD方案治疗后,血清蛋白电泳、血尿免疫固定电泳均阴性,骨髓浆细胞约占3%。疗效评估为CR。
第一次复发
2019年4月26日,患者出现右侧股骨疼痛
2019年5月4日,右股骨MRI平扫:双侧股骨干多发异常信号,结合病史,符合多发性骨髓瘤改变;
2019年5月5日,血清蛋白电泳:M蛋白12g/L;
2019年5月、2019年6月,行V-DECP方案化疗(硼替佐米:2.4mg d1、4、8、11,顺铂:18.55mg 静滴 d1-4,环磷酰胺:742mg 静滴 d1-4,依托泊苷: 74.2mg d1-4,地塞米松:40mg d1-4);
2019年6月28日,左股骨MRI平扫:双侧股骨干多发异常信号,病变范围较 2019年5月4日片减小;
2019年7月、2019年8月行V-DECP方案
2019年10月1日行右侧股骨放疗,PTV:4000cGY/20f;
2019年11月9日,M蛋白4g/L,疗效评估为PR;

2020年6月2日,行7周期VRD方案(硼替佐米:2.4mg d1、4、8、11,来那度胺:25mg 每晚口服 d1-21,地塞米松:20mg d1-2,d4-5,d8-9,d11-12)治疗后,血清蛋白电泳、血尿免疫固定电泳均阴性,骨髓浆细胞约占1%,右股骨MRI平扫阴性,疗效评估为CR;
第一次复发后维持治疗
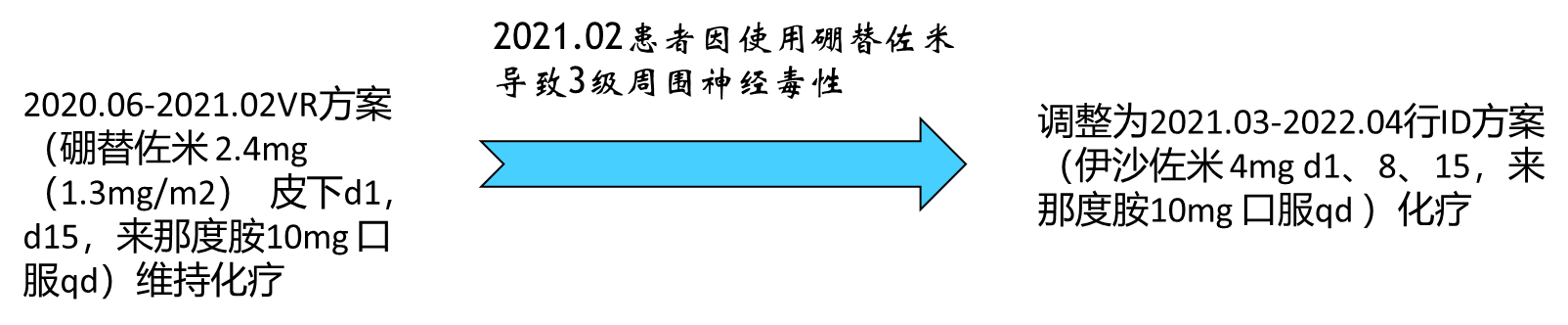
2022年4月,血清蛋白电泳、血尿免疫固定电泳均阴性;
第二次复发
2022年5月28日,血清M蛋白5.43g/L,诊断为生化复发;

2023年3月,血清蛋白电泳、血尿免疫固定电泳均阴性,骨髓浆细胞约占2%,疗效评估为CR;
第三次复发
2023年7月15日,患者再次出现右大腿疼痛;
2023年7月19日,骨髓免疫分型:原始区域细胞约占有核细胞的0.1%,血清蛋白电泳:血清M蛋白含量16.62g/L,免疫固定电泳:IgA-LAM型血症;

第三个治疗阶段(第三次复发)
2023年7月21日,经外周血进行单个核细胞单采,共采集60ml;
桥接治疗:2023年7月22日~2023年8月5日,予以3次KPD方案化疗,患者关节疼痛缓解不明显;2023年8月12日~2023年9月20日,每周一次共进行8次DD方案化疗(达雷妥尤单抗,1000mg 静滴 qw,地塞米松20mg qw)患者关节疼痛明显缓解;
2023年10月,血清蛋白电泳:血清M蛋白含量3.4g/L。免疫固定电泳:IgA-LAM型血症;CT结果回示:左侧脾肾间隙、腹盆腔及腹膜后多发软组织结节;病例检查结果提示:非骨相关髓外多发性骨髓瘤(EM-E);
2023年10月11日,行FC方案预处理(氟达拉滨:30mg/㎡,50mg -5d、-4d、-3d,环磷酰胺:300mg/㎡,500mg -5d、-4d、-3d),于2023年10月17日,回输靶向BCMA CAR-T细胞7ml,细胞数 7*108/ml;
2023年12月,骨髓MRD检测:未见免疫表型明显异常的细胞(<10-4),血清蛋白电泳:血清M蛋白含量0g/L,免疫固定电泳:阴性;
2023年12月11日,CT结果回示:脾脏前缘软组织影,副脾待排,评估为髓外进展;
2023年12月26日,开始放疗(PGTV:40Gy/20),至2024年1月26日结束;

第四次复发
2024年2月,每周一次共进行4次DD方案化疗(达雷妥尤单抗:d1 1000mg,地塞米松:20mgd1-2);
2024年3月5日,患者出现右腹部疼痛;
2024年3月6日,CT结果回示:右侧胸腔内见弧形低密度影,右中腹部见结节状软组织密度,直径约25mm;直肠右侧可见软组织密度影,边界清,大小约20mm×17mm
2024年3月6日,血清蛋白电泳:血清M蛋白含量8.32g/L,免疫固定电泳:IgA阳性、λ链阳性;
2024年3月6日,予以多柔比星脂质体+地塞米松+塞利尼索方案化疗(多柔比星脂质体:静脉滴注 40mg d1,地塞米松:15mg 口服qw,塞利尼索:60mg 口服 qw);
2024年4月,患者开始予以SD方案化疗(地塞米松:15mg 口服qw,塞利尼索:60mg 口服 qw);
2024年4月15日、2024年6月21日、2024年8月16日、2024年9月6日,行CT检查,结果回示:腹盆腔及腹膜后软组织结节,持续缩小
2024年9月,血清蛋白电泳:血清M蛋白含量0.7g/L;免疫固定电泳:IgA阳性、λ链阳性,疗效评估为VGPR。
病例总结
本病例分享聚焦于一例MM的男性患者,该患者历经多线治疗且表现出多重耐药性和复杂的病情演变。在长达六年的治疗过程中,该患者经历了PAD、VRD等标准方案,以及多次复发后接受包括放疗和多种新型药物的干预。在多次病情进展中,患者先后出现骨髓外病变及髓外复发,展现了MM疾病的高度异质性和挑战性。在第四次复发后,,患者从塞利尼索联合多柔比星脂质体+地塞米松方案开始,后调整为SD方案治疗,疗效显著。连续CT检查结果显示腹盆腔及腹膜后软组织结节持续缩小,血清M蛋白从下降至0.7g/L,免疫固定电泳依然显示IgA及λ链阳性,疗效评估达到VGPR。此病例显示,SD方案在复发难治性MM患者中的应用具有显著疗效,尤其在多次复发及耐药后仍可观察到病灶的持续改善。
该病例为多次复发的MM治疗提供了重要的参考价值。尽管患者病情复杂且历经多线治疗失败,SD方案的有效性和耐受性为该类难治患者提供了新的治疗策略,并为未来个体化治疗方案的优化积累了宝贵经验。后续需持续观察其长期疗效及对患者预后的改善情况。
排版编辑:肿瘤资讯-小编











 苏公网安备32059002004080号
苏公网安备32059002004080号


