来源:肿瘤资讯
肺癌是中国发病率和死亡率均位列第一的癌症[1],其中85%为非小细胞肺癌(NSCLC)。在NSCLC患者中,EGFR Exon 20ins突变目前被认为是继19Del及L858R 点突变之后的第三大突变,发生率在EGFR阳性NSCLC患者中占4%~12%[2-4]。EGFR Exon 20ins突变患者缺乏高效的靶向治疗,对现有治疗手段疗效差、生存率低[5-9]。
Amivantamab(JNJ-61186372)是一种靶向EGFR及c-MET的人源化双特异性抗体,通过肿瘤细胞上与EGFR和c-MET相关的多种Fc非依赖性和Fc依赖性作用机制产生抗肿瘤活性[10-12]。基于2020年WCLC会议上公布的I期CHRYSALIS研究中Amivantamab单药治疗结果[13],Amivantamab 已获得美国食品药品监督管理局(FDA)批准,用于治疗铂类化疗后进展的EGFR 20外显子插入突变的NSCLC。
1. 研究目的
在EGFR非经典突变中,Exon 20ins最常见,其发生率仅次于19del和L858R。EGFR Exon 20ins突变患者对现有治疗手段疗效差、生存率低,缺乏高效的靶向治疗药物。Amivantamab是一种EGFR/c-Met双抗,本研究报道了Amivantama在EGFR 20ins突变NSCLC患者中疗效和安全性的最新结果[14]。
2. 研究方法
CHRYSALIS是一项I期、开放标签、剂量递增和剂量扩展的临床研究(NCT02609776),自2016年5月27日至2020年6月8日期间,共纳入81例含铂化疗进展后的EGFR Exon 20ins NSCLC患者,前4周每周给予Ⅱ期临床研究推荐的剂量1050 mg Amivantamab(≥80kg患者为1400mg),第5周开始每2周给予1次。主要研究终点是剂量限制性毒性和客观缓解率(ORR)。
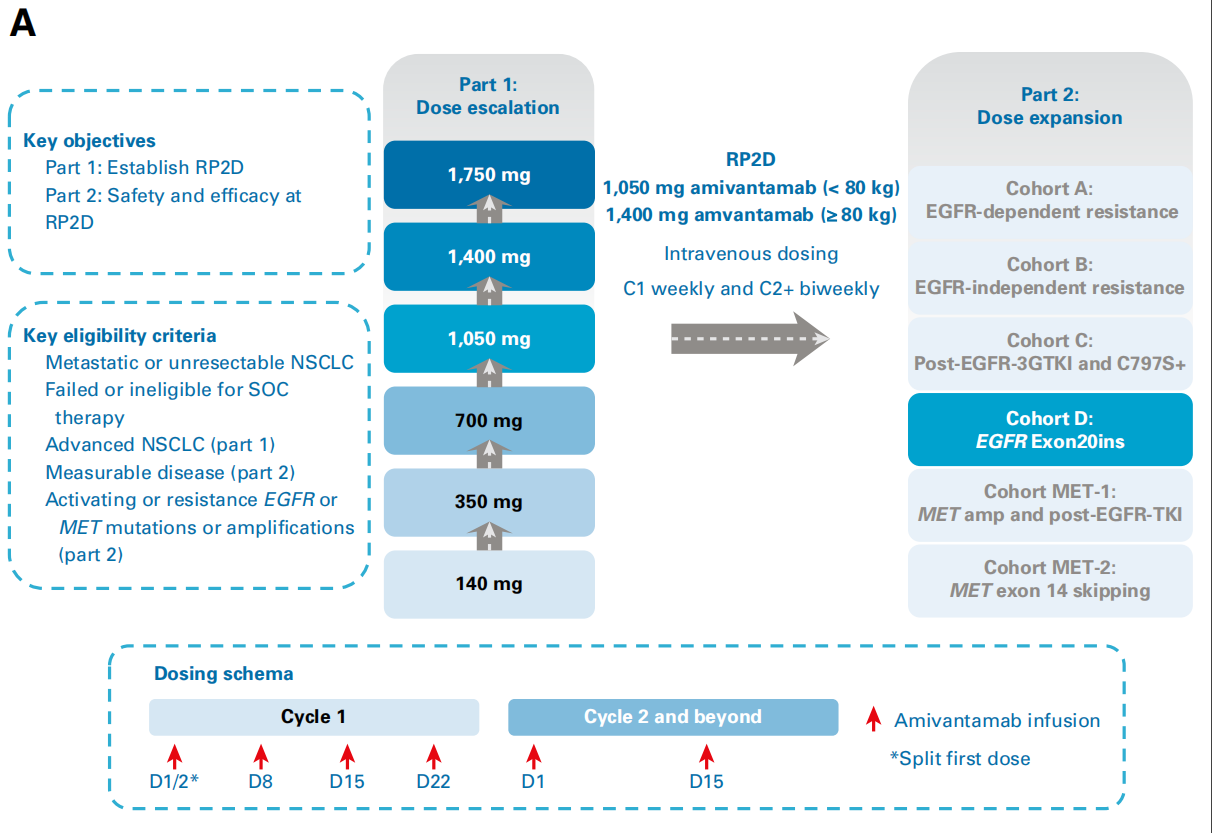

3. 研究结果
3.1 疗效分析
81例接受治疗的患者,独立评审委员会(BICR)评估的客观缓解率(ORR)为40%(32/81),其中3例证实完全缓解(CR),29例部分缓解(PR)。数据截止时,仍有15例患者在接受治疗,中位缓解持续时间(DOR)11.1个月。47例(58%)患者发生疾病进展或死亡, BICR 和研究者评估的中位无进展生存期(PFS)均为 8.3 个月(95% CI, 6.5 - 10.9)。中位总生存期(OS)为 22.8 个月(95% CI,14.6 -未达到)。
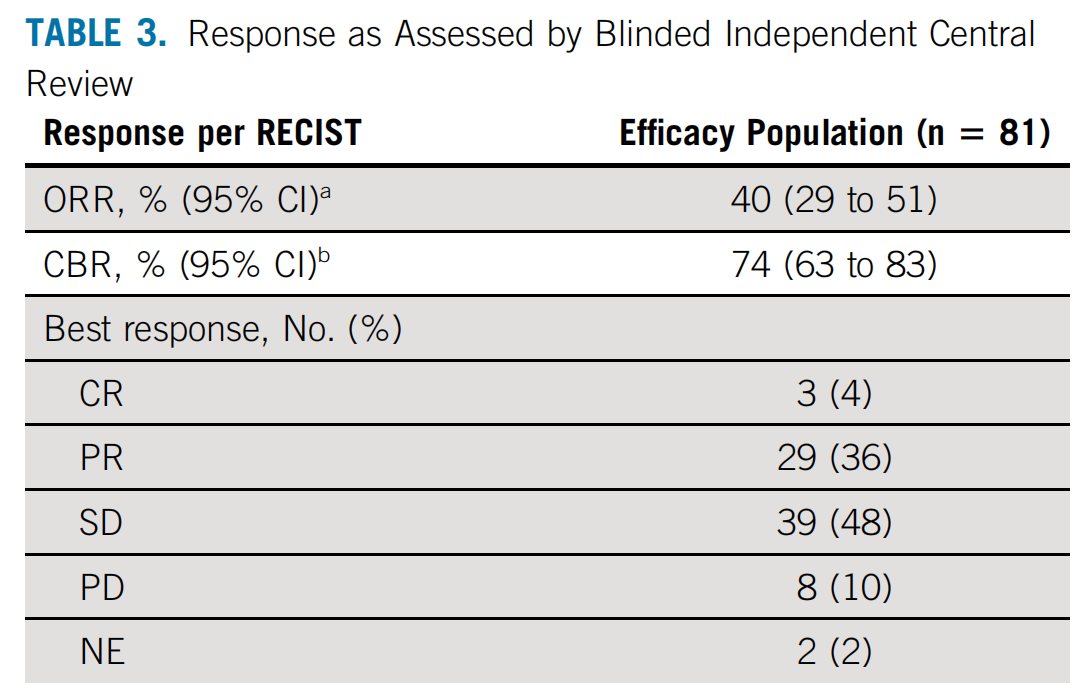
81例患者均有ctDNA或肿瘤样本提交中心检测,其中63例患者有可检测的ctDNA,这63份ctDNA样本共检测出25种不同的Exon 20ins亚型。在20号外显子的螺旋区、近环和远环区域内有插入突变的患者中均观察到抗肿瘤反应。
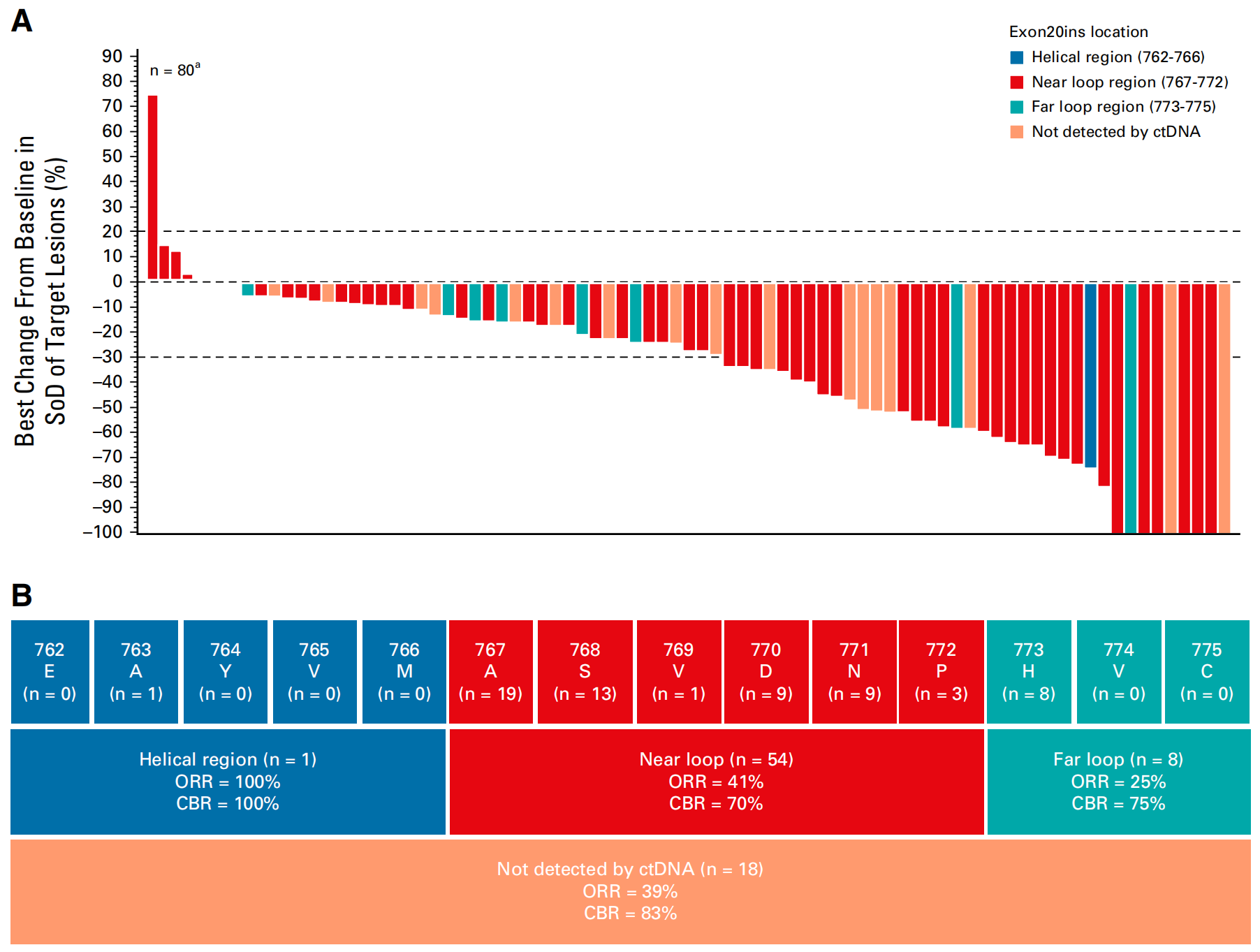
3.2 安全分析
不良反应方面,与EGFR抑制相关的不良反应包括:皮疹(86%)、甲沟炎(45%)、口腔炎(21%)、瘙痒(17%)、腹泻(12%);与MET抑制相关不良事件包括:低蛋白血症(27%)和外周水肿(18%)。在安全性分析人群中,18例(16%)患者发生≥3级治疗相关不良反应,最常见的是皮疹(4%)、输注反应(3%)和中性粒细胞减少(3%)。10例(9%)患者发生治疗相关严重不良反应,包括输注反应(2%)和腹泻(2%)等。15例(13%)患者因无法忍受的毒性而减少了剂量,5例(4%)患者因不良反应而停止了用药。无治疗相关5级不良反应发生。
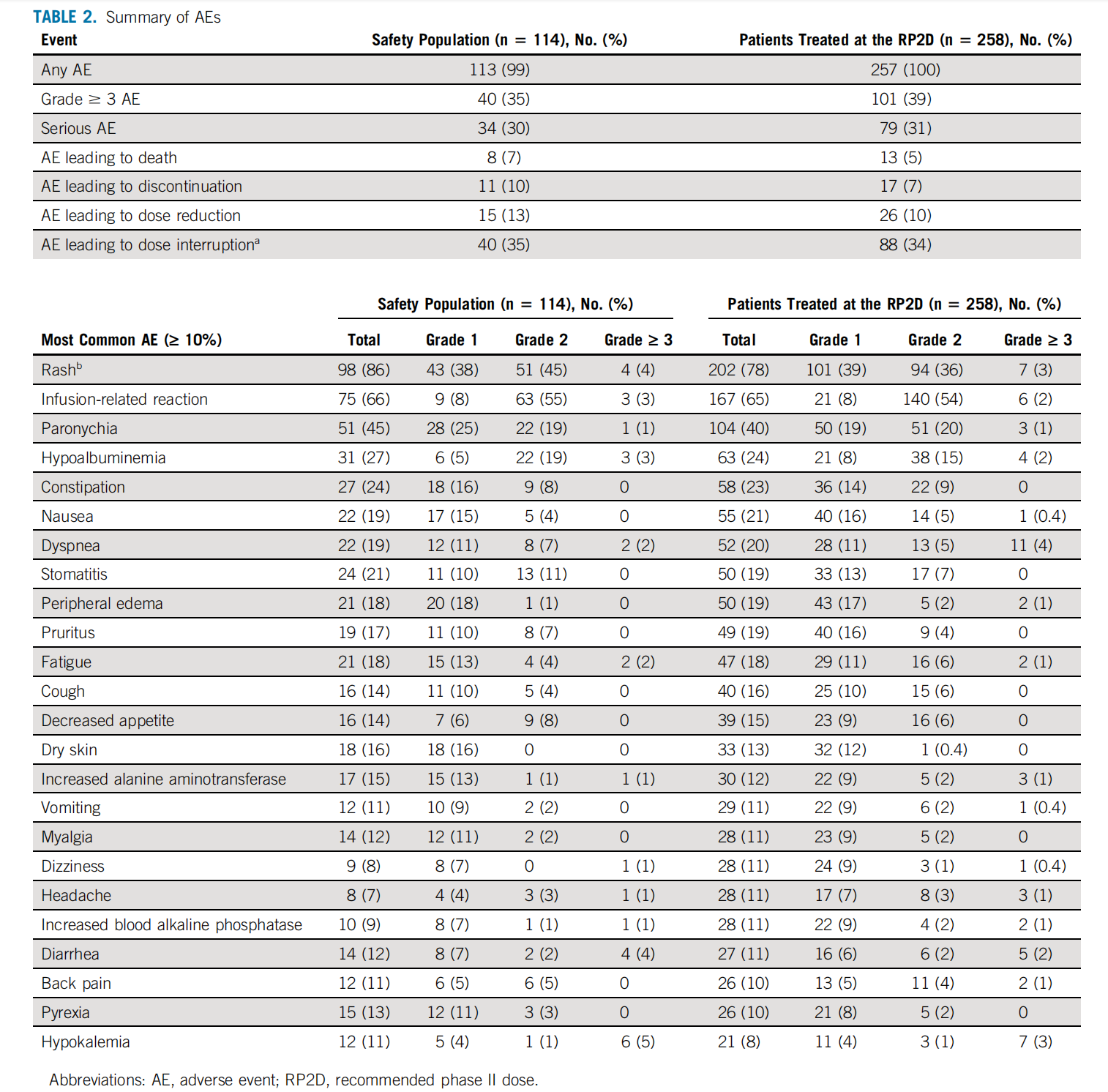
4. 研究结论
在该I期临床研究中,Amivantamab治疗EGFR Exon 20ins突变的NSCLC患者具有良好的抗肿瘤活性,并且安全性可控,是EGFR Exon 20ins突变NSCLC患者有效的治疗方法。
国内临床进展
在中国,Amivantamab已经被中国国家药监局(NMPA)纳入突破性治疗药物,目前已在中国内地展开临床试验。因此,非小细胞肺癌患者如果携带EGFR Exon 20ins变异可以通过肿瘤基因检测,寻求潜在的靶向治疗获益。阔然基因肺癌检测产品包含EGFR Exon 20ins检测,并且具有高灵敏度和特异性,助力非小细胞肺癌患者精准诊疗。
[1].Rongshou Zheng, Jie He, et al. Cancer incidence and mortality in China, 2016[J]. Journal of the National Cancer Center, 2022 March 9;5:38.
[2].Arcila ME, Nafa K, Chaft JE, et al. EGFR exon 20 insertion mutations in lung adenocarcinomas: prevalence, molecular heterogeneity, and clinicopathologic characteristics. Mol Cancer Ther. 2013;12(2):220-229.
[3].Oxnard GR, Lo PC, Nishino M, et al. Natural history and molecular characteristics of lung cancers harboring EGFR exon 20 insertions. J Thorac Oncol. 2013;8(2):179-184.
[4].Riess JW, Gandara DR, Frampton GM, et al. Diverse EGFR Exon 20 Insertions and Co-Occurring Molecular Alterations Identified by Comprehensive Genomic Profiling of NSCLC. J Thorac Oncol. 2018;13(10):1560-1568.
[5].Yang JC, Sequist LV, Geater SL, et al. Clinical activity of afatinib in patients with advanced non-small-cell lung cancer harbouring uncommon EGFR mutations: a combined post-hoc analysis of LUX-Lung 2, LUX-Lung 3, and LUX-Lung 6. Lancet Oncol. 2015;16(7):830-838.
[6].Chouaid C, Filleron T, Debieuvre D, et al. A Real-World Study of Patients with Advanced Non-squamous Non-small Cell Lung Cancer with EGFR Exon 20 Insertion: Clinical Characteristics and Outcomes. Target Oncol. 2021;16(6):801-811.
[7].Ramalingam SS, Vansteenkiste J, Planchard D, et al. Overall Survival with Osimertinib in Untreated, EGFR-Mutated Advanced NSCLC. N Engl J Med. 2020;382(1):41-50.
[8].Beau-Faller M, Prim N, Ruppert AM, et al. Rare EGFR exon 18 and exon 20 mutations in non-small-cell lung cancer on 10 117 patients: a multicentre observational study by the French ERMETIC-IFCT network. Ann Oncol. 2014;25(1):126-131.
[9].Lee CK, Davies L, Wu YL, et al. Gefitinib or Erlotinib vs Chemotherapy for EGFR Mutation-Positive Lung Cancer: Individual Patient Data Meta-Analysis of Overall Survival. J Natl Cancer Inst. 2017;109(6):10.1093/jnci/djw279.
[10].Moores SL, Chiu ML, Bushey BS, et al. A Novel Bispecific Antibody Targeting EGFR and cMet Is Effective against EGFR Inhibitor-Resistant Lung Tumors. Cancer Res. 2016;76(13):3942-3953.
[11].Vijayaraghavan S, Lipfert L, Chevalier K, et al. Amivantamab (JNJ-61186372), an Fc Enhanced EGFR/cMet Bispecific Antibody, Induces Receptor Downmodulation and Antitumor Activity by Monocyte/Macrophage Trogocytosis. Mol Cancer Ther. 2020;19(10):2044-2056.
[12].Yun J, Lee SH, Kim SY, et al. Antitumor Activity of Amivantamab (JNJ-61186372), an EGFR-MET Bispecific Antibody, in Diverse Models of EGFR Exon 20 Insertion-Driven NSCLC. Cancer Discov. 2020;10(8):1194-1209.
[13].Sabari JK, Shu CA, Park K, et al. Amivantamab in Post-platinum EGFR Exon 20 Insertion Mutant Non-small Cell Lung Cancer [EB/OL]. WCLC 2020, abstract OA.04.04.
[14].Park K, Haura EB, Leighl NB, et al. Amivantamab in EGFR Exon 20 Insertion-Mutated Non-Small-Cell Lung Cancer Progressing on Platinum Chemotherapy: Initial Results From the CHRYSALIS Phase I Study. J Clin Oncol. 2021;39(30):3391-3402.
















 苏公网安备32059002004080号
苏公网安备32059002004080号


