针对分子分型较为复杂的、HR阳性/HER2阴性复发型乳腺癌患者,氟维司群是作为疗效最强的单药内分泌治疗方案,多项临床试验的结果已经证实其疗效优于芳香化酶抑制剂。与此同时,氟维司群能够通过与其他药物的联用、进一步显著延长患者的生存获益。在此介绍一例在接受多线治疗失败以后、长期氟维司群治疗后达到部分缓解的绝经后HR阳性HER2阴性晚期乳腺癌病例

中国抗癌协会乳腺癌专业青年委员会 委员
中国癌症康复与姑息青年委员会 委员
黑龙江省慢病协会乳腺癌专业委员会副主任 委员
黑龙江省乳腺癌专业青年委员会 委员
黑龙江省医学会淋巴瘤分会 委员
黑龙江省医促会乳腺疾病专业 委员
黑龙江省医学会老年肿瘤分会 委员
主持国家自然科学基金项目3项,发表SCI收录文章30余篇。获省科技进步一、二等奖3项,中国抗癌协会科技奖二等奖1项。
患者,女性,初诊年龄52岁。生育状况:G1P1 已绝经(43岁)
2010-10患者以“左乳癌术后化疗后3个半月,左胸壁肿物20天”为主诉就诊。
患者2010年3月7日于外院行左乳癌仿根治术,术后病理示:(左乳)浸润性导管癌2级,腋下淋巴结见有癌转移29/31。术后免疫组化示:ER(+)较弱表达,PR(+-++),C-erbB2(-),Ki67(+)<5%,p53(-)。4月至5月行氟尿嘧啶联合表柔比星化疗2周期(具体治疗剂量不详),因不能耐受未继续治疗。
第一次复发:2010年10月
患者左胸壁手术区域发红,左胸壁可触及略隆起于皮肤表面的肿块,直径约2.5cm,左上肢活动明显受限。否认肿瘤家族史,否认家族性遗传性疾病史。
检查:2010-10-01CT示:双颈部及左锁上,右腋下小淋巴结,最大者11mm×4 mm。
治疗:2010-10-01起口服来曲唑(2.5 mg 1/日)治疗。
2010-10-19行左胸壁及左侧锁上及锁下放射治疗。
第二次复发:2012年4月
患者自觉背痛,右乳肿块,约2 cm×2 cm,右腋下可触及肿块,约1 cm×1 cm,质硬,活动度差,有压痛。
检查:CT示:新发纵隔淋巴结肿大,双侧胸腔积液。
B超示:右乳实性占位伴右腋下多发淋巴结肿大(CA可能性大),新发右锁上多发小淋巴结,新发双侧胸腔积液。
右乳肿物病理穿刺示:右乳浸润性癌,IHC:ER(+)阳性细胞约占90%,染色强度为强;PR(+)阳性细胞10%,染色强度为中,HER-2(+)。
治疗:TE(多西他赛120 mg联合表柔比星120 mg)方案化疗4周期。
疗效:右乳肿块缩小至1 cm×1 cm,右腋下、锁骨上淋巴结消失,双侧胸腔积液消失。
第三次复发:2014年12月
患者发现右锁上及左颈部肿物,质硬,活动度差,无压痛。
检查:ECT示:全身骨显像见骨放射性异常分布,胸骨角、左侧前臂近端放射性异常浓聚,另见腰4椎体放射性轻度聚集,其余诸骨未见明显异常。
CT示:右锁骨上区淋巴结较前增大,最大者大小约16 mm×29 mm,多发性骨质改变。
B超:右乳结节性占位(BI-RADS 4类),右锁上,左中颈外侧多发淋巴结肿大。
新增病灶:检查提示右锁上、左颈部淋巴结及骨转移。
治疗:2014-01-22入组临床研究,口服卡培他滨(希罗达 2000 mg bid)6周期,疗效为SD,患者因自身原因出组。
2014-07-01起持续三苯氧胺(他莫昔芬 10 mg po bid)至2015-01-20。
第四次复发:2015年1月
患者常规来院复查。
检查:ECT示:全身骨骼显像清晰,骨代谢活跃,见胸骨放射性轻度聚集,其余未见异常。
CT示:胸骨转移瘤可能,双侧胸腔积液(复发)。
治疗:GP方案3周期(注射用盐酸吉西他滨1.4 g,d1、d8联合顺铂100 mg,d1)。
2015-04行阿那曲唑(1 mg po 1/日)治疗。
疗效:双侧胸腔积液消失。
第五次复发:2017年8月
患胸闷气短月余。
检查:CT示:新发胸壁皮肤增厚,双侧胸腔积液量较前明显增多。
超声示:左侧大量胸腔积液(大量),右侧胸腔积液(中等量)。
治疗:行胸腔穿刺置管术,排放胸腔积液双侧各200 ml,给予300 mg卡铂胸腔灌注,紫杉醇240 mg化疗3周期。疗效:患者胸腔积液消失。
卡培他滨(2g bid po )治疗。
第六次复发:2018年9月
患胸痛一周。
查体:胸壁皮肤发红,可触及略隆起于皮肤表面的肿块。
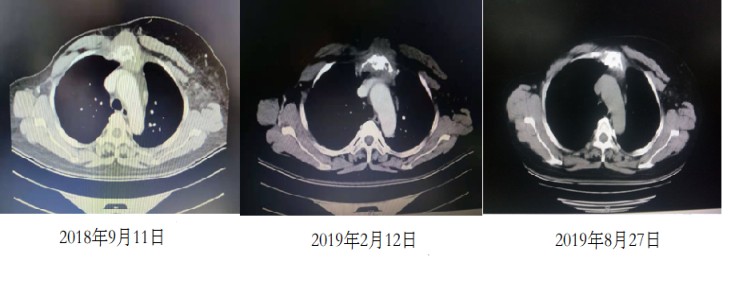
检查:2018-9-11CT示:左乳术后缺如,胸骨及肋骨周围见软组织肿块影。骨窗示:胸骨及右侧部分肋骨骨质破坏。
诊断:左乳癌术后 右乳癌 骨转移 胸壁肿物
治疗:2018-09-11日起氟维司群(0.5g IM) 治疗,首次在d1 、d15、d29予以治疗,之后每28天给予治疗。
疗效:29天疗效:患者胸痛症状消失,胸壁皮肤红肿症状消失,皮肤表面肿块较前减小。
5个月疗效:患者皮肤表面肿块较前进一步减小。2019-02-12CT示:胸骨及肋骨周围软组织肿块影较前缩小,但并未恢复正常,胸骨及肋骨修复性改变。
11个月疗效:患者皮肤表面肿块消失。2019-08-27CT示:胸骨及肋骨周围软组织浸润不明显,胸骨及肋骨修复性改变。
患者目前无进展生存期17个月,尚在观察中。


黑龙江省肿瘤防治研究所所长
黑龙江省教学名师
哈尔滨医科大学附属肿瘤医院副院长
肿瘤学国家重点专科带头人
国家百千万人才工程入选者
国家突出贡献中青年专家
中国抗癌协会淋巴瘤专业委员会候任主任委员
中国抗癌协会化疗专业委员会副主任委员
中国抗癌协会乳腺癌专业委员会常委
中国临床肿瘤学会(CSCO)乳腺癌专家委员会副主任委员
该病例为绝经后的HR阳性晚期乳腺癌患者,经过多线化疗和阿那曲唑内分泌治疗失败后,开始接受氟维司群内分泌治疗长达17个月,综合疗效评价为PR并能继续维持。结合美国NCCN 2019 V3乳腺癌指南和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019)》分析,针对绝经后的HR阳性晚期复发转移型乳腺癌患者,临床医生在诊断治疗过程中需要考虑以下重要因素:
1. 晚期恶性肿瘤:一线治疗方案的选择,很大程度上决定了患者的总体生存
作为生物学行为较为复杂的实体肿瘤,乳腺癌的治疗通常需要经过多线的治疗、才能达到控制疾病的目的。通过综合考虑乳腺癌的复杂生物标记物阳性状态,通常是有多种不同的治疗方案可供选择。那么,选择方案的原则即是首先尽量选取有效率最高、毒性和副作用相对较低、对患者自身伤害较低、且在患者经济条件承受范围内的最好方案,以此作为一线治疗。同时,患者在一线治疗期间的身体状态较好,依从性较佳,更能够从中获益。一线治疗失败以后,肿瘤细胞或者出现耐药性、或者对一线药物的敏感性降低,则将出现肿瘤的复发或进展;此后的二线或者后线治疗,将不得不面对这些经过药物选择压力的、耐药性较强的肿瘤细胞,疗效大打折扣,进而导致患者的总体生存期大大缩减。因此,实体肿瘤的治疗原则,是“好钢用在刀刃上”。
2. HR阳性复发转移型乳腺癌患者:一线氟维司群治疗,有效应答率和患者生存期显著改善
根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019)》推荐,对于复发转移型HR阳性乳腺癌患者接受内分泌治疗,对于既往非甾体类内分泌治疗失败的HR阳性复发转移型乳腺癌,I级推荐为氟维司群或者内分泌治疗(均为IA类证据)。
目前,已有多项三期临床试验证实了氟维司群在晚期复发型乳腺癌患者中的重要角色。既往的FIRST研究显示,氟维司群500 mg能够比阿那曲唑、更能延长晚期乳腺癌患者的总生存期[1]。FIRST研究纳入既往未经治疗的绝经后激素受体阳性、局部晚期或转移性乳腺癌患者,接受氟维司群500 mg(第0,14,28天,此后每28天一次)或阿那曲唑1 mg/日。氟维司群500 mg对比阿那曲唑OS风险比为0.70(P = 0.04),中位OS分别为54.1个月和8.4个月。
但是,FIRST研究的OS分析是在疾病进展时分析后增加的、其原方案并无该计划;此外,也不是所有患者都进入了新增的OS随访。因此,FIRST研究的生存分析具有一定的局限性。于是,更大规模的前瞻性的三期随机对照研究,FALCON研究[2]应运而生。FALCON研究纳入经病理学证实的雌激素受体(ER)和(或)孕激素受体(PR)阳性的局部晚期或转移性乳腺癌患者,以对比氟维司群、阿那曲唑的疗效。结果显示,与阿那曲唑治疗组相比,氟维司群能够显著改善患者PFS,分别为16.6个月对比13.8个月,风险比(HR)为0.797(95%CI 0.637 ~ 0.999;P=0.0486)。
另外,氟维司群还能够作为晚期乳腺癌患者在一线治疗后的维持治疗方案。在2017年的ASCO会议上,来自中山大学肿瘤防治中心的王树森教授作为PI、汇报了FANCY研究的结果[3]。FANCY研究结果显示,适合化疗的HR+/HER2-晚期乳腺癌患者,在一线化疗结束后后、继续氟维司群维持治疗,其临床获益率达到76%,中位PFS为16.1个月,而若从化疗算起,中位PFS为19.5个月,最长PFS近60个月。
由此可见,氟维司群是HR阳性晚期复发型乳腺癌患者的最强内分泌治疗单药,并能通过协同不同药物的作用机制(比如CDK4/6抑制剂)、进一步提高患者的生存获益。其联用方案的疗效,在PALOMA-3 [4] [5]、MONALEESA-3研究[6]、MONALEESA-7[7]研究等中已经得到了有力验证。
该病例为绝经后的HR阳性晚期乳腺癌患者,术后辅助化疗后,出现疾病复发。2019版 CSCO指南推荐内分泌治疗。但是,患者既往接受过来曲唑、阿那曲唑等治疗,无进展生存期较短,难以维持较长的疾病控制期。第六次复发后,患者开始接受氟维司群治疗长达17个月,疗效评估可达到PR并继续维持。在该例患者的多线治疗过程中,六线治疗氟维司群仍能维持患者的长期PFS获益;氟维司群治疗HR阳性晚期乳腺癌患者的显著疗效、由此可见一斑。如果在患者的前线甚至一线治疗过程中即开始氟维司群内分泌治疗、联合或不联合其他作用机制的药物,患者的一线PFS、甚至OS均有望得到延长、获益更为显著,因此内分泌最强单药氟维司群,应当从后线推荐至一线。
[1] Ellis MJ, Llombart-Cussac A, Feltl D et al. Fulvestrant 500 mg Versus Anastrozole 1 mg for the First-Line Treatment of Advanced Breast Cancer: Overall Survival Analysis From the Phase II FIRST Study. JCO 2015; 33(32):3781–3787.
[2] Robertson JFR, Bondarenko IM, Trishkina E et al. Fulvestrant 500 mg versus anastrozole 1 mg for hormone receptor-positive advanced breast cancer (FALCON): an international, randomised, double-blind, phase 3 trial. Lancet 2016; 388(10063):2997–3005.
[3] Wang S, Zheng Q, Xu F et al. Fulvestrant as maintenance therapy after first-line chemotherapy in patients with hormone receptor-positive, HER2-negative advanced breast cancer (FANCY), a prospective, multicenter, single arm phase 2 study. JCO 2017; 35(15_suppl):1066–1066.
[4] Turner NC, Ro J, André F et al. Palbociclib in Hormone-Receptor–Positive Advanced Breast Cancer. New England Journal of Medicine 2015; 373(3):209–219.
[5] Turner NC, Slamon DJ, Ro J et al. Overall Survival with Palbociclib and Fulvestrant in Advanced Breast Cancer. New England Journal of Medicine 2018; 379(20):1926–1936.
[6] Slamon DJ, Neven P, Chia S et al. Phase III Randomized Study of Ribociclib and Fulvestrant in Hormone Receptor–Positive, Human Epidermal Growth Factor Receptor 2–Negative Advanced Breast Cancer: MONALEESA-3. JCO 2018; 36(24):2465–2472.
[7] Im S-A, Lu Y-S, Bardia A et al. Overall Survival with Ribociclib plus Endocrine Therapy in Breast Cancer. New England Journal of Medicine 2019; 381(4):307–316.
排版编辑:肿瘤资讯-frank















 苏公网安备32059002004080号
苏公网安备32059002004080号


