
对于HR+/HER2+的转移性乳腺癌患者,持续抗HER2是基本治疗,联合化疗或内分泌治疗是基本策略。《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019)》建议:对于这部分患者,优先考虑曲妥珠单抗联合化疗,对于部分不适合化疗或进展缓慢的患者如果考虑联合内分泌治疗,可在HER2靶向治疗的基础上联合内分泌治疗。
抗HER2治疗联合内分泌治疗相比于单纯内分泌治疗可以显著提高疗效。本文分享一例HR+/HER2+乳腺癌患者在辅助靶向治疗和内分泌治疗后疾病进展的晚期一线解救治疗,该病例选择抗HER2治疗联合氟维司群内分泌治疗的方案,获得较长时间的疾病缓解。

福建省肿瘤医院 乳腺内科副主任医师
中国抗癌协会乳腺癌专业委员会青年委员
中国医药教育协会乳腺疾病专业委员会委员
中国医师协会乳腺疾病培训专家委员会委员
CSCO药物安全管理委员会委员
福建省医师协会肿瘤内科医师分会常委
福建省抗癌协会肿瘤内科治疗专业委员会委员
基本情况
2015年3月,女性患者51岁,已绝经2年,因“发现右乳腺肿物2月余”于当地医院就诊。既往否认慢性病、传染病、家族病史。
既往手术病史
患者入院后查体:双侧乳房对称,双侧乳头无内陷,无异常分泌物,右乳外上象限可触及一约5cm × 3cm大小肿物,质硬,活动度差,边界不清晰,形态不规则,表皮无红肿触痛。双乳头及左乳无异常,双侧腋窝及锁骨上淋巴结未触及明显异常及肿大。乳腺MR示:右乳外上象限可见一大小约52 mm × 33 mm × 15 mm肿物,BI-RDAS 5类。余肺部CT、骨扫描、血常规、生化、肿瘤标志物等检查未见明显异常。排除明显禁忌后,患者行超声引导下右乳腺肿物穿刺活检术,病理示:浸润性导管癌。免疫组化示:ER(+80%),PR(+10%),HER2(++),Ki-67(+约20%)。
因患者拒绝保乳和术前新辅助化疗,遂于2015年3月在当地医院行右乳癌改良根治术+右侧腋窝淋巴结清扫术,术后病理示:(右乳)IDC,肿瘤大小5.5 cm × 3 cm,组织Ⅱ级,脉管内见癌栓,周边可见导管原位癌成分,各切缘未见癌浸润。腋窝淋巴结见2/15枚癌转移。IHC示:ER(+85%),PR(+10%),HER2(++),Ki-67(+ 25%),FISH提示:HER2扩增。结合患者病史及病理结果,诊断明确为:右侧乳腺浸润性导管癌腋窝淋巴结转移改良根治术后(pT3N1M0 ⅢA期,分子分型:HR+/HER2+)。
患者术后恢复尚可,于2015年5月于日本完成 EC × 4 → TH × 4术后辅化疗及放疗,曲妥珠单抗靶向治疗1年至2016年9月。于2015年10月起口服阿那曲唑内分泌治疗。
第一次疾病进展与一线治疗
患者2017年8月主诉“胸部隐痛2月余”就诊于我院。体检可触及左腋窝淋巴结一枚,大小约2 cm × 3 cm,右前胸壁皮下散在多发结节,最大约0.5 cm × 1 .0 cm。后行PET-CT检查示(图1):①左腋窝多发淋巴结转移,最大径约2 cm × 3 cm;②胸骨体溶骨性破坏伴软组织肿块累及纵隔,高代谢,以上均考虑转移;③右前胸壁皮下散在结节,考虑转移。余血常规、血生化、肿瘤标志物未见异常。结合患者病史行超声引导下左腋窝淋巴结穿刺活检术,病理示:(左腋窝)纤维结缔组织中见低分化腺癌浸润,结合病史,考虑乳腺来源。IHC:ER(+75%),PR(+20%),HER2(++),Ki-67(+40%), FISH提示HER2扩增。无病生存期(disease-free survival,DFS)为29个月。

图1. 患者胸壁复发后PET-CT显像(左:治疗基线,右:4周期治疗后)
患者入院后因疼痛予“胸骨”局部调强放疗DT250CGY/次,总量DT4000cGy/16次/3.2周。患者拒绝化疗,经与患者反复商议,故于2017年8月起一线给予氟维司群 500mg D0,14,28+拉帕替尼1250 mg/日治疗。患者于2018年1月复查PET-CT示:①左腋窝多发淋巴结转移灶较前退缩,代谢减低;②胸骨体转移灶较前退缩,大部分成骨修复,代谢较前减低;③右前胸壁皮下散在结节,代谢较前减低,综合疗效评价为部分缓解(PR),治疗期间多次复查疗效均维持PR。
第二次疾病进展与晚期二线治疗
2018年12月复查PET-CT示:①原胸壁正中皮下高代谢结节消失;②胸骨体转移灶与前相仿,代谢较前略减低;③左侧腋窝转移淋巴结较前增大,代谢较前增高,纵隔高位气管左前新增肿大淋巴结,高代谢,考虑肿瘤转移;④双肺新增多发结节,高代谢,考虑肿瘤转移;⑤右侧髋臼新增高代谢灶,考虑肿瘤转移。结合上述复查结果,综合疗效评价为病情进展(progressive disease,PD),无进展生存期(progression-free survival,PFS)为16个月。2018年12月起至病例征集时间止,给予T-DM1进行晚期二线治疗,最佳疗效评价为PR。
总结
患者为绝经后中老年女性,主因“发现右乳腺肿物2月余”于2015年3月入院。穿刺示:IDC。IHC:ER(+80%),PR(+10%),HER2(++),Ki-67(+约20%),FISH提示:HER2扩增。患者拒绝新辅助化疗及保乳,后行乳腺癌改良根治术,诊断明确为:右侧乳腺浸润性导管癌伴腋窝淋巴结转移(pT3N1M0 ⅢA期,分子分型:HR阳性HER2阳性型)。术后完成EC → TH辅化疗及放疗,曲妥珠单抗靶向治疗1年至2016年9月。并于2015年10月起口服阿那曲唑内分泌治疗。2017年8月提示疾病转移,患者拒绝化疗,晚期一线治疗予以氟维司群联合拉帕替尼,最佳疗效评价为PR,2018年12月,患者病情进展,PFS为16个月。随后予以T-DM1进行晚期二线治疗,最佳疗效评价为PR。
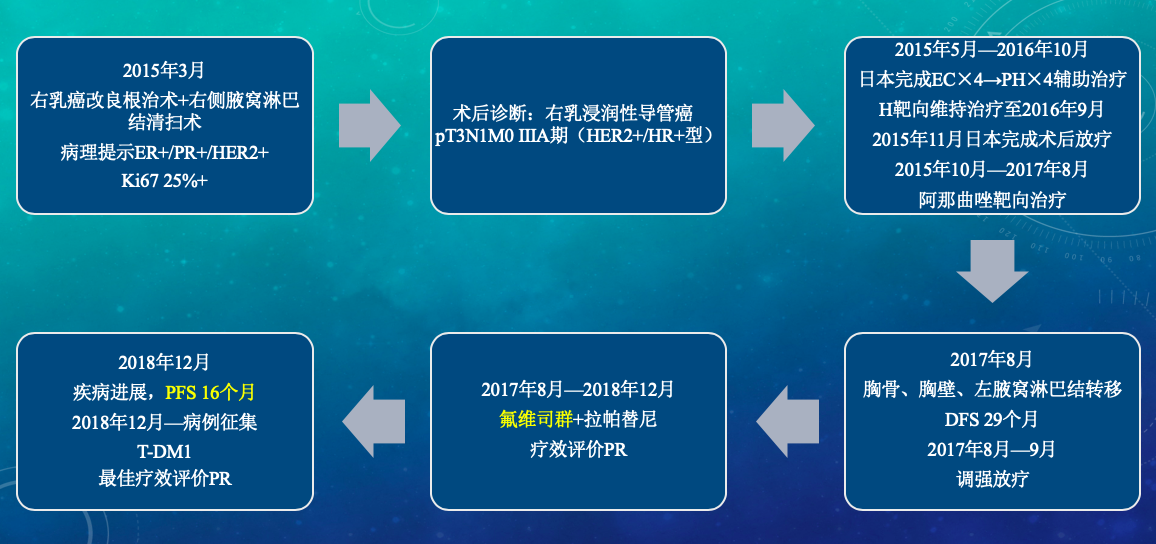
患者诊疗流程图

民进福建省委副主委
福建人大常委会委员
福建省肿瘤医院乳腺内科主任、硕导、省保健委专家
中国医师协会乳腺疾病专家培训委员会副主任委员
中国抗癌协会乳腺癌专业委员会常务委员
中国临床肿瘤学会(CSCO)乳腺癌专业委员会常务委员
国家卫生计生委合理用药专家委员会乳腺肿瘤组委员兼秘书
国家肿瘤质控中心乳腺癌专家委员会委员
中华医学会乳腺学组委员
中华预防医学会乳腺学组委员
福建省医师协会肿瘤内科医师分会主任委员
福建省抗癌协会乳腺癌专业委员会副主任委员
福建省抗癌协会内科治疗专业委员会副主任委员
福建省红十字会大病救助基金监委会副主任
《医学参考(乳腺频道)》常务编委
《JCO中文版乳腺肿瘤专刊》编委
《欧洲肿瘤年鉴中文版(乳腺癌)》编委
《中华内分泌外科杂志》编委
《中华肿瘤防治杂志》编委
《临床肿瘤学杂志》编委
《肿瘤学杂志》编委
《中国肿瘤》编委

福建省肿瘤医院乳腺内科副主任医师
肿瘤学博士
中国抗癌协会乳腺癌专业委员会青年委员
中华医学会肿瘤分会乳腺学组青年委员
中国医药教育协会乳腺疾病专业委员会委员
福建省抗癌协会肿瘤内科专业委员会青年委员
结合国内外指南(2019),该病例有以下几点值得探讨:
(1)内分泌联合抗HER2治疗HR+/HER2+晚期乳腺癌
转移性乳腺癌的治疗,应在遵循国内外指南的基本原则下进行个体化治疗。HER2阳性、激素受体阳性的复发转移乳腺癌患者,抗HER2治疗是基石。早期的H0648g、M77001、US Oncology、CHAT等研究均证实曲妥珠单抗联合化疗作为一线治疗优于单纯化疗,而CLEOPATRA研究则证实曲妥珠+帕妥珠双靶联合紫杉类化疗不但延长PFS(中位PFS延长6.3个月),而且显著延长OS(中位OS延长15.7个月),双靶联合化疗组OS达到目前最长的57.1个月,而且双靶并不增加心脏毒性。基于上述研究,抗HER2靶向联合化疗成为CSCO指南中HR+/HER2+晚期乳腺癌的优选治疗。
但对于不适合化疗,或进展缓慢的患者,或拒绝化疗的患者,也可考虑抗HER2靶向联合内分泌治疗。早期的TAnDEM和EGF30008研究提示抗HER2靶向联合内分泌较单纯内分泌治疗能够提高PFS,但中位PFS延长仅2.5 ~ 5个月,且OS并无改善。对于抗HER2双靶联合内分泌治疗,2016年SABCS公布的PERTAIN研究和2017年ASCO公布ALTERNATIVE研究发现,抗HER2双靶联合内分泌较单靶联合内分泌也能够延长PFS,但ALTERNATIVE研究显示双靶联合内分泌没有延长OS,PERTAIN研究OS数据尚未成熟。
2019年ASCO年会报道了一项真实世界研究【1】,对比了多种方案在HR+/HER2+晚期乳腺癌患者中一线应用的疗效。研究共计入组6234例患者,一线治疗中,3770例(60)接受内分泌治疗±抗HER2治疗,2464例(40%)接受化疗±抗HER2治疗,结果显示内分泌治疗联合抗HER2治疗方案患者获益最为显著,优于单纯内分泌治疗、化疗±抗HER2治疗(表1)。OS结果支持将抗HER2联合内分泌治疗作为HR/HER2 晚期乳腺癌一线治疗的选择。因此,内分泌治疗联合抗HER2治疗也是目前的可选方案之一。
表1. 真实世界研究中HR+/HER2+晚期乳腺癌一线治疗对比

(2)氟维司群一线治疗,给HR+/HER2+晚期乳腺癌患者带来获益
既往临床研究和临床前研究证据证实,HER2通路和ER通路之间存在交互作用,从而介导内分泌治疗和HER2治疗耐药。在HER2+/HR+的转移性乳腺癌中,在芳香化酶抑制剂(AI)基础上联合使用曲妥珠单抗或拉帕替尼,相比于单纯AI治疗可以显著提高疗效。II期PERTAIN研究【2】是将入组的HR+/HER2+乳腺癌患者随机1:1分配接受帕妥珠单抗+曲妥珠单抗+AI或曲妥珠单抗+AI治疗,研究对患者根据辅助内分泌治疗是否耐药进行了分层,结果显示,对于辅助内分泌治疗耐药的患者,AI联合单靶抗HER2治疗的中位PFS为10.86个月。
结合本病例,患者辅助内分泌治疗不到2年、曲妥珠单抗辅助靶向治疗结束不到1年即出现转移,提示患者对内分泌耐药、对曲妥珠单抗耐药。患者拒绝化疗,在晚期一线治疗时选择氟维司群联合单靶抗HER2方案,获得PFS达到16个月。这比临床试验中对辅助内分泌耐药人群选择AI+单靶抗HER2治疗患者的中位PFS显著延长。
对于部分HR+/HER2+晚期乳腺癌,指南也推荐在抗HER2治疗的同时联合内分泌治疗,而大样本真实世界研究亦显示,内分泌联合抗HER2治疗方案优于单纯内分泌治疗、单纯化疗、化疗联合抗HER2治疗。因此,内分泌治疗联合抗HER2治疗是HR+/HER2+晚期乳腺癌的可选方案。而在内分泌治疗方案中,氟维司群作为一类雌激素受体下调剂,不仅可以与雌激素受体竞争性结合,亲和力与雌二醇相似,还可以阻滞受体,抑制雌激素的结合并激发受体发生形态改变,降低ER浓度而杀死肿瘤细胞。既往的FIRST研究【3】、FALCON【4】研究多次证实,氟维司群一线治疗绝经后激素受体阳性晚期乳腺癌的疗效优于AI,奠定了其作为激素受体阳性晚期乳腺癌的一线治疗地位。本例患者为HR+/HER2+乳腺癌,在晚期一线治疗时明确拒绝化疗,但临床氟维司群内分泌治疗联合靶向治疗带来较好的生存获益。
1. Statler Abby, et al. Real-world treatment patterns and outcomes in ER+/PR+/HER2+ metastatic breast cancer (MBC) patients: A National Cancer Database analysis. 2019 ASCO. Abrstract:1033.
2. Rimawi Mothaffar,Ferrero Jean-Marc,de la Haba-Rodriguez Juan et al. First-Line Trastuzumab Plus an Aromatase Inhibitor, With or Without Pertuzumab, in Human Epidermal Growth Factor Receptor 2-Positive and Hormone Receptor-Positive Metastatic or Locally Advanced Breast Cancer (PERTAIN): A Randomized, Open-Label Phase II Trial.[J] .J. Clin. Oncol., 2018, 36: 2826-2835.
3. Ellis M J , Llombart-Cussac A , Feltl D , et al. Fulvestrant 500 mg Versus Anastrozole 1 mg for the First-Line Treatment of Advanced Breast Cancer: Overall Survival Analysis From the Phase II FIRST Study[J]. Journal of Clinical Oncology, 2015:JCO.2015.61.5831.
4. Robertson J F R , Bondarenko I M , Trishkina E , et al. Fulvestrant 500 mg versus anastrozole 1 mg for hormone receptor-positive advanced breast cancer (FALCON): an international, randomised, double-blind, phase 3 trial[J]. The Lancet, 2016:S0140673616323893.











 苏公网安备32059002004080号
苏公网安备32059002004080号


