
摘要TPS601:帕博丽珠单抗与安慰剂对照联合新辅助化疗与辅助内分泌治疗在ER+/HER2−早期、高危乳腺癌患者中的随机、双盲、III期临床试验。
虽然ER+/HER2−乳腺癌相较于其他分子亚型具有更好的总体预后,但其中的高危亚群却具有更高的肿瘤级别、更低的内分泌治疗敏感性、更高的化疗反应性以及更差的预后。基于既往研究结果,新辅助化疗后病理完全缓解(pCR) 比率的提升对ER+/HER2−早期、高危乳腺癌患者的预后具有重要影响。KEYNOTE-756研究(ClinicalTrials.gov、NCT03725059)是一项全球性、随机、双盲、III期临床试验,旨在ER+/HER2−早期、高危乳腺癌患者中,对比观察在新辅助化疗序贯内分泌治疗的基础上加用帕博丽珠单抗的疗效与安全性。
ER+/HER2−、T1c-2c N1-2(肿瘤≥2 cm)或T3-4c N0-2、III级、浸润性导管癌患者根据淋巴结状态的不同(阳性或阴性)、肿瘤组织中PD-L1表达状态的不同(阳性,即联合阳性评分[CPS]≥1或阴性,即CPS<1)、ER阳性比率的不同(ER阳性≥10%或ER阳性<10%)以及蒽环类药物给药计划的不同(每3周或每2周)进行分层,按照1:1随机分组进入新辅助治疗阶段,具体方案为:帕博丽珠单抗200毫克或安慰剂、每3周,联合紫杉醇(80毫克/平米、单周)共四个周期序贯阿霉素(60毫克/平米)或表阿霉素(100毫克/平米)+环磷酰胺(600毫克/平米)、每3周或每2周,共四个周期。在根治性手术(±放疗)之后,患者进入辅助治疗阶段,具体方案为:帕博丽珠单抗200毫克或安慰剂、每3周,共九个周期,联合内分泌治疗。内分泌治疗可延长至10年。在新辅助治疗阶段与辅助治疗阶段之间,患者不会换入另外一组。双重主要终点为pCR比率(定义为:ypT0/Tis ypN0)和无事件生存期(EFS)。次要终点包括全体患者的ypT0/Tis和ypT0 ypN0的pCR比率以及PD-L1阳性患者中的上述三种pCR比率、PD-L1阳性患者的EFS、总生存期、安全性和耐受性以及健康相关生活质量(采用QLQ-C30、QLQ-BR23、EQ-5D-5L调查问卷进行评估)。本临床试验的中期分析已进行规划。患者招募正在进行之中。
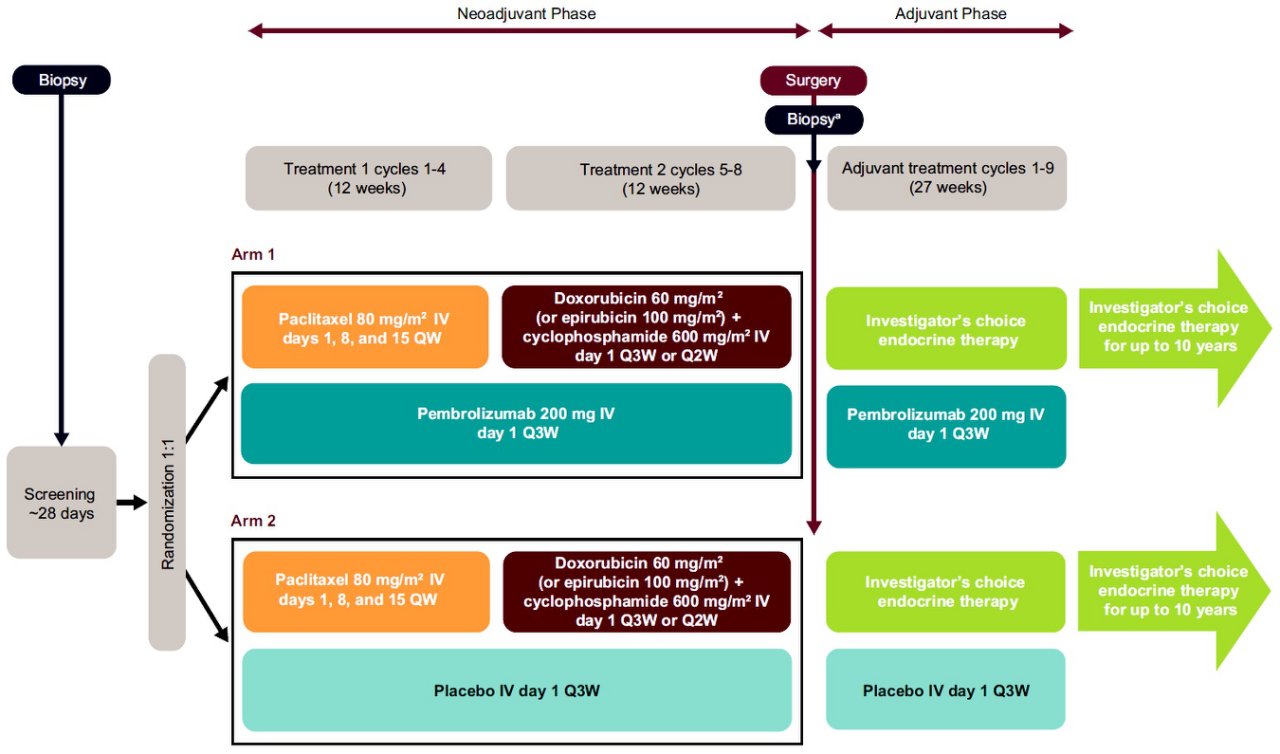
研究设计
本届ASCO大会上,Fatima Cardoso教授做出了有关在ER+/HER2−早期、高危乳腺癌患者中进行帕博丽珠单抗与安慰剂对照联合新辅助化疗与辅助内分泌治疗的随机、双盲、III期临床试验的口头报告。虽然该试验项目尚处于患者招募阶段,尚未产生试验结果,但由于其为默沙东组织开展的全球首个将肿瘤免疫治疗药物PD-1单抗可瑞达应用于ER+/HER2−早期乳腺癌新辅助治疗的临床试验,对未来乳腺癌新辅助治疗策略的制定可能产生重要影响,因而具有潜在的里程碑意义。
一、ER+/HER2−早期、高危乳腺癌治疗新希望,拭目以待
以PD-1单抗为代表的免疫检查点抑制剂通过封闭T细胞表面的PD-1蛋白、关闭PD-1/PD-L1通路而增强自身免疫反应,打破肿瘤免疫逃逸机制,其核心环节为T细胞对肿瘤细胞的杀伤作用[1]。由于化疗、放疗、手术等综合治疗手段均会不可避免地对机体免疫力造成一定程度的打击,从而削弱T细胞的杀伤作用,因此,在乳腺癌患者接受综合治疗的起点进行免疫治疗,有望为患者争取到最佳疗效。因此,如果帕博丽珠单抗能够在ER+/HER2−早期、高危乳腺癌患者接受新辅助化疗和内分泌治疗的基础上进一步提升疗效、达到临床试验的主要终点,将进一步丰富这部分患者的一线治疗方案选择。
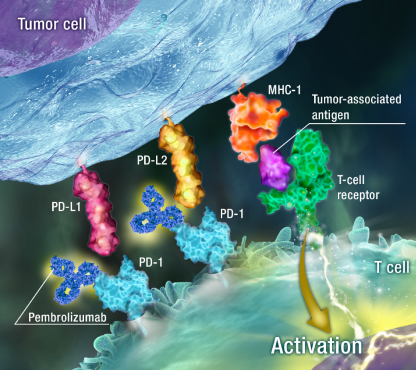
PD-1单抗与PD-1/PD-L1信号通路示意图
二、亦需精准探索获益患者亚群,上下求索
自2000年乳腺癌分子分型提出以来,基因检测结果越来越多地影响着治疗决策[2]。近年来,多家药企已收购了基因检测分析、液体活检公司以完善研发管线。基于NSABP B-14、NSABP B-20研究的回顾性分析和Plan B、TAILORx前瞻性研究结果以及MINDACT试验结果,21-基因中、低危和70-基因低危乳腺癌患者可以豁免化疗[3, 4]。本届ASCO会议亦报道了诸如APHINITY研究的生物标志物分析结果(摘要1012)、95-基因在ER+/HER2−、淋巴结阴性的中危、早期乳腺癌中的应用(摘要542)、TAILORx研究中临床风险与21-基因相结合预测化疗获益(摘要503)等基因检测与临床病理特征相结合的研究。然而,对于高危患者而言,化疗序贯内分泌治疗是否足够?除PD-L1、TILs、MSI等之外,尚有哪些免疫治疗疗效预测指标?免疫治疗获益患者亚群如何精准判定?免疫治疗的最佳时长为多久?同时,欧美国家ER+、淋巴结阴性乳腺癌患者超50%,而我国乳腺癌患者就诊时机偏晚,分子分型情况亦不相同,治疗策略差异很大[5]。希望本次临床试验不但能够给出理想的结果数据,亦能够通过对患者的基因特征进行分析,探寻免疫治疗获益的分子标志物。
三、未来治疗方案选择良多,任重道远
当前,国际、国内多家药企已有PD-1、PD-L1单抗产品进入临床试验或获批上市,但药物适应症尚未涵盖早期乳腺癌,且绝大多数临床试验均在晚期患者中展开,希望未来能够更多地在早期或新辅助免疫治疗患者中开展临床试验,在精细分层的基础之上,最大限度地寻找能够从免疫治疗中获益的患者亚群。同时, 国内外的PARP抑制剂、CDK4/6抑制剂等多种靶向药物已获批乳腺癌相关适应症,加之国家医保政策利好,相信乳腺癌患者将会不断获益。相应地,探寻新型靶向药物更多适应症的临床试验亦亟待开展。乳腺癌精准诊疗,永远在路上。
1. Boussiotis VA. Molecular and Biochemical Aspects of the PD-1 Checkpoint Pathway. N Engl J Med. 2016 Nov 3;375(18):1767-1778.
2. Perou CM, Sørlie T, Eisen MB, van de Rijn M, Jeffrey SS, Rees CA, Pollack JR, Ross DT, Johnsen H, Akslen LA, Fluge O, Pergamenschikov A, Williams C, Zhu SX, Lønning PE, Børresen-Dale AL, Brown PO, Botstein D. Molecular portraits of human breast tumours. Nature. 2000 Aug 17;406(6797):747-52.
3. Sparano JA.et al. Prospective Validation of a 21-Gene Expression Assay in Breast Cancer. N Engl J Med 2015 Nov 19;373(21):2005-14.
4. Cardoso F, van't Veer LJ, Bogaerts J, Slaets L, Viale G, Delaloge S, Pierga JY, Brain E, Causeret S, DeLorenzi M, Glas AM, Golfinopoulos V, Goulioti T, Knox S, Matos E, Meulemans B, Neijenhuis PA, Nitz U, Passalacqua R, Ravdin P, Rubio IT, Saghatchian M, Smilde TJ, Sotiriou C, Stork L, Straehle C, Thomas G, Thompson AM, van der Hoeven JM, Vuylsteke P, Bernards R, Tryfonidis K, Rutgers E, Piccart M; MINDACT Investigators. 70-Gene Signature as an Aid to Treatment Decisions in Early-Stage Breast Cancer. N Engl J Med. 2016 Aug 25;375(8):717-29.
5. Waks AG, Winer EP. Breast Cancer Treatment: A Review. JAMA. 2019 Jan 22;321(3):288-300.











 苏公网安备32059002004080号
苏公网安备32059002004080号


