当地时间2019年5月31日—6月4日,美国临床肿瘤学会(ASCO)年会在芝加哥盛大举行。ASCO年会是世界上规模最大、学术水平最高、最具权威的临床肿瘤学会议。本届年会的主题为“Caring for Every Patient, Learning from Every Patient”。作为年会的重头大戏,免疫治疗再度成为各方关注的焦点。6月2日胃肠道肿瘤的口头摘要专场,来自加州大学洛杉矶分校的Richard S Finn教授汇报了肝癌领域的重磅研究KEYNOTE-240的结果,这一Ⅲ期研究中,帕博利珠单抗用于晚期肝细胞癌(HCC)二线治疗表现出与Ⅱ期KEYNOTE-224研究基本一致的结果,帕博利珠单抗的疗效得到进一步验证。
Abs 4404. III期KEYNOTE-240研究:帕博利珠单抗对比最佳支持治疗用于晚期HCC二线治疗

Richard S Finn教授现场汇报
研究背景
近些年,肝癌的系统性治疗进展迅猛,新药频出,10年前索拉非尼问世并获批肝癌一线治疗,开辟了肝癌靶向治疗新时代,此后,其他靶向新药如一线仑伐替尼、二线瑞戈非尼和卡博替尼纷纷获批,为肝癌内科治疗注入了新的活力。2018年,免疫治疗新药帕博利珠单抗和纳武利尤单抗也获美国FDA批准肝癌二线治疗适应证,为肝癌治疗带来了新的希望。帕博利珠单抗获批是基于开放标签的Ⅱ期单臂研究KEYNOTE-224,该研究纳入104例既往索拉非尼经治的患者,客观缓解率(ORR)达到17%,疾病控制率(DCR)达62%,中位无进展生存(PFS)和总生存(OS)分别达到4.9个月和12.9个月。KEYNOTE-240(NCT02702401)是一项随机、安慰剂对照的Ⅲ期研究,在经治晚期HCC患者中对比帕博利珠单抗和最佳支持治疗,以进一步验证帕博利珠单抗的疗效。
研究方法
研究入组了影像学或病理学确诊的HCC,接受索拉非尼治疗进展或不可耐受,Child-Pugh A级,ECOG PS 0~1分。患者按2∶1随机分配接受帕博利珠单抗200 mg + 最佳支持治疗或安慰剂 + 最佳支持治疗,每3周为1个周期。分层因素包括患者地域来源、大血管侵犯和AFP水平,最多治疗35个周期或直至确认的进展或出现不可耐受的毒性。采用RECIST v1.1标准由中心影像评估委员会每6周进行一次疗效评估。共同主要终点为OS和PFS。次要终点包括ORR、DOR和安全性。数据截止日期分别为:OS 2019年1月2日;PFS和ORR,2018年5月26日。
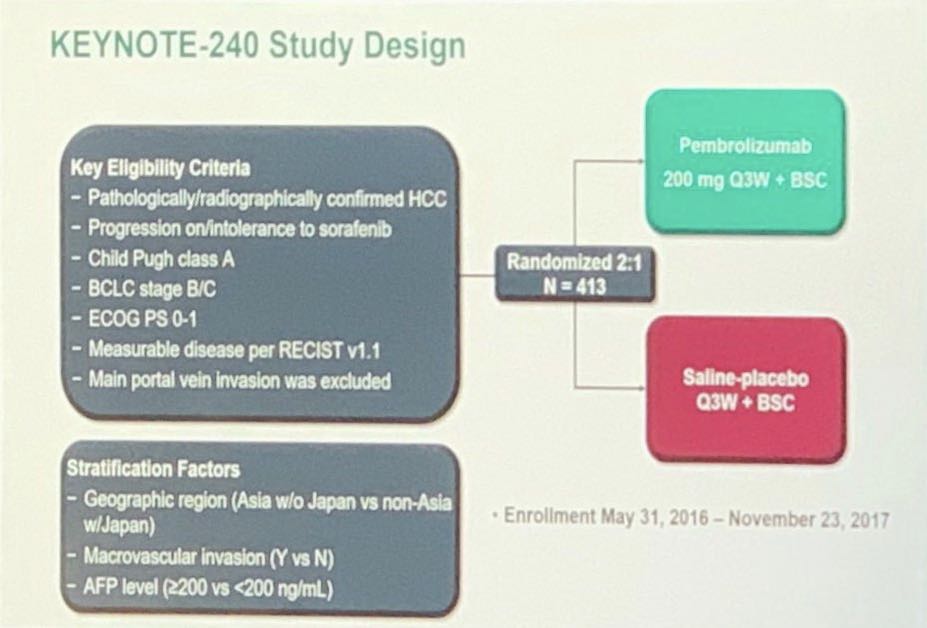
图. KEYNOTE 240研究设计
研究结果
共413例患者参与随机分组,帕博利珠单抗和安慰剂组分别为278例和135例,两组患者的基线特征均衡。在中位随访13.8个月后,帕博利珠单抗和安慰剂组分别有10.1%和3.0%的患者仍在接受治疗。相比于安慰剂,帕博利珠单抗延长了3个月的OS(13.9个月vs 10.6个月,HR,0.78;单侧P = 0.0238),PFS也有改善(HR,0.718;单侧P = 0.0022),可惜的是这一差异未达到既定的显著性水平。OS和PFS亚组分析显示,大多数亚组均观察到帕博利珠单抗治疗更优的趋势。
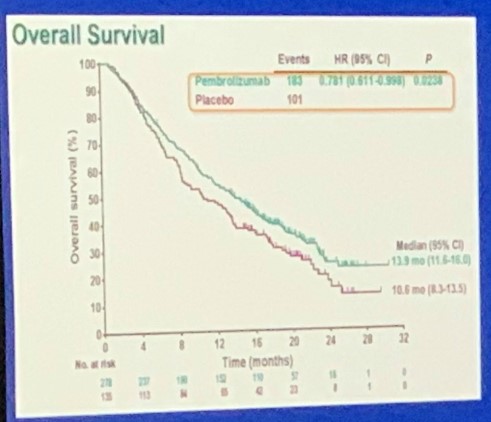
图. 两组的OS对比
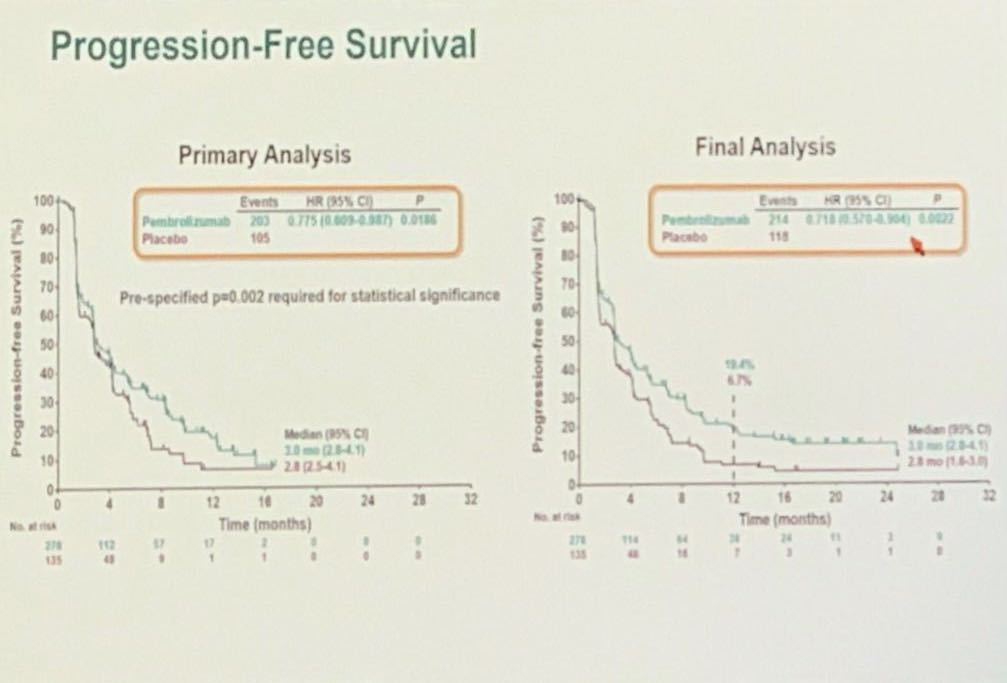
图. 两组的PFS对比
帕博利珠单抗和安慰剂组的ORR分别为18.3%(95% CI,14.0%~23.4%) vs 4.4% (95% CI,1.6%~9.4%),单侧P = 0.00007);帕博利珠单抗组的疗效持久,中位DOR为13.8个月(1.5~23.6+)。
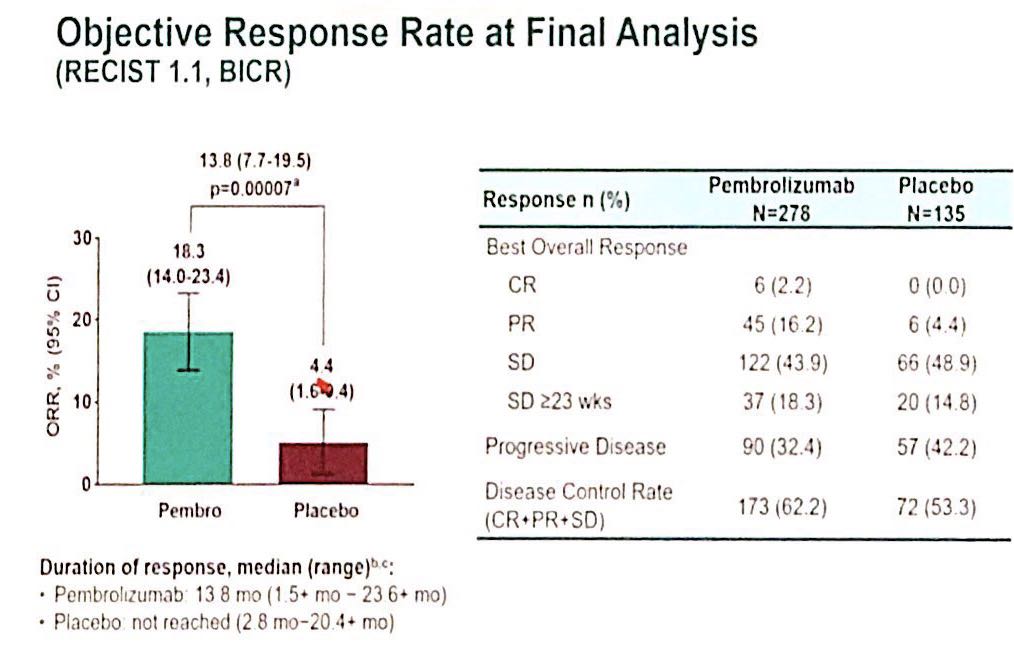
图. 两组的ORR对比
安全性评估方面,肝炎和其他免疫介导的不良事件发生率,帕博利珠单抗组与既往报道相似,未观察到HBV/HCV感染患者出现疾病爆发。帕博利珠单抗组常见的(发生率>15%)不良事件包括AST升高、血胆红素升高、疲劳、瘙痒、转氨酶升高、食欲减低和腹泻,大多数不良事件为1~2级,3级不良事件发生率较低。
进一步对比两组在停止研究药物治疗后的治疗,帕博利珠单抗和安慰剂组分别有41.7%和47.4%的患者接受了后续治疗,其中后续接受免疫治疗的患者比例分别为6.8%和10.4%。敏感性分析评估了后续抗肿瘤治疗对两组患者OS的影响,结果显示,当以开始后续抗肿瘤治疗作为删失数据,帕博利珠单抗组的OS显著优于安慰剂组。
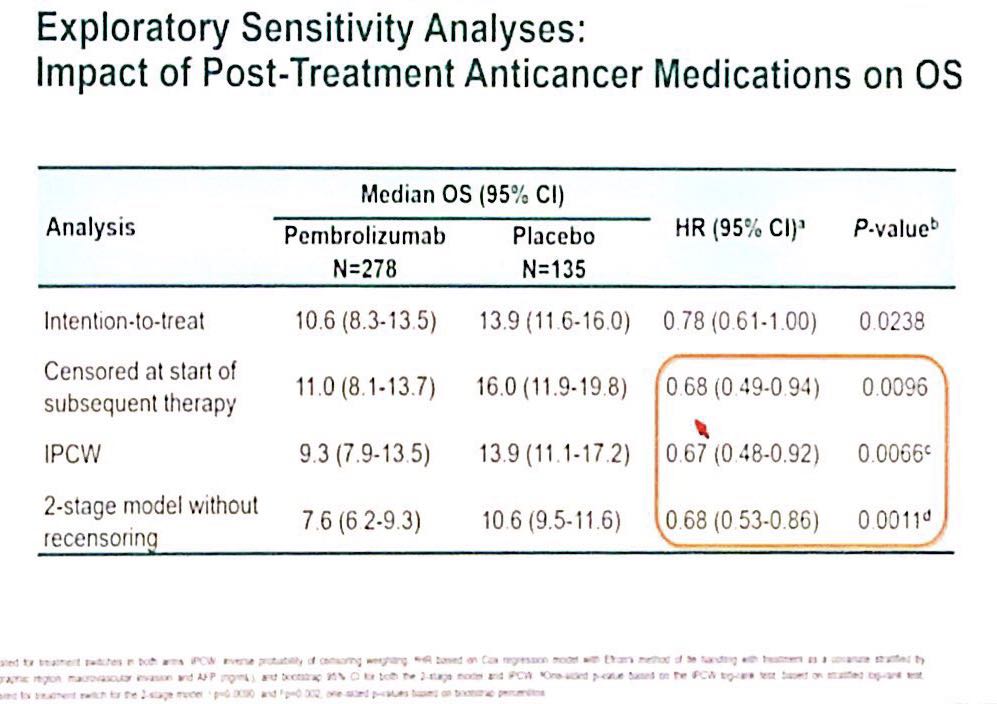
图. 敏感性分析后续抗肿瘤治疗对OS的影响
小结
帕博利珠单抗相比于安慰剂治疗晚期HCC,虽然OS和PFS未达到统计学终点,但与安慰剂相比,治疗组OS和PFS均有所改善:死亡和进展风险均下降22%,95%可信区间高限小于1,提示临床获益。帕博利珠单抗组的ORR与KEYNOTE-224研究报道结果一致,显著高于安慰剂组,且疗效持久。安慰剂组的后续抗肿瘤治疗可能影响了患者的OS结果,帕博利珠单抗的安全性和既往报道的单药安全性相当。这一研究结果与KEYNOTE-224研究的结果总体一致,进一步支持帕博利珠单抗用于晚期HCC二线治疗。
晚期消化道肿瘤的治疗进展——William Proctor Harris教授现场点评
William Proctor Harris教授现场点评
来自华盛顿大学医学院的William Proctor Harris教授对这一研究进行现场点评。基于CheckMate 040研究和KEYNOTE-224研究,美国FDA加速批准了纳武利尤单抗和帕博利珠单抗用于晚期HCC二线治疗。在KEYNOTE-224研究基础上,进一步进行的Ⅲ期KEYNOTE-240研究,虽然OS和PFS未达到统计学意义的既定终点,但是从OS和PFS曲线来看,两组是完全分开的。横向对比既往在晚期HCC二线治疗上进行的Ⅲ期研究,如CELESTIAL研究、RESOURCE研究、REACH-2研究,KEYNOTE-024研究,帕博利珠单抗带来的中位OS最长。
总体而言,KEYNOTE-240研究结果与Ⅱ期研究结果相似,ORR为18.3%,中位DOR为13.8个月,中位OS为13.9个月。Richard S Finn教授也解释道,研究在设计时,对Ⅰ类错误设定了严格的界值,这可能导致统计效能不足。如2次中期分析耗尽了α值,两个共同主要终点导致α值分割。此外,此研究中安慰剂组的生存数据也优于其他研究,这可能是因为研究对入组人群进行了高选择,排除了合并大静脉侵犯的患者;同时,安慰剂组后续有很高比例的患者接受了系统性抗肿瘤治疗(47.4%,包括10.4%的患者接受抗PD-1/L1单抗治疗)。
最后,William Proctor Harris教授对KEYNOTE-240研究作出如下评论:
1. 虽然研究未达到既定的疗效界值,但帕博利珠单抗对比安慰剂显示出很强的OS和PFS获益趋势。
2. 帕博利珠单抗用于晚期HCC二线治疗,取得了较好的ORR,较长的疗效持续时间,且安全性较优,是非常具有临床实际意义的。在今后的临床实践中,将会继续推荐PD-1单抗用于晚期HCC二线治疗,尤其是那些对TKI耐受性较差的患者。
3. 未来进行相关的研究设计时,研究者应该考虑到患者的三线治疗,重新进行统计学假设;同时需要进行新的免疫治疗研究,期望观察到长尾现象。
4. 关于FDA对帕博利珠单抗加速获批用于晚期HCC的适应证,建议继续保持,FDA应该认真考虑这一研究敏感性分析的结果,同时等待KEYNTOE-394研究的结果。
周俭教授点评

国家杰出青年科学基金获得者
教育部长江学者特聘教授
国家“万人计划”科技创新领军人才
国家卫计委有突出贡献中青年专家
科技部“肝癌转移复发精准医学研究”创新团队负责人
上海市领军人才,优秀学科带头人
复旦大学附属中山医院副院长兼徐汇区中心医院院长
复旦大学肝癌研究所副所长,肝外科主任
上海市肝病研究所副所长
中国抗癌协会肝癌专业委员会主任委员
中华医学会肿瘤学分会副主任委员
中国免疫学会移植免疫分会副主任委员
中国医师协会外科医师分会肝脏外科医师委员会副主任委员
上海市医学会肿瘤专科分会候任主任委员等
我国肝癌发病率高,发病例数约占全球总例数的一半以上。与其他瘤种相比,肝癌的治疗效果较差,一直是肿瘤治疗中的难点。近几年,在肝癌的免疫治疗上,国内外开展了很多重要的研究,基于CheckMate 040和KEYNOTE-224研究的结果,纳武利尤单抗和帕博利珠单抗获批用于晚期HCC的二线治疗,并被列入《CSCO原发性肝癌诊疗指南》推荐,相信也会被纳入今年即将公布修订的国家卫健委《原发性肝癌诊疗规范》2019版中的二线治疗药物中。此次ASCO大会公布了KEYNOTE-240研究的结果,ORR达到18.3%(KEYNOTE-224 ORR为17%),与KEYNOTE-224研究结果基本一致,显示出帕博利珠单抗用于晚期肝癌二线治疗的获益,也再次验证了PD-1单药二线治疗肝癌的疗效。
从既往的临床研究和实践中,可以感受到帕博利珠单抗对于肝癌患者是有明显临床获益的,KEYNOTE-224研究的结果也很好地说明了这一点,虽然很遗憾这次KEYNOTE-240研究在OS、PFS上没有达到统计学终点,但是从具体研究结果来看,死亡和进展风险均下降22%,95%可信区间高限均小于1,ORR达到18.3%,DOR也体现了免疫治疗疗效维持时间长的优势,因此临床获益还是很明显的。而未达到统计学终点的原因可能有如下几点:第一,在研究设计之初,当时并没有标准的肝癌后线治疗方法,然而近年来肝癌新药不断涌现,在停止研究药物治疗后,安慰剂组有接近一半的患者接受了后续治疗,后续抗肿瘤治疗的应用会稀释两组之间的OS差异;第二,KEYNOTE- 240研究采用OS和PFS双统计学终点设计,而且进行2次中期分析,这对于P值的要求更高;第三,接受二线治疗的晚期肝癌患者通常全身状况较差,因此对于免疫治疗的临床获益可能小于一线治疗。此次KEYNOTE-240的研究结果也提示我们对于Ⅲ期临床研究的设计要更加谨慎,尤其是在当今新的治疗手段不断涌现,后续治疗的影响等因素都要在研究设计之初进行充分的预测和考量。
另外值得注意的是,东西方肝癌患者在发病原因、流行病学特征、分子生物学行为、临床表现和分期上具有高度异质性,KEYNOTE-240研究未纳入中国人群,而目前针对中国肝癌患者的KEYNOTE-394研究正在进行中,也是目前唯一一项免疫治疗用于肝癌二线治疗的Ⅲ期临床研究,结果值得期待。
目前,除了免疫单药用于晚期肝癌二线治疗以外,免疫联合治疗在晚期肝癌一线治疗中也进行了大量探索,这一治疗模式将是未来的趋势。其中 2018年ASCO会议上公布的帕博利珠单抗联合仑伐替尼用于晚期肝癌一线治疗的Ⅰb期研究,结果令人振奋。在纳入疗效分析的26例患者中,1例完全缓解,10例部分缓解,15例疾病稳定,ORR达到42.3%,DCR达100%,PFS达到9.69个月。众所周知,中晚期肝癌的5年生存率很低,大部分患者在2年左右复发,最终走向生命终点。因此,保持疾病稳定对于延长生存期意义重大。更为可喜的是2019年AACR又对这一研究数据进行了更新,相比于2018年ASCO大会上公布的数据,研究者评价取得客观缓解的患者从11例增加到13例,独立评估委员会按mRECIST标准评价达到完全缓解的患者有3例,部分缓解15例,ORR高达60%,DCR 为93.3%。该结果展现了免疫联合治疗非常有希望的前景。最近,仑伐替尼联合帕博利珠单抗治疗晚期HCC的全球Ⅲ期临床试验LEAP-002已经启动,我国约有20个临床研究中心参与了这项研究,结果值得期待。











 苏公网安备32059002004080号
苏公网安备32059002004080号


