作者单位:中山大学附属肿瘤医院
时光易逝,岁月难留。转眼间2018年末已至,回眸岁月,往事悠悠。这一年,淋巴瘤领域取得了哪些重磅研究进展呢?【肿瘤资讯】特邀中山大学附属肿瘤医院的黄慧强教授,针对淋巴瘤在这一年内取得的重磅研究成果,为我们作了精彩盘点,详情如下。

中山大学附属肿瘤医院大内科副主任
中国抗癌协会淋巴瘤专业委员会常委
中国抗癌协会淋巴瘤专业委员会青年委员会 主委
CSCO中国淋巴瘤联盟副主席
广东省抗癌协会血液肿瘤专业委员会主委
广东省抗癌协会淋巴瘤专业委员会副主委
精准医疗时代:弥漫性大B细胞淋巴瘤“里程碑式的研究”─精准分类
弥漫性大B细胞淋巴瘤(diffuse large B-cell lymphoma,DLBCL)根据其细胞来源将过往可分为生发中心来源B细胞样(GCB)、活化B细胞样(ABC)及未能确定细胞来源三种类型,而不同亚型DLBCL的远期预后存在差异,同种亚型的预后也存在着差异。
2018年4月发表于《新英格兰医学杂志》的文章中[1],美国的部分科学家联合加拿大、德国部分科学家对DLBCL 复杂的分子生物学特征进行了梳理,并为未来找出新的治疗方法指明了方向。他们对574份肿瘤样本进行外显子测序及转录组测序、基于芯片技术的DNA拷贝数分析、有针对性的扩增子测序等方法对372个基因进行了分析。结果确定了BN2、EZB两种治疗效果好的基因分型和MCD、N1两种治疗效果差的基因分型。研究人员发现,4种基因分型在弥漫性大B细胞淋巴瘤过去两种分类中都能发现。研究负责人路易斯·施托德解释说,肿瘤可能既属于预后较差的“活化B细胞样型”,同时又拥有BN2基因分型,而后者的预后较好。这一分类解释了三分类时某一分类内患者的预后的差异,以及对R-CHOP治疗效果差异的原因。这一分子分类将在DLBCL患者的预后预测、治疗方案筛选方面发挥重要作用,并指引未来的研究方向。
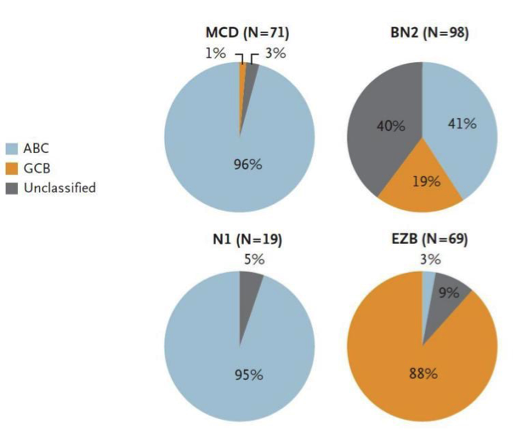
今年5月,《Nature Medicine》杂志[2]发表了另外一项关于DLBCL分子亚型的研究。研究人员对304例DLBCL患者整合基因组分析,定义了5个不同的DLBCL子集: 具有外滤泡、可能边缘区起源、预后好的ABC-DLBCL(C1);具有TP53双等位基因失活、921.3/CDKN2A缺失和相关基因组不稳定性并独立于COO(C2) ;具有BCL2 结构变异、PTEN和表观遗传学酶改变的预后不良的GCB-DLBCL(C3);具有BCR/PI3K、JAK/STAT和BRAF通路和多个组蛋白改变的预后好的GCB-DLBCL (C4);具有CD79B, MYD88, TBL1XR1 等突变以原发睾丸和原发中枢为代表的结外ABC-DLBCL(C5)。新特征亚群的遗传特征、突变特征和已识别改变的时间顺序为DLBCL的发病机制提供了新的见解。遗传特征独立于临床国际预后评分系统(IPI),提出新的可能的联合治疗策略。

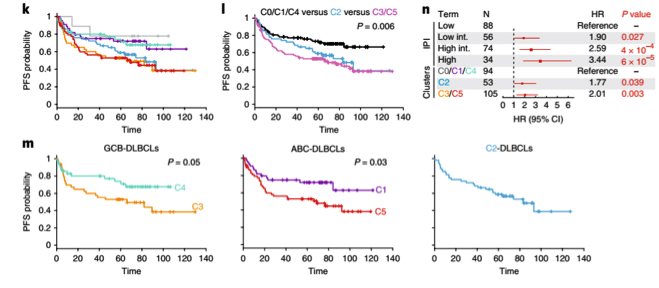
尽管两篇文章同在R-CHOP治疗时代,分别将DLBCL分为4种和5种亚型,但本质是相似的。导致结果一些区别原因是采用的检测方法有所区别,从而导致其亚型的名称不一样,同时也体现了DLBCL的强异质性。这两项研究主要建立在DLBCL全基因组测序结果上进行的遗传学特点分析,对未来DLBCL的预后精准判断和精准治疗临床研究指明方向,值得进一步深入研究。
一线弥漫大B细胞淋巴瘤治疗新突破(PHOENIX研究)
R-CHOP方案是治疗弥漫性大B细胞淋巴瘤(DLBCL)的金标准。虽然R-CHOP方案改善了整体生存,但高危患者5年总生存仍不及50%,尤其是非GCB型,预后仍不理想。近年来,众多创新药在DLBCL治疗的研究中却纷纷以失败告终。
PHOENIX研究为一项随机对照研究,共纳入838例非GCB型弥漫大B细胞淋巴瘤(DLBCL)患者,按照1:1比例进行分组,分别接受伊布替尼(Ibr, 560mg/d)+R-CHOP方案(n=419)、安慰剂+ R-CHOP方案(n=419)治疗(21天为1周期,共6~8周期)。 2018年ASH会议[3]报道了中位随访34.8月的结果。伊布替尼+R-CHOP方案可明显改善年龄<65岁的非GCB型DLBCL患者的EFS(HR=0.702,风险下降30%)、PFS(HR=0.671,风险下降33%)和OS(HR=0.573,风险下降43%),并且EFS/PFS/OS的生存获益在ABC型的亚组患者中同样存在。在安全性方面,全组≥3级的不良反应(AEs)发生率两组基本无明显差异,分别为89.9%(伊布替尼+R-CHOP方案)vs 87.1%(安慰剂+ R-CHOP方案),严重不良反应(SAE)分别为53.1% vs 34%,尽管伊布替尼的加入并未改善年龄≥65岁患者生存,但在年轻患者中为久未突破的DLBCL领域带来一线曙光。
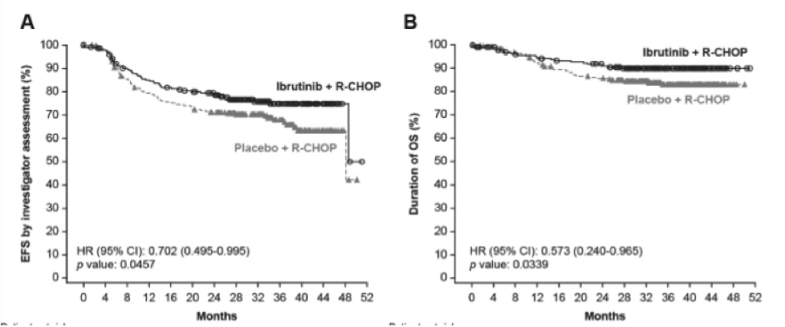
PD-1单抗之后的明日之星:CD47抗体
CD47广泛地表达在正常细胞的表面,避免正常细胞被免疫系统清除。肿瘤细胞表秒表达更高水平的CD47从而导致免疫系统无法识别及清除肿瘤细胞。PD-1单抗、CTLA-4单抗等免疫检查点抑制剂仅对一小部分恶性肿瘤发挥作用的一个重要的原因是无法形成肿瘤特异性的T细胞启动点。然而,CD47抗体可以介导CD8+T对肿瘤的特异性杀伤作用,从而“更好地唤醒免疫系统”。CD47抗体是巨噬细胞免疫检查点抑制剂,可阻断CD47,其诱导肿瘤细胞吞噬作用。与利妥昔单抗具有协同作用,通过增强巨噬细胞介导的抗体依赖性细胞吞噬作用来消除B细胞非霍奇金淋巴瘤细胞
2018年11月新英格兰杂志[4]公布了5F9 (抗CD47单克隆抗体)联合利妥昔单抗在复发/难治性DLBCL和FL的临床1b/2期结果。1b 期试验入组22 例患者(15例DLBCL,7例FL)。患者既往接受过中位4线治疗。在所有 22 名可评估患者中,数据显示客观缓解率(ORR)为 50%,完全缓解率(CR)为 36%。其中,在DLBCL中,ORR达到了40%,CR达到了33%;在FL中,ORR达到了71%,CR达到了43%。DLBCL患者中位随访6.2个月,滤泡性淋巴瘤患者中位随访8.1个月,91%患者持续获益。5F9普遍耐受良好,常见不良反应为1级或2级,最常见的毒性贫血和输液反应,均为可逆性。
Hu5F9-G4,作为一种潜在的新型免疫疗法,其试验结果相当令人鼓舞。这是第一个抗体可以激活巨噬细胞去对抗癌症,未来疗效值得期待。
Pembrolizumab,治疗原发性纵膈B细胞淋巴瘤疗效独特
原发性纵膈B细胞淋巴瘤(PMBCL)总体预后良好,但对于难治复发PMBCL预后并不不理想,2年OS仅为20-30%。
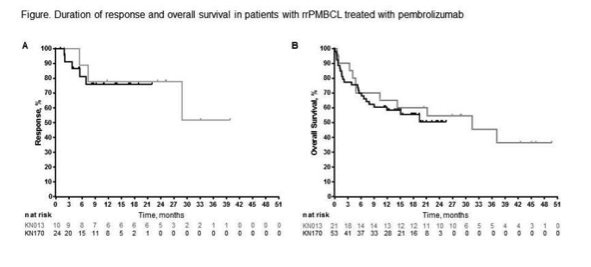
在一项多中心、开放标签、单臂临床研究KEYNOTE-170中[5]。入组了53例复发性或难治性PMBCL。患者接受每3周一次200mg剂量pembrolizumab治疗,直至病情进展或不可接受的毒性。全组患者既往已接受过化疗方案中位数为3(范围:2-8)。36%为原发性难治性疾病,49%为复发性且对前一次治疗难治,15%未治疗复发。26%患者之前接受自体造血干细胞移植,32%接受了放射治疗。所有患者均接受了利妥昔单抗的一线治疗。研究的主要疗效指标是总缓解率(ORR)以及缓解持续时间(DOR)。中位随访9.7个月的数据显示,ORR为45%(24例,95%CI:32-60),CR11%,24例获得缓解的患者中,中位DOR尚未达到(1.1-19.2+月),获得缓解的中位时间为2.8个月(2.1-8.5月)。26%的患者出现严重不良反应,包括心律失常(4%)、心包填塞(2%)、心肌梗死(2%)、心包积液(2%)和心包炎(2%)。基于上述研究结果,2018年6月18日FDA批准pembrolizumab治疗难治复发纵膈大B细胞淋巴瘤。
这项研究提示,对于那些经历过大量、多次化疗的难治复发PMBCL患者来说,pembrolizumab提供了一个很好的治疗选择,其潜在的治疗效果和可以接受的不良反应值得我们持续关注。
2018年ASH会议[6]报道了KEYNOTE-013和KEYNOTE-170延长随访的结果。两项研究进一步确立了pembrolizumab在难治复发PML的作用,缓解时间长,安全性满意。
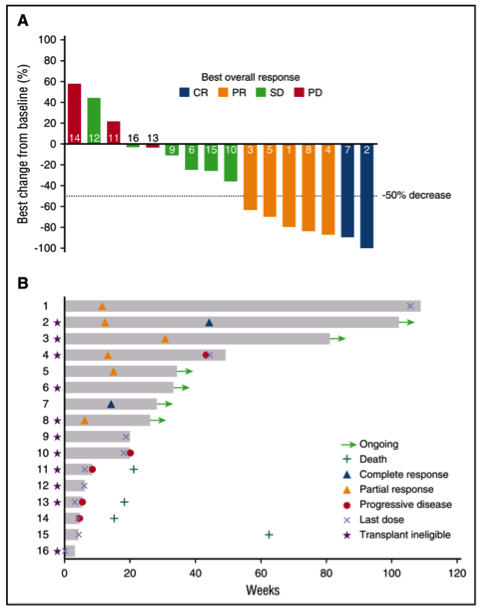
液体活检更上一层楼:血液ctDNA水平或可预测DLBCL早期治疗疗效
2016年,斯坦福大学医学院的研究人员在《 Science Translational Medicine》杂志中表示,对淋巴瘤患者血液循环肿瘤DNA (ctDNA)进行测序,可以确定淋巴瘤细胞的起源,预测预后。
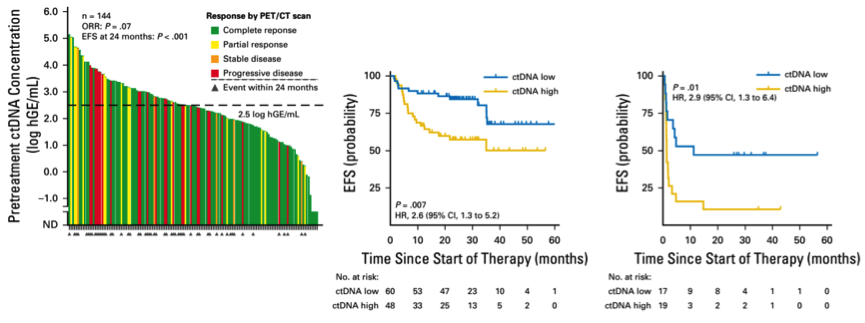
2018年10月在《J Clin Oncol》杂志[7]上的一项最新研究发现, ctDNA水平可成功预测DLBCL患者对初始治疗的反应。尽管大多数DLBCL患者可以治愈,仍有10%DLBCL患者对一线治疗无效,在该项研究中,研究者通过追踪患者血液中ctDNA水平,在治疗开始后的21天内即可预测出无效患者。该项研究共纳入了6个治疗中心的217例DLBCL患者,研究者采用深度测序的肿瘤个性化分析技术在治疗过程中对早期ctDNA动态进行了深入分析,定义了ctDNA变化预测结局的最佳阈值:1个疗程后ctDNA水平降低100倍(早期分子反应[EMR]),2个疗程后ctDNA水平降低200倍(主要分子反应[MMR])。接受一线化疗并达到EMR或MMR的患者24个月结局良好(EMR:无事件生存,83% vs 50%;MMR:无事件生存,82% vs 46%)。EMR还预测了该队列中接受挽救治疗患者24个月的结局(无事件生存,100% vs 13%)。研究结果在第二个验证队列中更进一步验证了EMR和MMR的预后价值。
这项研究结果再次证实了实时追踪ctDNA变化的价值,治疗前ctDNA水平和分子反应是侵袭性淋巴瘤结局的独立预后指标,未来,该项检测技术有望临床用于预测DLBCL患者接受治疗后的疗效评估,
愈发成熟: CAR-T治疗复发难治DLBCL长期随访结果
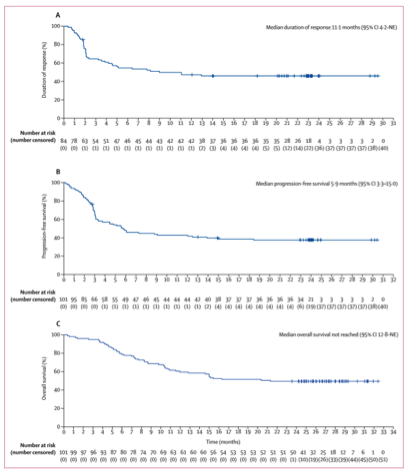
ZUMA-1研究入选111例至少接受过二线以上治疗的患者,其中101例成功接受了axicabtagene ciloleucel治疗。中位随访15.4个月,58%的患者继续保持完全缓解,ORR率82%。2018年11月Lancet Oncol杂志[8]公布了ZUMA-1研究中位随访27.1月的结果,ORR率83%,CR率58%,中位缓解时间11.1月(4.2-未达到),中位OS未达到(12.8-未达到),中位PFS为5.9月(3.3-15月)。常见的3/4级的副作用是:细胞因子释放综合征(CRS)发生率为11%,神经系统毒性32%。中位随访15.4个月时,2例患者死于神经系统毒性。本次随访没有出现新的治疗相关死亡。
另外,在今年ASH会议上[9]Loretta J. Nastoupil教授分享了Axicabtagene Ciloleucel治疗难治复发DLBCL真实世界的数据。截止2018年6月30日,17家美国独立学术中心的211例患者接受了治疗,其中安全性可评估的患者为163例,3级CRS和神经毒性发生率分别为7%和31%,无治疗相关死亡,中位住院时间为14天。疗效可评估的患者为112例,总有效率(ORR)为79%, CR 50%,SD为6%,PD为14%。第100天可评估的39例患者中,59%的患者仍具有持续缓解(CR 49%,PR 10%)。
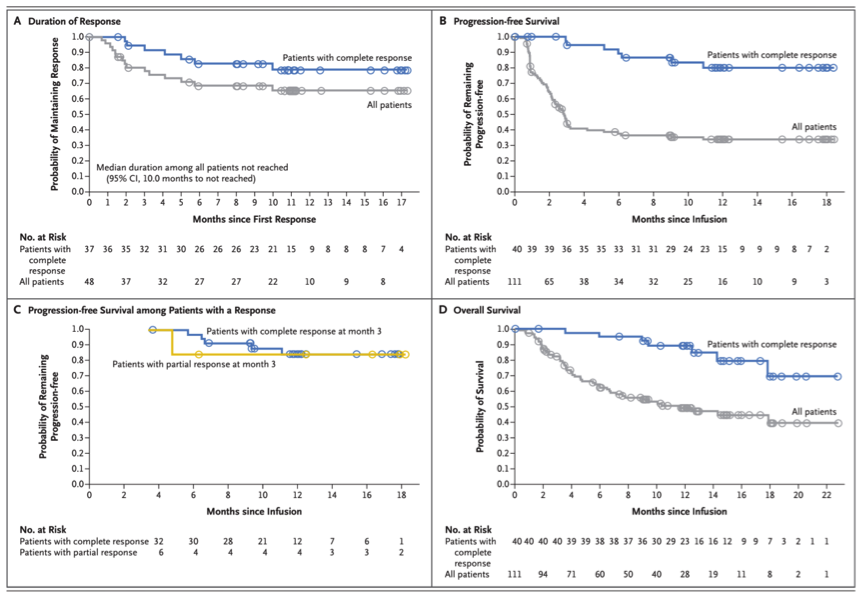
JULIET研究入组144名患者入选,99名患者接受了tisagenlecleucel治疗。中位随访28.6个月,治疗3个月时ORR率50%,治疗后6个月43%患者获得CR。2017年ASH会议报道了81例美国患者的疗效。其结果显示:治疗后6个月,OR率37%,CR率为30%。2018年12月新英格兰杂志[10]公布了长期随访结果。总共93名患者可进行疗效评估。输注至数据截止的中位时间为14个月(0.1~26月)。ORR率为52%,40%患者获得CR。有效患者治疗后12个月的无复发生存率估计为65%(CR患者为79%)。值得注意的是,在最初有部分缓解患者中,有54%最终获得CR,这表明CAR-T可持续存在并且随着时间推移在体内保持活性。毒性方面,最常见的3/4级不良反应包括CRS(22%)、神经事件(12%)、持续28天以上的细胞减少症(32%)、感染(20%)和发热性中性粒细胞减少症(14%)。三例患者在输液后30天内死于疾病进展,无治疗相关死亡。
Flyer研究:预后良好的年轻初治DLBCL可减少化疗
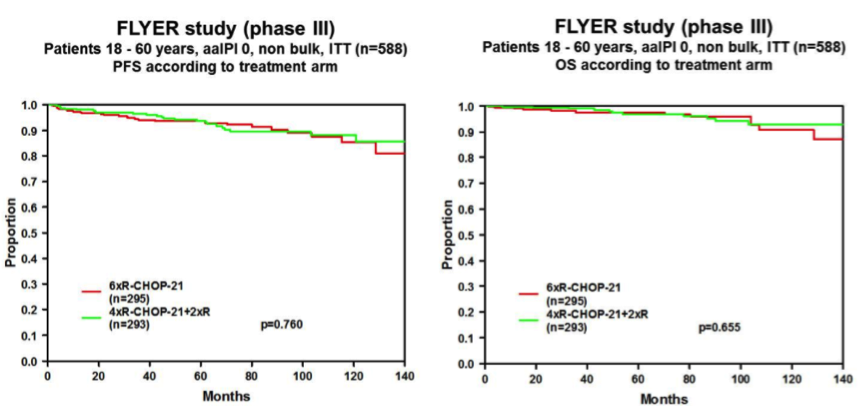
对于预后良好的DLBCL年轻患者,标准疗法为6个疗程R-CHOP方案,21天为一疗程。居于过往的研究结果,德国FLYER研究[11]首次在高询证医学水平的临床研究中探讨减少化疗的可行性。研究对比R-CHOP×6 vs R-CHOP×4+R×2在年轻低危DLBCL中疗效差异。研究入组592例18-60岁低危(aaIPI=0,不伴大包块≥7.5cm)初治DLBCL患者,随机分组至6个疗程R-CHOP组及4个疗程R-CHOP+2疗程R组,中位观察时间为66个月,3年PFS为96% vs 94%(P=0.760)、3年EFS均为89%,3年OS为99% vs 98%;且两组复发率无明显差异。4疗程R-CHOP方案组相比6疗程R-CHOP方案组报告的血液学事件更少,因此,现阶段年轻低危初治DLBCL患者中,R-CHOP×4+R×2是新的标准治疗方案。
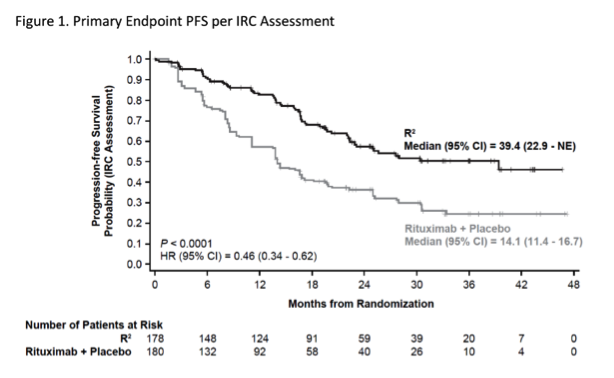
AUGMENT研究:来那度胺 + 利妥昔单抗(R2)显著改善复发惰性淋巴瘤远期生存
2018年ASH会议[12]上公布了3期临床试验AUGMENT中的随访结果。AUGMENT是一项多中心、双盲、随机3期研究,针对曾接受过至少一次全身治疗的FL和MZL、出现疾病复发或难治,但对利妥昔单抗仍有效。研究按照1:1的比例被随机分配,接受R2组或利妥昔单抗治疗组达一年。该研究的主要终点为由独立评审委员会(IRC)评估的无进展生存期(PFS)。结果显示,R2组的中位PFS为39.4个月,而但利妥昔单抗组的中位PFS只有14.1个月。该联合治疗使疾病进展或死亡风险降低了54%。在R2组中,有更多患者对治疗有效,ORR达到78%,而利妥昔单抗组为53%。CR在两组中的结果分别为34%和18%。中位DOR的结果分别为36.6个月和21.7个月。结果表明,Lenalidomide 联合Rituximab (R2)有望作为这类患者有效的Chemo-free方案,发挥重要作用。
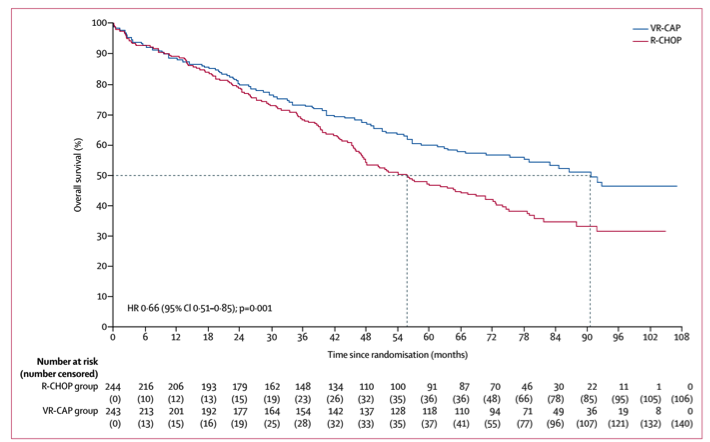
LYM-3002研究长期随访结果:Bortezomib明显提高R-CHOP初治不适合自体移植的套细胞淋巴瘤患者的OS
LYM-3002研究是由瑞士Cavalli教授牵头,包括我国多家医院参加的一项针对套细胞淋巴瘤一线治疗的III期临床试验。该研究为一项随机、开放、多中心研究,目的是对比R-CHOP和VR-CAP(硼替佐米、利妥昔单抗、环磷酰胺,多柔比星、泼尼松联合长春新碱)方案在初治II-IV期,ECOG评分≤2且选择不适合干细胞移植的套细胞淋巴瘤患者中的疗效和安全性。其疗效评估由独立的放射学审核委员会(IRC)完成,主要终点是无进展生存(PFS),次要终点ORR、CR、TTP、OS及不良事件。总共487例患者人组该研究,其中R-CHOP组244例,VR-CAP组243例;中位疗程数6个,中位随访期40个月,VR-CAP组中位PFS为24.7个月,而R-CHOP组仅为14.4个月,由硼替佐米替代长春新碱后,PFS率提高了59%。亚组分析结果显示,无论是性别、人种、分期、乳酸脱氢酶(LDH)、年龄及体质状况分层均提示VR-CAP组明显优于R-CHOP组。但OS数据尚未成熟,VR-CAP组患者的生存期有延长趋势。在安全性方面,VR-CAP组患者的不良反应有所增加,但均可控制。
Ghielmini教授在2018年EMSO会议[13]上报道了LYM-3002研究最终OS的结果。经过82个月的中位随访(出现241个事件:VR-CAP,42%,R-CHOP,57%),VR-CAP方案较R-CHOP方案提高了中位OS约3年(两组中位OS分别为90.7月和55.7月,HR 0.66[0.51;0.85];P=0.001)。与R-CHOP (n = 151; 62%),方案相比,接受VR-CAP方案治疗的患者较少(n=104;43%)需要后续治疗。20例患者出现第二原发肿瘤。268例患者(VR CAP:140例;R CHOP:128例)进入安全性随访。除了3次不良事件(VR-CAP:4级肺腺癌和4级胃癌各一例;R-CHOP:1例2级肺炎)外, VR-CAP和R-CHOP组分别有3例和5例患者发生致死性结果。
在初治不适合移植的MCL患者中,在无Rituximab的维持下,VR-CAP方案显示出明显优于R-CHOP方案的远期生存,且耐受良好。
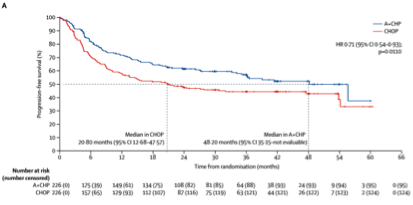
Brentuximab Vedotin两周获批!FDA批准首个外周T细胞淋巴瘤一线治疗新药
化疗仍是目前PTCL治疗的基础,但是PTCL的疗效及预后难以令人满意,因此,新型药物是未来改善PTCL生存的研究方向。
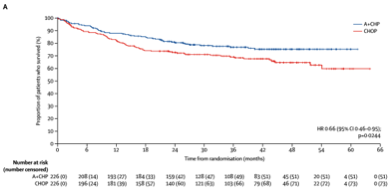
今年ASH会议上[14],ECHELON-2研究的获得了PTCL治疗的重大进展。ECHELON-2是一项3期的双盲、随机、对照的研究。患者来自17个国家的132个研究机构,筛选患者为未接受过治疗的CD30阳性外周T细胞淋巴瘤患者,按照1:1的比例随机分入A+CHP组或CHOP组,每21天为一个周期,治疗6或8个周期。2013年1月24日至2016年11月7日,对601名患者进行了评估,最终452名患者成功入组。2018年12月3日,Lancet杂志在线发表了ECHELON-2试验的结果。两组ORR率分别为72% vs 83%(P=0.003)、CR分别为56% vs 68%(P=0.007)。中位随访35.2月,两组中位PFS分别是20.8月vs 48.2月(HR=0.71,P=0.011)。中位随访42.1个月后,两组均未达到中位OS(分别为69.1%和76.8%)两组的不良事件的发生率和严重程度相似,包括发热性中性粒细胞减少(A+CHP组:18%,CHOP组:15%)和周围神经病变(A+CHP组117:52%,CHOP组:55%)。A+CHP组7名(3%)患者、CHOP组9名(4%)患者出现严重不良事件。
ECHELON-2试验的结果表明,Brentuximab Vedotin联合CHP方案(A+CHP)实现了CD30阳性PTCL治疗的重大突破。正是基于该研究的良好结果,Brentuximab Vedotin(Adcetris)被美国FDA列为“优先审批和突破性疗法”,罕见地利用RTOR(Real-Time Oncology Review Pilot Program,实时肿瘤学评估)试验性审批途径。并在sBLA完成提交不到2周时间就给予了批准,堪称“神速”。
HOVON试验结果:来那度胺联合R-CHOP提高MYC重排阳性DLBCL( 包括DHL )患者远期生存率
除了Burkitt淋巴瘤(MYC+LBCL)外,MYC重排阳性大B细胞淋巴瘤患者在R-CHOP标准一线治疗后预后不佳。回顾性研究报告完全缓解率<50%,2年总生存率(OS)约为35%。Lenalidomide是一种免疫调节药物,能够下调MYC及其靶基因和B细胞中的MYC重排。今年ASH会议来自于荷兰HOVON研究组首次报道了的MYC阳性高侵袭性B细胞淋巴瘤的治疗数据。
研究已入组85例患者,58例患者可进行中期分析。FISH分析显示41/58例患者(71%)有MYC和BCL2和/或BCL6重排,11/58(19%)有单个MYC重排,6/58(10%)有MYC重排,但没有关于BCL2和BCL6的信息。所有患者接受8×R+6×CHOP21联合来那度胺15mg,第1-14天治疗,并均接受鞘内注射氨甲喋呤中枢预防及G-CSF预防。治疗结束时PET/CT进行疗效评价,36例患者(62%)获得完全代谢缓解(CMR)。2例患者(3%)获得部分代谢缓解(PMR),20例患者(34%)出现PD。中期PET-CT显示CMR 39例(67%),其中29例持续CMR。中位随访17.2个月, 1年OS的估计值为79%,DFS为74%,PFS为60%。3例和4例不良事件(AE)分别为26例(43%),9例(15%)。最常见的3级至4级AES为胃肠道疾病、感染和中性粒细胞减少症。
此次ASH会议[15]上报告的这项研究的结果显示,患者的远期生存率较好,1年PFS/OS分别高达60%及79%,而之前研究显示此类患者2年生存率约35%。该研究是目前首项针对双打击/三打击淋巴瘤患者的前瞻性随机对照研究,并且目前已经获得了不错的疗效,其未来的随访结果值得关注。这种治疗方案比较简单,而且不良反应更少、疗效更好,该研究结果对临床工作具有积极现实指导意义。
[1]Schmitz R, Wright GW, Huang DWN,et al. Engl J Med. 2018 Apr 12;378(15):1396-1407
[2]Chapuy B, Stewart C, Dunford AJ, et al.Nat Med. 2018 May;24(5):679-690.
[3]Anas Younes, Laurie H Sehn, Peter Johnson, et al. 2018 ASH meeting,abstract 784.
[4]Advani R, Flinn I, Popplewell L,et al.N Engl J Med. 2018 Nov 1;379(18):1711-1721.
[5]Zinzani PL, Ribrag V, Moskowitz CH,et al.Blood. 2017 Jul 20;130(3):267-270.
[6]Philippe Armand, Scott J Rodig, Vladimir Melnichenko, et al.2018 ASH meeting,abstract 228.
[7]Kurtz DM, Scherer F, Jin MC,et al.J Clin Oncol. 2018 Oct 1;36(28):2845-2853.
[8]Locke FL, Ghobadi A, Jacobson CA, et al.Lancet Oncol. 2018 Nov 30.
[9]Loretta J. Nastoupil, Michael D. Jain, Jay Y. Spiegel,et al.2018 ASH meeting,abstract 91.
[10]Schuster SJ, Bishop MR, Tam CS,et al.N Engl J Med. 2018 Dec 1.
[11]Viola Poeschel,Gerhard Held, Marita Ziepert,et al.2018 ASH meeting,abstract 781.
[12]John P. Leonard, Marek Trněný, Koji Izutsu,et al.2018 ASH meeting,abstract 445.
[13]Robak T, Jin J, Pylypenko H, et al.Lancet Oncol. 2018 Nov;19(11):1449-1458.
[14]Steven M. Horwitz, Owen A. O'Connor, Barbara Pro,et al.2018 ASH meeting,abstract 997
[15]Martine E.D. Chamuleau,Marcel Nijland,JoséijlaZijlstra,et al.2018 ASH meeting,abstract 626.
欲了解更多血液肿瘤、淋巴瘤相关资讯,与全国各地血液肿瘤、淋巴瘤医生交流与讨论,请扫描以下二维码,添加肿瘤资讯-娜小编,备注“血液肿瘤”!















 苏公网安备32059002004080号
苏公网安备32059002004080号


