2026年中国临床肿瘤学会(CSCO)指南会于2026年4月24日-25日在哈尔滨盛大召开。此次盛会由中国临床肿瘤学会(CSCO)与北京市希思科临床肿瘤学研究基金会联合主办,汇聚国内肿瘤学领域知名专家学者,共同交流肿瘤规范化诊疗、精准治疗及指南更新的重要进展。
本届指南会上,中国科学院院士、中山大学肿瘤防治中心马骏教授围绕鼻咽癌领域年度重要进展进行了系统报告。报告从早期筛查、局部晚期鼻咽癌免疫增效、放疗与化疗降阶减毒,以及复发/转移鼻咽癌新药突破等多个维度,全面呈现了我国鼻咽癌诊疗研究从“跟跑”走向“并跑”乃至部分领域“领跑”的发展态势。【肿瘤资讯】特整理核心内容,以飨读者。

早筛突破:从EBV抗体检测到多维分子标志物
鼻咽癌起源于鼻咽上皮,具有颈部淋巴结转移及远处转移倾向。我国是鼻咽癌高发国家之一,病例负担在全球占比较高。尽管鼻咽癌对放疗和综合治疗较为敏感,但临床仍面临早诊率偏低、高危患者复发转移风险较高,以及治疗后生活质量受损等问题。因此,如何提高早诊早治水平,是改善鼻咽癌整体预后的关键入口。
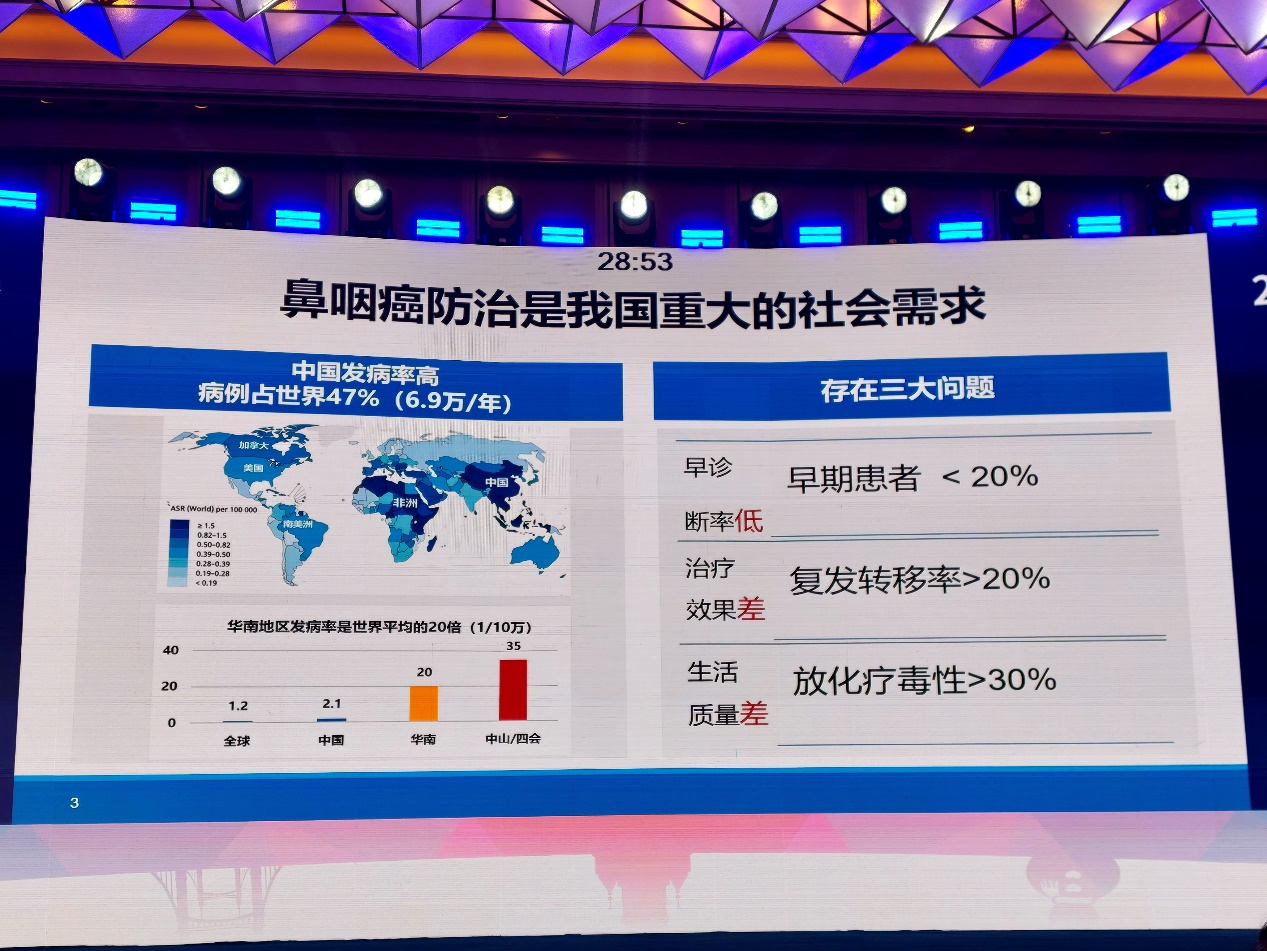
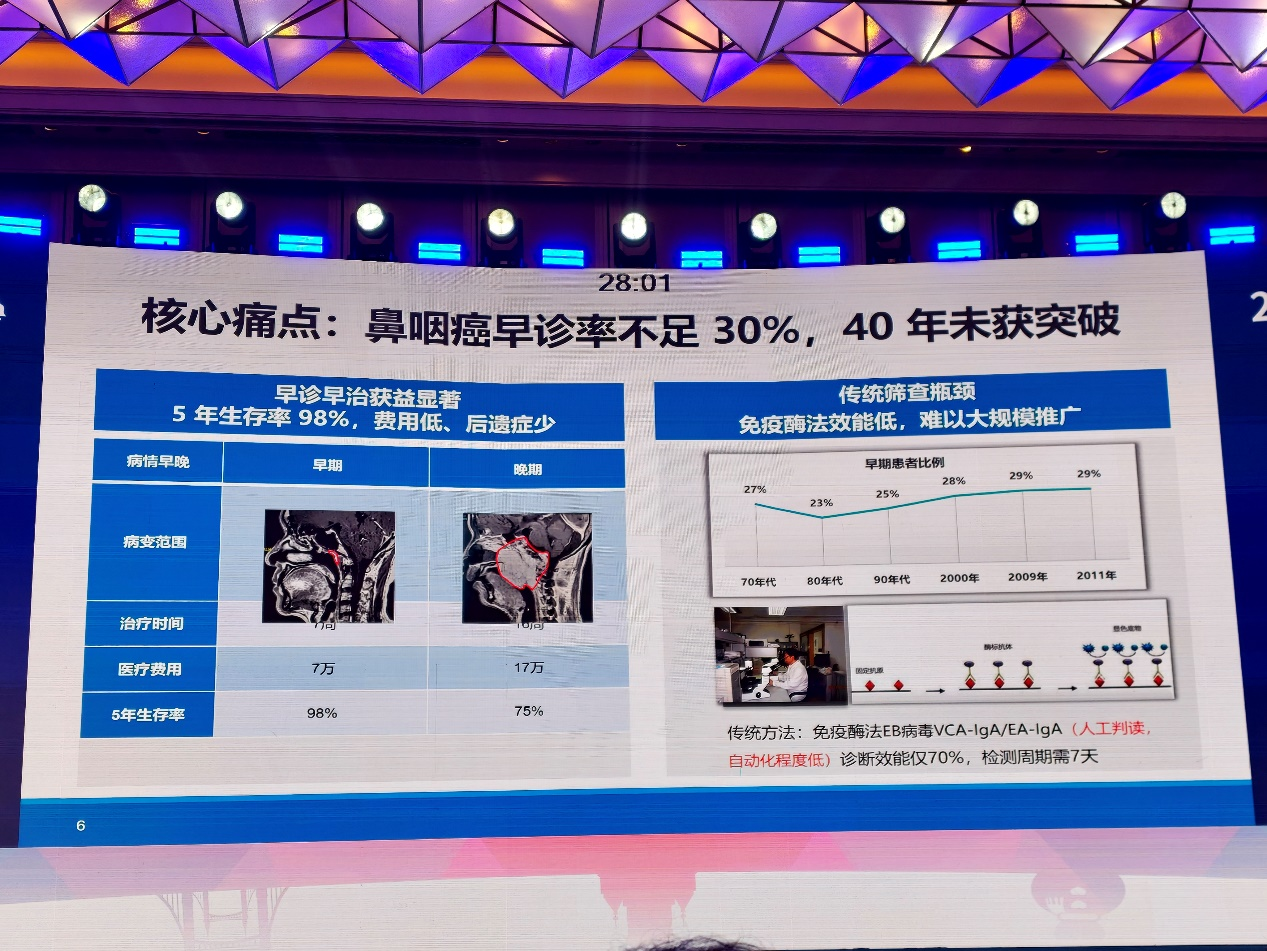
既往鼻咽癌筛查主要依赖EB病毒相关抗体检测,但传统免疫酶法存在人工判读依赖强、检测周期较长、诊断效能有限等不足,难以完全满足高发区大规模人群筛查需求。
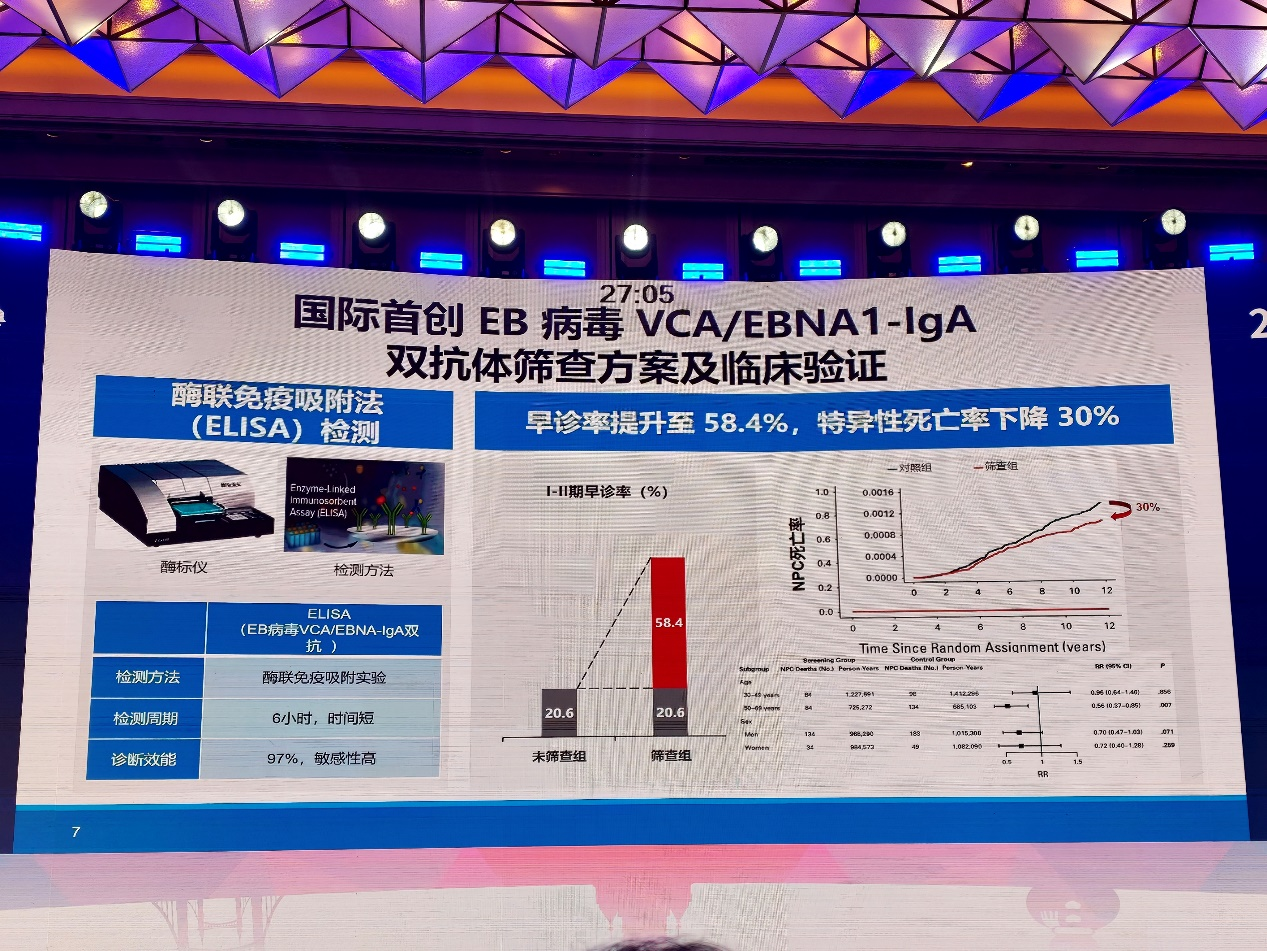
针对这一瓶颈,研究团队围绕EB病毒双抗体检测进行优化,采用VCA-IgA和EBNA1-IgA双抗体ELISA方法,将检测周期明显缩短,并显著提升筛查效能。相关前瞻性高发区整群随机对照研究显示,该策略可将I~II期鼻咽癌早诊率由20.6%提高至58.4%,并降低鼻咽癌特异性死亡风险,为我国高发区人群筛查提供了重要循证依据。
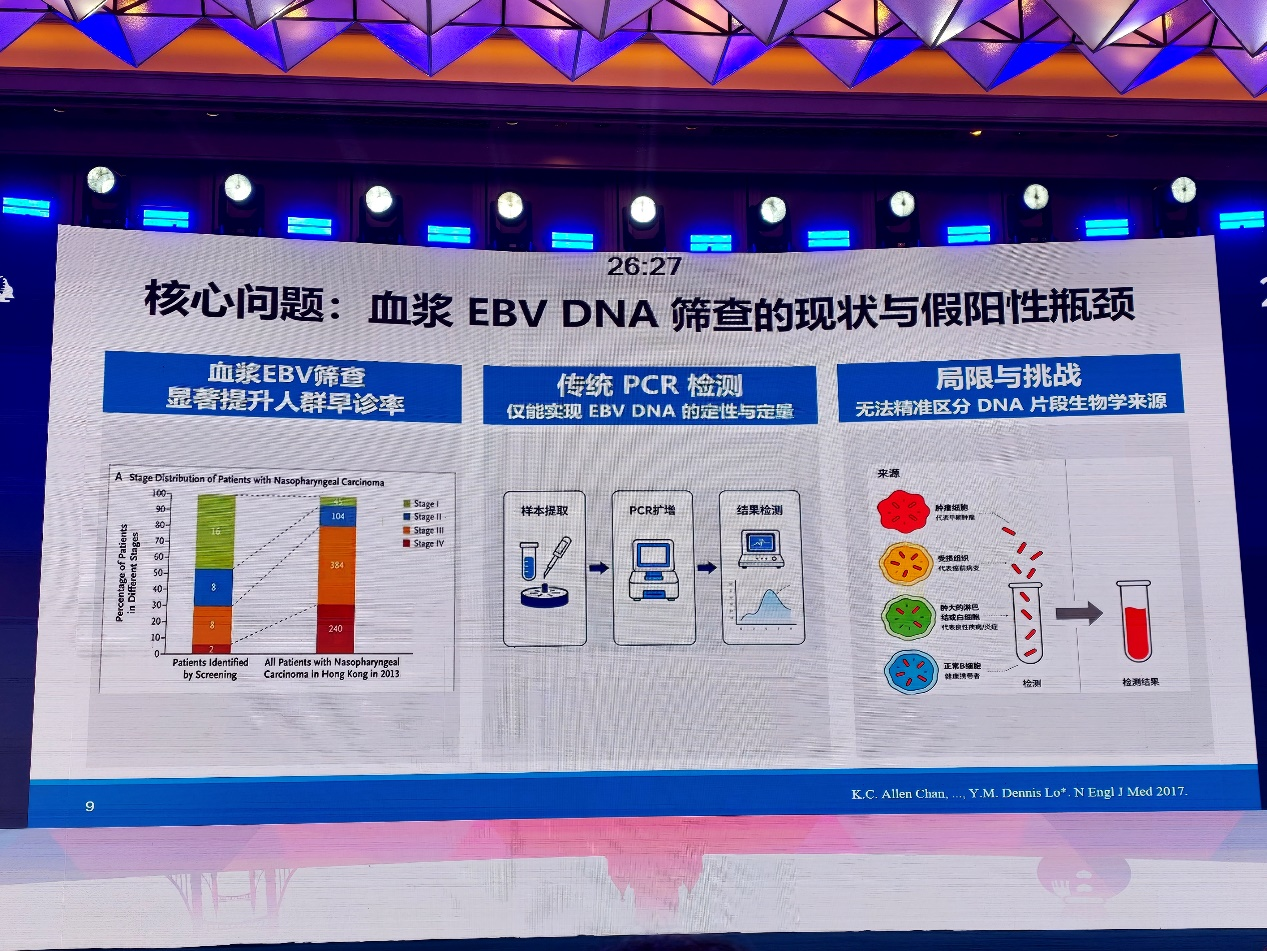
在血清学抗体检测之外,血浆EBV DNA检测及片段组学进一步拓展了鼻咽癌早诊思路。相较于抗体反映既往感染状态,血浆EBV DNA更能直接反映肿瘤负荷。通过整合DNA定量、片段大小、末端序列及甲基化等多维分子特征,研究者可更精准识别未来发病高风险人群,为早期干预提供新的分子工具。
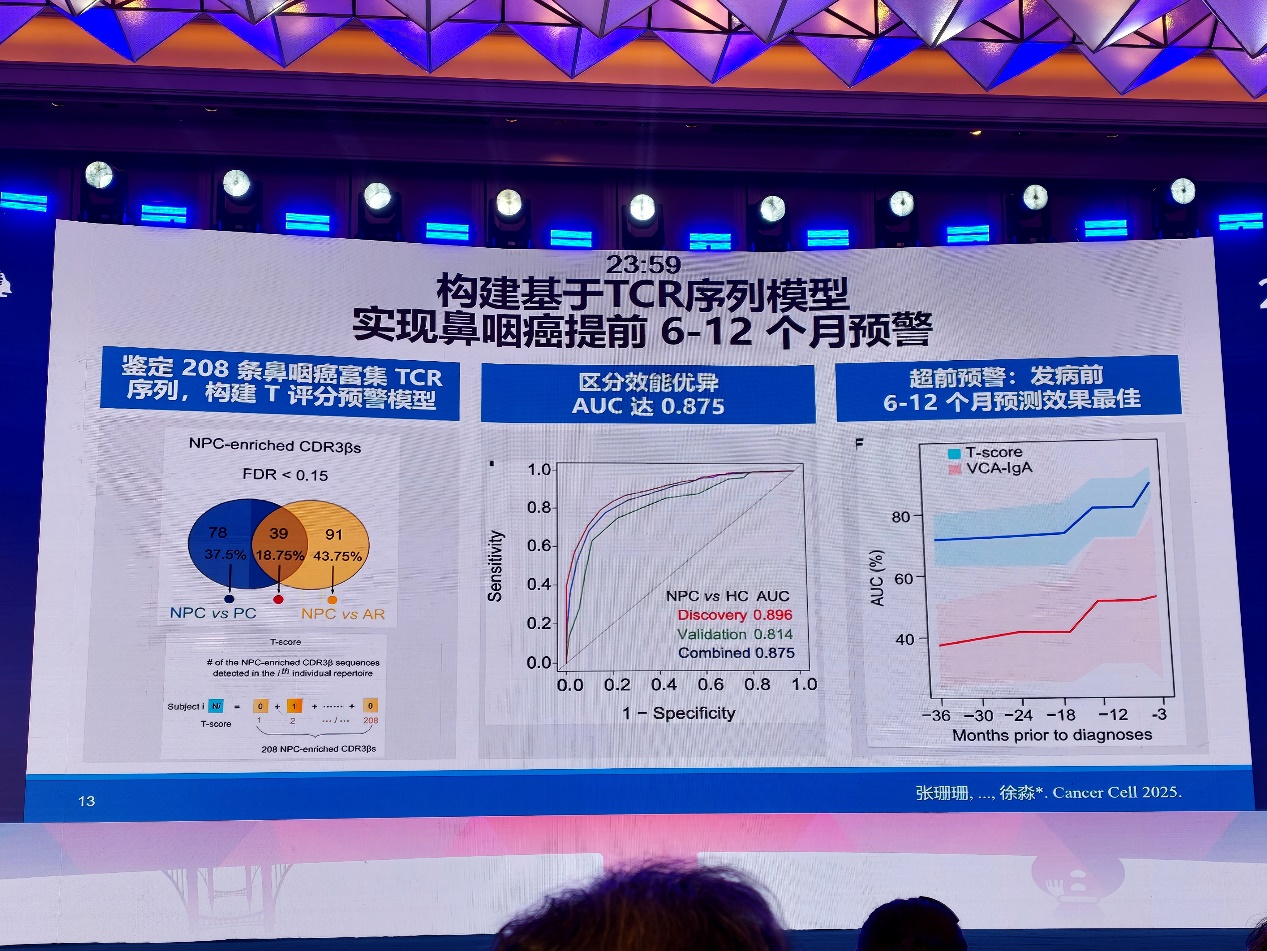
同时,T细胞受体(TCR)库也成为鼻咽癌早诊的新维度。TCR库记录了机体对病原体及肿瘤抗原的免疫识别“足迹”。随着EB病毒感染及肿瘤发生发展,T细胞识别谱系可发生动态变化。基于这一机制,研究团队构建了T评分早期预测模型,AUC可达0.87,并在确诊前6~12个月显示出较佳预警效果,提示免疫监测有望成为鼻咽癌超早期发现的重要补充。
免疫增效:PD-1单抗推动局部晚期治疗模式更新
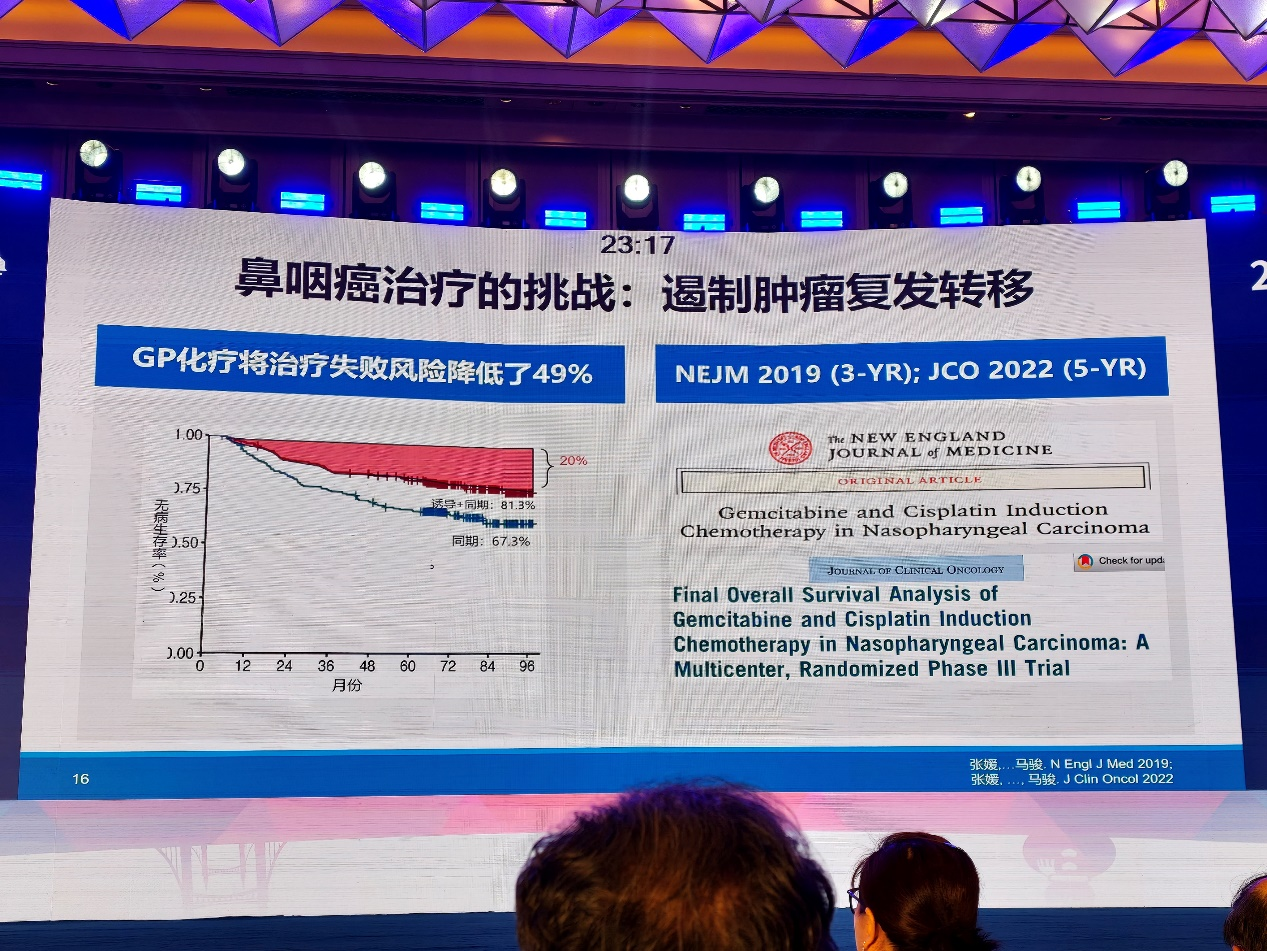
对于局部晚期鼻咽癌,吉西他滨联合顺铂诱导化疗序贯同步放化疗已成为重要标准方案。该模式显著降低了复发转移风险,但长期随访仍显示,约20%的患者会发生复发或转移,提示高危人群仍需进一步优化治疗策略。
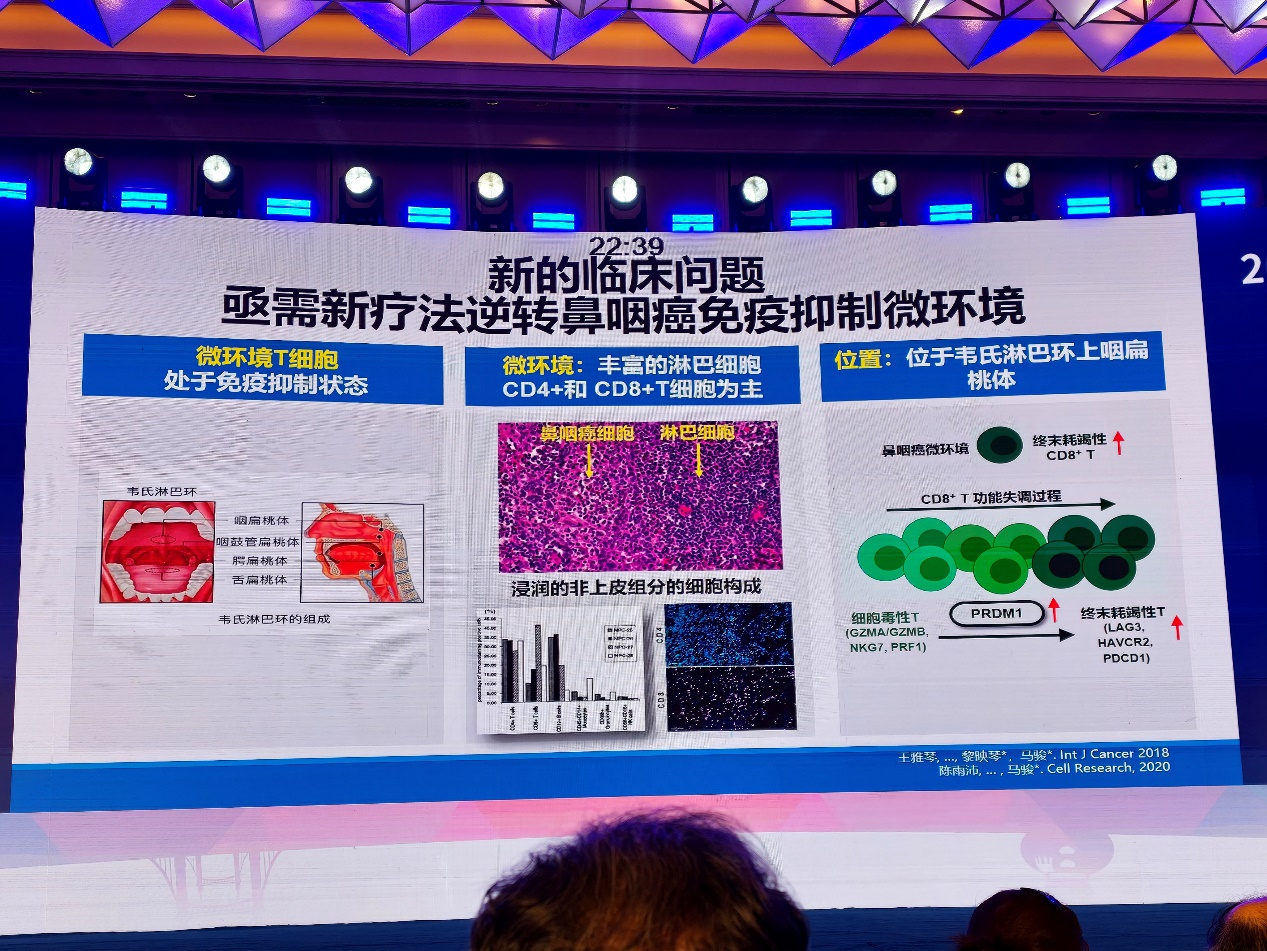
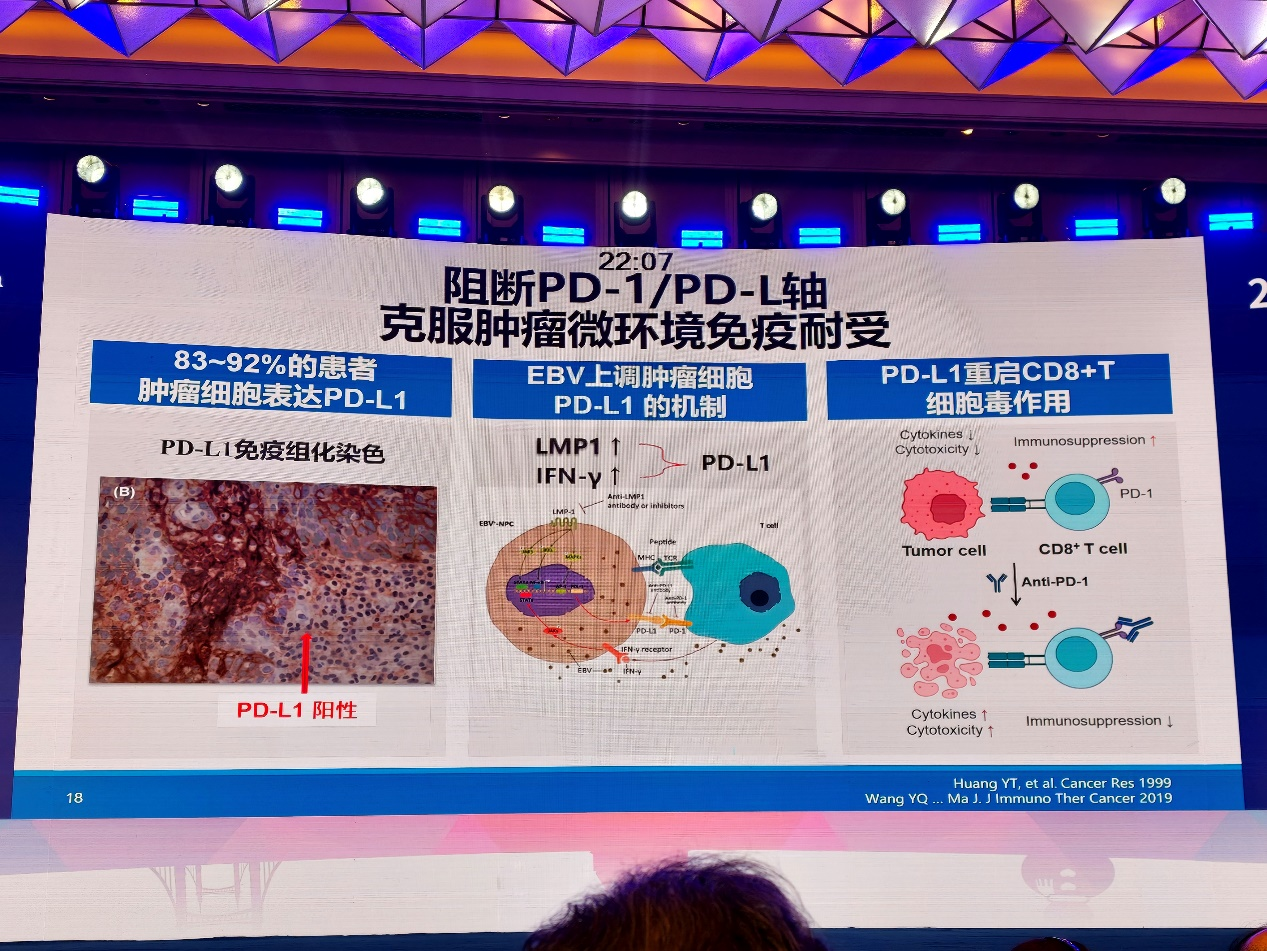
鼻咽癌具有明确的免疫治疗生物学基础。其发生发展与EB病毒感染密切相关,肿瘤微环境中可见大量淋巴细胞浸润,但部分T细胞呈耗竭状态;同时,PD-L1在鼻咽癌中表达比例较高,EB病毒相关信号及抗肿瘤免疫激活均可诱导PD-L1表达。因此,通过阻断PD-1/PD-L1通路重启T细胞功能,具备较强理论依据。
在局部晚期鼻咽癌中,PD-1单抗与放化疗的联合方式逐渐形成多种探索路径。其一是在诱导、同步及巩固全程治疗中加入PD-1单抗。相关III期研究显示,在标准放化疗基础上联合PD-1单抗,可进一步降低局部晚期鼻咽癌复发风险,推动治疗模式从单纯放化疗向免疫联合综合治疗演进。

其二是借鉴肺癌PACIFIC模式,在标准治疗结束后给予辅助免疫治疗。DIPPER研究显示,对于局部晚期鼻咽癌患者,在诱导化疗及同步放化疗后给予卡瑞利珠单抗辅助治疗,可使3年无事件生存率由77.3%提高至86.9%,疾病复发或死亡风险降低44%,且整体耐受性可控。这一结果提示,辅助PD-1阻断可能成为局部晚期鼻咽癌治疗的重要新方向。

其三是“放疗前+放疗后”联合免疫的“三明治”模式。麦海强教授团队开展的研究显示,在诱导化疗及辅助治疗阶段加入替雷利珠单抗后,诱导期完全缓解率由16.7%提高至30.5%,两组不良事件发生率相当,提示该策略在提高早期肿瘤退缩深度方面具有潜力,远期生存结果值得进一步期待。
放疗降阶:从扩大控制走向精准保护
放疗是鼻咽癌根治性治疗的核心手段。鼻咽部解剖位置深在,毗邻颅底、脑神经及重要血管结构,手术难以整块切除且损伤较大;同时,鼻咽癌以非角化性癌为主,对放射治疗高度敏感,因此放疗长期处于鼻咽癌治疗体系的核心位置。

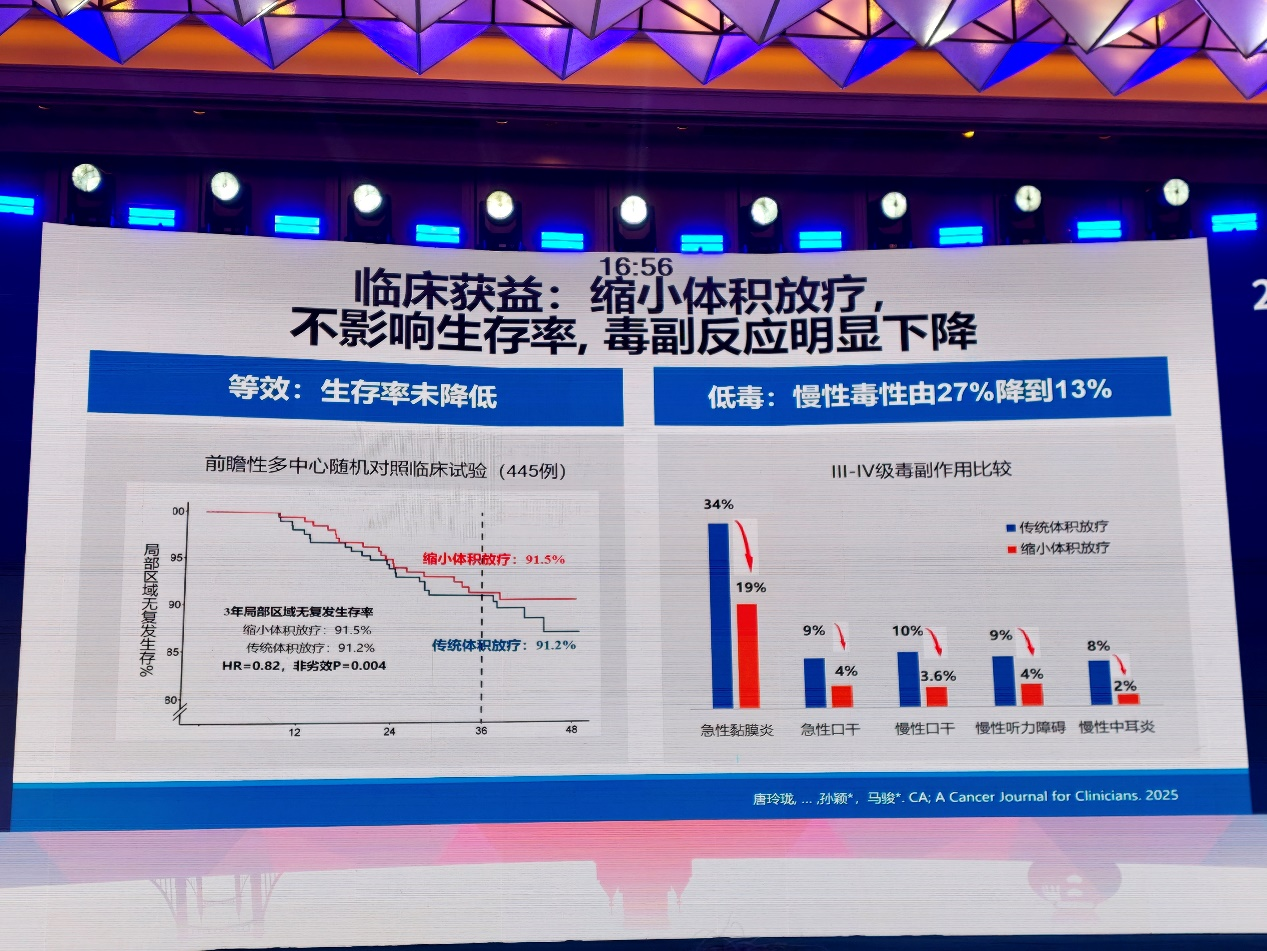
随着诱导化疗及PD-1单抗联合治疗提高肿瘤退缩率,新的临床问题随之出现:后续高剂量照射范围应依据治疗前肿瘤范围,还是依据治疗后残留肿瘤范围?针对这一问题,研究团队开展了全球首个豁免诱导治疗后退缩区高剂量照射的III期临床研究。该方案对残留肿瘤仍给予70 Gy照射,而对诱导治疗后退缩区域降至60 Gy,旨在不降低疗效的前提下降低放疗毒性。

结果显示,该策略未损害患者生存获益,同时显著降低放射性黏膜炎、口干等毒副反应。高剂量照射总体积减少17%,鼻咽部及颈部照射体积均显著下降,腮腺等正常器官受量减少,患者总体健康状况、体力状态、情绪功能、口干及唾液黏稠度等生活质量指标均得到改善。这一研究体现了鼻咽癌放疗理念的重要转变:从单纯追求局部控制,逐步走向疗效、毒性和生活质量兼顾的精准放疗时代。
与此同时,鼻咽癌放疗靶区勾画的国际规范化也取得重要进展。既往不同医生间靶区勾画差异较大,国际指南中对鼻咽癌放疗靶区的细化描述相对有限。基于这一临床需求,由中国团队牵头,联合全球17个国家和地区50位专家,严格遵循国际指南开发流程,完成鼻咽癌放疗靶区勾画及图谱制定。该指南整合多学科专家意见、循证证据等级及共识推荐强度,并通过多轮国际会议、专题讨论、邮件沟通和投票形成最终共识,推动中国鼻咽癌放疗经验转化为国际可共享、可推广的新标准。



化疗减负:豁免同期顺铂探索“减毒不减效”
在标准综合治疗中,化疗毒性同样是影响患者治疗体验和生活质量的重要因素。同步顺铂虽可提高疗效,但也可能带来口腔黏膜炎、恶心呕吐、体重下降、肾损伤及听力损伤等不良反应。如何在不牺牲疗效的基础上豁免或减少同步顺铂,是局部晚期鼻咽癌降阶梯治疗的重要方向。
研究团队首先开展了全程PD-1单抗联合化疗、豁免同步顺铂的II期临床研究,结果显示,3年无失败生存率达到88.5%,3~4级不良反应发生率降至40.2%,提示该方案具备“减毒不减效”的潜力。随后开展的全国多中心随机对照III期研究进一步证实,去同期化疗策略可实现与标准同步化疗相当的无失败生存率,两组均约为88%;同时,呕吐发生率由60%降至26.2%,患者生活质量明显改善。

这一结果为局部晚期鼻咽癌降阶梯治疗提供了新的视角。随着免疫治疗在综合治疗中的地位提升,未来鼻咽癌治疗并非一味“做加法”,而是在明确获益人群和风险分层基础上,实现治疗强化与治疗降阶的动态平衡。
后线突破:ADC为复发/转移鼻咽癌提供新选择
对于复发/转移鼻咽癌,一线治疗已形成以吉西他滨、顺铂联合PD-1单抗为代表的标准方案,并显著改善患者生存。然而,一线治疗失败后的二线及后线治疗选择仍相对有限,是当前临床亟需突破的难点。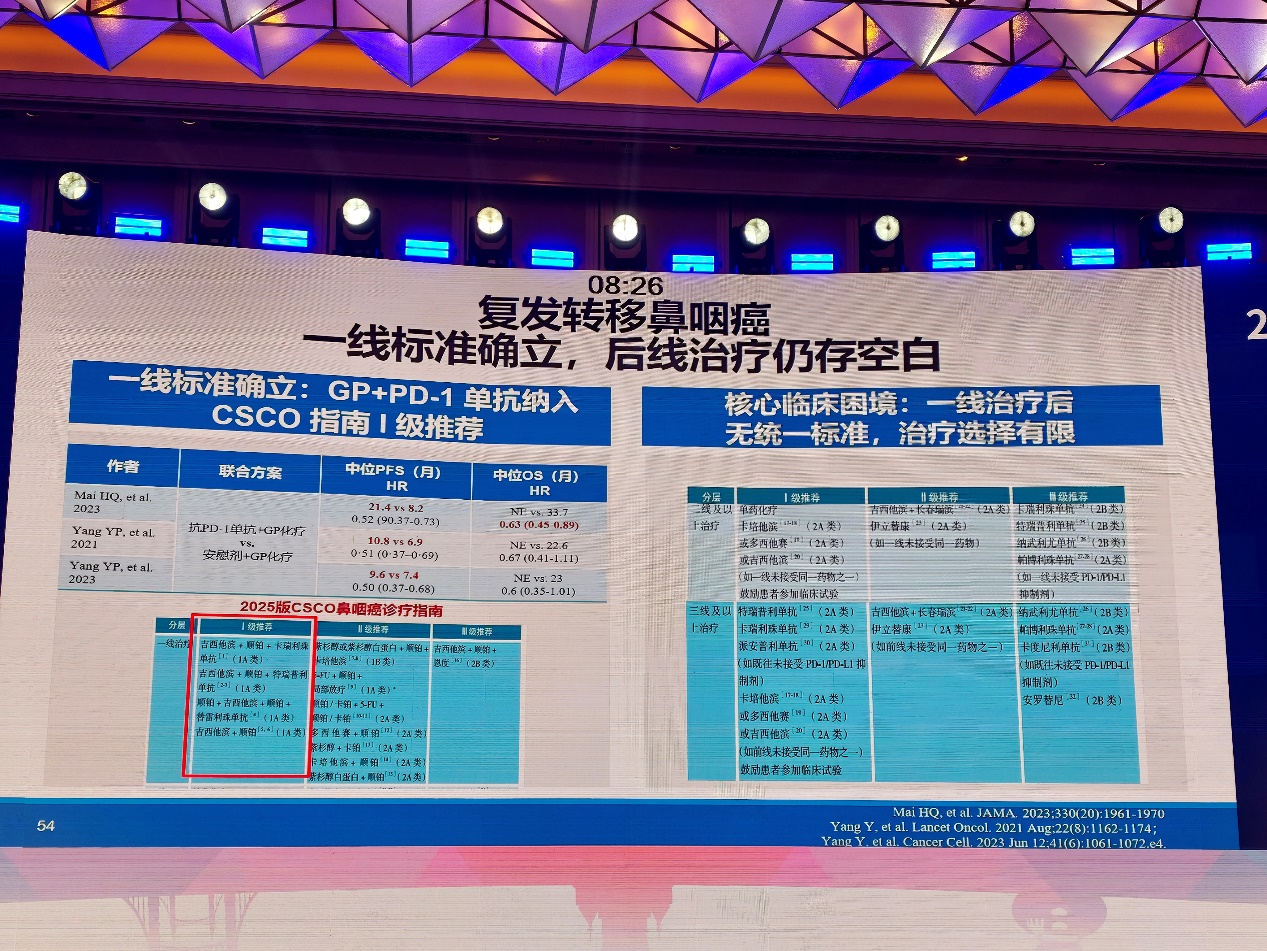
从复发转移病灶的生物学特征出发,研究者通过单细胞测序、全外显子测序及空间转录组分析,进一步描绘复发鼻咽癌免疫微环境全景,揭示了复发病灶中间质成分增加、免疫功能耗竭等关键特征。相关机制研究提示,TGF-β诱导肿瘤相关成纤维细胞富集,并通过胶原沉积介导治疗抵抗;多通路协同抑制免疫反应,则进一步促进免疫逃逸。这些均构成传统治疗难以突破的生物学屏障。
ADC药物凭借“抗体精准导航+连接子释放载荷+强效细胞毒作用”的特征,为复发/转移鼻咽癌后线治疗带来新可能。

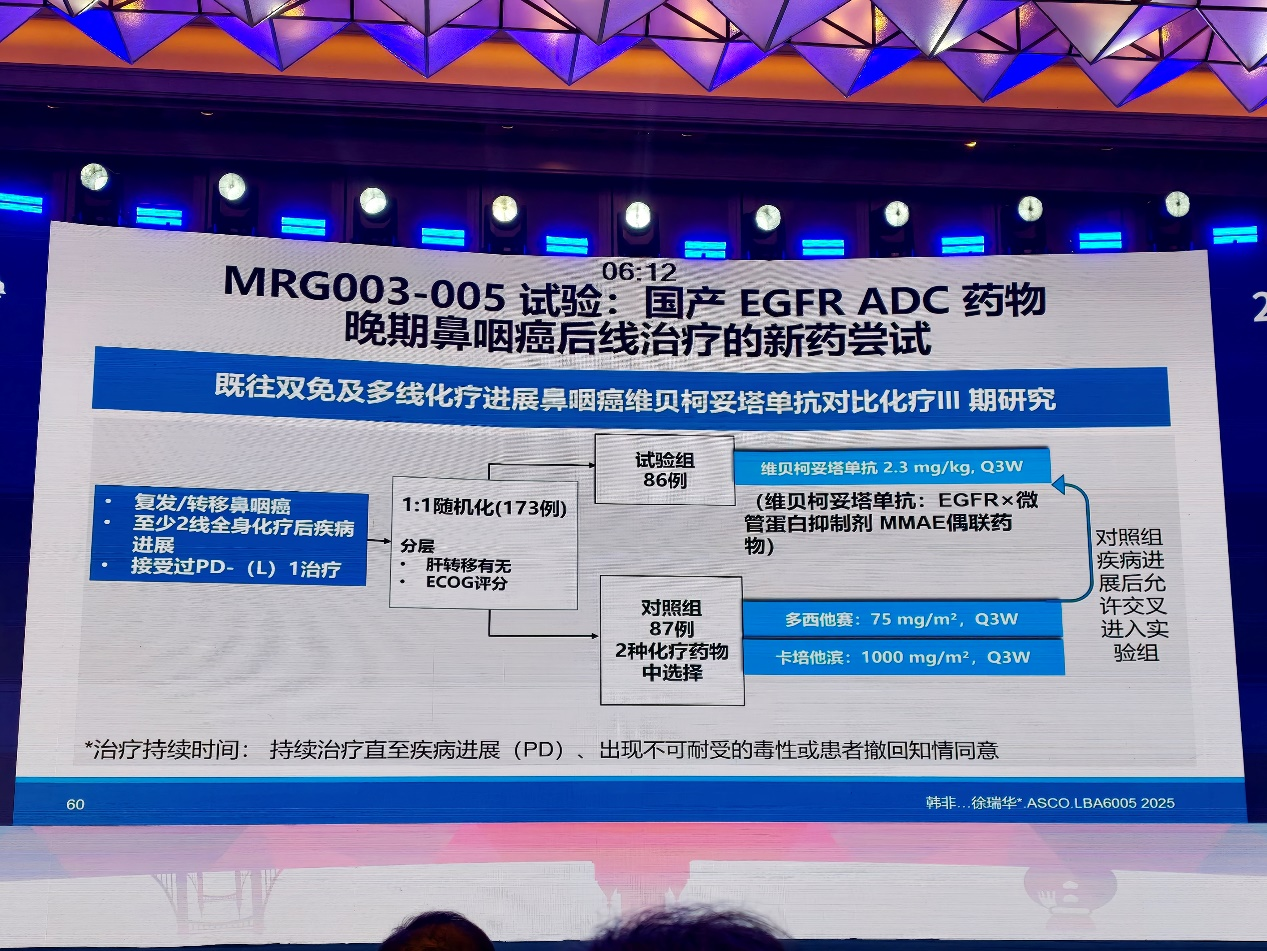
报告中提到,张力教授团队开展的III期研究聚焦既往接受二线化疗及相关治疗失败的患者,探索双抗ADC药物的疗效与安全性;徐瑞华教授团队开展的国产EGFR ADC注册研究,则对比ADC药物与临床可选单药化疗,并允许对照组进展后交叉接受ADC治疗。研究显示,相关ADC药物较化疗显著提高客观缓解率,延长中位PFS,并展现出OS获益趋势,为后线患者提供了更优治疗选择,也体现了我国原创新药在鼻咽癌领域的重要突破。

总结
总体来看,过去一年鼻咽癌诊疗在多个关键方向取得重要进展。早筛方面,EBV双抗体、血浆EBV DNA片段组学及TCR库等多维标志物推动鼻咽癌从传统筛查迈向精准早诊;局部晚期治疗方面,以PD-1单抗为核心的免疫联合策略持续提升患者生存获益;放疗与化疗方面,通过缩小照射范围、豁免退缩区高剂量照射及去同期顺铂等策略,实现了疗效与生活质量的再平衡;复发/转移疾病方面,以ADC为代表的新型药物为后线治疗带来新的突破口。
从早诊早治到免疫增效,从精准放疗到降阶减毒,再到ADC后线创新,鼻咽癌治疗正逐步形成以风险分层、精准干预和全程管理为核心的新格局。未来,随着更多高质量中国研究持续产出,我国鼻咽癌诊疗经验有望进一步转化为国际标准,为全球患者带来更多获益。
排版编辑:肿瘤资讯-slb











 苏公网安备32059002004080号
苏公网安备32059002004080号


