
在医药创新的前沿浪潮中,“天生爆品”从来不是一句简单的宣传语,而是科学逻辑、研发速度与临床价值交织出的必然结果。在即将到来的2026 年ASCO年会上,全球首创的EGFR×HER3双抗ADC—iza-bren,将重磅披露两项Ⅲ期研究数据:三阴性乳腺癌(BL-B01D1-307)、食管鳞癌(BL-B01D1-305),再次刷新iza-bren循证高度。
而在这之前,以鼻咽癌Ⅲ期研究数据领衔(ORR 55%、中位PFS8.4个月[1]),iza-bren已在多个实体瘤领域展现出了同类最佳(Best-in-class, BIC)的数据潜力。凭借独特的创新机制底色,iza-bren正展现出跨越单一瘤种的广谱抗肿瘤潜力。站在2026上市元年的门槛上,iza-bren以硬核的循证证据向全球兑现其“天生爆品”的临床价值。
2026 ASCO 重磅前瞻:
两项Ⅲ期研究发声,再度刷新其循证高度
在即将举行的2026年ASCO年会上,iza-bren将再度刷新其循证高度。凭借极具竞争力的临床获益,其两项重磅Ⅲ期研究:三阴性乳腺癌(BL-B01D1-307)、食管鳞癌(BL-B01D1-305),将分别以LBA和oral形式进行汇报。这一突破不仅标志着国际学术界对iza-bren创新机制与临床价值的最高认可,更是对产品10大重点适应症版图布局的有力兑现。从“概念验证”到“全球领先”,iza-bren正在顶级学术舞台上,以硬核证据链逐步夯实其同类最佳(Best-in-class,BIC)的领航地位。
iza-bren(BL-B01D1),作为全球首创的EGFR×HER3双抗 ADC,自2021年开启临床征程以来,正以其跨瘤种、多维度的突破性表现,重新定义全球ADC研发的“中国高度”。继2025年ESMO会议上鼻咽癌(NPC)Ⅲ期研究(303研究)数据震撼亮相、开启实体瘤双抗ADC治疗元年后,iza-bren的循证步伐再迎巅峰。

2026 ASCO重磅研究概览

<向右滑动进行查看>
Pan-tumor全域布局的机制底色
iza-bren“天生爆品”的底色,源于其在单靶点ADC基础上的机制迭代。iza-bren是一款EGFR×HER3双抗ADC,兼具靶向和细胞毒双重作用,或将发挥更强的抗肿瘤作用,可同时与EGFR和HER3两个靶点结合,可更加精准、高效的与肿瘤细胞结合;细胞毒性载荷为拓扑异构酶I抑制剂Ed-04,且药物抗体比(DAR)为8;连接子部分采用公司自主研发的Ac接头,可保障药物在体内循环的稳定性,并能在肿瘤细胞内部被组织蛋白酶水解,释放毒性载荷从而发挥肿瘤细胞的杀伤作用;采用可裂解连接子同时保证iza-bren 具有旁观者效应。作为双抗ADC,其较传统的单靶点ADC 具有更精准的肿瘤组织选择,提高疗效的同时降低脱靶毒性,从机制层面实现治疗策略优化。
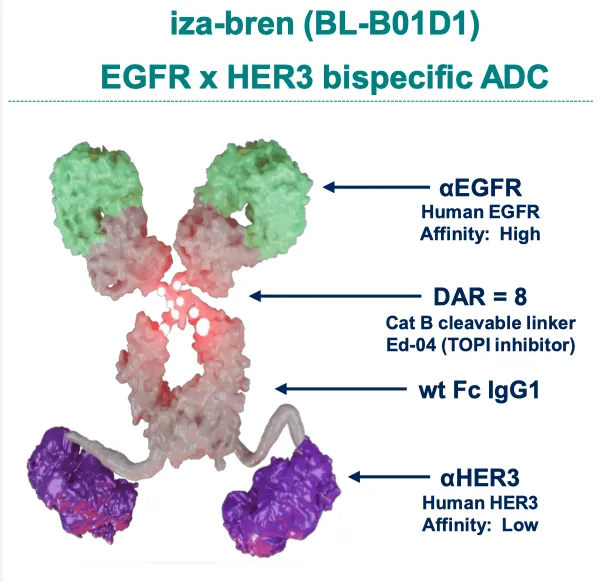
在精准治疗时代,iza-bren通过EGFR与HER3的双向锁定,有效突破了单一靶点在不同肿瘤组织中表达异质性(表达不均)或易产生耐药的局限。这种机制上的协同增效,使其不仅具备了极高的靶向精度,更拥有了改写多瘤种治疗格局的“全域广度”。
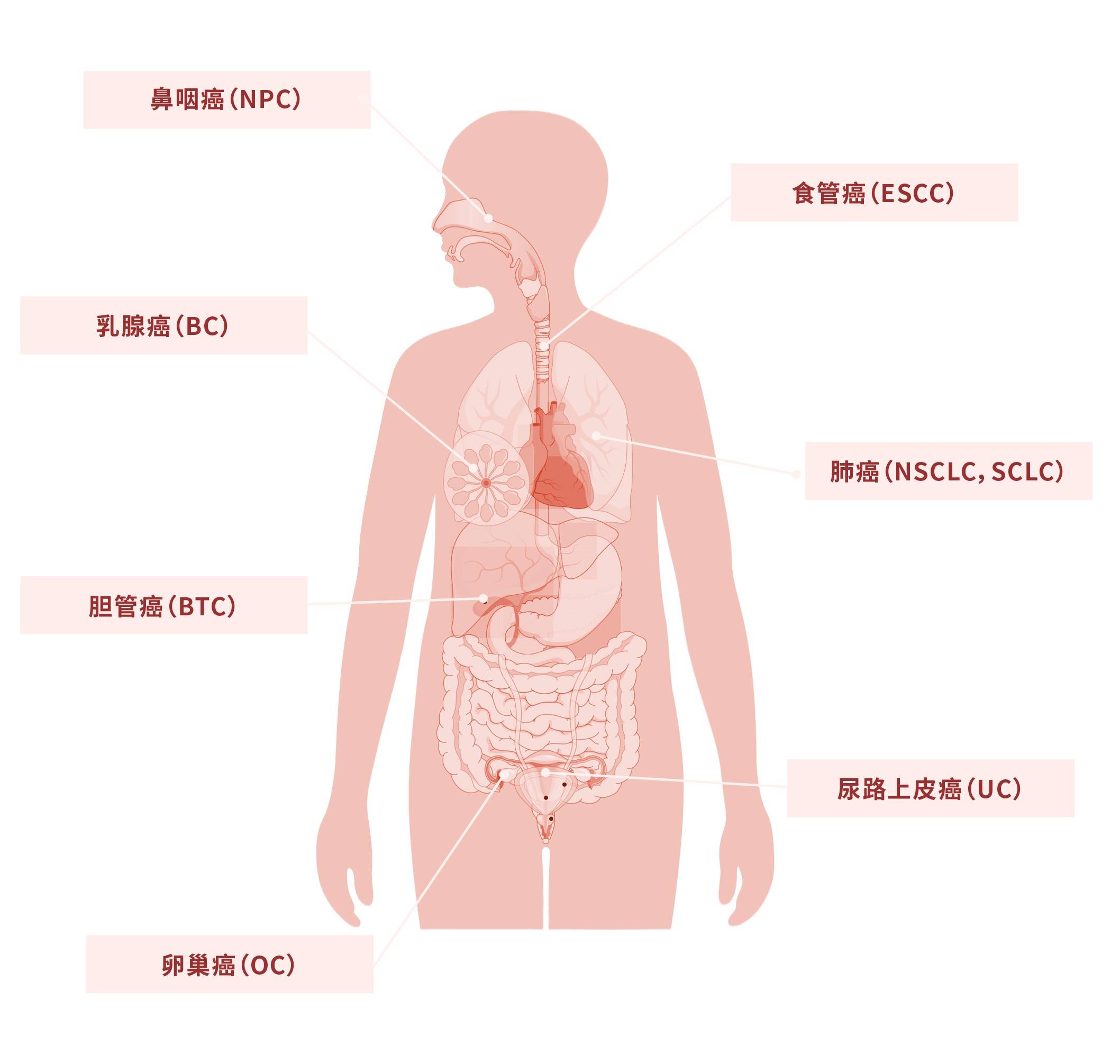
多瘤种BIC证据链的深度解码
从关键研究数据的重磅公布,到突破性疗法的官方认定,再到国际重磅期刊的学术背书,每一个里程碑事件都在客观记录着iza-bren循证壁垒的持续筑高。

鼻咽癌(NPC)
iza-bren单药用于复发/转移性鼻咽癌后线治疗,疗效显著优于单药化疗,实现获益翻倍提升
疗效全面领跑:ORR最高,达55%(单药化疗 27%,维贝柯妥塔单抗30%),研究中观察到CR 病例;PFS最长,达8.4m(单药化疗4.3m,维贝柯妥塔单抗5.8m[1]);
安全性可控:不良反应以血液学毒性为主,≥3 级不良事件经干预后可快速纠正;患者无显著不适症状,不影响长期持续用药[1];
适用人群广泛:疗效不受年龄、性别、既往治疗史等临床因素影响,亦不依赖EGFR、HER3表达水平,无需提前进行基因检测,全人群均可获益;
机制先进,精准强效:创新EGFR×HER3双靶点结构,药物抗体比(DAR)≈8,搭载Ed-04毒素,抗肿瘤活性优于DXd毒素,实现精准强效杀伤[2];
循证证据权威充分:全球首个且唯一针对复发/ 转移性鼻咽癌后线治疗的III期随机对照试验(RCT),凭借高级别证据获NCCN指南列为后线治疗优选推荐方案[3]。

肺癌(NSCLS,SCLC)
非小细胞肺癌:全人群覆盖+全病程突破,树立NSCLC治疗新标杆
全球首个在EGFR突变及野生型NSCLC领域均展现BIC潜力的双抗ADC:两项适应症均斩获CDE 突破性疗法认定,疗效优势获得官方权威认可。
颠覆EGFR-TKI耐药后的治疗范式:治疗EGFR-TKI耐药患者mPFS首超12个月,iza-bren单药彰显硬核实力,且安全性良好,仅1.2%的患者因TRAEs停药[4]。常见血液学毒性,≥G3级中性粒细胞减少纠正快(中位4-6天)。
重塑EGFRm NSCLC一线联合治疗标准:iza-bren联合奥希替尼ORR100%,成为全球首个达到“满分”应答的ADC方案。12个月PFS率为 92.1%、OS率高达94.8%、mDoR及mPFS尚未达到。安全可耐受,血液学毒性为主,≥G3级中性粒细胞减少纠正快(中位6-7天)且停药率低(0.8%),未报告发热性中性粒细胞减少症[5]。
小细胞肺癌:iza-bren联合PD-1单抗重塑ES-SCLC一线格局,或开启慢病管理新时代
疗效标杆:1年OS率高达85.7%、mPFS长达8.2 m、100%靶病灶缩瘤率与85%ORR创下BIC疗效标杆,有望改写广泛期小细胞肺癌一线治疗临床实践[6]。
格局重塑:不仅实现mPFS与1年OS率双重超越,疗效优于传统三/四药标准方案;更完整保留了传统化疗用于后线治疗的可能性,推动ES-SCLC从“一线用尽”向“阶梯有序、慢病化管理”转型。
安全可控:以血液学毒性为主且可通过临床规范治疗有效管理,因TRAE导致iza-bren停药率低至 2.4%,为临床落地与患者长期持续获益奠定坚实基础,彰显我国创新药研发的国际竞争力[6]。

尿路上皮癌(UC)
iza-bren用于经治UC患者ORR达80.0%,展现出突破性价值,获CDE突破性治疗认定
在2.2mg剂量组中,iza-brenORR为44.1%,DCR达88.2%,mPFS为7.3个月,mDOR达11.3个月,显示出持久的抗肿瘤活性[7]。
在仅接受过1线化疗进展的患者中,ORR达 80.0%,DCR达100%,且6个月PFS率为 100%,患者获益显著,有望重塑UC后线治疗格局[7]。
此项研究标志着全球首个针对EGFR×HER3的双抗ADC为尿路上皮癌治疗领域带来全新的潜在治疗方案,iza-bren 顺利获得CDE的BTD认定,用于经治的局部晚期或转移性尿路上皮癌患者。

卵巢癌 (OC)
iza-bren Ib/II期研究实现复发卵巢癌全人群突破,破解铂耐药困局
打破了传统治疗中“按人群分型选药”的局限,展现出“全人群单药高效治疗”的潜力:全人群的mOS随访至12.5个月,尚未达到终点,生存趋势呈平稳上升,显示出延长生存期的可能[8]。
为铂耐药复发患者带来多方面突破:铂耐药亚组,cORR达到49.0%,mPFS为7个月,突破了传统治疗方案的6个月“瓶颈”[8]。
III期临床研究正在积极开展,未来有望成为复发性卵巢癌患者,尤其是铂耐药复发患者新的治疗标准!

胆管癌 (BTC)
I期数据初露锋芒,ORR近40%,胆管癌后线治疗迎来“双抗ADC”破局之势
全球首个EGFR×HER3双抗ADC在胆管癌经治人群中展现初步疗效信号,为后线治疗探索注入新动能。
胆管癌后线治疗选择有限,iza-bren作为全球首个EGFR×HER3双抗ADC,I期研究中纳入≥1线经治的晚期BTC患者,ORR达约39%,DCR接近 90%,mPFS为4.2个月,mDoR达5.9个月,初步数据展现出明确的疗效优势[9]。
联合PD-1/PD-L1抑制剂的研究已同步推进,后续组合策略的探索值得关注。
立足中国,辐射全球
领航BIC新征程
iza-bren的高光时刻,正沿着其实体瘤全域布局的脉络,从中国延伸至全球。目前,3项全球多中心(MRCT)II/III期注册临床研究正在同步加速推进。从各项指标的数据厚度,到国际重磅期刊与中美BTD认定的认可高度,再到从“概念验证”到“上市在即”的转化速度,iza-bren已然具备了极强的同类最佳(BIC)潜能。
天生爆品,实力铸就。站在2026上市元年的关键时间节点回望,iza-bren正以“全能战士”的姿态,为全球实体瘤患者开启一个充满希望的创新ADC治疗新时代。而这一切远非终点—属于它的高光传奇,仍在不断被创造与刷新。
[1] Yang Y, et al. Izalontamab brengitecan, an EGFR and HER3 bispecific antibody-drug conjugate, versus chemotherapy in heavily pretreated recurrent or metastatic nasopharyngeal carcinoma: a multicentre, randomised, open-label, phase 3 study in China. Lancet. Published online October 19, 2025. doi:10.1016/S0140-6736(25)01954-3
[2] Y.Yang, H.Zhou, L.Q et al., Izalontamab Brengitecan, An EGFR×HER3 Bispecific Antibody-drug Conjugate, versus Chemotherapy in Heavily Pretreated Recurrent/Metastatic Nasopharyngeal Carcinoma: A Multicenter, Randomized, Open-label, Phase III Study. Presented at 2025 ESMO. LBA 35.
[3] 中国版NCCN肿瘤学临床实践指南(NCCN指南®)头颈部肿瘤(鼻咽癌).
[4] Fang WF, et al. Phase I/II Study of Iza-Bren (BL-B01D1) as Monotherapy in Patients With Locally Advanced or Metastatic EGFR Mutated NSCLC. 2025 WCLC. OA10.03.
[5] Zhou F, et al. Phase II Study of Iza-Bren (BL-B01D1) Combo With Osimertinib in EGFR Mutated Locally Advanced or Metastatic NSCLC Patients. 2025 WCLC. OA10.04.
[6] Zhou F, et al. Phase II Study of iza-bren (BL-B01D1) in Combination with Serplulimab in Patients with Small Cell Lung Cancer (SCLC). 2026 ELCC. Abstract 938.
[7] Bian X, Yang T, Yin H, et al. Efficacy and Safety of BL-B01D1 in Patients With Locally Advanced or Metastatic Urothelial Carcinoma: A Phase II Clinical Trial. J Clin Oncol. 2025 Nov 10;43(32):3505-3515. doi: 10.1200/JCO-25-00109. Epub 2025 Oct 8. PMID: 41061200.
[8] Xiaohua Wu, Yong Wu, Jian Zhang, et al. Phase lb/ll Study of iza-bren (BL-B01D1), an EGFR×HER3 Bispecific Antibody-drug Conjugate, in Patients with Recurrent Metastatic Ovarian Cancer. ESMO Congress 2025. Berlin: European Society for Medical Oncology, 2025: Abstract 933P.
[9] ZhiHao L, et al. BL-B01D1, an EGFR x HER3 bispecific antibody-drug conjugate (ADC), in patients with locally advanced or metastatic biliary tract carcinoma (BTC). 2024 ESMO 54P
排版编辑:肿瘤资讯-老猫











 苏公网安备32059002004080号
苏公网安备32059002004080号


