乳腺癌作为危害女性健康的一种常见恶性肿瘤,其发病率在全球女性恶性肿瘤中位居首位,已成为一项亟待应对的公共卫生挑战。恰值2025年欧洲肿瘤内科学会(ESMO)年会刚刚落下帷幕,NATALEE研究的亮眼结果宣告CDK4/6抑制剂在广泛Ⅱ-Ⅲ期人群中的证据日益充分。
在此,山西医科大学第一医院郭昱君医生报告一例69岁HR+/HER2-晚期乳腺癌病例,患者曾于十余年前确诊为右乳浸润性导管癌(T3N2M0 III期),术后辅助内分泌治疗五年。十余年后,患者出现疾病转移,在接受瑞波西利联合来曲唑一线治疗后,实现快速肿瘤缩小,疗效评价达到部分缓解(PR)。【肿瘤资讯】邀请北京大学肿瘤医院邸立军教授,结合ESMO 2025会议的最新学术进展,对本病例的诊疗过程进行深度点评,探讨相关研究进展剖析临床路径管理优化的可能。
北京大学肿瘤医院乳腺肿瘤内科
北京乳腺病防治学会内科分会主任委员
北京肿瘤防治研究会乳腺癌分委会候任主任委员
外科学硕士研究生
山西医科大学第一医院乳腺科主治医师
山西省医师协会乳腺医师分会委员
山西省抗癌协会乳腺疾病腔镜治疗专业委员
病例介绍
基本情况
吴某,69岁,绝经后女性
现病史:患者于2006年5月行右乳癌改良根治术,术后病理:右乳浸润性导管癌,肿物大小:5.5*1*1.2cm,乳头及皮肤未见特殊,淋巴结可见癌转移(腋窝5/16)。免疫组化: ER (+), PR (-), cerbB -2(-)。术后辅助化疗6次(单药紫杉醇240mg),规律放疗(具体部位、剂量不详),内分泌治疗5年(依西美坦25mg)。治疗结束后未规律复查。患者于2024年2月自觉右侧胸壁多发结节以及左侧腋窝肿块,不伴有特殊不适,未予重视。后自觉右侧胸壁结节增大,增多。不伴皮肤红肿、疼痛;不伴皮肤破溃、流脓。2024年3月右侧近腋窝处胸壁皮肤破溃,患者自行给予消毒换药等,破溃范围较前有所增大。患者遂就诊于我院。
既往史:于7岁时确诊肺结核,规律治疗,现病情稳定。2003年01月曾摔倒行左侧股骨颈骨折内固定术,2007年行内固定取出术。曾于2003年因骨折输血“A”型血,具体剂量不详。否认高血压、心脏病史,否认糖尿病、脑血管疾病病史,预防接种是不详。
查体:胸廓无畸形,右乳缺如,右侧胸壁可见一长约15cm的陈旧性手术瘢痕。局部皮肤色泽正常,切口上方可及多个结节,较大3*2cm,稍红肿、表面无破溃,质硬。右侧近腋窝处可见一处皮肤破溃,范围为2*2cm,周围皮肤稍红肿。左侧乳头无内陷,无溢液。左乳内上象限可及一肿物,大小约2*1cm,质韧,边界不清,活动度欠佳。左侧腋窝可及一肿物,质硬,大小约3*3cm,相对固定。
辅助检查:
乳腺彩超(2024年05月24日 我院):
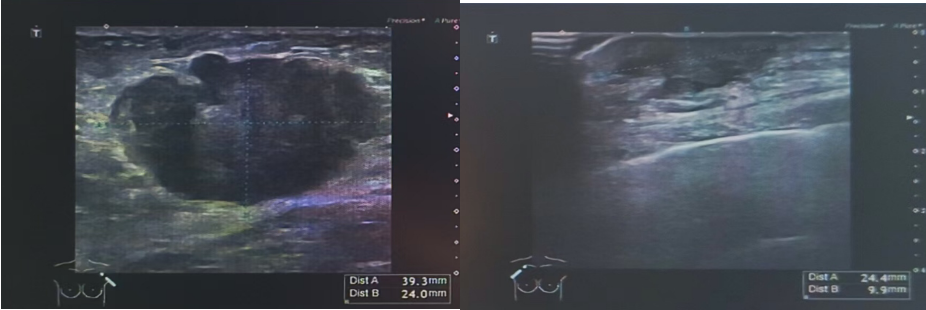 图 乳腺彩超(2024年05月24日 我院)
图 乳腺彩超(2024年05月24日 我院)
(左):左侧腋窝淋巴结3.93*2.40cm;(右):右侧腋窝淋巴结2.44*0.99cm
1、右侧胸壁可及低回声结节,大小约2.04*0.46cm,边界欠清,形态不规则。
2、胸骨偏右侧皮下脂肪层可及多发低回声结节,较大者约0.91*0.42cm,中间高回声,外周低回声,边界欠清,形态不规则,未见明显明显异常血流信号。
3、左乳11点距乳头2.0cm可及低回声结节,大小约1.75*0.99cm,形态规则,边界清,周边可及高回声声晕,血流信号较丰富。
4、双侧腋窝处可及多发低回声结节,右侧较大者约2.44*0.99cm,左侧较大者3.93*2.40cm,边界欠清,形态不规则。
左侧乳腺钼靶(2024年05月22日 我院):
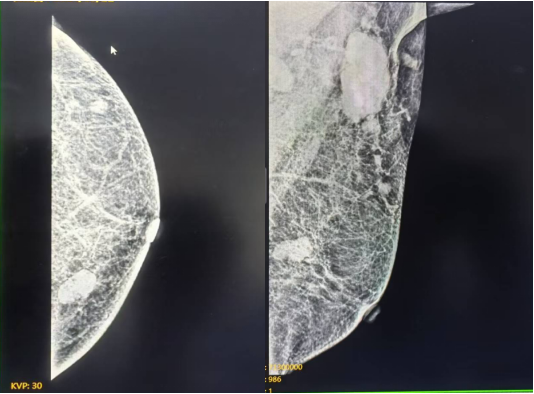 图 左侧乳腺钼靶:(2024年05月22日 我院)
图 左侧乳腺钼靶:(2024年05月22日 我院)
1、左乳多发结节,BI-RADS 3类
2、左侧腋下多发肿大致密淋巴结,建议进一步检查
胸部CT(2024年05月22日 我院):
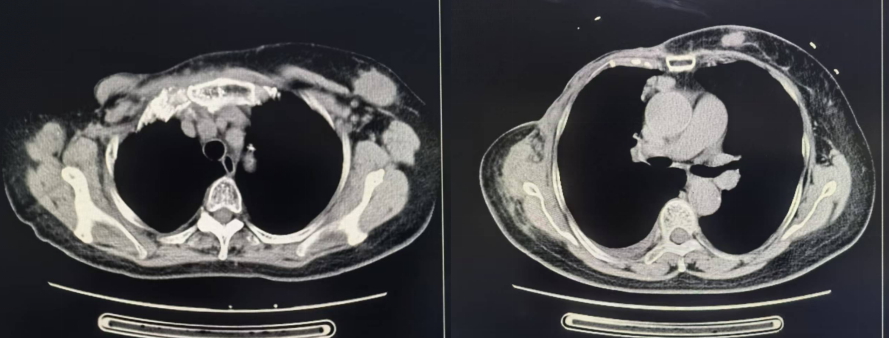 图 胸部CT(2024年05月22日 我院)
图 胸部CT(2024年05月22日 我院)
1、右侧乳腺术后改变,术区周围皮肤增厚,考虑复发可能,请结合临床。
2、右侧胸背部肌肉肿胀,肌间隙及皮下多发结节影,右前上纵隔及左侧腋窝多发增大淋巴结影,最大约3.6*2.7cm,左前胸壁皮下多发结节影,最大约1.6*1.1cm。
3、右侧胸膜多发结节状增厚,右侧少量胸水,右肺下叶实性小结节影,考虑转移。
腹部CT、锁骨淋巴结彩超、头颅核磁、全身骨扫描未见明显全身转移征象。
穿刺病理结果(2024年05月22日 我院):
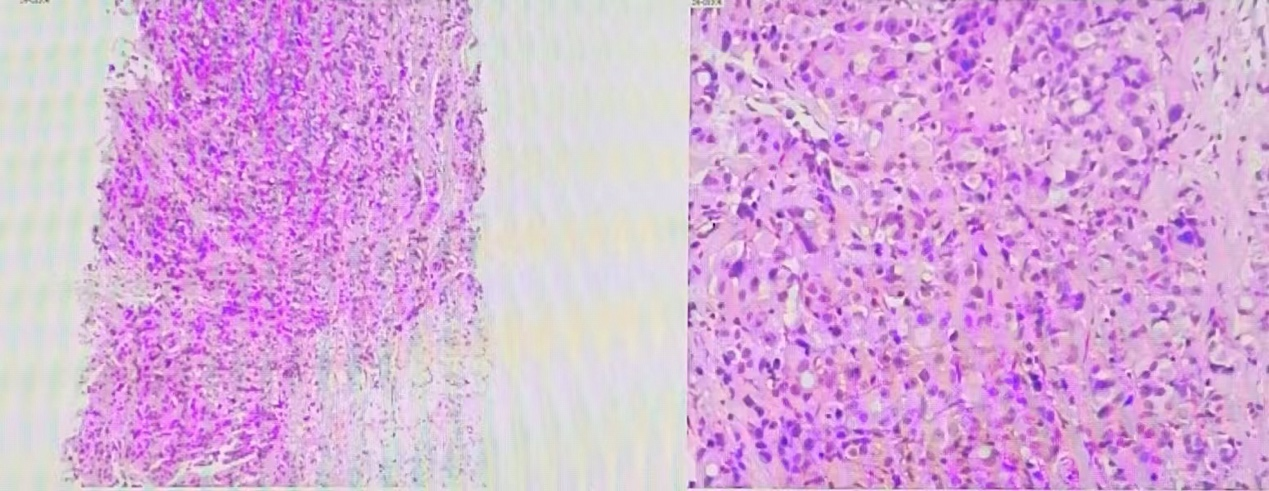 图 穿刺病理结果(2024年05月22日 我院)
图 穿刺病理结果(2024年05月22日 我院)
(左乳11点结节)浸润性癌。
(左侧腋窝淋巴结)可见癌转移。
免疫组化结果:ER (90%,+++), PR (80%,+++), Ki67(40%+), CK5/6(-), P63(-), E - cad (+), P120(膜+), AR (+), EGFR (-), Her-2(0), GATA3(+), CK14(-), GCDFP -15(+)。
穿刺病理结果(2024年05月24日 我院):
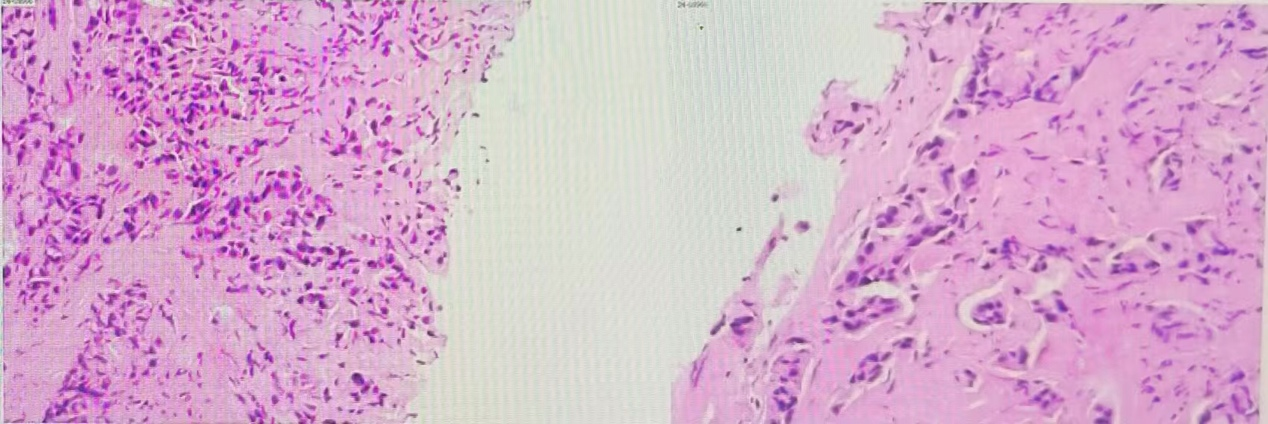 图 穿刺病理结果(2024年05月24日 我院)
图 穿刺病理结果(2024年05月24日 我院)
(右侧胸壁结节)穿刺组织内见条索样、腺样排列的肿瘤细胞,细胞具有异型性,结合病史及免疫组化表型,符合乳腺癌转移。
免疫组化结果:Ckpan(+),GATA3(+),GCDFP-15(+),ER(90%,+++),PR(80%,+++),Her-2(0),Ki67(30%+),S100(-),Mammaglobin(-),Myogenin(-),MyoD1(-),Vimentin(-)。
诊断:
1、右侧胸壁复发
2、左乳浸润癌伴腋窝淋巴结转移cT1N2Mx
3、肺结节:乳腺癌转移?
治疗经过
治疗方案:
综合患者情况,绝经后女性,晚期一线治疗。
CDK4/6抑制剂(瑞波西利 600mg/日q1-21d/28d)+AI(来曲唑 2.5mg po qd)
治疗后效果评估:
乳腺彩超(2024-7-25):
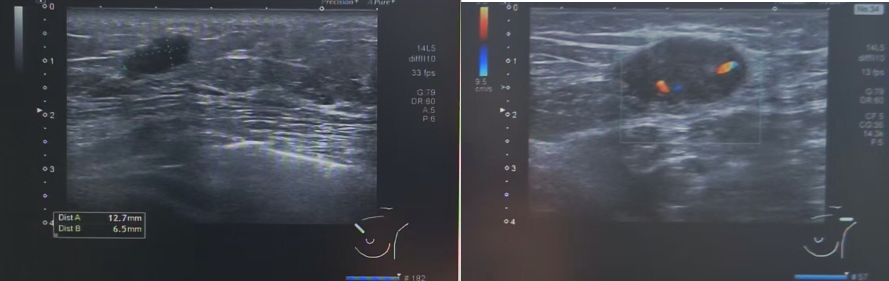 图 乳腺彩超(2024-7-25)
图 乳腺彩超(2024-7-25)
(左):左乳11点结节:1.27*0.65cm;(右):左侧腋窝淋巴结:2.7cm*1.3cm
右侧胸壁结节:较大者约1.22*0.30cm。
左乳11点结节:大小约1.27*0.65cm。
右侧腋下可及低回声区,范围约1.96*0.62cm。
左侧腋窝淋巴结:较大者约2.7*1.3cm。
乳腺彩超(2024-9-2):
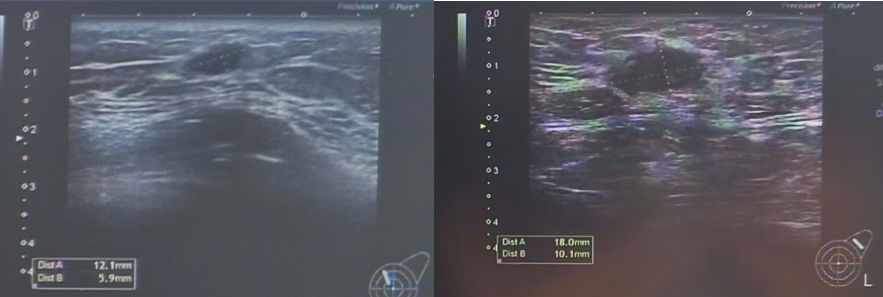 图 乳腺彩超(2024-9-2)
图 乳腺彩超(2024-9-2)
(左):左乳11点结节:1.21*0.59cm;(右):左乳11点结节:1.21*0.59cm
右侧胸壁结节:较大者约1.01*0.35cm。
左乳11点结节: 大小约1.21*0.59cm。
右侧腋下可及低回声区,范围约2.01*0.54cm。
左侧腋窝淋巴结: 较大者约1.8*1.0cm。
乳腺彩超(2024-12-4):
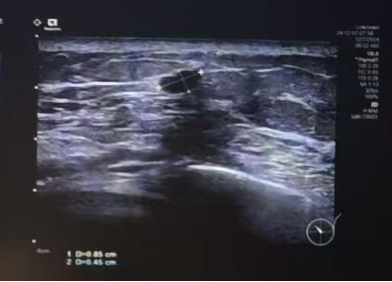 图 乳腺彩超(2024-12-4)
图 乳腺彩超(2024-12-4)
左乳11点结节:0.85*0.45cm
右侧胸壁结节:较大者约0.98*0.25cm。
左乳11点结节: 大小约0.85*0.45cm。
右侧腋下可及低回声区,范围约2.2*0.5cm。
左侧腋窝淋巴结: 较大者约1.4*0.5cm。
乳腺彩超评估肿物变化:
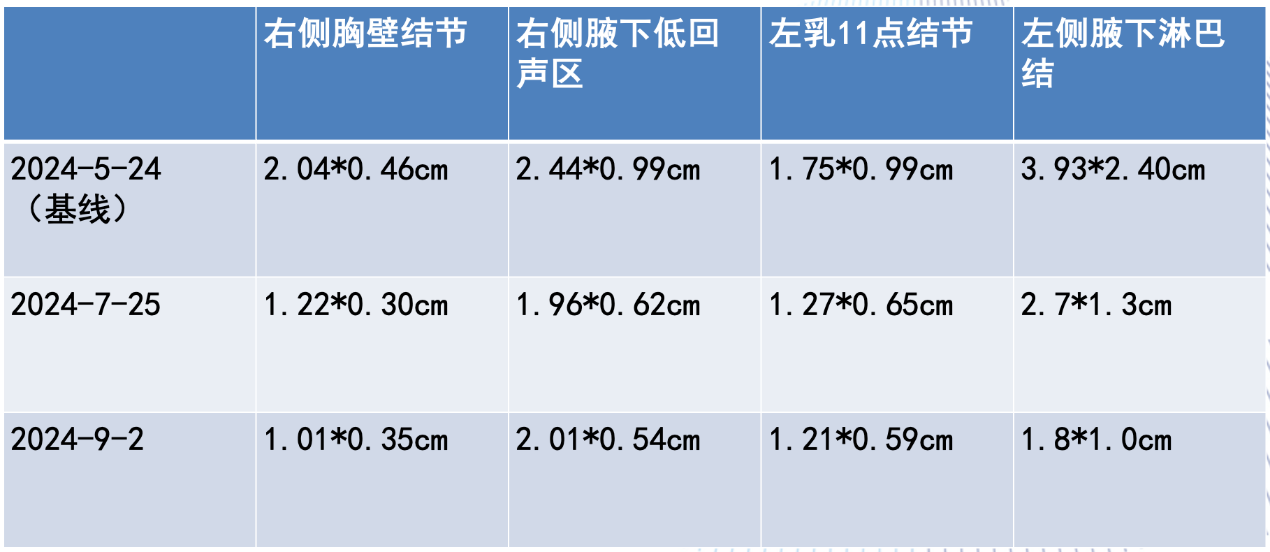 图 乳腺彩超评估肿物变化,见进行性缩小
图 乳腺彩超评估肿物变化,见进行性缩小
胸部CT+冠状面重建(2024-9-2):
1、右侧乳腺术后改变,术区周围皮肤增厚,较前(2024-05-22)减轻,请结合临床。
2、右侧胸背部肌肉肿胀,肌间隙密度增高,较前减轻;右前上纵隔及左侧腋窝多发增大淋巴结影,较前明显减小;左前胸壁皮下多发结节影,较前减小;右侧少量胸水,较前变化不大;右肺下叶实性小结节影,较前变化不明显;均考虑转移,请结合临床。
3、右肺上叶及中叶胸膜下密度增高影,放疗后改变?较前未见明显变化,请结合临床病史考虑。
4、左肺上叶舌段及右肺中叶陈旧索条。
5、双肺肺气肿,右肺下叶肺大泡。
6、主动脉钙化。
胸部CT+冠状面重建(2024-12-4):
1、右侧乳腺术后改变,术区周围皮肤增厚,较前(2024-9-2)未见明显变化,请结合临床。
2、右侧胸背部肌肉肿胀,肌间隙密度增高,较前减轻;右前上纵隔及左侧腋窝多发增大淋巴结影,较前减小;左前胸壁皮下多发结节影,较前减小;右侧胸膜多发结节状增厚,较前程度减轻;右侧少量胸水,较前增多;右肺下叶实性小结节,较前变化不明显;均考虑转移,请结合临床。
3、右肺上叶及中叶胸膜下密度增高影,放疗后改变?较前未见明显变化,请结合临床病史考虑。
4、左肺上叶舌段及右肺中叶陈旧索条。
5、双肺肺气肿,右肺下叶肺大泡。
6、主动脉钙化。

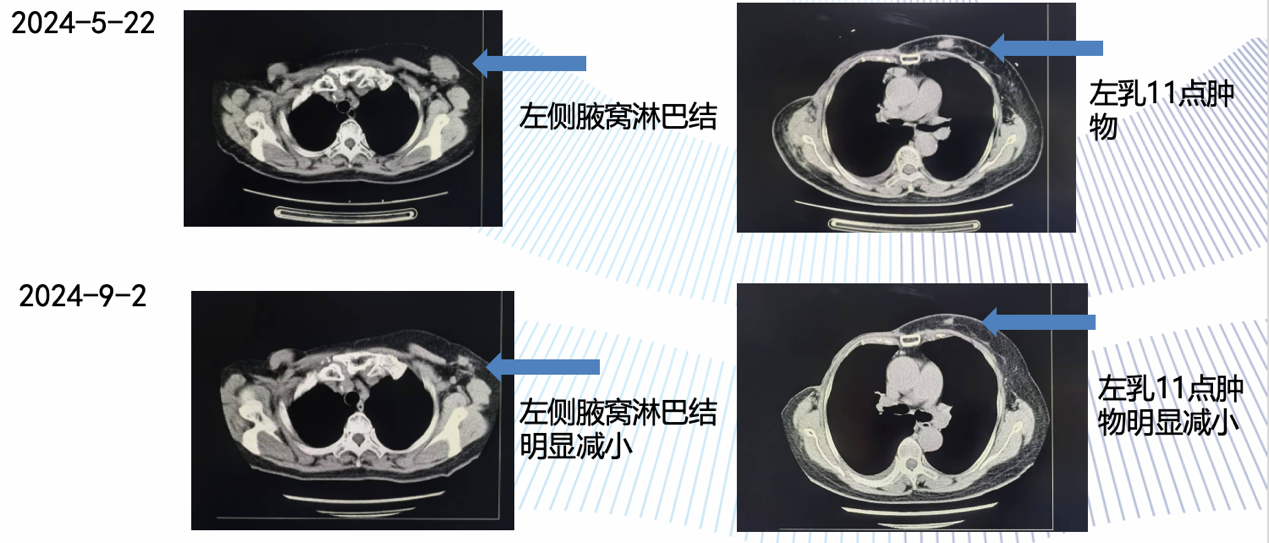 图 胸部CT检查
图 胸部CT检查
总体疗效评估:部分缓解(PR)
病例点评
探寻HR+早期乳腺癌复发风险与管理之策
该病例为69岁HR+/HER2-晚期乳腺癌女性患者,患者曾于十余年前确诊为右乳浸润性导管癌(T3N2M0 III期),术后进行辅助放化疗(单药紫杉醇化疗方案)及内分泌单药治疗(来曲唑),后未及时进行随访复查,于十几年后出现复发转移。
HR+/HER2-作为最常见的乳腺癌亚型,占所有乳腺癌的70%,其中绝大部分为早期可手术患者[1]。辅助内分泌治疗已经显著改善这部分患者的疾病预后,提高患者的生存期,但仍有大约 20% 至 30% 的早期乳腺癌患者面临局部区域或远处的复发风险[2],并且复发风险累积可长达20年[3]。NATALEE研究以临床需求为核心,精准定位HR+早期乳腺癌高复发风险人群,并开创这一类型乳腺癌的全新标准辅助治疗方案。日前,2025欧洲肿瘤内科学会(ESMO)公布的一项真实世界研究,以中、美大样本真实世界数据进一步明确了HR+/HER2-早期乳腺癌的高复发风险人群标准(摘要号:438eP)[4]。该研究指出,符合NATALEE研究入组标准的HR+/HER2-早期乳腺癌患者,复发风险不容小觑,且中美患者表现相似,凸显了符合 NATALEE 纳入标准的患者群体未被满足的治疗需求。
此外,本次ESMO还公布了基于NATALEE研究数据构建的复发风险预测的机器学习模型,预测真实世界中未使用CDK4/6抑制剂的HR+/HER2-早期乳腺癌患者的远处转移、治疗有效性的情况(摘要号:372P)[5]。该研究基于现有的大量真实世界数据构建预测复发风险的模型,展现了未接受CDK4/6抑制剂治疗HR+/HER2-早期乳腺癌患者的复发风险,并推测了瑞波西利辅助治疗为这部分患者带来的潜在获益,再次从统计的角度验证了瑞波西利辅助治疗的临床意义与价值。
本次ESMO中,NATALEE研究亦有重磅更新,其以LBA形势(摘要号:LBA 14)亮相的5年随访数据进一步夯实了瑞波西利辅助治疗的坚实获益,提示意向治疗(ITT)人群中,瑞波西利组5年iDFS率为85.5%(HR=0.716,95%CI 0.618-0.829,P<0.0001)[6],且在各预设亚组中,瑞波西利组展现出一致的获益趋势[6]。
多重循证表明,符合NATALEE研究入组标准的HR+早期乳腺癌复发风险不容小觑,亟需采取瑞波西利联合内分泌治疗方案对复发风险进行管理。本例患者初诊时即为符合NATALEE研究入组特征的患者,然而,十余年前,瑞波西利相关适应症国内尚未获批,且临床及学界对HR+乳腺癌复发风险的认知尚有待提高,因而未使用内分泌联合CDK4/6抑制剂治疗,留下遗憾。并且,该患者术后化疗方案所采取的“单药紫杉醇方案”对于III期乳腺癌患者而言强度偏低,非标准辅助化疗方案,这或许同样为后期复发的隐患之一。
瑞波西利斩获唯一晚期一线PFS、OS双重获益
回到本病例,乳腺癌进入晚期后,临床予以瑞波西利联合来曲唑一线治疗后实现了快速缩瘤的满意效果,令人欣慰。
当前,晚期乳腺癌的临床治疗目标聚焦于缓解临床症状、改善生活质量并尽可能延长患者生存期[7]。在众多CDK4/6抑制剂中,瑞波西利是唯一一款在HR+/HER2-晚期乳腺癌(涵盖绝经前及绝经后人群)一线治疗中同步证实无进展生存期(PFS)与总生存期(OS)双重获益的药物[8,9]。
针对绝经后患者群体的MONALEESA-2研究显示,瑞波西利联合来曲唑相较于安慰剂联合来曲唑,在中位OS方面表现出显著优势,超过63.9个月,较对照组提升逾12个月(风险比[HR]=0.76;p=0.004)[10],使死亡风险下降24%(HR=0.76,P=0.008)。在PFS方面,瑞波西利联合治疗组的中位PFS亦显著优于对照组(25.3个月 vs 16.0个月)[11]。基于其在PFS与OS方面展现的显著临床获益,瑞波西利联合内分泌治疗已成为HR+/HER2-晚期乳腺癌的一线优选方案,并获得美国国家综合癌症网络(NCCN)乳腺癌指南的唯一1类推荐[12],同时被CSCO乳腺癌诊疗指南纳入一线治疗推荐[13]。
除生存获益外,晚期肿瘤的疗效评估日益重视以患者为中心的综合结局。欧洲肿瘤内科学会(ESMO)制定的临床获益量表(MCBS)作为重要评估工具,从生存改善、安全性与生活质量等多维度综合评价药物价值。在此体系下,瑞波西利在HR+晚期一线乳腺癌治疗中获得迄今同类药物中的最高ESMO-MCBS评分[14-16]*,凸显其在疗效与生活质量兼顾方面的卓越表现。
综上,瑞波西利联合内分泌治疗是HR+/HER2-晚期乳腺癌患者实现长期生存与生活质量优化的重要一线治疗选择。
本病例报告展示一例初诊III期、十余后进展为IV期的HR+/HER2-老年乳腺癌患者。尽管其在早期阶段因多方原因未能接受“NATALEE方案”治疗,但在晚期一线使用瑞波西利联合内分泌治疗仍展现出优异疗效。展望未来,期待瑞波西利治疗方案在临床实践中进一步普及,其卓越的临床价值将贯穿乳腺癌诊疗全程,为更多患者带来长期、高质量的生存希望。
*截止目前:2025年10月27日。
[1] 国家肿瘤质控中心乳腺癌专家委员会,等.HR+/HER-2-早期乳腺癌复发风险与临床管理专家共识(2025版).中华肿瘤杂志,2025,47(7):599—616.
[2]Sheffield KM, et al. Future Oncol 2022;18(21):2667-2682.
[3]Pan H, et al.N Engl J Med. 2017;377(19):1836-1846.
[4] Real-world characteristics, treatment patterns, and outcomes in patients with HR+/HER2− early breast cancer from China and the US.2025 ESMO 438eP.
[5] A NATALEE data–based machine learning (ML) model to predict distant recurrence (DR) and treatment (tx) effect in real-world (RW) patients (pts) with HR+/HER2– early breast cancer (EBC) without CDK4/6 inhibitor (CDK4/6i) tx.372P
[6] Adjuvant ribociclib (RIB) plus nonsteroidal aromatase inhibitor (NSAI) in patients (pts) with HR+/HER2− early breast cancer (EBC): NATALEE 5-year outcomes.2025 ESMO LBA14.
[7]国家肿瘤质控中心乳腺癌专家委员会,中国抗癌协会乳腺癌专 业委员会,中国抗癌协会肿瘤药物临床研究专业委员会. 中国晚期乳腺癌规范诊疗指南( 2020 版) [J]. 中华肿瘤杂志,2020,42( 10) : 781-797.
[8]Dickler, Maura N et al. Journal of clinical oncology : official journal of the American Society of Clinical Oncology vol. 34,22 (2016): 2602-9.
[9]Finn Rs, et al.ASCO 2022.LBA1003.
[10]Hortobagyi, et al. Overall survival (OS) results from the phase III MONALEESA (ML)-2 trial of postmenopausal patients with hormone receptor positive/human epidermal growth factor receptor 2 negative (HR+/HER2−) advanced breast cancer (ABC) treated with endocrine therapy (ET) ± ribociclib. Presented at the European Society of Medical Oncology (ESMO) Congress, September 16-21, 2021, (Abstract #LBA17).
[11]Hortobagyi GN, et al. Ann Oncol. 2018 Jul 1;29(7):1541-1547.
[12] NCCN Guidelines Breast Cancer.
[13]CSCO BC诊疗指南(2025年版)
[14] https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-for-solid-tumours/esmo-mcbs-scorecards?scorecard=9.[MONALEESA-2]
[15] https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-for-solid-tumours/esmo-mcbs-scorecards?scorecard=159.[monarch 3]
[16] https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-for-solid-tumours/esmo-mcbs-scorecards?scorecard=7.[PALOMA-2]
[17] US Food and Drug Administration. Clinical trial endpoints for the approval of cancer drugs and biologics. Available at: https://www.fda.gov/media/71195/download. Accessed December.
[18] Matthew P, Masakazu T, Jens H, et al. 2023 SABCS. GS01-12.
[19] Hortobagyi GN, et al. N Engl J Med. 2022;386(10):942-950.
[20] Richard S. Finn, et al.N Engl J Med 2016;375:1925-1936.
[21] Yen-Shen Lu, et al. 2022 Mar 1;28(5):851-859.
[22] Bishal Gyawali, et al. Nat Rev Clin Oncol. 2022 Oct;19(10):613-614.
[23] Oosting SF, et al. Ann Oncol. 2023 Apr;34(4):431-439.
[24] https:// www.esmo.org/guidelines/ esmo-mcbs/ esmo-mcbs-for-solid-tumours/ esmo - mcbs-scorecards/scorecard-338-1. [NATALEE]
排版编辑:肿瘤资讯-CYX












 苏公网安备32059002004080号
苏公网安备32059002004080号


