B细胞急性淋巴细胞白血病(B-ALL)是一种高度侵袭性的血液系统恶性肿瘤,传统治疗手段包括高强度化疗和异基因造血干细胞移植。近年来,免疫疗法的兴起为B-ALL的治疗带来了新的曙光。近日,发表于Journal of the National Comprehensive Cancer Network(JNCCN)杂志的一项重磅综述研究显示,靶向CD19的双特异性抗体贝林妥欧单抗与靶向CD22的抗体药物偶联物奥加伊妥珠单抗(INO),在成人B-ALL一线治疗中展现出显著疗效,不仅大幅提高深度微小残留病造(MRD)阴性率,还能减少高强度化疗依赖,甚至降低异基因干细胞移植需求,为不同年龄、不同分子分型(费城染色体阳性/阴性)的患者带来新希望。此外,嵌合抗原受体T细胞(CAR-T)疗法在复发/难治性(R/R)B-ALL患者中疗效显著,其在一线高危患者中的应用潜力也成为研究焦点。【肿瘤资讯】现将该研究重点内容整理如下,以飨读者。
 本研究为系统性综述,纳入全球多项针对成人B-ALL一线免疫治疗的Ⅱ期、Ⅲ期临床试验,涵盖费城染色体(Ph)阳性与Ph阴性患者,按年龄分层(≤55~60 岁、≥55~60岁)及分子分型分类分析。研究核心评估指标包括完全缓解(CR)率、MRD阴性率[采用多参数流式细胞术(MFC)或下一代测序(NGS)检测]、3年/5年总生存期(OS)率、无复发生存(RFS)率等,同时对比免疫联合方案与传统化疗的安全性差异,简化分析不同免疫药物(贝林妥欧单抗、奥加伊妥珠单抗、CAR-T)与化疗、酪氨酸激酶抑制剂(TKI)的联合策略。
本研究为系统性综述,纳入全球多项针对成人B-ALL一线免疫治疗的Ⅱ期、Ⅲ期临床试验,涵盖费城染色体(Ph)阳性与Ph阴性患者,按年龄分层(≤55~60 岁、≥55~60岁)及分子分型分类分析。研究核心评估指标包括完全缓解(CR)率、MRD阴性率[采用多参数流式细胞术(MFC)或下一代测序(NGS)检测]、3年/5年总生存期(OS)率、无复发生存(RFS)率等,同时对比免疫联合方案与传统化疗的安全性差异,简化分析不同免疫药物(贝林妥欧单抗、奥加伊妥珠单抗、CAR-T)与化疗、酪氨酸激酶抑制剂(TKI)的联合策略。
Ph阴性成人B-ALL:年龄分层显疗效,免疫联合方案优势显著
年轻患者(≤55~60 岁):CR率达100%,3年OS率最高突破100%
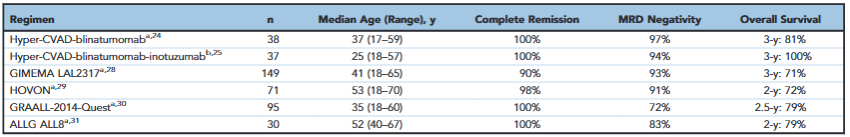
在Ph阴性年轻患者中,多项Ⅱ期试验证实免疫联合方案的卓越疗效。其中,Hyper-CVAD化疗联合贝林妥欧单抗的方案纳入38例中位年龄37岁的患者(55%为高危细胞遗传学特征),患者先接受4周期Hyper-CVAD化疗,高危者(如2周期化疗后MRD阳性、CRLF2过表达等)提前加用贝林妥欧单抗,最终CR率达100%,MRD阴性率97%,3年OS率 81%。
在此基础上加入奥加伊妥珠单抗的优化方案(Hyper-CVAD+贝林妥欧单抗+奥加伊妥珠单抗),纳入3 例中位年龄25岁患者(19%携带TP53突变、13% CRLF2过表达),CR率仍维持100%,MRD阴性率 94%,中位随访26个月时 3年RFS率 90%、OS率 100%,且无肝窦阻塞综合征(SOS)及早期死亡事件。
国际多中心试验同样验证免疫方案的优势:GIMEMA LAL2317试验纳入149例中位年龄41岁患者(21%为Ph样表型、8%携带KMT2A重排),在儿童化疗方案基础上加用2周期贝林妥欧单抗,MRD阴性率从早期巩固后的70%提升至93%,3年OS率 71%,且18~40岁患者3年OS率达76%,显著高于55岁以上患者的49%;HOVON试验针对71例≤70岁患者(含26例Ph阳性),加用贝林妥欧单抗后MRD阴性率 91%,2年OS率 72%,其中≤60岁患者2年OS率 82%,远超61~70岁患者的52%。
Ⅲ期临床试验进一步确认贝林妥欧单抗的巩固价值:ECOG-ACRIN E1910试验纳入488例中位年龄51岁的Ph阴性患者,诱导后MRD阴性者随机分至“化疗+贝林妥欧单抗”组与单纯化疗组,中位随访43个月时,联合组3年OS率 85%(单纯化疗组68%),3年RFS率 80%(单纯化疗组64%),且<55岁患者获益更显著(3年OS率 95% vs 70%)。该结果直接推动2024年6月FDA批准贝林妥欧单抗用于Ph阴性B-ALL巩固治疗。
表1.贝林妥欧单抗和奥加伊妥珠一线治疗年轻新诊断B-ALL患者的研究汇总
老年患者(≥55~60岁):突破“低生存率”困境,无化疗方案显安全性
老年B-ALL患者因常合并TP53突变、不良核型等高危因素,且耐受高强度化疗能力差,传统治疗5年OS率仅10%~20%。而免疫联合低强度化疗或“无化疗”方案,将其生存率提升至40%~50%。
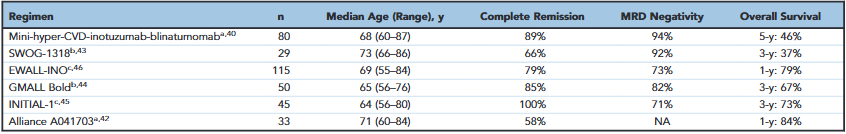
MD安德森癌症中心的Ⅱ期试验显示,60岁以上患者接受“mini-hyper-CVD(低剂量 Hyper-CVD)+奥加伊妥珠单抗+序贯贝林妥欧单抗”方案,80例中位年龄68岁患者(40%携带TP53突变、30%为高危核型)中,CR率 99%,MRD阴性率 94%,中位随访93个月时5年OS率 46%,其中60~69岁患者5年OS率 55%,70岁以上患者 30%,且仅8%患者发生SOS。倾向性评分匹配分析显示,该方案较传统剂量调整Hyper-CVAD化疗,CR率更高(98% vs 88%)、早期死亡率更低(0% vs 8%),3年OS率提升近一倍(63% vs 34%)。
“无化疗”方案进一步降低老年患者治疗毒性:Alliance A041703试验中,33例≥60岁患者接受“奥加伊妥珠单抗诱导+贝林妥欧单抗巩固”,97%患者实现缓解(58%为CR),1年OS率 84%;GMALL Bold试验纳入50例中位年龄66岁患者,采用“低强度化疗+贝林妥欧单抗”,CR率 85%,MRD阴性率 82%,3年OS率 67%,显著高于传统化疗的49%;INITIAL-1试验则用“奥加伊妥珠单抗+地塞米松诱导”,45例中位年龄64岁患者CR率 100%,MRD阴性率 71%,3年OS率 73%。
表2. 贝林妥欧单抗和奥加伊妥珠一线治疗老年新诊断B-ALL患者的研究汇总
Ph阳性成人B-ALL:TKI联合免疫,改写“移植依赖”历史
Ph阳性B-ALL曾因预后极差被称为“白血病中的难题”,传统化疗5年OS率<10%,异基因造血干细胞移植后仅提升至30%~40%。而BCR::ABL1 TKI(伊马替尼、达沙替尼、尼洛替尼、泊那替尼)的应用彻底改变这一局面,尤其泊那替尼可抑制T315I耐药突变,与免疫药物联合后疗效再突破。
泊那替尼联合方案展现“高分子缓解”优势:一项Ⅱ期试验纳入86例新诊断Ph阳性患者(中位年龄46岁),采用“Hyper-CVAD+泊那替尼”,3个月完全分子学缓解(CMR,BCR::ABL1转录本不可检测)率75%,总体CMR率 86%,中位随访6年时6年OS率 75%,且仅23%患者接受异基因造血干细胞移植,landmark分析显示移植未显著提升生存率(6年OS率:移植组 70% vs 非移植组 87%),挑战了异基因造血干细胞移植的标准地位。
PhALLCON Ⅲ期试验进一步验证泊那替尼的一线价值:154例患者接受“泊那替尼+低强度化疗”,34.4%实现诱导后MRD阴性CR,显著高于伊马替尼组的16.7%(尤其≥60岁患者:40.0% vs 10.3%),且泊那替尼组中位无事件生存(EFS)未达到,伊马替尼组仅29个月,安全性方面未增加动脉/静脉血栓风险。该结果推动2024年3月FDA批准泊那替尼用于Ph阳性 B-ALL一线治疗。
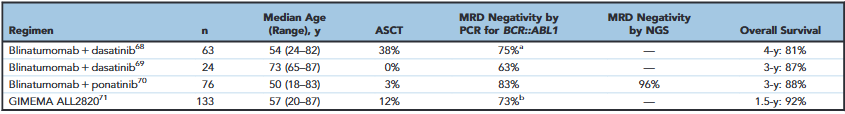
免疫与TKI的“无化疗”联合方案更具突破性:D-ALBA试验中,63例中位年龄54岁的Ph阳性患者接受“达沙替尼+皮质类固醇诱导+贝林妥欧单抗巩固”,60%实现深度分子学缓解(CMR率为41% ),4年OS率 81%;MD安德森试验采用“贝林妥欧单抗+泊那替尼”,60例中位年龄55岁患者(含83岁高龄者)总体CMR率 83%,NGS检测MRD阴性率 98%,仅 3%患者接受泊那替尼,中位随访24个月时3年OS率 91%、EFS率 77%,且未影响贝林妥欧单抗介导的T细胞应答。
表3. 新诊断Ph阳性急性淋巴细胞白血病的无化疗方案
免疫疗法清除MRD:改善预后的“关键一步”
MRD是B-ALL预后的核心预测因素,即使患者达到CR,MRD阳性仍意味着高复发风险。研究显示,贝林妥欧单抗与奥加伊妥珠单抗在MRD清除中表现优异:一项多中心研究纳入116例MRD阳性患者,接受贝林妥欧单抗治疗后78%实现MRD阴性,4年OS率 45%,其中MRD转阴者4年OS率 52%;MD安德森的Ⅱ期试验中,37例CR1/CR2期MRD阳性患者接受贝林妥欧单抗,73%实现MRD阴性的CR,3年OS率 67%,CR1期患者OS率达72%。
奥加伊妥珠单抗同样可有效清除MRD:MD安德森的Ⅱ期试验中,26例CR1/CR2期MRD阳性患者(13例曾接受贝林妥欧单抗)接受奥加伊妥珠单抗,69%实现MRD阴性,2年OS率 60%;GIMEMA ALL2418试验中,39例MRD阳性患者接受奥加伊妥珠单抗,44%患者MRD转阴,且10例成功桥接至移植。
CAR-T疗法:一线高危患者的“新选项”
CAR-T疗法在复发/难治B-ALL中疗效显著,目前正探索其在一线高危患者中的巩固价值。真实世界数据显示,低肿瘤负荷患者接受CAR-T治疗获益更显著:41例MRD阳性或CNS1/2期患者接受tisagenlecleucel,98%实现缓解,≥3级细胞因子释放综合征(CRS)发生率仅 10%(高肿瘤负荷组35%),1年OS率 85%(高肿瘤负荷组58%)。
针对老年患者的CAR-T研究同样取得进展:一项Ⅰ/Ⅱ期试验采用“记忆细胞富集型CD19 CAR-T”治疗14例≥55岁CR1期患者(中位年龄68岁),无≥2级CRS或免疫效应细胞相关神经毒性综合征(ICANS),中位随访244天无死亡,仅1例Ph阳性患者出现分子复发,经移植后仍维持缓解。
在Ph阳性患者中,CAR-T联合TKI展现协同作用:18例新诊断Ph阳性患者接受“达沙替尼+长春新碱+泼尼松诱导+序贯CD19/CD22 CAR-T”,CD19 CAR-T后CMR率72%,CD22 CAR-T后提升至77%,中位随访13.5个月时14例维持CMR,且无需ASCT。
结论
本综述证实,贝林妥欧单抗与奥加伊妥珠单抗纳入成人B-ALL一线治疗,可显著提高CR率、MRD阴性率及长期生存率,减少高强度化疗及移植需求,且在Ph阳性与Ph阴性、年轻与老年患者中均具疗效。CAR-T疗法在一线高危患者(如持续MRD、TP53突变、KMT2A重排)中的巩固潜力值得期待,而NGS等超高敏MRD检测技术,可帮助精准筛选需强化治疗(如CAR-T、移植)的患者。
未来研究方向将聚焦三大领域:一是优化免疫药物联合策略(如皮下注射贝林妥欧单抗以提高便利性、降低成本);二是探索无化疗方案在≥70岁老年患者中的长期安全性与疗效;三是针对免疫治疗后复发患者,开发CD19/CD22双靶点CAR-T、维奈克拉为基础的联合方案等新疗法,进一步改善成人B-ALL的整体预后。
Haddad F G, Kantarjian H, Short N J, et al. Incorporation of Immunotherapy Into Adult B-Cell Acute Lymphoblastic Leukemia Therapy[J]. Journal of the National Comprehensive Cancer Network, 2025, 23(8).
排版编辑:mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


