不可切除的Ⅲ期非小细胞肺癌(NSCLC)因其高度异质性,成为了临床治疗领域中极具挑战性的一大难题。近年来,随着医学技术的不断发展和新治疗策略的不断涌现,患者的治疗效果和生存质量正在逐步提高。其中,同步放化疗(cCRT)后序贯免疫巩固治疗的出现,无疑是这一领域的重大突破,为患者带来了新的希望与曙光。然而临床中,很多患者因高龄、合并症或体能状态差等原因无法耐受cCRT。针对这些患者,临床研究和实践探索了多种替代方案。多项研究已证实[1-4],长春瑞滨在晚期NSCLC一线治疗以及局晚期NSCLC同步放疗中,具有显著的临床获益和良好的安全性,为临床优化放化疗管理策略提供了更多可能,对于无法耐受静脉含铂化疗方案的患者,口服单药长春瑞滨也展现出很好的临床疗效。本期特别分享一例老年ⅢB期NSCLC患者的治疗经历。该患者确诊为低分化鳞癌后接受了4周期的新辅助化疗联合免疫治疗。虽然最佳疗效达到了部分缓解(PR),但患者在治疗期间出现2级骨髓抑制,出现贫血貌并合并高血压等。由于患者身体状态较差,外科团队评估手术风险大,建议放疗。基于指南推荐和患者综合身体状态评估,经过多学科会诊(MDT)的综合评估,临床团队决定为患者采用口服长春瑞滨软胶囊节拍化疗同步放疗的方案,随后进行PD-L1单抗免疫维持治疗。目前,该患者已坚持免疫治疗23个月,病情持续PR状态,且耐受性良好。
病例分享
中国医学科学院肿瘤医院
中国临床肿瘤学(CSCO)会员
主持CSCO青年课题1项,参与多项国内多中心的临床研究
以第一作者发表学术论文SCI数篇
病例介绍
患者:男,61岁。
主诉:诊断左肺下叶低分化鳞癌3月余。
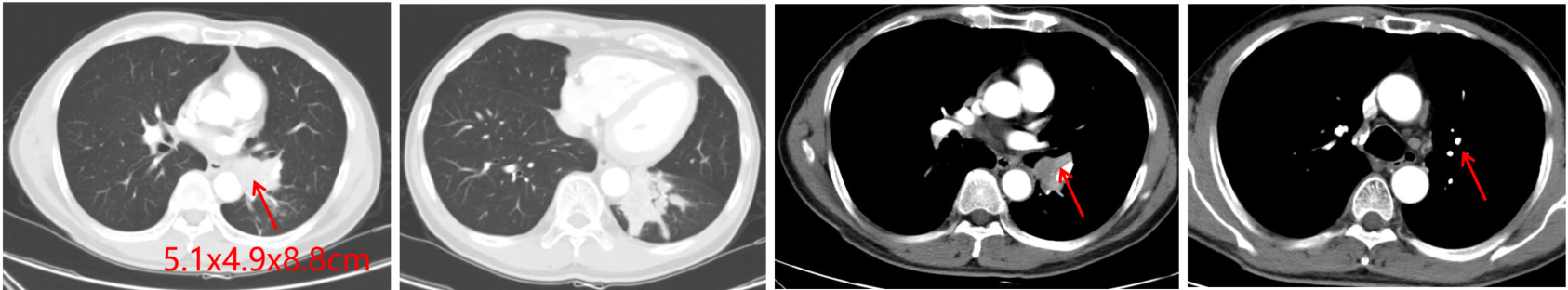
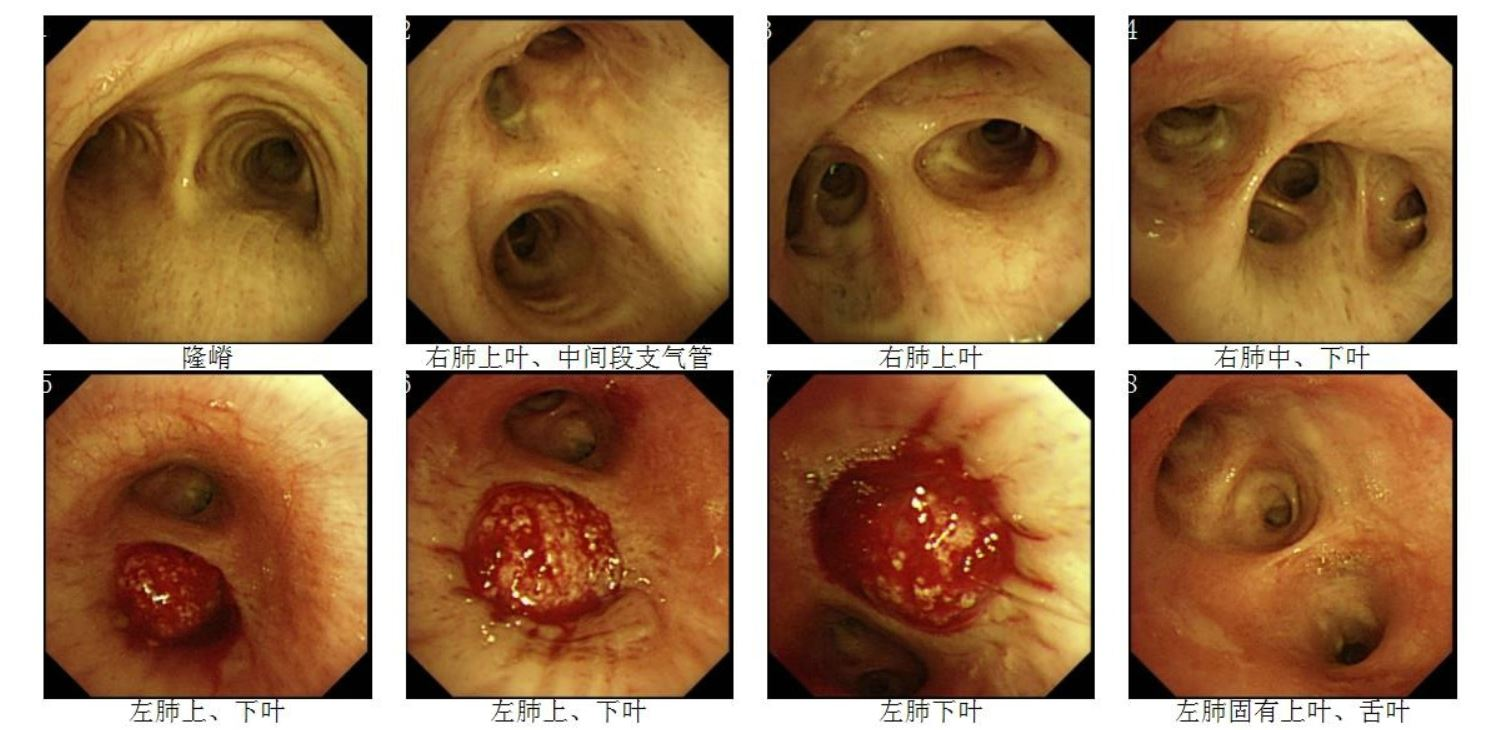
现病史:2022年11月,患者因咯血于我院行CT检查,结果示:左肺下叶肿物,大小约5.1×4.9×8.8cm,伴左肺门和纵隔淋巴结转移(图1)。行支气管镜活检示:左肺下叶,低分化鳞癌;免疫组化:PD-L1 Neg(-),PD-L1(22C3)(TPS=1%),AE1/AE3(3+)(图2)。2022年12月至2023年2月,患者于外院行4周期新辅助化免治疗(TP方案+ PD-L1单抗),期间出现2级骨髓抑制。2023年3月,患者完成4周期化免治疗后来我院继续治疗。
既往史及个人史:既往高血压病史,有吸烟史(20支/日×40年),无饮酒史,无肿瘤家族史。
体格检查:ECOG评分1分,贫血貌,头顶部可见一皮下结节,双颈未及肿大淋巴结。
辅助检查:
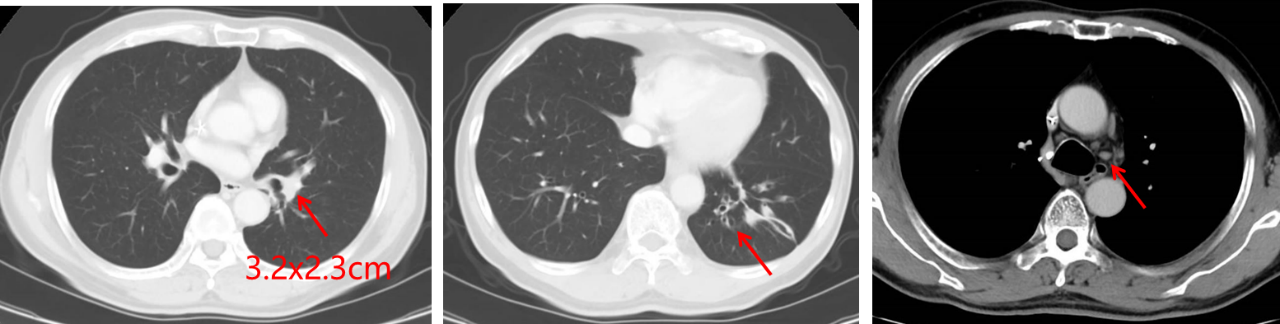
放疗前CT示(2023-03-14,图3):原左肺下叶支气管根部不规则肿物,边界不清,最大截面约3.2×2.3cm,支气管狭窄较前减轻、减少;纵隔8区、左肺门淋巴结,较前缩小、减少,其中孤立大者短径约0.4cm;纵隔4R/L、5、7区及右肺门多发淋巴结,大者短径约0.9cm,同前相仿;右肺多发磨玻璃密度结节,同前相仿,大者约0.8x0.8cm;肝脏多发囊肿,同前相仿;甲状腺多发低密度结节。
肿瘤标志物:细胞角蛋白19片段(cyfra21-1):3.33ng/ml;鳞状细胞癌相关抗原(SCC):2 pg/ml。
血液检查:肝肾功能、电解质、血常规无明显异常。
肺功能检查:轻度阻塞性通气功能障碍。
脑MR(2022-11-21、2023-03-14):1、右侧顶部皮下结节,考虑良性;2、右侧枕部皮肤表面外突结节,请结合临床查体。
全身骨扫描(2022-11-25、2023-03-16):全身骨骼未见明显异常。
临床诊断:左肺下叶低分化鳞癌(AJCC第8版分期:T3N2M0 ⅢB期)
左肺门和纵隔7区、8区、4L区淋巴结转移
4周期化免治疗后PR
高血压3级(低危)
肝囊肿
甲状腺结节
治疗过程
口服长春瑞滨节拍化疗同步放疗:
2023.4.01-2023.5.23,自放疗定位时开始,口服长春瑞滨软胶囊 30mg(周一、三、五),直至放疗结束。
2023.4.10-2023.5.23,予局部容积调强放疗(VMAT),放疗靶区如图4,具体剂量:95% PGTV 60.2Gy/2.15Gy/28F,95% PTV 50.4Gy/1.8Gy/28F。
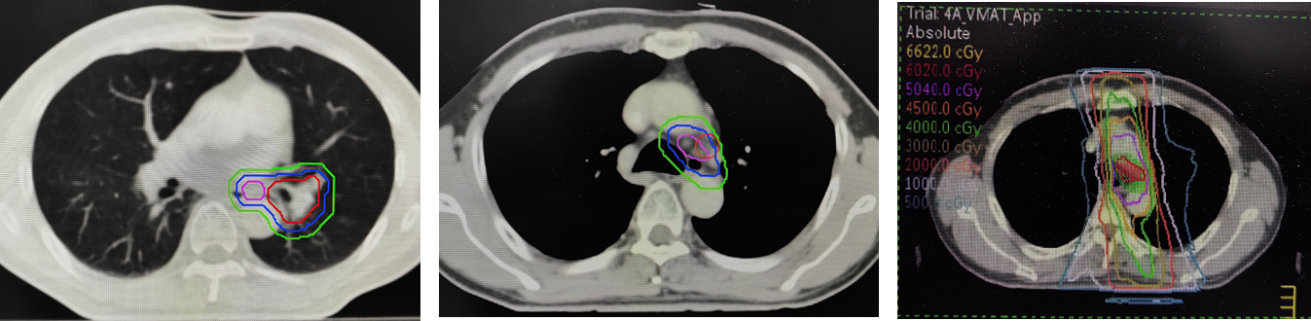
治疗期间出现的不良反应:
首次口服长春瑞滨时出现1级消化道反应:恶心、呕吐,当天自行缓解;
放疗期间出现Ⅰ级白细胞减少(3.29x10^9/L);轻度贫血,血红蛋白Ⅰ级降低;
放疗期间出现放疗相关1级放射性食管炎,给予康复新口服液治疗后缓解。
免疫维持治疗:
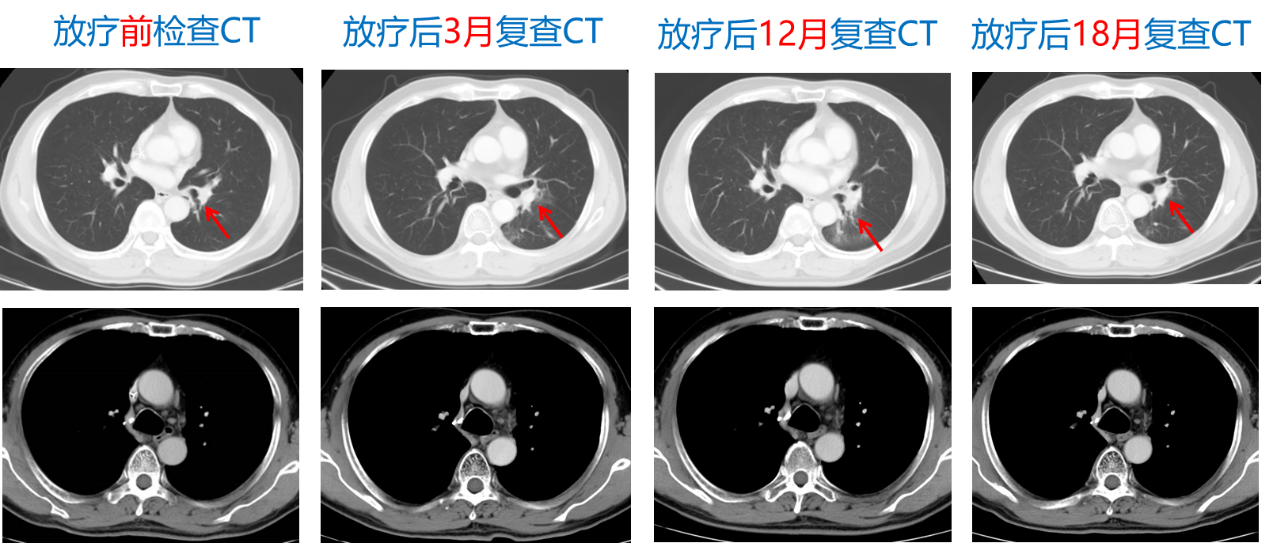
2023-07至今,给予PD-L1单抗巩固免疫维持治疗,疗效复查:持续PR状态。
专家点评
国家癌症中心
中国医学科学院肿瘤医院放疗科胸部肿瘤组
中华放射肿瘤学编委
中国抗癌协会放疗专委会青年委员
中国老年学和老年医学学会老年肿瘤分会委员
华人肿瘤放射治疗协作组放射免疫工作委员会委员
中国人体健康科技促进会肿瘤化疗专业委员会委员
北京肿瘤防治研究会转化医学分委委员
北京肿瘤病理精准诊断研究会青委会委员
擅长肺癌、食管癌和胸腺恶性肿瘤的放射治疗、同步放化疗以及放疗与免疫治疗的综合治疗
新辅助化免治疗带来临床挑战,后续治疗方案亟待优化
约20%~25%的NSCLC患者初诊时处于Ⅲ期[5]。Ⅲ期NSCLC具有高度异质性,其中大多数患者肿瘤不可切除,病情更为复杂,这使得临床治疗面临更大的挑战。近年来,免疫治疗在可切除NSCLC患者中取得了里程碑式进展。对于驱动基因阴性的潜在可切除和不可切除Ⅲ期NSCLC患者,新辅助/诱导治疗有机会缩小肿瘤体积、消除微转移、降低肿瘤复发风险,从而增加根治性切除的机会。新辅助化疗联合免疫治疗也逐渐成为可切除NSCLC(Ⅱ-Ⅲ期)患者的常见治疗策略。然而,尽管新辅助治疗能够降低患者的死亡风险,但避免不了免疫治疗相关毒副反应的增加。其中,3级~4级的不良反应发生率高达66%,会严重影响患者的预后[6]。此外,从外科角度来看,新辅助化疗联合免疫治疗可能会使手术切除变得更加复杂。在接受新辅助化疗联合免疫治疗的患者中,16%~22%的患者未能按计划接受NSCLC切除术,主要原因包括疾病进展、不良反应(AE)或变得不适合手术[7],但这些患者绝大部分对静脉含铂方案的同步放化疗耐受性明显降低。在临床实践中,也有部分不可切除Ⅲ期NSCLC患者因年老、虚弱、合并症等原因无法耐受cCRT。临床需进一步优化治疗方案,以提高临床获益。
口服长春瑞滨节拍化疗同步放疗减毒不减效,成为临床治疗更优解
在化疗方面,节拍化疗是一种持续、高频率、低剂量的新型给药模式。相比常规化疗,节拍化疗以肿瘤组织内增殖的血管内皮细胞和基质细胞为靶点,在减少药量的同时加大给药频率,使血药浓度长时间维持在较低的稳定水平,不仅能够减少不良反应,而且可以减缓耐药[8-10]。此外,研究表明,节拍化疗可以通过影响肿瘤细胞及肿瘤微环境发挥抗肿瘤效应,还表现出了激活免疫作用[8-10]。而放疗能够通过破坏肿瘤细胞的DNA来杀死肿瘤细胞,但肿瘤细胞的增殖和修复能力会影响放疗的效果。节拍化疗可以通过抑制肿瘤细胞的增殖和修复能力,改善肿瘤微环境,增加肿瘤细胞对放疗的敏感性。同时,放疗可以影响药物的药代动力学特性,例如通过改变局部组织的血流和通透性,影响化疗药物的分布和代谢。可见,节拍化疗同步放疗可以更好地发挥药物的抗肿瘤作用,同时减少药物的毒副作用[11]。
长春瑞滨作为微管蛋白抑制剂,是节拍化疗最理想的药物之一[8]。口服制剂在临床应用中更具便捷性优势,对患者的生活质量影响更小,更易被患者接受,能够显著提升患者的治疗依从性和医疗体验。一项针对中国晚期NSCLC患者的Ⅱ期研究,评估了口服与静脉注射长春瑞滨联合顺铂的疗效、耐受性及药代动力学特性。研究结果显示,口服长春瑞滨在维持与静脉注射相当的高疗效的同时,优化了治疗的便利性,可作为静脉注射长春瑞滨用于一线治疗晚期NSCLC的有效替代方案[1]。MOVE研究探索了口服长春瑞滨节拍化疗在老年晚期NSCLC患者中的疗效与安全性。结果显示[2],长春瑞滨一线治疗的总体临床获益率达58.1%,中位无进展生存期(PFS)为5个月,中位OS为9个月,且安全性良好,严重毒性反应罕见。可见,在年老体弱患者中,口服长春瑞滨节拍化疗是一种安全且有效的治疗选择。RENO研究结果亦显示[3],口服剂型长春瑞滨+顺铂与依托泊苷+顺铂并联合放疗在局部晚期NSCLC中的疗效相似,且口服剂型长春瑞滨联合治疗的毒副作用更少。HORG研究探索了口服长春瑞滨节拍化疗联合顺铂一线治疗ⅢB/Ⅳ期NSCLC的疗效及安全性,结果显示[4],ORR达37.1%,DCR为65.7%,且安全性可接受,最常见的3~4级不良事件为中性粒细胞减少症。
先前亦有多项单臂、小型研究已证实,口服长春瑞滨用于局部晚期NSCLC同步放化疗的安全性及有效性[12]。容积调强弧形放疗(VMAT)是一种基于图像引导放疗,结合逆向优化治疗计划系统和高精度加速器,并在三维剂量验证的保证下实施的先进的放疗技术。VMAT具有更大的照射范围、更灵活的调整、更精准的照射和更好的剂量聚焦效果,能够更精确地针对肿瘤进行治疗,最大限度地保护周围正常组织[13,14]。
经充分讨论,本例患者在完成新辅助化疗联合免疫治疗后,接受了口服长春瑞滨节拍化疗联合VMAT的方案进行治疗,并在治疗后接受了巩固免疫维持治疗。至今,患者已坚持免疫治疗23个月,病情保持PR状态,且耐受性良好。可见,对于老年、体弱、伴有多种并发症以及新辅助化疗联合免疫治疗后因不良反应无法耐受静脉化疗的不可切除Ⅲ期NSCLC患者,口服长春瑞滨节拍化疗联合放疗后免疫维持治疗可以为患者带来持久的疗效、良好的安全性和更佳的生活质量。
近期,中国医学科学院肿瘤医院在JNCC杂志发表的一项Ⅱ期前瞻性研究进一步验证了这一方案的价值。研究结果显示[15],中位随访22.5个月,中位PFS达18.0个月,中位OS尚未达到,且治疗相关不良反应可控,未观察到任何3/4级毒性事件。该研究再次夯实了口服长春瑞滨联合放疗在不可切除Ⅲ期NSCLC中的循证基础,为临床实践提供了有力证据。
[1] Yunpeng Yang, Jianhua Chang, Cheng Huang, et al. A randomised, multicentre open-label phase II study to evaluate the efficacy, tolerability and pharmacokinetics of oral vinorelbine plus cisplatin versus intravenous vinorelbine plus cisplatin in Chinese patients with chemotherapy-naive unresectable or metastatic non-small cell lung cancer[J]. J Thorac Dis. 2019 Aug;11(8):3347-3359.doi: 10.21037/jtd.2019.08.22.
[2]Andrea Camerini , Cheti Puccetti , Sara Donati ,et al. Metronomic oral vinorelbine as first-line treatment in elderly patients with advanced non-small cell lung cancer: results of a phase II trial (MOVE trial).BMC Cancer . 2015 May 6;15:359.
[3]Dolores Isla, Ramón De Las Peñas, Amelia Insa, et al. Oral vinorelbine versus etoposide with cisplatin and chemo-radiation as treatment in patients with stage III non-small cell lung cancer: A randomized phase II (RENO study). Lung Cancer. 2019 Sep:135:161-168. doi: 10.1016/j.lungcan.2018.11.041. Epub 2018 Dec 1.
[4] P Katsaounis, A Kotsakis, S Agelaki, et al. Cisplatin in combination with metronomic vinorelbine as front-line treatment in advanced non-small cell lung cancer: a multicenter phase II study of the Hellenic Oncology Research Group (HORG)[J]. Cancer Chemother Pharmacol. 2015 Apr;75(4):821-7.
[5]Bartolomeo V, Cortiula F, Hendriks LEL, De Ruysscher D, Filippi AR. A Glimpse Into the Future for Unresectable Stage Ⅲ Non-Small Cell Lung Cancer. Int J Radiat Oncol Biol Phys. 2024 Apr 1;118(5):1455-1460. doi: 10.1016/j.ijrobp.2023.11.005. Epub 2023 Dec 27. PMID: 38159097.
[6]倪军,黄淼,张力,等.非小细胞肺癌围手术期免疫治疗相关不良反应管理的临床诊疗建议[J].中国肺癌杂志,2021,24(03):141-160.
[7]Paula Ugalde Figueroa, Valérie Lacroix, Paul E Van Schil. Neoadjuvant Chemoimmunotherapy Complicates Subsequent Surgical Resection and Adjuvant Immunotherapy Is Preferable From the Surgical Standpoint. J Thorac Oncol. 2024 Jun;19(6):858-861. doi: 10.1016/j.jtho.2024.02.009.
[8]祝情情,谢超,宋宝,等.节拍化疗在晚期非小细胞肺癌治疗中的应用[J].国际肿瘤学杂志, 2019, 46(6):4.DOI:10.3760/cma.j.issn.1673-422X.2019.06.013.
[9]Browder T, Butterfield CE, Kräling BM, Shi B, Marshall B, O'Reilly MS, Folkman J. Antiangiogenic scheduling of chemotherapy improves efficacy against experimental drug-resistant cancer. Cancer Res. 2000 Apr 1;60(7):1878-86.
[10] Cem,Simsek,Ece,et al.Metronomic Chemotherapy: A Systematic Review of the Literature and Clinical Experience[J].Journal of Oncology, 2019.DOI:10.1155/2019/5483791.
[11] Yu-Jen Chen, Tung-Hu Tsai, Li-Ying Wang, et al. Local Radiotherapy Affects Drug Pharmacokinetics—Exploration of a Neglected but Significant Uncertainty of Cancer Therapy[J]. Technol Cancer Res Treat. 2017 Dec;16(6):705-716. doi: 10.1177/1533034617737011.
[12] Francesco Perri, Grazia Lazzari, Giuseppina Della Vittoria Scarpati, et al. Oral vinorelbine: a feasible and safe partner for radiotherapy in the treatment of locally advanced non-small cell lung cancer[J]. Onco Targets Ther. 2016 Apr 19:9:2359-64. doi: 10.2147/OTT.S103645. eCollection 2016.
[13]蔡俊涛,陈凡,王财,等.非小细胞肺癌容积旋转调强与适形调强放疗的剂量学比较[J].中国医学物理学杂志,2018,35(04):389-393.
[14]关明丽,雷亚楠,李贺.不同调强放疗技术在局部晚期非小细胞肺癌根治性放疗中的剂量参数比较[J].现代医药卫生,2023,39(22):3848-3854.
[15]Xinrong Lian, Gulidanna Shayan, Shijie Yang, et al. Efficacy and safety of oral vinorelbine with concurrent radiotherapy in unresectable stage III non-small cell lung cancer following neoadjuvant chemoimmunotherapy: a single-arm, phase 2 trial[J]. Journal of the National Cancer Center, Available online 21 July 2025.
排版编辑:TanRongbing











 苏公网安备32059002004080号
苏公网安备32059002004080号


