
李逸琪, 费凯伦, 王志杰. 抗体偶联药物在HER-2变异非小细胞肺癌中的治疗现状和未来[J]. 中华肿瘤杂志, 2025, 47(1): 86-93. DOI: 10.3760/cma.j.cn112152-20240416-00151.
非小细胞肺癌是肺癌主要的组织病理类型之一,约占肺癌总数的85%。人表皮生长因子受体2(HER-2)变异包括基因突变、基因扩增和蛋白过表达,是非小细胞肺癌的重要驱动靶点之一,在非小细胞肺癌患者中,HER-2基因突变、HER-2基因扩增和HER-2蛋白过表达的发生率分别在1%~6.7%、1.4%~22%和7.7%~23%之间。目前针对HER-2变异非小细胞肺癌的治疗方案仍比较有限,小分子抗肿瘤药物的开发进度不尽如人意,传统治疗效果欠佳,临床上迫切需要更为有效的治疗药物。抗体偶联药物(ADC)是靶向特定肿瘤细胞的单克隆抗体和细胞毒药物的高效组合,成为实现肿瘤“精准治疗”的新选择。在不同HER-2变异非小细胞肺癌患者亚型中,ADC药物已展开广泛的探索,并已在部分患者中取得较好的疗效。文章着重阐述HER-2变异非小细胞肺癌的治疗现状以及ADC类药物在HER-2变异非小细胞肺癌中的研究进展,探讨其在非小细胞肺癌中的发展前景。
【关键词】 肺肿瘤;非小细胞肺癌;人表皮生长因子受体2;抗体偶联药物;精准治疗
非小细胞肺癌(non-small cell lung cancer, NSCLC)是肺癌主要的组织病理类型之一,约占肺癌总数的85%。目前发现的NSCLC驱动基因达数十种,人表皮生长因子受体2(human epidermal growth factor receptor 2, HER-2)变异是NSCLC的重要基因异常之一,部分变异形式具有较强驱动性。在NSCLC中,HER-2变异可分为基因突变、基因扩增和蛋白过表达,三者的发生率分别在1%~6.7%、1.4%~22%和7.7%~23%。不同HER-2变异类型之间少有重叠,提示这些变异在影响肿瘤细胞命运及其转移侵袭能力方面可能存在差异,由此导致患者具有不同的临床特征及预后,诊疗策略也有所不同。目前在我国针对HER-2变异NSCLC的治疗方案主要参考无驱动靶点的NSCLC使用化疗或免疫治疗,而既往HER-2靶向疗法的探索中,HER-2酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKI)和抗HER-2单克隆抗体等治疗效果均不尽人意。因此,亟需探索更加有效且安全的HER-2靶向疗法。
靶向HER-2的新型抗体偶联药物(antibody-drug conjugate, ADC)由单克隆抗体、细胞毒性药物和连接子组成,通过精准靶向HER-2异常肿瘤细胞并经内吞作用释放毒性药物,为实现肿瘤的“精准治疗”提供了新的选择。临床前研究显示,HER-2基因突变或基因扩增可增强肺癌细胞对细胞膜上HER-2的受体内化作用,从而增强对HER-2-ADC的内吞作用。提示ADC类药物在HER-2变异NSCLC中,尤其是存在基因激活突变或基因扩增时,可能具有独特疗效。德曲妥珠单抗(DS-8201)是目前全球首个由美国食品药品监督管理局获批用于HER-2突变晚期NSCLC的HER-2靶向药物,并于2023年在我国获批用于HER-2阳性及HER-2低表达乳腺癌的治疗,也期待其在国内获得肺癌的适应证。鉴于HER-2-ADC药物在HER-2变异的NSCLC中的应用被广泛关注,本文将阐述HER-2变异NSCLC的治疗现状及探索,着重探讨HER-2-ADC在NSCLC中的研究现状及未来发展方向,以期帮助优化临床实践。
在我国,对于HER-2变异NSCLC患者的治疗主要参考无驱动基因NSCLC的治疗方案,通常选择含铂类药物的双药化疗±免疫检查点抑制剂或抗血管生成药物,但从现有研究结果来看,化疗联合免疫治疗疗效并不优于化疗,可能与HER-2激活下游PI3K/AKT信号通路导致免疫抑制有关,抗血管生成药物联合化疗虽有一定程度的改善,但仍无法满足临床需求。因此目前临床上亟需针对HER-2突变的NSCLC患者寻求更有效的靶向治疗策略和手段。
目前HER-2靶向药物主要有TKI、单克隆抗体以及ADC。既往临床数据表明,HER-2-TKIs在HER-2突变NSCLC中的疗效十分有限,其中表现相对较好的吡咯替尼在HER-2突变NSCLC的后线治疗中的中位无进展生存时间(progression-free survival, PFS)和中位总生存时间(overall survival, OS)仅为6.4~6.9个月及12.9~14.4个月。靶向HER-2的曲妥珠单抗联合化疗治疗HER-2突变NSCLC也不尽如人意,后线治疗的PFS仅为4.8个月;而对于HER-2基因扩增及过表达的NSCLC,曲妥珠单抗联合化疗的一线治疗客观有效率(objective response rate, ORR)仅为36%,PFS为6.1个月。此外,曲妥珠单抗和帕妥珠单抗联合双靶向治疗在HER-2变异NSCLC患者中的ORR也仅为13%~21%。
不同于HER-2-TKIs、单克隆抗体的临床疗效表现,HER-2-ADC的出现给HER-2变异NSCLC患者带来生存获益,尤其是HER-2基因突变NSCLC。目前以恩美曲妥珠单抗和德曲妥珠单抗为主的HER-2-ADC正在探索治疗HER-2变异NSCLC。相比于恩美曲妥珠单抗在HER-2突变的晚期NSCLC患者中ORR仅为38.1%,中位PFS和中位OS分别仅为2.8和8.1个月,德曲妥珠单抗给HER-2变异NSCLC患者带来了更为明显的生存获益,尤其是HER-2基因突变NSCLC。
德曲妥珠单抗的疗效优势可能得益于其特殊的结构优化。德曲妥珠单抗采用可裂解的四肽连接子及高毒性化疗药物喜树碱类似物DXd,增强了抗肿瘤活性,缩短了半衰期并提高了ADC复合体稳定性,同时具有旁观者效应。德曲妥珠单抗的旁观者效应降低了对靶抗原表达水平的需求,同时其链接的DXd能够对肿瘤细胞起到更强的杀伤作用。然而ADC在单纯HER-2蛋白过表达NSCLC中虽然有较好的疗效但相较于HER-2过表达乳腺癌仍有一定差距,推测可能与HER-2内在化及泛素化机制有关,但该领域仍需深入研究,这也表明不同肿瘤中HER-2过表达的机制和临床意义有所差异。
(一)HER-2-ADC在NSCLC中的疗效及安全性
1. 恩美曲妥珠单抗: 恩美曲妥珠单抗目前已获批用于治疗HER-2阳性转移性乳腺癌患者,既往在肺癌中的探索数据提示,HER-2基因突变NSCLC患者可能是潜在获益人群,在HER-2基因扩增及蛋白过表达人群中疗效则相对有限。一项单中心的Ⅱ期试验证实,49例HER-2基因突变或扩增的晚期NSCLC患者接受恩美曲妥珠单抗3.6 mg/kg 每3周1次治疗的ORR为51%,中位PFS为5个月。一项Ⅱ期试验显示,22例HER-2外显子20插入突变的NSCLC患者在接受恩美曲妥珠单抗治疗后,ORR为38.1%,中位PFS和中位OS分别仅为2.8和8.1个月。而对于HER-2蛋白过表达[免疫组织化学(immunohistochemistry, IHC) 2+或3+]NSCLC患者,既往研究提示IHC 2+和IHC 3+人群的临床获益率分别仅为7%和30%,其中IHC 3+组部分患者存在HER-2基因突变和基因扩增。另一项研究结果也表明,恩美曲妥珠单抗对经治HER-2 IHC/荧光原位杂交检测阳性患者治疗,无患者获得肿瘤应答,中位PFS和中位OS分别为2.0和10.9个月。整体来看,尽管美国国立综合癌症网络(National Comprehensive Cancer Network, NCCN)指南已将恩美曲妥珠单抗作为晚期HER-2突变NSCLC的治疗推荐,但其主要数据主要来源于小样本单臂研究,临床获益十分有限,且缺乏高级别证据支持其广泛应用于临床中。
2. 德曲妥珠单抗: 德曲妥珠单抗在HER-2基因突变晚期NSCLC患者后线治疗目前已有研究数据公布,其在HER-2突变NSCLC中展现出良好持续的抗肿瘤活性,并能够带来较为持久的临床获益。一项Ⅰ期研究中,德曲妥珠单抗对经治HER-2基因突变NSCLC患者显示出良好的抗肿瘤活性,ORR达到72.7%,中位PFS为11.3个月。随后,更大样本量的多中心、开放标签Ⅱ期临床研究DESTINY-Lung01探索了德曲妥珠单抗对HER-2基因突变(队列2)晚期非鳞NSCLC的疗效及安全性,其中队列2中91例HER-2基因突变的晚期NSCLC患者接受德曲妥珠单抗 6.4 mg/kg 每3周1次治疗的ORR为55%,中位PFS和中位OS分别为8.2和18.6个月;在不同HER-2突变类型的患者中均观察到治疗应答。但安全性方面,≥3级药物相关不良事件发生率为46%,尤其26%的患者发生了药物相关的间质性肺病,也使其安全性问题引发重视。为了更好的平衡疗效和安全性,随机、多中心、国际、双臂Ⅱ期临床试验DESTINY-Lung02对德曲妥珠单抗5.4 mg/kg或6.4 mg/kg两种剂量治疗经治晚期HER-2基因突变NSCLC的疗效和安全性进行了探索,其中102例患者接受5.4 mg/kg 每3周1次和50例患者接受6.4 mg/kg每3周1次治疗的ORR分别为49.0%和56.0%,中位PFS分别为9.9和15.4个月,中位OS分别为19.5个月和未达到。而安全性方面,两组药物相关≥3级治疗中出现不良反应的发生率分别为38.6%和58.0%,其中药物相关间质性肺病发生率分别为12.9%和28.0%,与6.4 mg/kg组相比,德曲妥珠单抗 5.4 mg/kg组的安全性明显更优。近期公布的亚洲亚组的疗效和安全性结果与总人群分析一致,提示其在亚洲患者中可取得同样的治疗获益。此外,德曲妥珠单抗DESTINY-Lung01和DESTINY-Lung02研究的汇总分析显示出良好的颅内疗效,5.4 mg/kg和6.4 mg/kg组的颅内ORR分别为25.0%和18.5%,部分患者实现了颅内完全缓解。在我国开展的一项开放标签、Ⅱ期临床研究DESTINY-Lung05显示,在72例既往经治HER-2基因突变晚期NSCLC患者中,接受5.4 mg/kg德曲妥珠单抗治疗后ORR为58.3%,12个月内PFS率为55.1%。总体而言,德曲妥珠单抗在HER-2突变的转移性NSCLC中表现出剂量依赖性的疗效,但其不良反应也与剂量有着较为密切的联系,因此综合考虑疗效及安全性后,5.4 mg/kg成为推荐剂量,并也取得了较为令人满意的疗效。基于此,NCCN、美国临床肿瘤协会、欧洲肿瘤内科学会及中国临床肿瘤学会等国内外权威指南也已将德曲妥珠单抗作为既往经治HER-2基因突变晚期NSCLC的治疗推荐。德曲妥珠单抗5.4 mg/kg也在美国、欧盟、日本等多个国家地区获批用于治疗既往接受过全身治疗的不可切除或转移性HER-2突变NSCLC患者。
对于HER-2蛋白过表达NSCLC,在DESTINY-Lung01研究的队列1中对HER-2蛋白过表达(IHC 2+或3+)进行了探索,提示德曲妥珠单抗 6.4 mg/kg 和5.4 mg/kg 每3周1次的ORR分别为26.5%和34.1%,中位缓解持续时间(median duration of response, DoR)分别为5.8和6.2个月,中位PFS分别为5.7和6.7个月,中位OS分别为12.4和11.2个月。在DESTINY-Lung 01中,接受德曲妥珠单抗治疗的经中心确认的HER-2阳性(IHC 3+)NSCLC患者确认的ORR为52.9%,中位DoR为6.2个月。近期基于DESTINY-PanTumor02、DESTINY-Lung01和DESTINY-CEC02研究,德曲妥珠单抗在美国食品药品监督管理局获批用于既往接受过系统治疗且没有其他有效治疗方案的不可切除或转移性HER-2阳性(IHC 3+)实体瘤成人患者。目前正在进行的DESTINY-Lung 03正在评估HER-2过表达(IHC 2+或3+)NSCLC患者对于德曲妥珠单抗联合免疫治疗及化疗的安全性及耐受性。一项Ⅰ期临床试验(NCT04042701)正在评估HER-2过表达NSCLC患者对于德曲妥珠单抗联合免疫治疗的安全性及耐受性。同时目前有研究提到德曲妥珠单抗在HER-2低表达(IHC 1+或IHC 2+/原位杂交阴性)的乳腺癌中也能发挥疗效,德曲妥珠单抗在HER-2低表达的NSCLC中是否也能同样存在良好的临床效果也是未来值得探索的方向之一。
综上,德曲妥珠单抗在HER-2基因突变或过表达NSCLC中均表现出抗肿瘤活性,其中对HER-2基因突变NSCLC的疗效尤为明显。但也应注意,在肺癌患者中,5.4 mg/kg德曲妥珠单抗治疗后3级及以上药物相关间质性肺炎的发生率(2.4%)要高于乳腺癌患者(0.8%),既往接受过和未接受过程序性死亡受体1(programmed cell death-1, PD-1)/程序性死亡受体配体1(programmed cell death-ligand 1, PD-L1)单抗治疗的患者在接受5.4 mg/kg德曲妥珠单抗治疗后间质性肺炎发生率分别为14.9%和7.4%,因此德曲妥珠单抗与PD-1/PD-L1单抗的联合方案是否会进一步提高3级及以上间质性肺炎发生率仍需进一步观察。德曲妥珠单抗在乳腺癌患者中间质性肺炎的发生率下降,这得益于相关指南共识的指导,加强了预防和管理措施。因此,在NSCLC患者接受德曲妥珠单抗治疗过程中,可根据2022年发表的《抗肿瘤药物相关间质性肺病诊治专家共识》,通过早期发现和预防以降低间质性肺炎的发生率。此外,除了HER-2-ADC药物,目前临床上还有其他在研的ADC类药物值得关注。
(二)HER-2-ADC在NSCLC中的在研临床研究
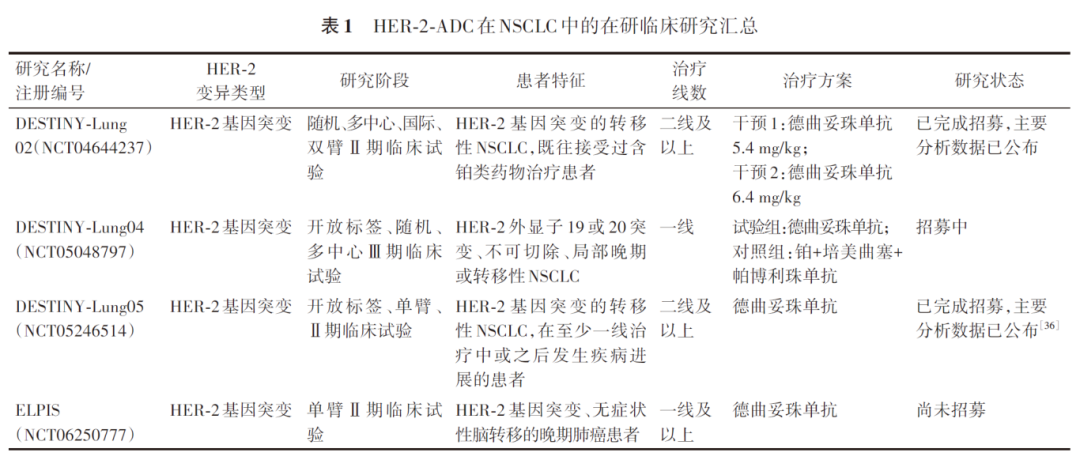
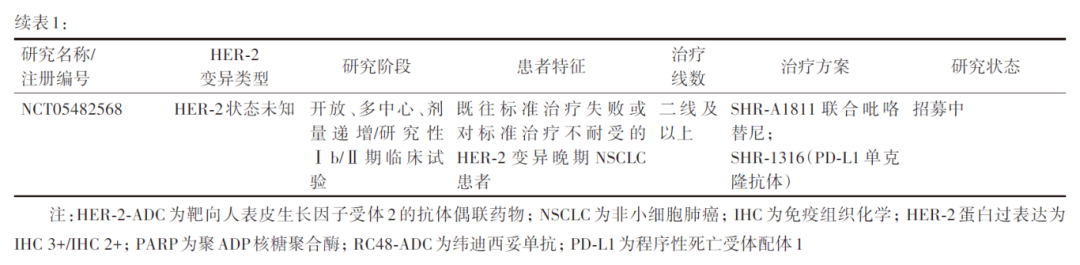
以德曲妥珠单抗为代表的HER-2-ADC作为HER-2突变NSCLC新的标准治疗方案,开启了肺癌HER-2靶向疗法的探索之路。当前,包括德曲妥珠单抗在内的多款HER-2-ADC(如A166、RC48、SHR-A1811等)都在肺癌领域开展疗效和安全性的初步研究(表1)。
其中A166的Ⅰ~Ⅱ期临床试验主要分析已公布,其披露结果显示,在HER-2蛋白过表达患者中,在4.8 mg/kg剂量下,A166获得了100%的ORR,其中1例为NSCLC阳性患者。在一项Ⅰ/Ⅱ期单臂临床研究中,50例既往接受3线及以上治疗的HER-2基因突变晚期NSCLC患者接受SHR-A1811治疗后,ORR为40.0%,中位PFS为10.8个月,但间质性肺炎仍是需要关注的不良反应。鉴于小样本研究所固有的偏差风险,A166和SHR-A1811的治疗效果和安全性尚待更大规模研究的验证与确认。尽管如此,不断积累的临床研究成果正在巩固HER-2-ADC在肺癌治疗领域的重要角色,并昭示着未来随着更多详尽临床研究的开展,HER-2-ADC药物有望为携带HER-2突变的NSCLC患者提供更多生存获益的可能性。


目前临床上对于HER-2变异NSCLC的治疗存在显著未满足的需求。以德曲妥珠单抗为代表的HER-2-ADC通过结构优化,兼具靶向和高效杀伤肿瘤细胞的作用,在晚期HER-2基因突变及蛋白过表达NSCLC的治疗中展现疗效。当前安全性数据显示患者可耐受适当剂量,部分不良反应如胃肠道反应、血液学不良反应、间质性肺病等可通过早期监测和干预得以控制。安全性是ADC药物是否可以广泛应用的重要制约因素,因此尚需进一步探索其特有的不良反应及处理方法。
鉴于HER-2-ADC在后线治疗中的积极成果,有望向前线及早期围术期治疗推进,并拓宽至HER-2基因扩增、蛋白过表达以及中枢神经系统转移的NSCLC患者群体。同时也应意识到,ADC类药物的本质是更精准的化疗,精准的使用高毒性药物杀伤肿瘤细胞,因此耐药是必然需要面对的问题。联合治疗可能是解决这一问题的重要方法,ADC与免疫检查点抑制剂或选择性HER-2-TKIs联合可能产生协同效应,这为解决预后差的HER-2过表达NSCLC及耐药问题提供新的治疗策略。
进一步改进HER-2-ADC设计,如提升载药效率、优化连接子及载荷新型药物等,提升抗肿瘤效果并降低不良反应将有助于提升ADC类药物的疗效。同时需深入探索不同HER-2变异类型在肺癌中的作用机制及其靶向治疗反应,并建立针对肺癌患者的HER-2变异诊断标准。深入了解各类HER-2变异的分子生物学基础,对于实现个性化精准治疗至关重要。未来,随着HER-2-ADC应用范围的扩大及更多治疗方案的研发,将有望为HER-2变异肺癌患者提供更多个性化治疗选择。
最后,优化HER-2变异检测技术标准,以及确立明确的cut-off阈值,是确保HER-2-ADC有效应用不可或缺的前提步骤。针对HER-2变异的不同检测技术手段对ADC治疗反应预测价值亟待深化研究和论证。
参考文献略。











 苏公网安备32059002004080号
苏公网安备32059002004080号


