随着奥希替尼联合化疗(FLAURA2研究)以及埃万妥单抗联合Lazertinib(MARIPOSA研究)的成功,EGFR突变阳性的晚期非小细胞肺癌(NSCLC)的一线治疗进入了新的“十字路口”。在2025年美国临床肿瘤学会(ASCO)年会教育专场上,开启了一场题为“艰难抉择:EGFR+转移性NSCLC的一线治疗困境”的激烈辩论。会议由来自Fox Chase癌症中心的Jessica R. Bauman博士主持,她首先强调了共同决策(Shared Decision-Making)和姑息治疗在复杂治疗选择中的核心作用。随后,来自丹娜法伯癌症研究所的Julia K. Rotow博士与来自罗马生物医学大学的Alessio Cortellini博士就“奥希替尼单药”与“联合治疗”作为一线标准的优劣展开了激烈辩论。
背景:一线治疗的复杂新格局
奥希替尼基于FLAURA研究显示的生存获益,已成为EGFR突变NSCLC一线治疗的基石 。然而,近期公布的FLAURA2和MARIPOSA研究数据打破了这一稳定格局。两项研究均表明,与奥希替尼单药相比,奥希替尼联合化疗或埃万妥单抗联合Lazertinib能够显著延长无进展生存期(PFS),其中MARIPOSA研究还显示了总生存期(OS)的获益趋势。这为临床医生和患者带来了“幸福的烦恼”:是选择更强的联合方案以追求最长生存,还是坚守耐受性更优的单药治疗?
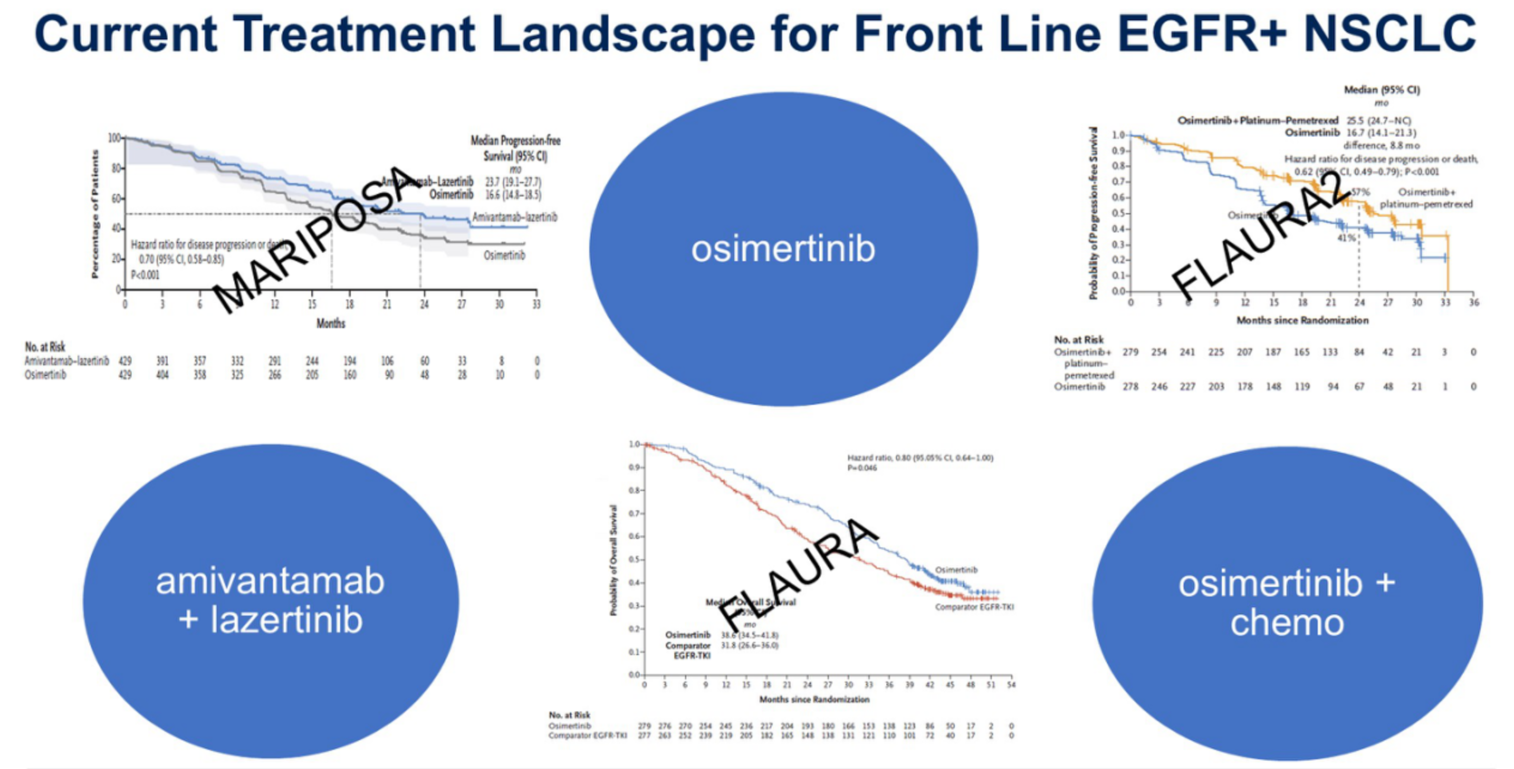
主持人观点:共同决策与早期整合姑息治疗是抉择的核心
Bauman博士在开场演讲中指出,理想的治疗应兼具“高效、低毒、低成本、高便利性”。然而,当前的三种主要选择各有侧重:
奥希替尼单药:中高疗效,毒性较低,成本相对较低,便利性高(口服)。
奥希替尼+化疗:疗效更高(PFS),但毒性、成本更高,便利性更低(含静脉输注)。
埃万妥单抗+Lazertinib:疗效更高(PFS和OS趋势),但同样伴随更高的毒性、成本和更低的使用便利性。
Bauman博士强调,选择的关键在于平衡疗效与毒性,而这种平衡的支点因人而异。研究表明,尽管许多患者愿意为生存获益承受更大毒性,但仍有相当一部分患者(约21%)会因毒性增加而拒绝能带来6个月OS获益的治疗方案。大多数患者希望深度参与治疗决策过程。
此外,Bauman博士提出,肺癌诊断本身会给患者带来巨大的生理、心理和经济负担。早期整合姑息治疗作为循证的干预措施,能有效改善患者的生活质量、情绪状态、疾病认知,并为家属提供支持,是实现整体护理(Holistic Care)的重要组成部分。
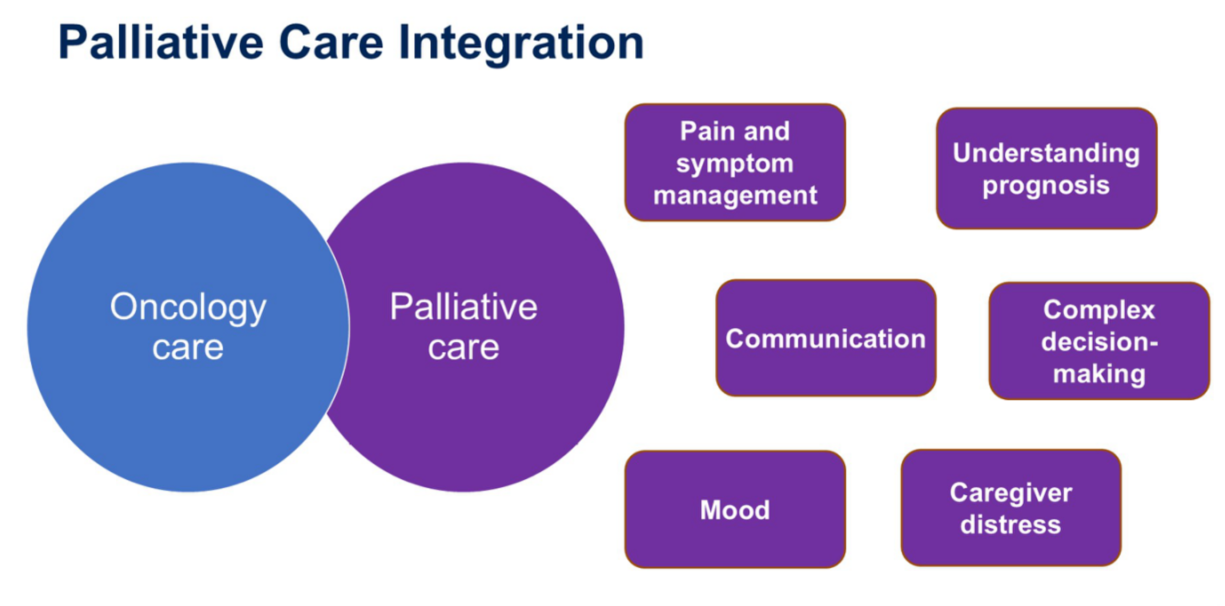
正方观点:奥希替尼单药仍是许多患者的优选
Rotow博士主张奥希替尼单药治疗在当前格局下依然是许多患者的最佳选择。其核心论点如下:
临床试验与真实世界的差距:FLAURA2和MARIPOSA研究的入组标准严格,排除了许多体能状态不佳或伴有合并症的患者。一项真实世界研究显示,超过半数的患者不符合FLAURA研究的入组标准。因此,将试验数据直接外推至更广泛、更脆弱的真实世界人群时需格外谨慎。
低风险患者从联合治疗中获益有限:对于携带EGFR 19外显子缺失、无TP53共突变或基线ctDNA阴性等“低风险”特征的患者,奥希替尼单药本身就能带来较长的PFS。在这些亚组中,联合治疗带来的PFS绝对获益可能仅有数月,患者是否值得为此承受显著增加的毒性和生活质量的下降,是一个需要深思的问题。
毒性与生活质量的代价是真实存在的:联合治疗显著增加了血液学毒性、皮疹、甲沟炎等不良事件的发生率和严重程度。更重要的是,它带来了巨大的“时间毒性”,患者需要更频繁地往返医院接受静脉输注和处理不良反应。Rotow博士强调,一线治疗或许是患者唯一能经历“口服、耐受性良好”治疗的窗口期,一旦选择联合方案,便意味着放弃了这段宝贵的高质量生活时间,因为后续治疗几乎都是毒性更大、更不便的静脉方案。
真实世界的治疗策略可延长单药疗效:临床实践中,对于单药治疗后出现寡进展的患者,可通过局部放疗等手段处理进展病灶,从而继续从奥希替尼治疗中获益,这种策略在临床试验的PFS分析中并未得到充分体现。
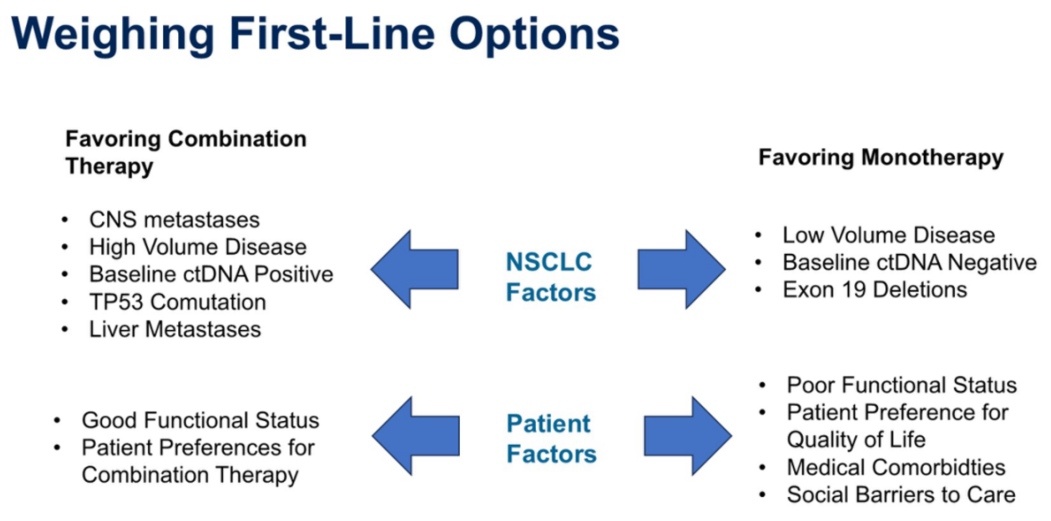
反方观点:联合治疗应作为一线首选以实现疗效最大化
Cortellini博士认为联合治疗应作为所有适合患者的一线标准。其主要论据包括:
避免跨线治疗失败的巨大风险:这是Cortellini博士最核心的论点。他引用数据显示,无论是在历史上的TKI试验还是在最新的FLAURA2和MARIPOSA研究中,都有大量(25%-54%)患者在疾病进展后因各种原因未能接受有效的二线治疗。这意味着,如果不在一线使用最有效的方案,将有近三分之一的患者可能永远失去从该方案中获益的机会。
亚组分析的局限性与“好预后”患者的潜在治疗不足:他指出,不应依赖探索性的亚组分析来筛选出所谓的“低风险”患者。在MARIPOSA研究中,即使是在没有脑转移、TP53野生型等“好预后”特征的亚组中,联合治疗依然显示出优于单药治疗的趋势。仅对高风险患者使用强化方案,可能意味着对“好预后”患者的治疗不足。
毒性的可管理性与长期耐受性:Cortellini博士认为,联合治疗的毒性是可控的。毒性反应多在治疗早期出现,并会随着时间推移和剂量调整而减轻。同时,随着预防性方案(如针对皮疹的COCOON方案)和给药方式的改进(如皮下注射的埃万妥单抗),毒性管理将愈发成熟,从而实现长期耐受。
一线治疗是一项“长期投资”:他引入了“限制平均生存时间(RMST)”这一统计学概念,指出在生存曲线延迟分离的情况下,RMST能更好地评估长期获益。分析显示,联合治疗的生存获益随时间推移呈指数级增长,这是一项着眼于未来的“长期投资”。此外,联合方案可能诱导更简单的耐药机制,为后续治疗创造有利条件。
现场讨论
在讨论环节中,专家们就几个关键问题进行了探讨:
进展后如何排兵布阵:一线奥希替尼单药进展后,目前的主流选择是埃万妥单抗联合化疗(MARIPOSA-2方案)。而一线联合方案进展后的治疗选择则更为棘手和缺乏数据。与会者一致认为,在疾病进展时进行再次活检基因检测至关重要。
年龄的角色:专家们普遍认为,生理年龄本身不是决定治疗强度的唯一标准,患者的生理功能、合并症和整体健康状况更为重要。
试验设计:对于MARIPOSA研究未允许对照组交叉使用埃万妥单抗的问题,专家们认为未来的临床试验应强制或强烈鼓励交叉设计,以便更真实地回答“联合在前”与“单药序贯治疗治疗”的优劣。
结论
本次辩论会清晰地展示了EGFR突变晚期NSCLC一线治疗选择的复杂性。不存在适用于所有患者的“唯一正确答案”。
Rotow博士的观点代表了对生活质量、患者个体耐受性和避免过度治疗的深切关注,尤其是在获益尚不明确的低风险人群中。
Cortellini博士的观点则强调了最大化一线疗效、克服治疗线间患者流失的紧迫性,代表了对延长生存的追求。
最终的临床决策必须回归到以患者为中心的共同决策模式。医生需要综合评估疾病的生物学特征(如突变类型、肿瘤负荷)、患者的个体因素(如年龄、体能、合并症),并与患者及其家属进行充分沟通,清晰阐述不同方案的潜在获益(PFS、OS)与风险(毒性、生活成本、时间成本),最终共同选择最符合患者个人价值观和生活目标的治疗策略。同时,整合姑息治疗,为患者提供全程的身心支持,是应对这一复杂决策过程不可或缺的一环。
排版编辑:肿瘤资讯-TY











 苏公网安备32059002004080号
苏公网安备32059002004080号


