尽管激素受体阳性(HR+)/人表皮生长因子受体2阴性(HER2-)早期乳腺癌患者经过标准内分泌治疗后普遍预后良好,但临床实践证实部分患者仍受疾病复发的威胁。为进一步了解过去十年内在中国接受标准治疗的HR+/HER2-早期乳腺癌患者的3年和5年的复发风险,帮助患者实现早期治愈目标,中国医学科学院肿瘤医院的徐兵河院士团队开展了一项《基于中国国家癌症数据库的HR+/HER2-早期乳腺癌患者早期复发风险评估的回顾性研究》1。这项针对中国人群的大样本量研究于2024年SABCS大会公布,【肿瘤资讯】特邀徐兵河院士详细解读中国HR+/HER2-早期乳腺癌的复发风险及本研究的重要意义。
肿瘤内科专家,北京协和医学院长聘教授、博士生导师
曾任中国医学科学院肿瘤医院大内科主任
现任国家新药(抗肿瘤)临床研究中心主任
国家肿瘤质控中心乳腺癌专家委员会主任委员
国家抗肿瘤药物临床监测专家委员会主任委员
中国抗癌协会肿瘤药物临床研究专业委员会主任委员
中国抗癌协会乳腺癌专业委员会名誉主任委员
中国医药教育协会肿瘤临床科研创新发展专业委员会主任委员
中国医师协会内科医师分会副会长
北京乳腺病防治学会理事长
跨度十年、大样本量回顾性分析证实,中国HR+早期乳腺癌存在巨大未被满足的需求
2024 SABCS公布的回顾性分析中,纳入了2013年1月至2022年12月期间在中国国家癌症数据库中的3295例HR+/HER2-早期乳腺癌 (I-III期患者)。患者年龄中位数为49岁(范围为22-80岁)。I期、II期和III期患者占比分别为22.1%、47.3%和30.6%。62%的患者有淋巴结转移(LN+)。92.1%的患者接受了辅助内分泌治疗,其中96例(3.2%)接受了CDK4/6抑制剂联合治疗。无复发生存期(RFS)定义为从手术到复发的时间。
表1. HR+/HER2-早期乳腺癌患者的基线特征和治疗模式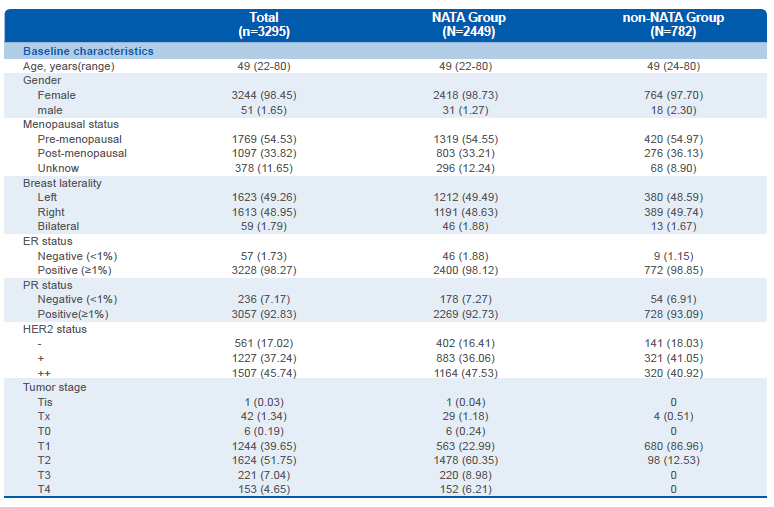
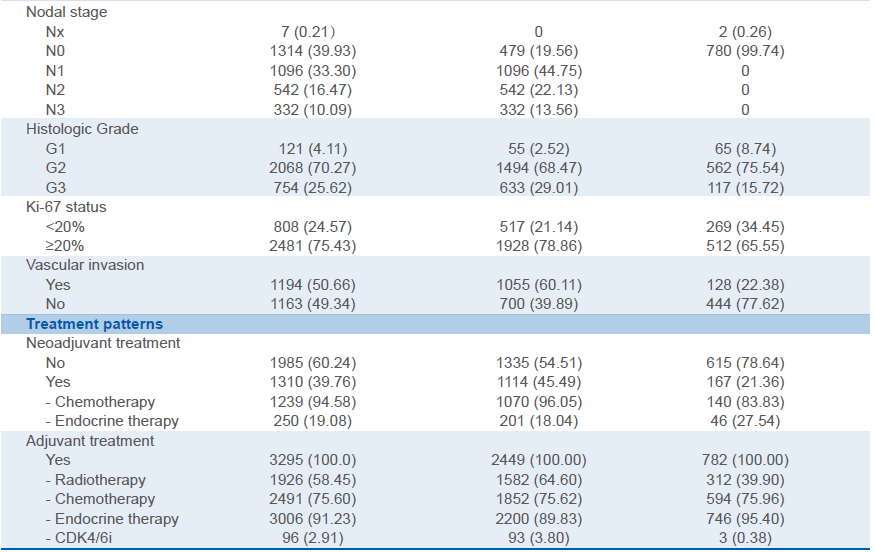
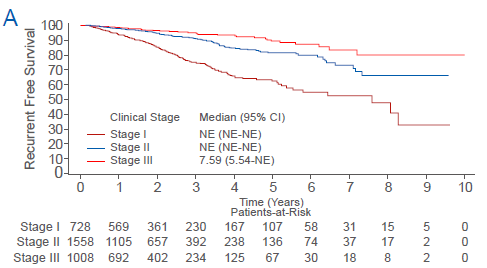
分析结果显示,随访中位时间为20.8个月,总人群的3年和5年RFS率分别为87.3%和77.5%。III期、II期和I期患者的3年RFS率分别为75.1%、91.2%和95.2%。与I期相比,III期(HR= 4.77,95% CI 3.35-6.79)和II期(HR=1.51,95% CI 1.03-2.20)患者的复发风险显著较高。更重要的是,符合NATA Group条件的患者的复发风险高于不符合条件(non-NATA Group)的患者(3年RFS率分别为83.9%和95.3%,HR=2.90, 95% CI 2.08-4.04)。其中,NATA-Group的患者定义为II~III期、淋巴结阳性(N+)或淋巴结阴性(N0)伴高危因素的患者。
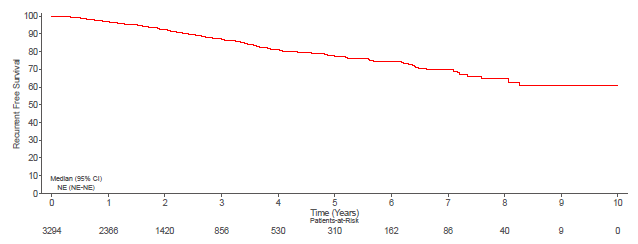
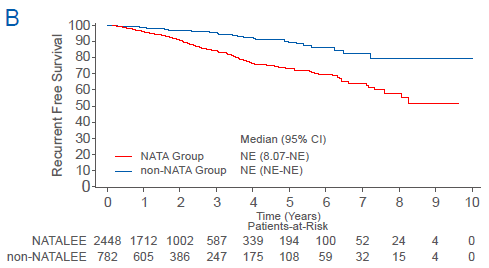
本研究证实,II-III期中国早期乳腺癌的3年复发风险较高,并且符合NATA Group条件的患者复发风险显著更高。未来如何降低这部分HR+/HER2-早期乳腺癌患者的复发风险,实现更多患者临床治愈成为临床医生特别关注的问题。
纵观全球,中国HR+乳腺癌患者具有年轻化、分期晚、预后差等特点,复发风险不容轻视
乳腺癌是全球以及中国女性最常见的恶性肿瘤之一。根据最新全球癌症统计报告显示, 2022年全球女性新发乳腺癌为230.9万人,死亡人数为66.6万人,发病和死亡均位居女性恶性肿瘤的首位2。与此同时,2022年中国乳腺癌发病人数为35.7万人,死亡人数为7.5 万人,发病和死亡分别位居中国女性恶性肿瘤的第2位和第5位,而且由于我国人口数量巨大,乳腺癌发病人数与死亡人数均居世界前列3。此外,相较于美国乳腺癌患者,中国乳腺癌的发病年龄更为年轻(45-55岁 vs 64岁)4和确诊时分期更晚(II-III期: 68% vs 45%)5,这也就意味着中国患者的复发风险更高,预后更差。
HR+/HER2-是乳腺癌中最常见的分子亚型,约占所有乳腺癌的70%6。同时HR+乳腺癌具有以下特征:
HR+乳腺癌的复发风险持续存在,并呈线性递增。据报道,HR+/HER2- 早期乳腺癌患者中,短期复发率(<5 年)为 20%~30%7,且复发风险在手术后 2-3 年内达到高峰8,而对于 5 年内未复发的 HR+/HER2- 早期乳腺癌患者,现有循证证据表明复发风险将持续存在并随时间累积可长达 20 年9。
中国HR+乳腺癌确诊时分期较晚,复发风险更高。本研究中,II-III期患者占比接近80%,并且相较于I期患者,II期和III期中国患者的3年复发风险增加了1.5倍和4.8倍。同时,相较于美国真实世界研究,我国接受过标准辅助内分泌治疗后的II期(6.3% vs 8.8%)和III期(10.5% vs 24.9% )HR+/HER2-患者3年复发风险明显更高10。
HR+早期乳腺癌中,不论淋巴结是否转移(N+和N0伴高危因素),患者的复发风险均需要临床重视。众所周知,淋巴结状态是影响HR+/HER2-早期乳腺癌复发风险的重要独立预后因素之一,本研究显示与既往询证结果一致,相对于淋巴结阴性的患者,随着淋巴结数量增多,患者的复发风险逐步上升。同时,本研究通过复发风险分层观察到所有N+和N0伴高危因素患者的复发风险均不容忽视,相对于non-NATA Group,NATA Group的复发风险升高至2.9倍,3年RFS为83.9%。这一结果与2024 SABCS公布的一项美国真实世界研究不谋而合。美国真实世界研究结果11显示,这部分患者的3年无浸润性乳腺癌生存期(iBCFS)为89.2%,5年iBCFS为81.4%。两项真实世界研究结果充分证实,NATA Group患者具有较高的复发风险,需要采取更有效的辅助强化治疗措施以降低复发风险,改善预后。
响应“健康中国2030”号召,走向HR+早期乳腺癌治愈之路
随着治疗手段的不断升级,乳腺癌已从一种无法治愈的疾病转变为可控的恶性肿瘤。《“健康中国2030”规划纲要》中提出,到2030年,实现全人群、全生命周期的慢性病健康管理,总体癌症5年生存率提高15%12。因此重视数量庞大的HR+/HER2-早期乳腺癌的复发风险,升级辅助治疗策略,改善患者生存甚至实现治愈,势在必行。
与此同时,在《“健康中国2030”规划纲要》指导下,肿瘤管理政策正在全面升级。临床医疗机构需要在关注规范化诊疗同时深入探索我国乳腺癌的发病与复发特点,在早期阶段识别高复发风险患者,并予以重点关注,以提高长期生存率,实现治愈目标。本项回顾性研究立足中国数据,时间跨度长、纳入样本量大,结果证实中国HR+/HER2-早期乳腺癌中II-III期患者占比更高,并且不管是淋巴结转移阳性还是淋巴结阴性伴有高危因素的患者,复发风险同样不容忽视,都需要更有效的辅助强化治疗手段以改善预后。
综上,如何精准识别这部分高复发风险的HR+/HER2-早期乳腺癌患者,探索更精准、个体化、科学合理的辅助强化治疗策略,从而为患者带来更大的生存获益是临床实践工作的重中之重。期待未来有更多临床研究成果,帮助医生精准制定临床治疗策略,造福更多乳腺癌患者。
审批码KIS0035502-81252,有效期为2024-12-16至2025-12-15,资料过期,视同作废
1. Li Q, Jiang MX, Liu JX, et al. Evaluation of the Early Risk of Recurrence in HR+/HER2- Early Breast Cancer Patients A Retrospective Study Based on the Chinese National Cancer Database. SanAntonio: SABCS abstract, 2024: P3-12-09.
2. Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024 May-Jun;74(3):229-263.
3. 邬昊, 吕青. 全球及中国乳腺癌的流行病学趋势及防控启示:2018–2022年《全球癌症统计报告》解读. 中国普外基础与临床杂志, 2024, 31(7): 796-802.
4. Fan L, Strasser-Weippl K, Li JJ, et al. Breast cancer in China. Lancet Oncol. 2014 Jun;15(7):e279-89.
5. Li J, Zhou J, Wang H, Liu Z, et al. Trends in Disparities and Transitions of Treatment in Patients With Early Breast Cancer in China and the US, 2011 to 2021. JAMA Netw Open. 2023 Jun 1;6(6):e2321388.
6. Huppert LA, Gumusay O, Idossa D, et al. Systemic therapy for hormone receptor-positive/human epidermal growth factor receptor 2-negative early stage and metastatic breast cancer. CA Cancer J Clin. 2023 Sep-Oct;73(5):480-515.
7. Sheffield KM, Peachey JR, Method M, et al. A real-world US study of recurrence risks using combined clinicopathological features in HR-positive, HER2-negative early breast cancer. Future Oncol. 2022 Jul;18(21):2667-2682.
8. 刘玲玲,林芳,韩耀风,等.不同分子分型乳腺癌术后复发转移风险及其时间分布规律.中国卫生统计, 2017, 34(1):5.
9. Pan H, Gray R, Braybrooke J, et al. 20-Year Risks of Breast-Cancer Recurrence after Stopping Endocrine Therapy at 5 Years. N Engl J Med. 2017 Nov 9;377(19):1836-1846.
10. Razavi P, Ahmed M, Roush A, et al. Real-world (RW) risk of recurrence among patients (pts) diagnosed with stage II-III HR+/HER2− early breast cancer (EBC) treated with endocrine therapy (ET) in the US. JCO.2024.42.16_suppl.e12533.
11. Tarantino P, Rugo HS, Curigliano G, et al. Risk of recurrence in real-world (RW) NATALEE- and monarchE-eligible populations of patients with HR+/HER2- early breast cancer (EBC) in an electronic health record (EHR)-derived database. SanAntonio: SABCS abstract, 2024: P2-12-02.
12. 曾钊,刘娟.中共中央 国务院印发《"健康中国2030"规划纲要》.中华人民共和国国务院公报, 2016(32):5-20.
排版编辑:肿瘤资讯-C Y X











 苏公网安备32059002004080号
苏公网安备32059002004080号


