乳腺癌是造成女性癌症死亡的主要原因[1]。乳腺癌中HER2阳性患者占比20-30%,该类型患者疾病进展迅速,恶性程度较高,预后不良。靶向HER2的抗体偶联药物(ADC)对于HER2阳性的乳腺癌具有重要疗效。然而,该类药物治疗过程中常引起血小板减少症,影响患者的治疗进程和疾病预后。因此,积极控制肿瘤治疗所致血小板减少症(CTIT)对提高HER2阳性乳腺癌患者的治疗效果,改善患者的生活质量至关重要。
本期内容带来了浙江大学医学院附属第二医院田伟副主任医师分享的1例HER2阳性乳腺癌患者ADC治疗期间反复出现血小板减少症的治疗过程,并邀请浙江大学医学院附属第二医院陈益定教授对该病例诊疗过程进行精彩点评,一探乳腺癌HER2阳性患者ADC治疗相关CTIT升板治疗究竟。
病例分享者简介
浙江大学医学院附属第二医院 乳腺外科
浙江省医师协会乳腺肿瘤专委会 青委副主委
中国医药教育协会乳腺疾病专业委员会浙江分会委员
浙江省康复医学会 肿瘤康复委员会委员
一般资料
基本情况
患者女,54岁,2022-02-14因“发现左乳肿块5月余”入院。
现病史
患者5月前自检发现左乳肿块,大小约2cm×1cm,质硬,边界欠清,难推动,当时无红肿疼痛,无乳头溢血溢液,未重视就诊,自觉肿块缓慢增大。患者1天前至当地医院体检,行乳腺超声(2022-02-13)提示:“左乳低回声区伴钙化点,考虑恶性可能”。患者为求进一步诊治,至我院门诊,门诊建议患者住院治疗,拟“左乳肿块”收治入院。
月经婚育史
初潮16岁,经期7天,周期30天,末次月经2021-09-01。23岁结婚,育有1子,配偶及儿子均体健。
既往史、个人史、家族史无特殊
查体
双侧乳房对称,外观正常,表面无“酒窝征”、“橘皮征”等。左乳内上象限可触及一大小约3.5cm×3.0cm肿块,质硬,边界欠清,活动度差;右乳未触及肿块;左侧腋下可及大小约3.0cm肿大淋巴结,质硬,边界欠清,融合固定;右侧腋下未触及肿大淋巴结。
辅助检查
影像学检查
2022-02-14钼靶提示:左乳上象限非对称性致密伴沿导管分布的成簇状细颗粒状钙化,性质难以确定,恶性不能除外,BI-RADS 4B,建议穿刺活检。
2022-02-14乳腺及腋下淋巴结超声提示:左乳肿块BI-RADS 4B(左乳11点钟结节 3.3×1.1cm)伴左侧腋下淋巴结肿大。
2022-2-15行超声引导下穿刺活检,病理提示:(左乳肿物)浸润性癌;(左腋窝淋巴结穿刺)见转移性癌。免疫组化结果:ER 80% 2-3+,PR 90% 3+,Ki-67 20% +,c-erbB-2(BC)2+,GATA-3 +。FISH检测提示:左侧浸润性乳腺癌细胞HER2基因扩增呈阳性。
2022-02-16行乳腺磁共振提示:左侧上象限乳腺肿块,倾向恶性,BI-RADS 4C类。
2022-02-16至2022-02-18浅表淋巴结超声、胸部CT、全腹部增强CT及头颅MR未见明显异常。
诊断
左乳浸润性癌cT2N1M0(Ⅱb期 HER2型)
治疗经过
1、患者抗肿瘤治疗过程
【术前新辅助治疗】
2022-02-24至2022-06-09
行6个周期TCbHP方案(多西他赛+卡铂+曲妥珠单抗+帕妥珠单抗)。
【手术治疗】
2022-06-29
行左乳癌改良根治术(左乳单乳切除+左腋窝淋巴结清扫)。
【术后评估】
2022-07-13
术后常规病理提示:(左乳改良根治术标本)浸润性微乳头状癌,伴部分非特殊类型浸润性癌(约占20%),大小约3cm×2.5cm;自检腋窝淋巴结6/21阳性(其中2枚为宏转移,2枚为微转移,2枚为孤立肿瘤细胞团)。免疫组化结果:原发灶:ER 80% 1-3+,PR 约5% 1-3+,Ki-67 +,约10%,c-erbB-2(BC) 2+,GATA-3 +;(转移淋巴结):ER 80% 1-3+,PR 约10% 1-3+,Ki-67 +,约10%,c-erbB-2(BC) 2+ 。FISH检测:(左乳浸润癌)HER-2基因扩增呈阳性。
【术后治疗】
2022-08-12至2022-09-09
行HP方案(曲妥珠单抗+帕妥珠单抗) 治疗+辅助放疗
【入组3期临床试验,ADC治疗】
2022-09-13:行1个周期德曲妥珠单抗 375.3mg治疗。
2022-09-23:出现血小板减少,予以升板治疗。
2022-10-07至2022-12-09:行4个周期德曲妥珠单抗 375.3mg治疗。
2022-12-16:出现血小板减少,予以血小板输注、升板药物治疗。
023-01-12:行1个周期德曲妥珠单抗 305.8mg治疗。
2023-02-02:出现血小板减少,予以升板治疗。
2023-04-07至2023-06-29:行6个周期德曲妥珠单抗 222.4mg方案治疗。
2、患者CTIT治疗过程
【首次升板治疗经过】
2022-09-20
患者经1个周期德曲妥珠单抗治疗后,血小板(PLT)计数下降至62×109/L,予以重组人血小板生成素(rhTPO) 15000U 每日一次(qd),经治疗后PLT计数上升至110×109/L。
【第二次升板治疗经过】
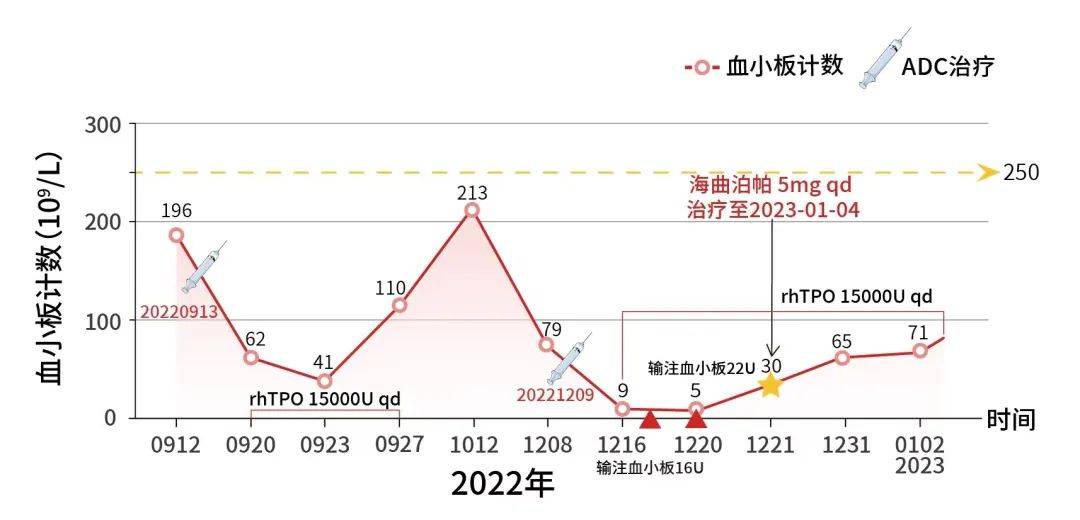
2022-12-16:患者经4个周期德曲妥珠单抗治疗后PLT计数降为9×109/L,予以rhTPO 15000U qd治疗。
2022-12-17予以输注血小板16U。
2022-12-20:测PLT计数下降至5×109/L,予以输注血小板22U,PLT计数升至30×109/L。
2022-12-21至2023-01-04:在rhTPO的基础上联合应用海曲泊帕 5mg qd,经治疗后血小板计数稳步上升,2023-01-04测PLT计数恢复至117×109/L。
【第三次升板治疗经过】
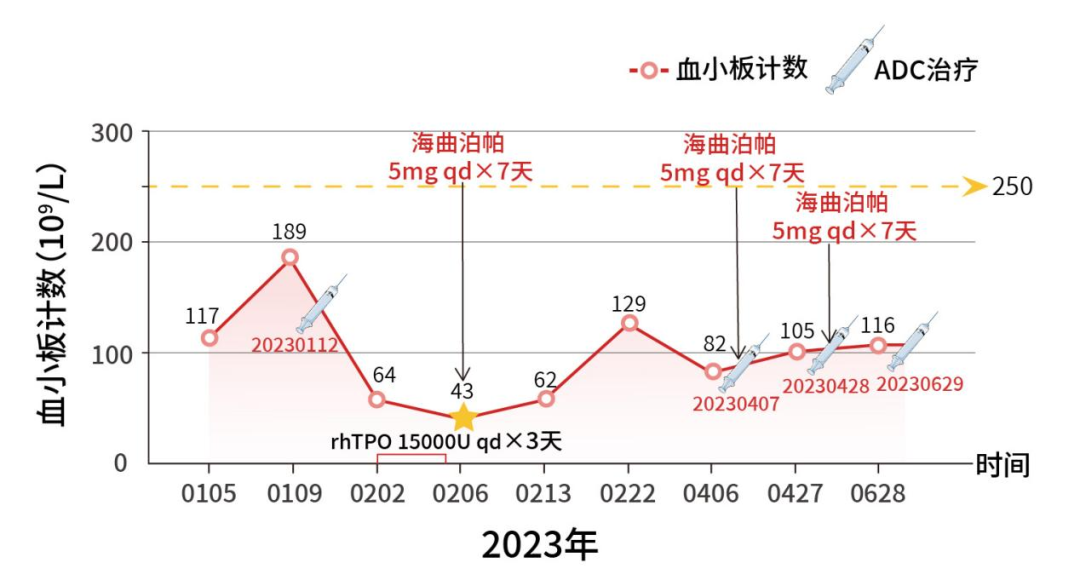
2023-02-02:患者经1个周期德曲妥珠单抗治疗后再次出现2级血小板减少,予以rhTPO 15000U qd治疗3天后,PLT计数降至43×109/L。
2023-02-06:转换海曲泊帕 5mg qd治疗7天后,PLT计数升至62×109/L,患者出院后继续服用海曲泊帕治疗7天,2023-02-22测PLT计数升至129×109/L。
【预防性治疗经过】
此后每次德曲妥珠单抗治疗后均予以口服海曲泊帕 5mg qd×7天预防性治疗,PLT计数始终保持正常平稳。
病例总结
HER2阳性乳腺癌是一种侵袭性癌症亚型,复发率高,预后差。靶向HER2的ADC药物出现为HER2阳性乳腺癌的治疗提供了新选择。T-DM1是首个获批用于实体瘤治疗的ADC,在HER2阳性的乳腺癌的治疗中拥有充分的循证医学证据。德曲妥珠单抗是一种新型靶向HER2的ADC,DESTINY Breast 03研究证实了其在HER2阳性的乳腺癌患者中二线治疗的临床获益[2]。
本例为老年女性患者,乳腺癌HER2扩增。根据2023年《美国国立综合癌症网络(NCCN)乳腺癌临床实践指南》以及《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》推荐,予以患者新辅助治疗TCbHP方案。APHINITY研究显示,对于有高危复发风险,尤其是腋窝淋巴结阳性的患者,推荐使用帕妥珠单抗和曲妥珠单抗双靶向治疗。根据患者术后病理予以HP方案及辅助放疗。此后,患者入组一项3期临床研究,后续均采用德曲妥珠单抗治疗。
既往研究显示,血小板减少症是ADC药物常见的不良反应之一。而本例患者首次经ADC治疗后就出现3级血小板减少,在应用rhTPO治疗后,血小板水平得以恢复。后续接受ADC治疗后,患者出现了更为严重的血小板减少(PLT计数:9×109/L),并导致后续治疗延期及减量,在先后经历rhTPO、血小板输注、海曲泊帕联合rhTPO治疗后,血小板恢复正常。为避免后续治疗过程中反复出现CTIT,而导致患者抗肿瘤治疗减量或推迟,从而影响临床治疗效果。因此,根据最新版《CSCO肿瘤治疗所致血小板减少症诊疗指南》[3]推荐,予以该患者海曲泊帕进行二级预防,此后患者血小板水平维持稳定,ADC治疗得以如期进行。
总体而言,海曲泊帕单药及联合rhTPO治疗可有效提升HER2阳性乳腺癌ADC治疗相关CTIT患者的血小板水平,同时,在这类患者的二级预防中也具有显著的效果,是提高肿瘤患者生活质量、保证抗肿瘤治疗顺利完成的重要“武器”。
专家简介
浙江大学医学院附属第二医院乳腺外科主任,博士生导师
中国抗癌协会乳腺癌专委会常务委员
中国抗癌协会家族遗传性肿瘤专委会常务委员
CSCO乳腺癌专家委员会委员
浙江省抗癌协会乳腺癌专委会候任主委
中国医促会乳腺疾病分会常务委员
浙江省医师协会乳腺肿瘤专委会副主委
[1]Wilkinson L, et al. Br J Radiol. 2022 Feb 1;95(1130):20211033.[2]Cortés J, et al. N Engl J Med. 2022 Mar 24;386(12):1143-1154.[3]中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症指南2023[M].北京:人民卫生出版社,2023.[4]Fu Z, et al. EClinicalMedicine. 2022 Dec 27;55:101795.[5]Mamounas EP, et al. Ann Oncol. 2021 Aug;32(8):1005-1014.[6]Diéras V, et al. Lancet Oncol. 2017 Jun;18(6):732-742.[7]Rainone M, et al. Breast Cancer. 2023 Jun 16.[8]王佳玉,等.中国医学前沿杂志(电子版),2021,13(01):1-15.[9]Huang CS, et al. Breast Cancer Res Treat. 2021 Jun;187(3):759-768.[10]Liu F, et al. Biomed Pharmacother. 2020 Sep;129:110407.[11]Jun Ma, et al. 2023 European Congress of Internal Medicine, Abstract 2360.[12]Haifeng Qin.Annals of Oncology (2022) 33 (suppl_9): S1560-S1597.
排版编辑:肿瘤资讯-jyy











 苏公网安备32059002004080号
苏公网安备32059002004080号


