随着CDK4/6抑制剂、口服选择性雌激素受体降解剂(SERD)及抗体药物偶联物(ADC)等新型疗法的不断进展,个体化治疗策略日益成为临床实践中的主流选择。近日,美国罗斯威尔公园综合癌症中心肿瘤学系助理教授Shipra Gandhi博士通过分析多项关键III期临床试验数据,探讨了CDK4/6抑制剂、口服SERD和ADC药物在激素受体(HR)阳性乳腺癌个体化治疗中的应用和潜在治疗策略,为优化患者的长期管理提供了重要指导[1-2]。【肿瘤资讯】精心梳理访谈内容如下,以飨读者。
CDK4/6抑制剂的选择:患者特征和临床数据的综合考量
在CDK4/6抑制剂的选择上,Gandhi博士指出,临床实践中需将转移性和辅助治疗两种情境分别考量。在转移性HR阳性乳腺癌中,多项关键性III期临床试验数据为临床决策提供了依据。
PALOMA-3试验评估了哌柏西利联合内分泌治疗在既往接受过治疗的HR阳性转移性乳腺癌患者中的疗效,结果显示,联合治疗组的无进展生存期(PFS)较对照组显著延长。在MONALEESA-2试验中,瑞波西利联合内分泌治疗不仅显著延长了PFS,还显示出统计学显著的总生存期(OS)改善[3]。而在MONARCH 3试验中,阿贝西利联合芳香化酶抑制剂(AI)虽然在OS上未达到统计学显著性,但其OS延长具有临床意义。
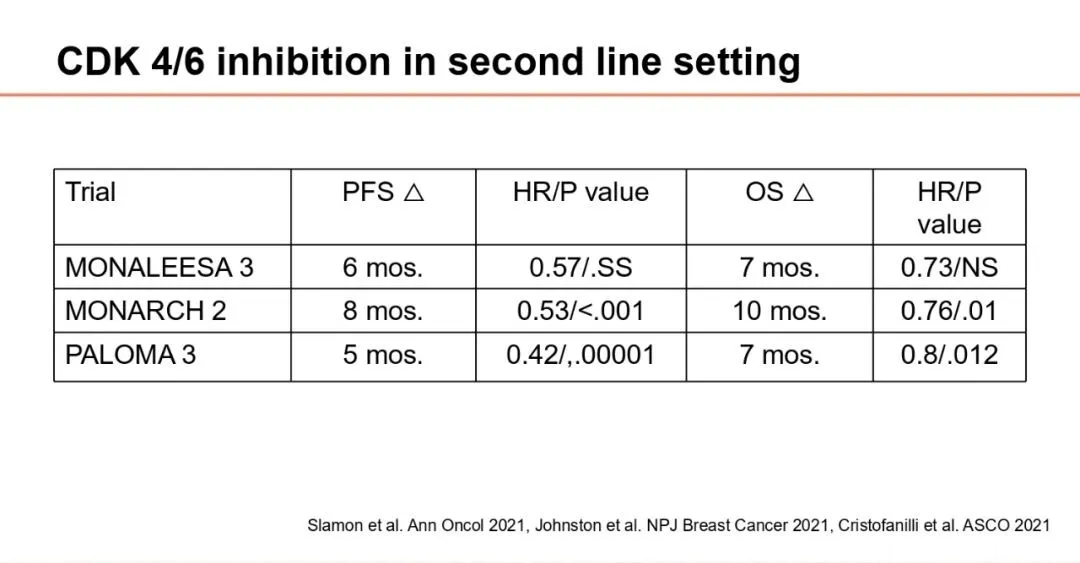
基于这些数据,Gandhi博士指出,临床实践中的CDK4/6抑制剂选择需要根据患者的具体情况进行权衡。对于一般患者,瑞波西利因其在OS方面的优势,通常是优先选择的方案之一。同时,对于因腹泻等副作用而对治疗耐受性较差的患者,哌柏西利以其相对良好的耐受性也是一种常用选择。此外,阿贝西利在中枢神经系统(CNS)转移的患者中显示出一定疗效,因此在CNS转移的情况下,该药物也常被考虑。
在辅助治疗中,monarchE试验的5年随访数据显示,阿贝西利联合内分泌治疗在淋巴结阳性HR阳性乳腺癌患者中的无侵袭性疾病生存期(IDFS)显著优于单纯内分泌治疗[4]。而NATALEE试验则进一步探讨了瑞波西利联合AI在高危淋巴结阴性患者中的应用,这些患者包括II级肿瘤、KI-67指数超过20%、Oncotype DX评分超过26或具有高危基因组特征的患者[5]。试验结果显示,这些高危患者在IDFS方面同样受益于瑞波西利联合AI治疗。因此,Gandhi博士建议,对于淋巴结阳性患者,应优先考虑阿贝西利,而对于高危淋巴结阴性患者,瑞波西利是有效的替代方案。
ADC:从HER2阳性到HER2低表达乳腺癌的治疗扩展
ADC的应用近年来在乳腺癌治疗中取得了显著进展,特别是在HR阳性和三阴性乳腺癌患者中。戈沙妥珠单抗(SG)和德曲妥珠单抗(T-DXd)是目前已由FDA获批用于治疗的两种ADC。T-DXd在多个III期临床试验中显著延长了患者的PFS和OS。
DESTINY-Breast02试验评估了T-DXd在重度治疗后的HER2阳性乳腺癌患者中的应用,结果显示T-DXd较医生选择的治疗方案显著延长了PFS和OS[6]。随后,DESTINY-Breast03试验进一步探讨了T-DXd在HER2阳性转移性乳腺癌二线治疗中的效果,并取得阳性结果[7]。DESTINY-Breast04试验则将T-DXd的适应症从HER2阳性扩展至HER2低表达乳腺癌患者,并显示出显著的PFS和OS改善[8]。这一系列的研究推动了T-DXd在HER2低表达患者中的广泛应用。
此外,TROPION-Breast01试验评估了Dato-DXd在既往接受治疗的HR阳性、HER2阴性乳腺癌患者中的疗效[9]。结果显示与化疗相比,Dato-DXd显著延长了PFS。目前,Dato-DXd可能很快获得批准,这使得临床医生面临如何合理排序使用这些ADC药物的新挑战。TRADE-DXd试验正在研究Dato-DXd和T-DXd的最佳用药顺序,这将是未来研究的重要领域。
CDK4/6抑制剂治疗进展后的选择:HR阳性乳腺癌的创新治疗方案与研究方向
对于CDK4/6抑制剂治疗后进展的患者,治疗选择日益多样化。Gandhi博士指出,如果患者没有可靶向的突变,可以继续使用CDK4/6抑制剂,或者使用依维莫司联合内分泌治疗,这是一种已被广泛应用的方案。然而,如果存在可靶向的突变,例如PIK3CA/AKT突变或PTEN改变,则可以使用Capivasertib;对于ESR1突变的患者,可以选择Elacestrant。
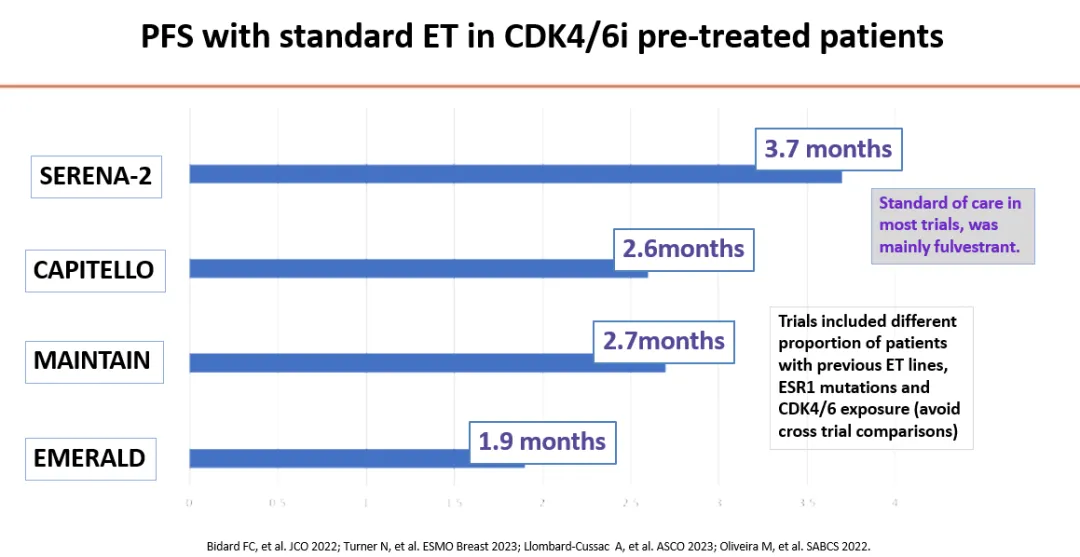
目前,口服SERD在HR阳性乳腺癌中的应用正在逐步扩大。唯一获批的口服SERD是Elacestrant,用于治疗转移性HR阳性乳腺癌。这一批准基于EMERALD研究,该III期随机临床试验纳入了接受过CDK4/6抑制剂治疗的晚期HR阳性乳腺癌患者。试验结果显示,在存在ESR1突变且对内分泌治疗敏感的患者中,Elacestrant组的中位PFS为8.6个月,而内分泌治疗组仅为1.9个月,两者差异为6.7个月[2]。
除了Elacestrant外,其他口服SERD也在积极开展临床研究。例如,SERENA-2研究是一项评估口服Camizestrant(AZD9833)疗效的II期临床试验,结果显示在ESR1突变患者中,Camizestrant较Fulvestrant具有PFS优势。目前,针对Camizestrant的III期研究SERENA-6正在招募转移性HR阳性乳腺癌患者,该研究采用循环肿瘤DNA(ctDNA)检测ESR1突变,阳性患者将随机接受口服Camizestrant联合更换CDK4/6抑制剂或继续使用原有CDK4/6抑制剂联合AI治疗。值得注意的是,在SERENA-6研究中,即便在ctDNA检测出ESR1突变但未出现影像学进展的情况下,患者也可接受Camizestrant治疗。这一研究的结果将备受期待。此外,口服Imlunestrant(LY3484356)也正在EMBER-3研究中进行III期评估,这同样是值得关注的研究。
针对携带胚系BRCA突变的患者,基于EMBRACA研究和OlympiAD研究的III期数据,PARP抑制剂已由FDA获批准应用于这类患者[10-11]。2024年ASCO年会上展示的TBCRC 048研究扩展队列数据表明,PARP抑制剂的应用范围可能扩展至携带体细胞BRCA突变或胚系PALB2突变的肿瘤[12]。数据显示,接受奥拉帕利单药治疗的携带胚系PALB2突变的患者的客观缓解率(ORR)为75%。
对于携带PIK3CA突变的患者,SOLAR-1研究的III期数据评估了Alpelisib的疗效[13]。然而,由于Alpelisib的不良事件较多,越来越多的临床医生倾向于使用Capivasertib替代该药物。
此外,Gandhi博士还提到了一些正在进行中的研究方向,例如在HR阳性、淋巴结阳性的年轻患者中探讨能否避免使用化疗,或在解剖学高危但基因组低危的肿瘤中避免化疗?CDK4/6抑制剂已经拓展至早期治疗,而ADC也正在新辅助和辅助治疗中进行评估,尽管尚未获批用于这些适应症。这引发了一个重要问题:如果患者在接受这些方案后出现复发,应选择何种治疗方案?在CDK4/6抑制剂治疗后的二线治疗中,存在两种可能的靶向突变。临床医生将面临的挑战是是否同时靶向这两种突变,还是继续采用序贯治疗?如果同时使用靶向药物,患者将面临哪些毒性?这些药物联合使用与序贯使用的优缺点是什么?这些都是目前尚未解答的重要问题,需要在未来的研究中进一步探索。
1. https://www.onclive.com/view/cdk4-6-inhibitors-adcs-and-pi3k-inhibitors-individualize-hr-breast-cancer-management?utm_source=www.onclive.com&utm_medium=relatedContent
2. https://www.onclive.com/view/the-hr-positive-breast-cancer-treatment-paradigm-sits-on-the-cusp-of-significant-shifts
3. Hortobagyi, et al. Overall survival (OS) results from the phase III MONALEESA (ML)-2 trial of postmenopausal patients with hormone receptor positive/human epidermal growth factor receptor 2 negative (HR+/HER2−) advanced breast cancer (ABC) treated with endocrine therapy (ET) ± ribociclib. Presented at the European Society of Medical Oncology (ESMO) Congress, September 16-21, 2021, (Abstract #LBA17).
4. Johnston, S. R. D., Harbeck, N., Hegg, R., Toi, M., Martin, M., Shao, Z., et al. (2020). Abemaciclib combined with endocrine therapy for the adjuvant treatment of HR+, HER2−, node-positive, high-risk, early breast cancer (monarchE). Journal of Clinical Oncology, 38(34), 3987-3998.
5. Kalinsky, K., Barlow, W. E., Meric-Bernstam, F., Gralow, J. R., Albain, K. S., Hayes, D. F., et al. (2023). Phase III NATALEE trial: Ribociclib with endocrine therapy as adjuvant treatment in HR-positive, HER2-negative, node-negative, high-risk early breast cancer. Annals of Oncology, 34(5), 559-570
6. Modi, S., Jacot, W., Yamashita, T., Sohn, J., Vidal, M., Tokunaga, E., et al. (2022). Trastuzumab deruxtecan in previously treated HER2-positive breast cancer. The New England Journal of Medicine, 386, 610-621. (DESTINY-Breast02)
7. Cortés, J., Kim, S. B., Chung, W. P., Im, S. A., Park, Y. H., Hegg, R., et al. (2022). Trastuzumab deruxtecan versus trastuzumab emtansine for breast cancer. The New England Journal of Medicine, 386, 1143-1154. (DESTINY-Breast03)
8. Modi, S., Ohtani, S., Lee, C., Vidal, M., Yamashita, T., Tokunaga, E., et al. (2022). Trastuzumab deruxtecan in HER2-low–expressing breast cancer. The New England Journal of Medicine, 387, 9-20. (DESTINY-Breast04)
9. Bardia A, Jhaveri K, Kalinsky K, et al. TROPION-Breast01: Datopotamab deruxtecan vs chemotherapy in pre-treated inoperable or metastatic HR+/HER2- breast cancer. Future Oncol. 2024;20(8):423-436. (TROPION-Breast01)
10. Litton, J. K., Rugo, H. S., Ettl, J., Hurvitz, S. A., Gonçalves, A., Lee, K. H., et al. (2018). Talazoparib in patients with advanced breast cancer and a germline BRCA mutation. The New England Journal of Medicine, 379, 753-763. https://doi.org/10.1056/NEJMoa1802905 (EMBRACA)
11. Robson, M., Im, S. A., Senkus, E., Xu, B., Domchek, S. M., Masuda, N., et al. (2017). Olaparib for metastatic breast cancer in patients with a germline BRCA mutation. The New England Journal of Medicine, 377, 523-533. (OlympiAD)
12. Tung, N. M., Robson, M. E., Ventz, S., Santa-Maria, C. A., Nanda, R., Marcom, P. K., et al. (2024). Olaparib in patients with metastatic breast cancer with germline PALB2 mutations: TBCRC 048. Journal of Clinical Oncology, 42(suppl 16; abstr 1021), 1021-1021. (TBCRC 048)
13. André, F., Ciruelos, E., Rubovszky, G., Campone, M., Loibl, S., Rugo, H. S., et al. (2019). Alpelisib for PIK3CA-mutated, hormone receptor–positive advanced breast cancer. The New England Journal of Medicine, 380, 1929-1940. (SOLAR-1)
排版编辑:肿瘤资讯-Kelly











 苏公网安备32059002004080号
苏公网安备32059002004080号


