2023年12月,Annals of Oncology (影响因子50.5)相继发表了关于拉索昔芬(Lasofoxifene)的两篇研究,分别为拉索昔芬联合CDK4/6抑制剂阿贝西利在ESR1突变的ER+/HER2-晚期乳腺癌的疗效(ELAINE-2)[1]以及拉索昔芬单药对比氟维司群的随机II期试验(ELAINE-1)[2]。【肿瘤资讯】对两篇研究主要内容予以整理,以飨读者。

概述
拉索昔芬是一种新型口服选择性ER调节剂(SERM),可拮抗恶性和恶性前乳腺癌细胞中的雌激素受体(ER),尤其是携带ESR1突变的细胞,拉索昔芬表现出独特的治疗优势。同时,拉索昔芬具有组织选择性,它在骨骼和阴道组织中是ER激动剂,在子宫中对ER的作用是中性的,不会增加子宫瘤变。绝经后骨质疏松症妇女中开展的的III期PEARL试验显示,拉索昔芬0.5mg/天可使浸润性ER+乳腺癌风险降低83%。因此,展现出对ER+晚期乳腺癌(mBC)的治疗潜力。特别是对于ESR1基因突变的患者,表达ESR1突变(尤其是Y537S突变)的乳腺癌细胞对他莫昔芬、氟维司群和其他ER靶向化合物的敏感性降低,但对拉索昔芬的敏感性却没有降低。拉索昔芬能破坏和灭活Y537S突变ER的组成激动剂构象,在携带ESR1突变的mBC模型中,单独或与CDK4/6抑制剂连用时,对肿瘤抑制和转移的抑制作用明显高于氟维司群。
ELAINE-1& ELAINE-2研究核心发现
ELAINE-1研究背景:
乳腺癌是美国最常见的女性癌症,2022年美国女性浸润性乳腺癌的年新增病例约为287850例,死亡人数为43250例,预计到2025年,将有169347名妇女罹患mBC。大约80%的乳腺癌是ER+,内分泌治疗(ET)是治疗ER+ mBC的主要方法,如芳香化酶抑制剂(AI)和氟维司群(雌激素受体降解剂,SERD),单独使用或与细胞周期蛋白依赖性激酶4/6抑制剂(CDK4/6i)联合使用。虽然这种疗法通常很有效,但几乎所有肿瘤都会出现内分泌耐药,而高达40%的肿瘤是由于配体结合域中的ESR1突变所致。ESR1突变赋予ER不依赖配体的组成型活性和形态、促进转移的特性,并丰富了ER+乳腺癌的基底样特征,导致内分泌耐药和随后的肿瘤进展。
内分泌药物具有良好的安全性,连续使用时,可以推迟对毒性更强的化疗的需求。氟维司群单药治疗出现进展的晚期乳腺癌患者的中位无进展生存期(PFS)通常为4.6-10.2个月;然而,在CDK4/6i使用后治疗(主要是哌柏西利)数据显示,氟维司群单药治疗的PFS仅为1.9-4.8个月。而且,氟维司群或AI在肿瘤出现ESR1突变时,尤其是最常见的ESR1突变之一Y537S突变的患者中的抗肿瘤疗效有限,目前,另一种SERD药物Elacestrant最近被FDA批准作为ESR1突变、ER+/HER2- mBC患者的治疗选择,但其作为单药在CDK4/6i后治疗中的中位PFS为3.8个月。其他新型SERDs,包括giredestrant、imlunestrant和camizestrant,正在用于治疗ER+/HER2-mBC的临床开发中。最近,针对CDK4/6i进展后ESR1突变、ER+/HER2-mBC的SERDs联合CDK4/6i的小型研究显示,临床获益有限;例如,氟维司群联合瑞波西利的中位PFS为3个月,camizestrant联合哌柏西利或阿贝西利的临床获益率(CBR)为10%-38%,未观察到客观反应率(ORR)。因此,迫切需要新的治疗策略,尤其是针对获得性ESR1基因突变的治疗策略。
ELAINE-1研究设计与入组人群特征
ELAINE-1研究(NCT03781063)是一项II期、开放标签、随机试验,评估了拉索昔芬与氟维司群单药治疗的对比。
符合条件的参与者为绝经前或绝经后女性(年龄≥18岁),患有局部晚期或转移性、ER+/HER2-乳腺癌,且在既往使用AI加CDK4/6i作为最近ET的情况下病情有所进展;在无细胞循环肿瘤DNA (ctDNA)中发现一个或多个ESR1突变;东部合作肿瘤学组(ECOG)评分为0或1分;根据RECIST 1.1标准,有1或多个可测量病灶,或如果没有可测量的病灶,为淋巴性或混合性淋巴性/硬化性骨病变;以及经证实的适当器官功能。ESR1突变可能包括Y537S、Y537C、D538G、E380Q、S463P、V534E、P535H、L536H、L536P、L536R、L536Q或Y537N。患者肿瘤必须曾对ET敏感(在mBC治疗中≥12个月后复发或进展),且患者必须曾接受过一线及以下mBC化疗。
主要排除标准包括:曾使用依维莫司或其他哺乳动物雷帕霉素靶点抑制剂或磷酸肌酸3-激酶抑制剂(PI3K抑制剂);曾使用氟维司群导致病情恶化;脑转移;肺部淋巴管癌变;内脏危象化疗;30天内曾接受放疗;影响患者安全的重大合并症;长QTc综合征病史或QTc间期大于480ms;过去6个月内曾发生肺栓塞或深静脉血栓;过去一年内曾发生阴道出血;5年内曾患乳腺癌以外的其他恶性肿瘤。过去6个月内有肺栓塞或深静脉血栓形成、任何已知的血栓性疾病、过去一年内有阴道出血或5年内有乳腺癌以外的恶性肿瘤。研究期间不得接受任何其他研究性或商业性抗癌治疗、任何激素替代疗法或长期使用全身性皮质类固醇。任何为预防/控制骨转移而同时使用双膦酸盐或地诺单抗的情况均需记录在案。
研究程序
根据是否存在内脏转移和Y537SESR1突变对患者进行分层。每个分层组以1:1的比例随机接受口服拉索昔芬(5mg/天)或IM氟维司群(500mg,第1、15和29天,然后每月一次)治疗,直至疾病进展、出现不可耐受的毒性或退出治疗。治疗组之间不允许交叉。绝经前患者继续接受卵巢抑制治疗。
统计分析
目标样本量为100个(每个治疗组50个),预期PFS事件总数为86个,考虑到初始化期为1年,在初始化完成后再随访1年,然后进行主要PFS分析。
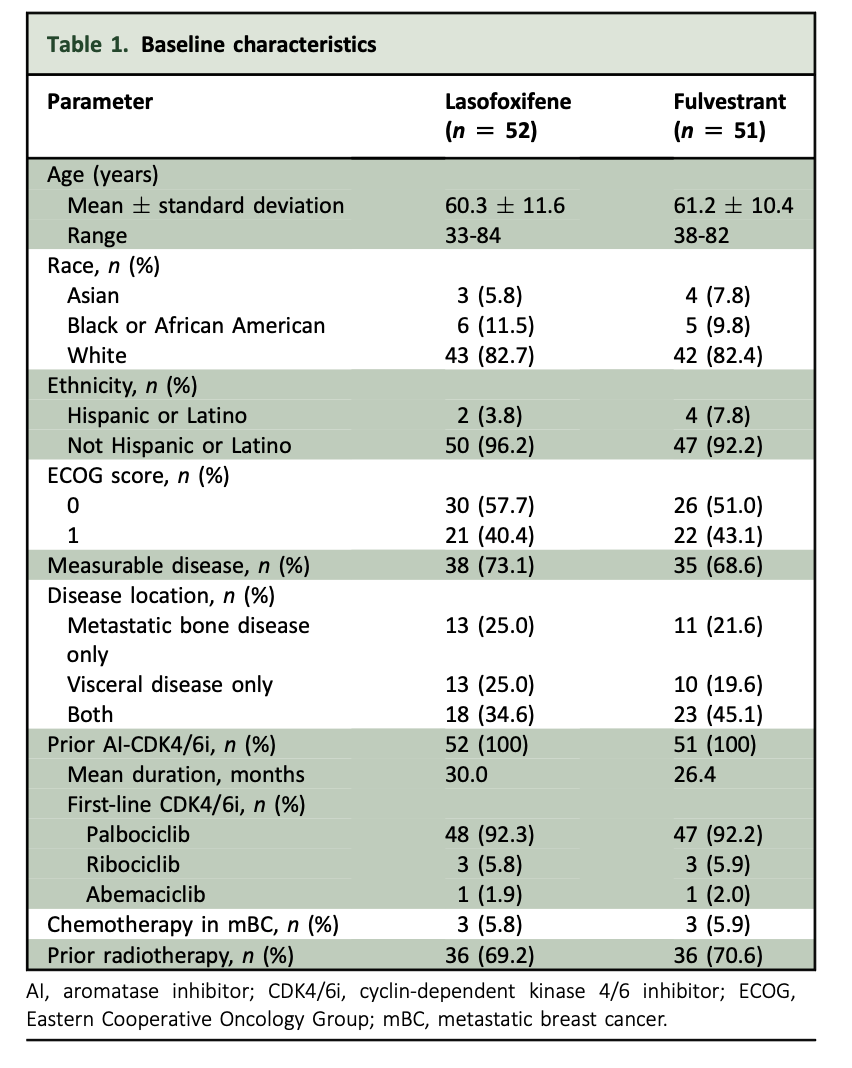
ELAINE-1研究入组患者特征(表1):
总计入组103名患者,其中拉索昔芬治疗组52例,氟维司群治疗组51例。
平均年龄60.8岁,年龄范围33-84岁。
种族包括亚裔(6.8%)、黑人(10.7%)、白人(82.5%),西班牙裔占6%。
大多数(92.2%)既往接受哌柏西利治疗。
54.4%的患者肿瘤存在多克隆ESR1突变。
基线时常见的ESR1突变包括D538G(56.3%)、Y537S(41.7%)、Y537N(29.1%)、E380Q(22.3%)和Y537C(10.7%)。
表1:ELAINE-1研究入组患者基线
疗效
拉索昔芬治疗组的中位PFS为24.2周(约5.6个月),相比之下,氟维司群治疗组的中位PFS为16.2周(约3.7个月,P=0.138);HR=0.699(95% CI 0.434-1.125),图1;
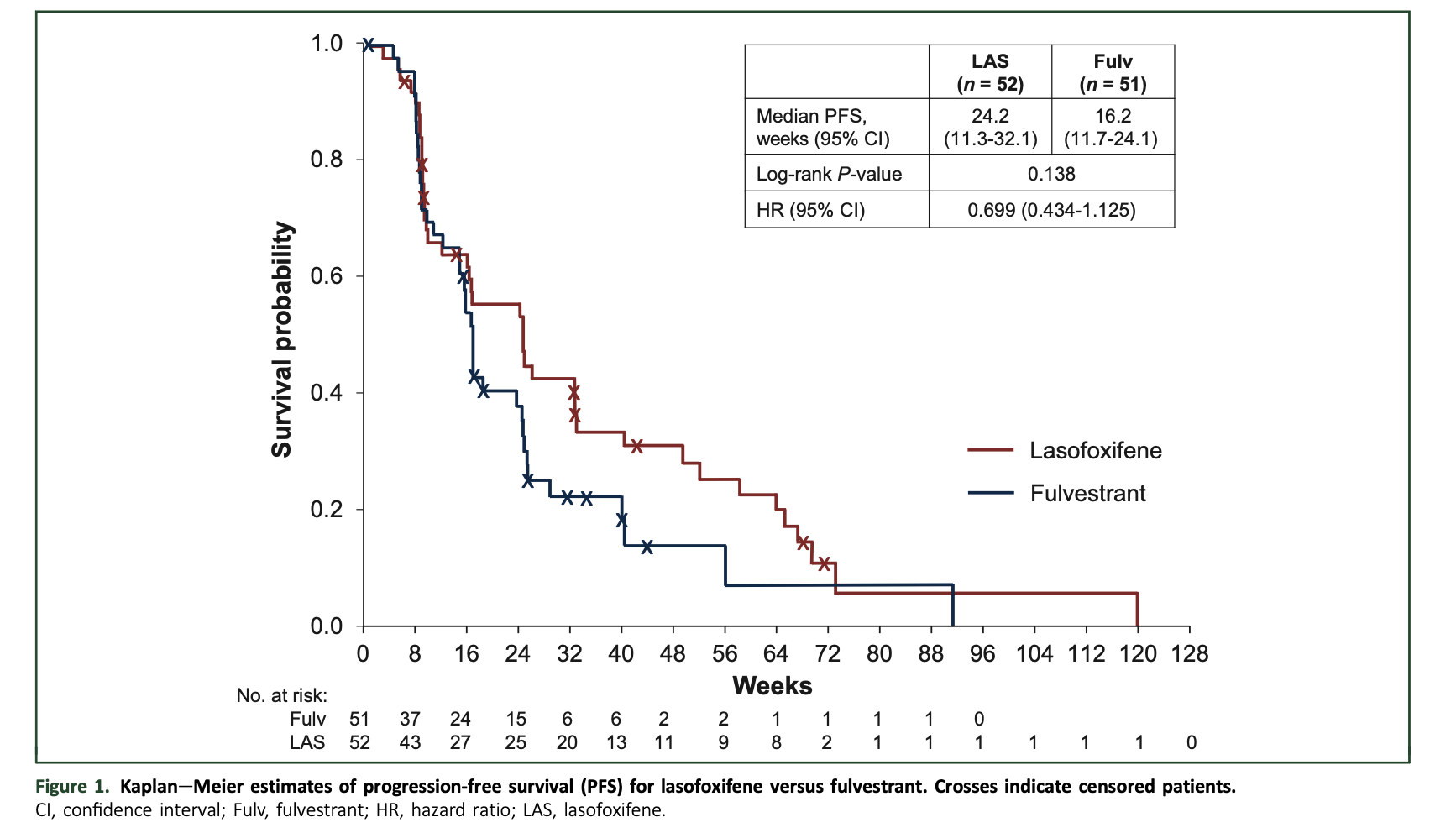
图1:拉索昔芬与氟维司群的PFS Kaplan-Meier 估计值。横线表示已剔除的患者
拉索昔芬治疗组的CBR为36.5%,氟维司群治疗组的CBR为21.6%,P=0.117;图2
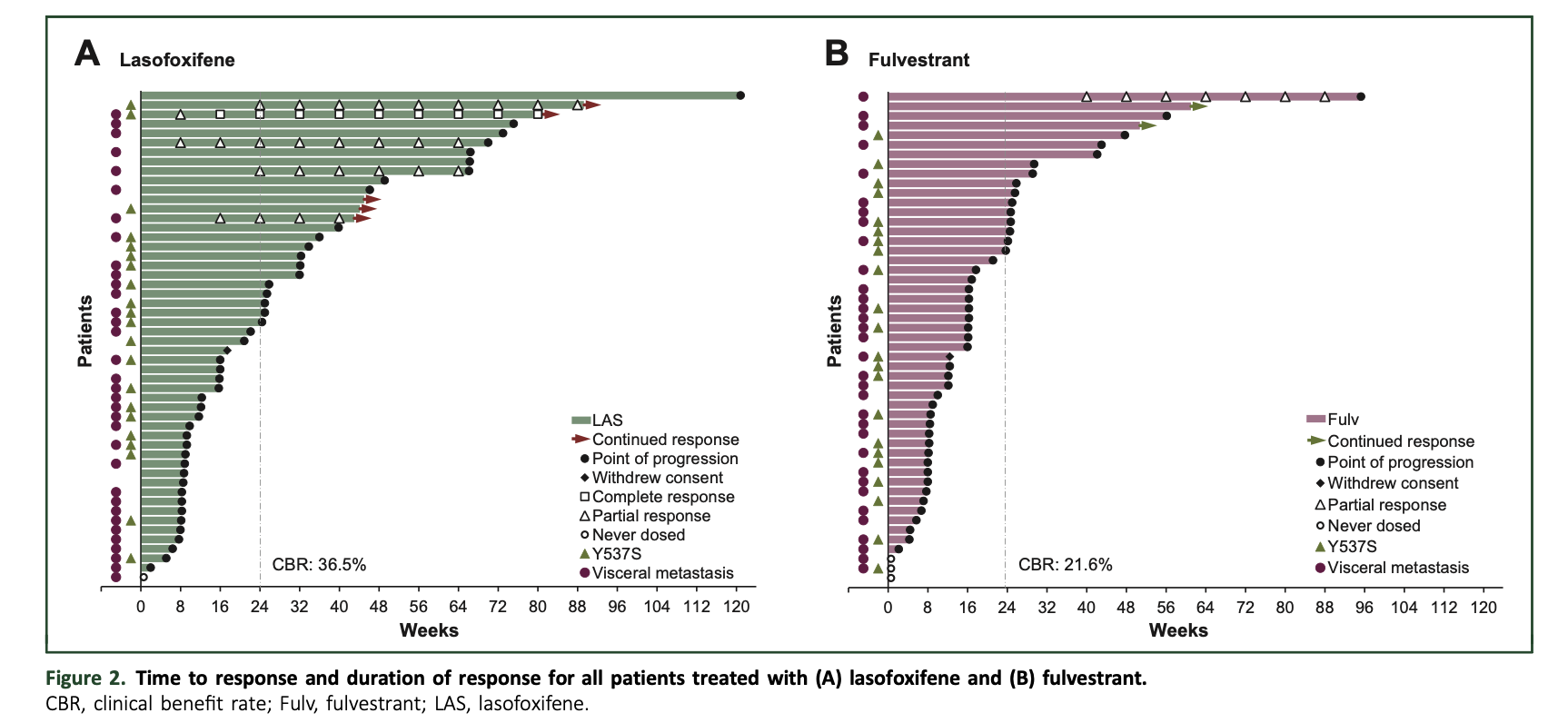
图2:所有接受(A)拉索昔芬和(B)氟维司群治疗的患者的应答时间和应答持续时间
ORR为拉索昔芬治疗组13.2%(1名拉索昔芬治疗患者达到完全缓解),氟维司群治疗组2.9%;P=0.124;图3
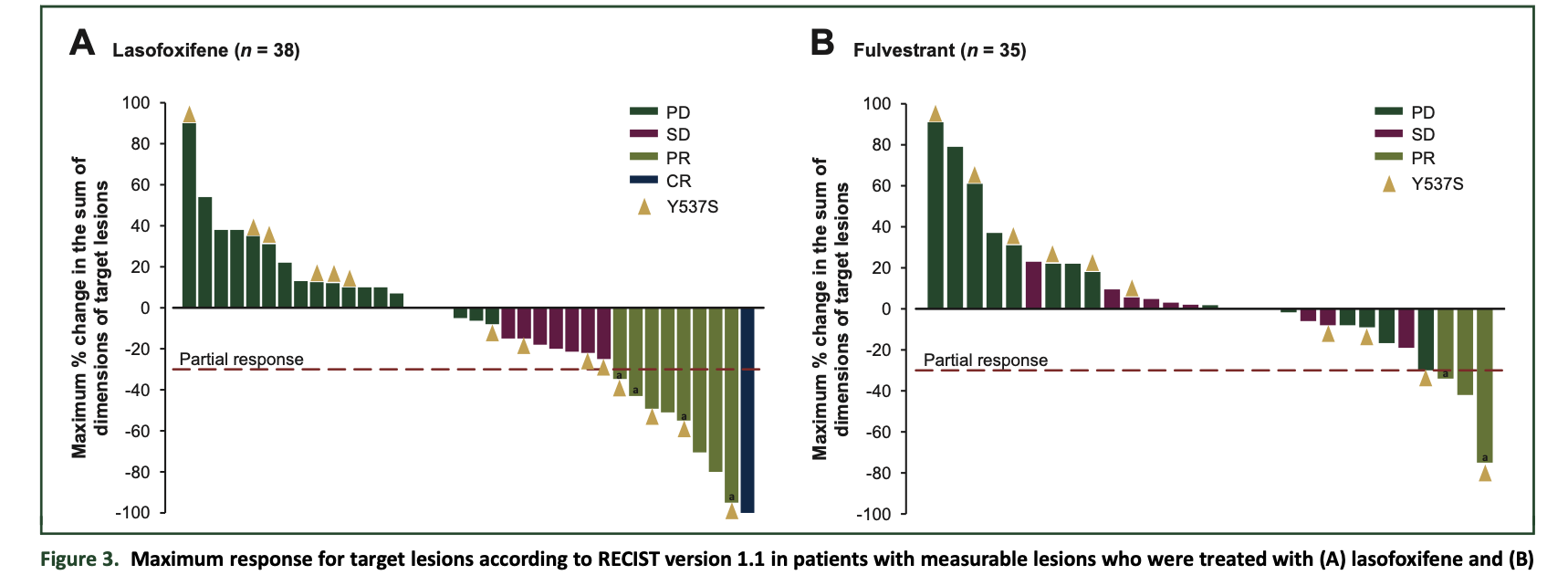
图3:根据RECIST1.1,接受(A)拉索昔芬和(B)氟维司群治疗的可测量病灶患者的靶病灶最大应答。基线检测到Y537S的患者用金色箭头标记。
ELAINE-2研究设计与入组人群特征
ELAINE-2研究(NCT04432454)是一项开放标签、II期、多中心、单臂试验。符合条件的参与者为绝经前后的女性(年龄≥18岁),患有局部晚期和/或转移性 ER+/HER2- 乳腺癌,且在接受一到两线ET治疗后病情恶化;通过使用SafeSeq分析法进行集中检测,在无ctDNA中发现≥1个ESR1 突变;ECOG评分为0或1分;通过实验室检测确认器官功能正常。ESR1突变包括Y537S、Y537C、D538G、E380Q、S463P、V534E、P535H、L536H、L536P、L536R、L536Q和/或Y537N突变。患者在首次接受基于ET的晚期乳腺癌治疗期间,必须在≥6个月内无疾病进展迹象。允许事先使用CDK4/6i和/或一种化疗方案治疗转移性疾病。
主要排除标准包括:淋巴管癌变;需要立即进行细胞毒性化疗的内脏危象;入组后30天内接受过放疗;已知RB1发生失活突变或缺失;有长QT综合征病史或QTc >480mc;6个月内有肺栓塞或深静脉血栓;任何已知的血栓性疾病;或在过去5年中有其他恶性肿瘤(不包括皮肤基底细胞癌或鳞状细胞癌)。患者不得服用任何其他研究或商业抗癌治疗药物、激素替代疗法、长期服用全身性皮质类固醇、强CYP 3A4抑制剂或中度或强CYP 3A4诱导剂。允许同时接受双膦酸盐疗法或用于治疗骨转移的地舒单抗。
研究程序
患者每天口服5mg拉索昔芬和150mg阿贝西利,每天两次(b.i.d),直到出现疾病进展、死亡、不可接受的毒性或退出研究。每次就诊(第2、4、6和8周,之后每月一次,直至疾病进展)都要进行安全性评估。
允许阿贝西利剂量减少或剂量中断,在阿贝西利中断治疗期间,拉索昔芬的剂量无需同时中断,但一些研究者选择这样做。如果患者不能耐受50mg阿贝西利(b.i.d),则可由主治医生决定继续单独使用拉索昔芬治疗,直至疾病进展。
不允许减少拉索昔芬的剂量;但是,如果出现相关的3/4级不良事件(AE),可暂停拉索昔芬的治疗,待毒性缓解至<2级或基线后,再按指定剂量恢复治疗。不能耐受拉索昔芬或连续3周未服用拉索昔芬的患者将退出研究;不允许继续单独服用阿贝西利。
ELAINE-2研究入组患者特征(表2):
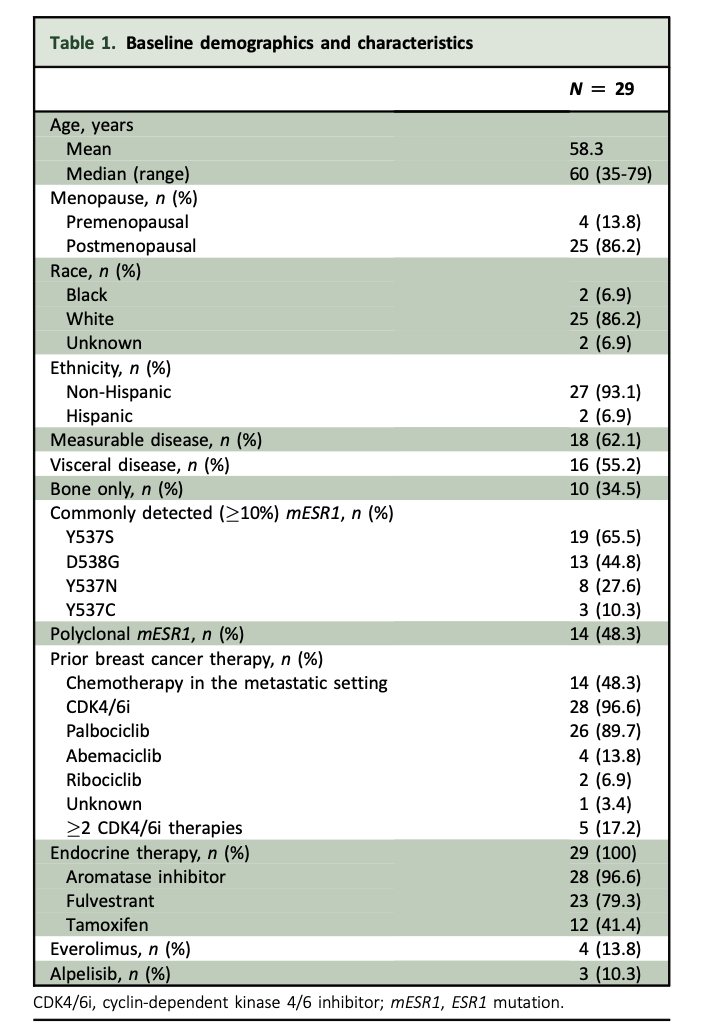
共纳入29例女性患者,中位年龄为60岁。
86.2%的患者为白人,62.1%在基线时有可测量病灶。患者在晚期治疗中接受过中位数为两线ET治疗,70%以上在接受过两次ET治疗后肿瘤进展。
除1名患者外,其他都曾接受过CDK4/6i治疗。
23名(79.3%)患者曾接受过氟维司群治疗,14名(48.3%)曾接受过晚期化疗。
基线ESR1突变包括Y537S(65.5%)、D538G(44.8%),48.3%的患者存在多克隆ESR1突变。
表2: 基线人口统计数据和特征
疗效
拉索昔芬-阿贝西利联合疗法的中位PFS为56.0周(约13个月)(95%CI 31.9周-NE);6个月PFS率 (95%CI)为76.1% (54.4%-88.5%),12个月PFS率为56.1%(34.9%-72.8%),18个月PFS率为38.8%(20.0%-57.3%);图4
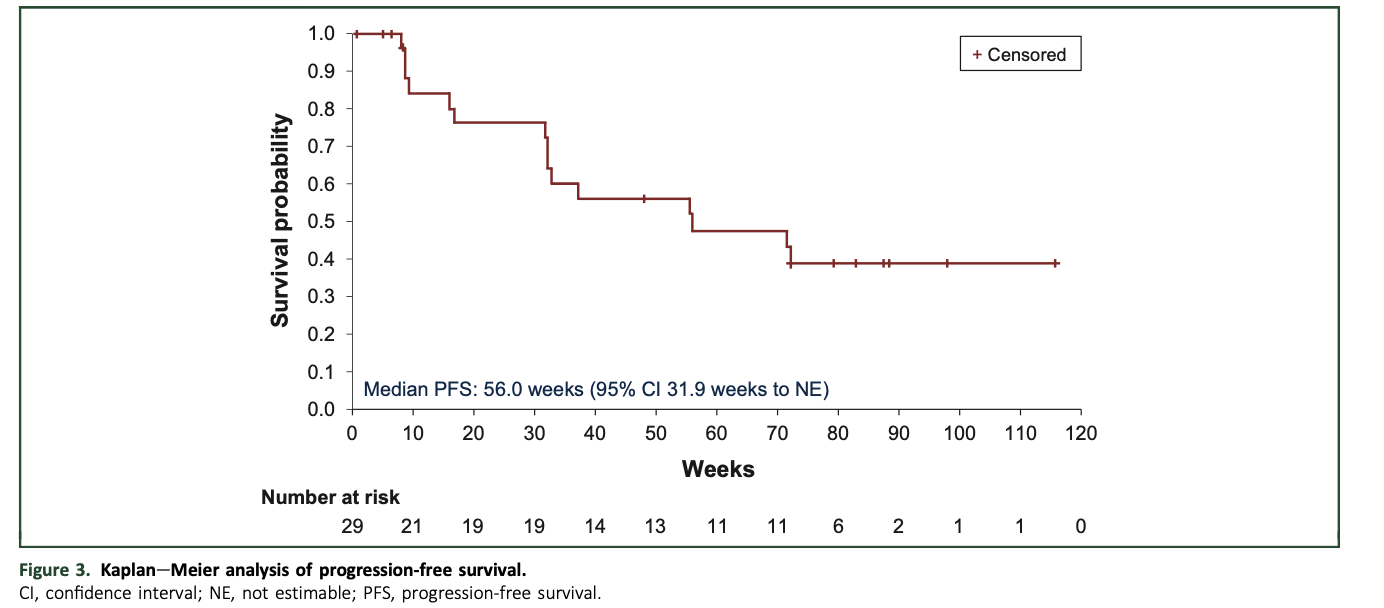
图4:PFS Kaplan-Meier分析
ORR为55.6% (95%CI为33.7%-75.4%),24周时的CBR为65.5% (95%CI为47.3%-80.1%),其中10名患者达到PR,9名患者病情稳定 (SD)≥24周;图5-6
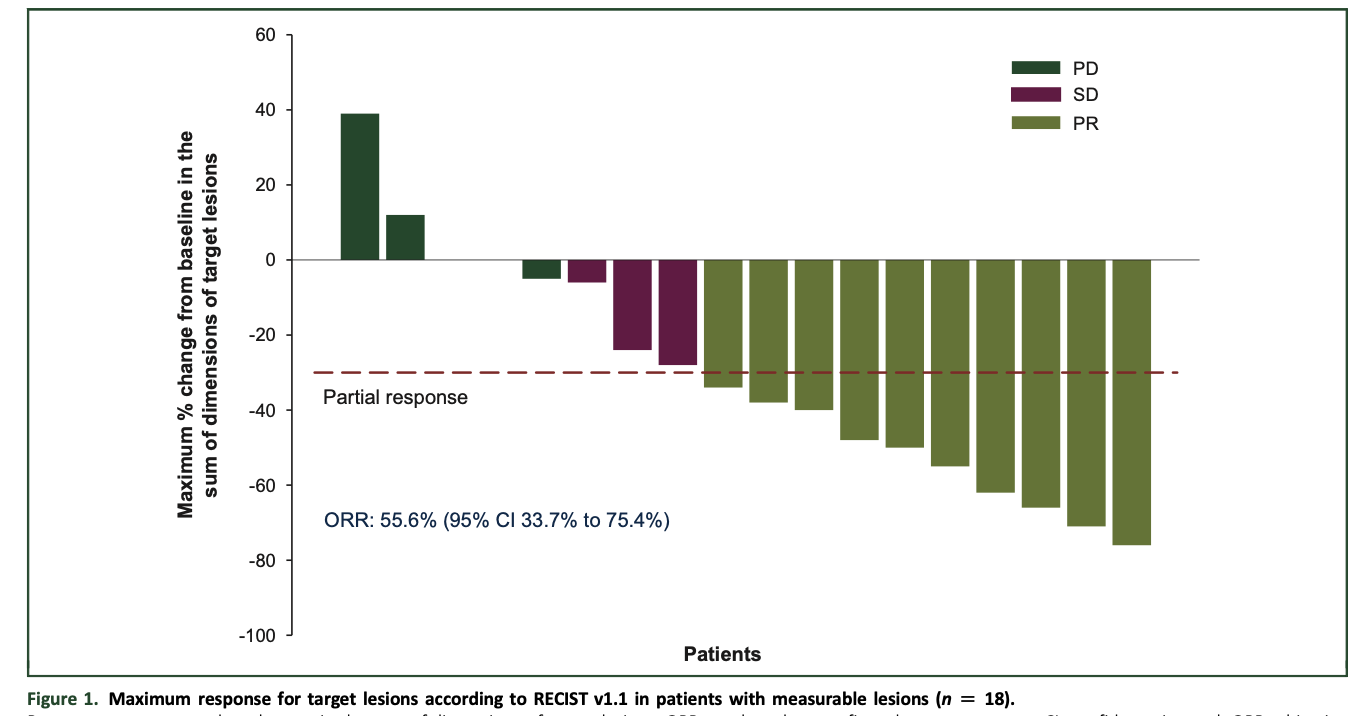
图5:根据RECIST v1.1,可测量病灶患者靶病灶的最大应答(n=18)
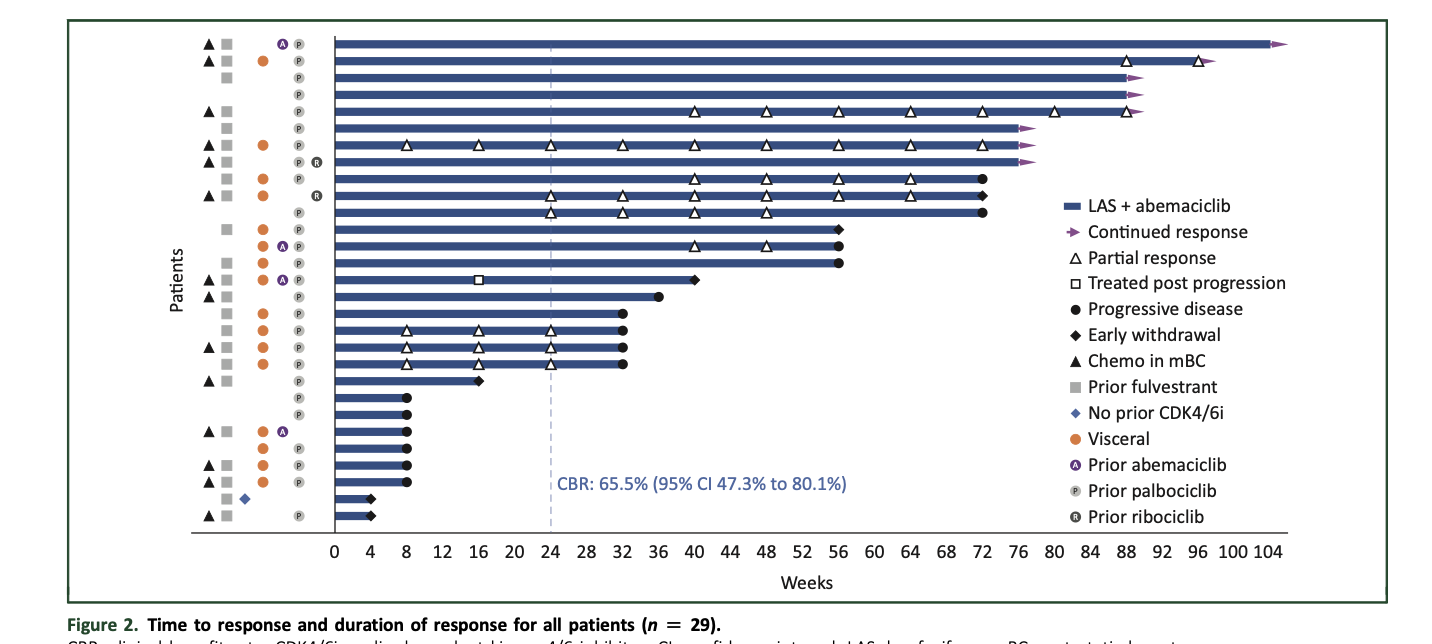
图6:所有患者的应答时间和应答持续时间(n=29)
安全性与耐受性
ELAINE-1(表3):
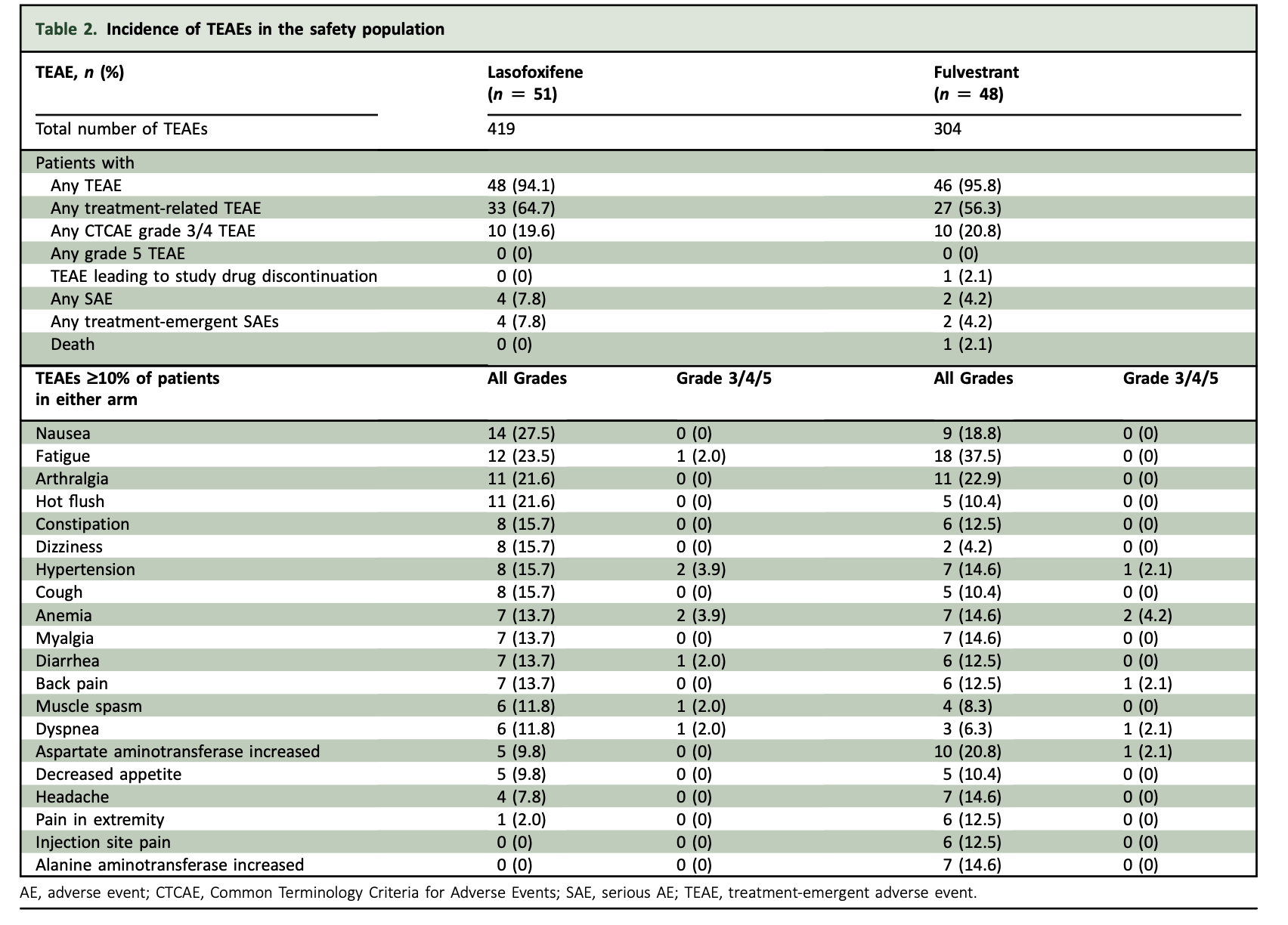
拉索昔芬治疗组的耐受性普遍良好。48例(94.1%)拉索昔芬治疗患者和46例 (95.8%)氟维司群治疗患者出现治疗相关不良事件(TEAE)。
拉索昔芬治疗组3/4级AE比例为19.6%,氟维司群治疗组为20.8%,未发现5级TEAEs。
拉索昔芬最常见的TEAEs (总发生率≥20%)为恶心、疲劳、关节痛和潮热,氟维司群最常见的TEAEs为疲劳、关节痛和天冬氨酸氨基转移酶升高;大多数为1/2级。
拉索昔芬治疗组和氟维司群治疗组中有1例和3例患者出现了严重不良事件 (SAEs)。
氟维司群治疗组中有1例死亡病例,死因是暴发性疾病进展(由于与疾病相关,因此不被视为5级AE)。
表3: 安全人群(Safety Population)中TEAEs的发生率
ELAINE-2 (表4):
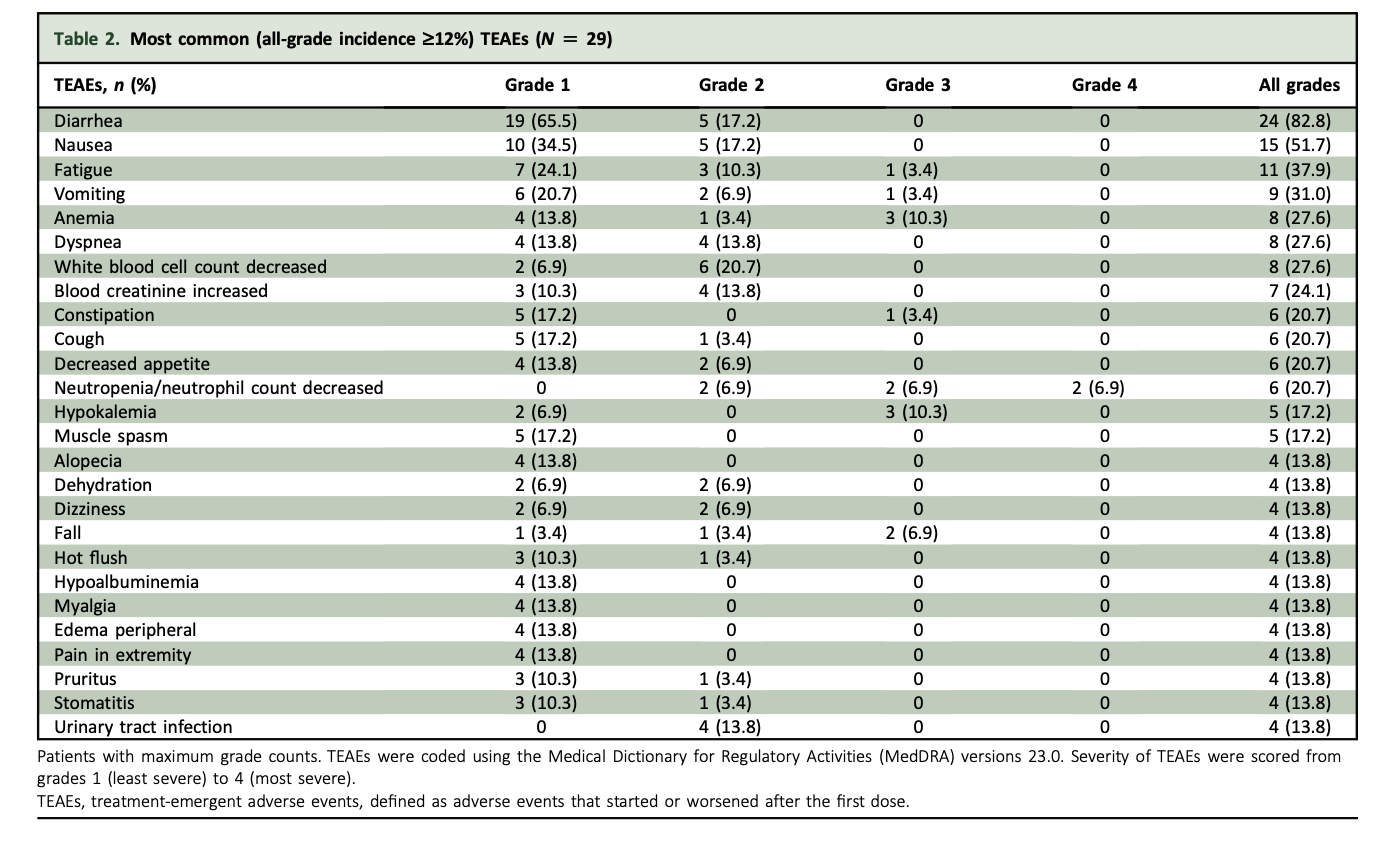
联合疗法中的不良事件主要为1/2级,包括腹泻、恶心、疲劳和呕吐。
研究期间无死亡病例,一名患者因2级腹泻中止治疗。
表4:最常见(任意等级发生率≥12%)的TEAE (N=29)
针对ESR1突变的靶向作用
ELAINE-1 (图7):
拉索昔芬治疗组中82.9%的患者从基线到第8周的ctDNA显示ESR1突变等位基因频率(MAF)有所下降。
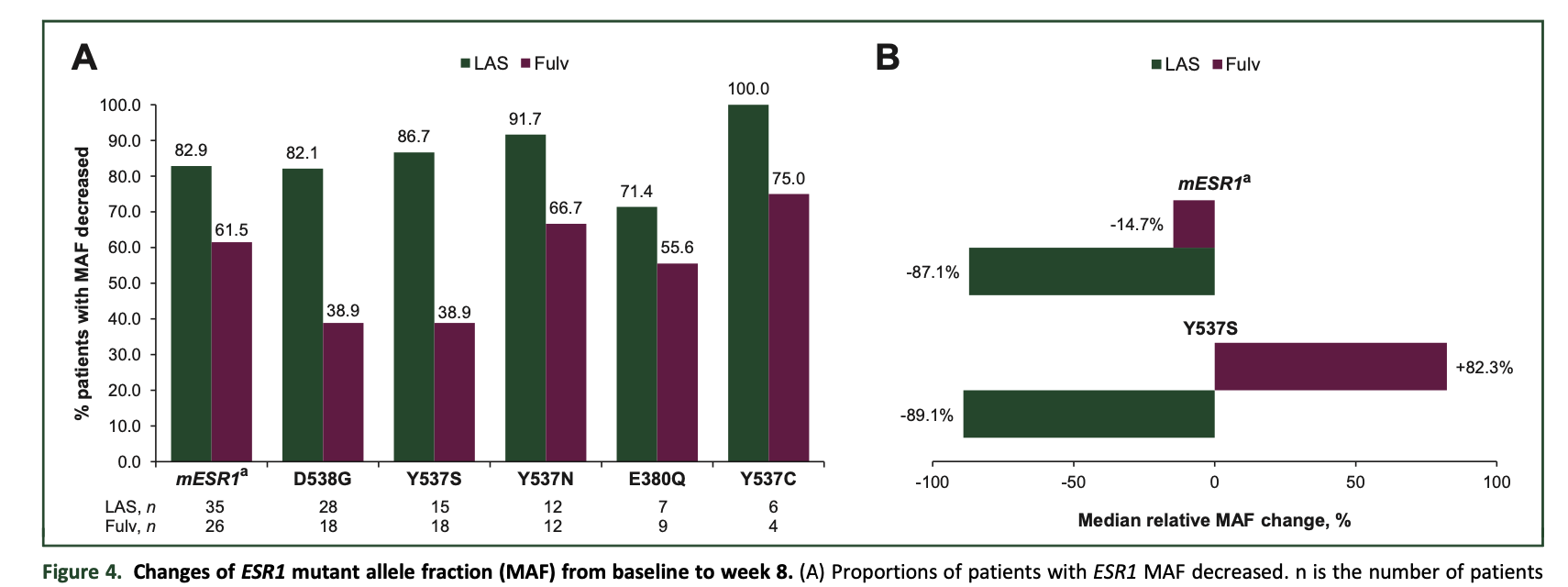
图7:ESR1突变MAF从基线到第8周的变化
ELAINE-2:
拉索昔芬-阿贝西利治疗后,80.8%的患者的ESR1突变ctDNA MAF有所下降,表明治疗具有良好的靶向效果。
临床意义与未来展望
改变治疗策略:
ELAINE系列研究揭示了拉索昔芬在处理CDK4/6i耐药的ER+/HER2- mBC中的潜力。尤其是针对ESR1突变导致的治疗耐药,拉索昔芬提供了一种新的治疗方向。期待更广泛的应用:
若ELAINE-2的研究结果能在进行中的ELAINE-3 III期试验 (NCT05696626)中得到证实,拉索昔芬-阿贝西利联合疗法有望成为CDK4/6i治疗后ESR1突变mBC的标准治疗方案。III期试验旨在一线AI+哌柏西利或瑞波西利治疗后出现进展的ESR1突变、ER+/HER2-患者中,比较拉索昔芬加阿贝西利与氟维司群加阿贝西利的疗效。综合治疗视角:
通过深入研究拉索昔芬的作用机制和临床效果,有望开发出更为精准和个性化的治疗方案,为ER+/HER2-mBC患者带来新的希望。
结论
拉索昔芬的出现不仅为乳腺癌治疗提供了新的视角,而且在于打破现有治疗方法的疗效局限,特别是针对CDK4/6抑制剂耐药后研究展现出鼓舞人心的潜力。随着更多研究的开展和数据的积累,我们有理由期待拉索昔芬将为乳腺癌患者带来更加有效、安全的治疗选择。
参考文献
[1]Damodaran,S.etal.AnnalsofOncology,Volume34,Issue12,1131
–1140
[2]Goetz,M.P.et al. Annals of Oncology, Volume 34, Issue12,1141-1151
排版编辑:肿瘤资讯-Kelly











 苏公网安备32059002004080号
苏公网安备32059002004080号


