乳腺癌已超越肺癌,成为全球发病率第一的恶性肿瘤[1]。与西方国家相比,我国年轻乳腺癌患者的占比更高[2]。且近年来,我国35岁以下年轻乳腺癌的发病率逐渐增加[2]。这些年轻乳腺癌患者在社会和家庭中承担着重要的角色和责任,对生活质量要求更高,临床需要进行更全面、系统的疾病管理,以改善患者预后。小分子酪氨酸激酶抑制剂(TKI)奈拉替尼强化辅助治疗能够显著降低人类表皮生长因子受体2(HER2)阳性乳腺癌患者的复发风险[3,4],使临床治愈成为可能。
本文特别分享一例年轻(28岁)Luminal B-HER2阳性型乳腺癌患者的病例。患者在接受6周期的TCbHP(多西他赛+卡铂+曲妥珠单抗+帕妥珠单抗)新辅助治疗后,最佳疗效达到部分缓解(PR)。随后行右乳癌改良根治术,术后病理显示存在病灶残留。为了巩固疗效、控制病情,术后行1周的局部放疗,并在完成1年的内分泌联合HP双靶(曲妥珠单抗+帕妥珠单抗)辅助治疗后,继续内分泌治疗联合奈拉替尼强化治疗1年。末次复查(2023年8月22日)显示,患者病情控制良好。
病例分享专家简介
甲状腺、乳腺外科副主任医师,科秘
江苏省抗癌协会乳腺癌专业委员会委员
江苏省抗癌协会甲状腺癌专业委员会委员
徐州抗癌协会乳腺癌专业委员会委员
徐州市抗癌协会肿瘤内分泌专业委员会副秘书长
徐州市抗癌协会肿瘤康复委员会常务委员
徐州甲状腺疾病研究会常务委员
淮海地区肿瘤防治联盟乳腺癌专业委员会副主任委员
病例分享
病例介绍
基本信息:女,28岁。
主诉:发现右乳肿块5月余。
个人史、既往史、家族史:
月经史:未绝经。
现病史:患者因“发现右乳肿块5月余”来我院就诊,查体示:双乳对称,右侧乳房皮肤稍红肿,右乳头稍凹陷,局部未见“酒窝征”,右乳晕周围及内象限可见“橘皮征”;右乳内侧3:00方向距乳头3cm处可触及一质硬肿块,大小约2cm×2cm,质硬,界不清,活动度差,挤压乳头无液体流出;右腋窝可及肿大淋巴结,大小约2.5cm×2cm,质偏硬,界不清,部分融合,活动度稍差;左乳各象限未及明显肿块,左乳头正常无凹陷,挤压乳头无液体流出,左腋下未及肿大淋巴结。查血常规、生化及肿瘤标志物,均正常;头颅MRI、胸部CT、消化系统及锁骨上淋巴结彩超、全身骨扫描未见明显异常。
超声(2021-8-26)示:右乳皮肤及皮下脂肪层水肿增厚,内象限为主。右乳探及多枚低回声结节,部分内示强回声,较大一枚位于3:30近乳头侧边缘距乳头约3.8cm,距皮肤约1.0cm处,范围约1.9cm×1.5 cm×1.0cm,边界不清晰,形态不规则,内示血流信号。右侧腋窝探及多枚淋巴结声像最大2.7cm×1.2cm,皮质增厚,左腋窝未探及明确肿大淋巴结。BI-RADS:4B-4C类。
乳腺MRI(2021-08-26)示:右侧乳腺较对侧增大,腺体结构不完整。乳头后上方腺体结构扭曲,强化不均,可见条状点状强化灶时间-信号强度曲线呈流入型。右乳腺体实质信号不均,外上象限、内下象限可见多发斑片状异常信号,呈段样分布。右侧乳头凹陷,右侧腋窝可见多发增大淋巴结影。BI-RADS:6类。(图1) 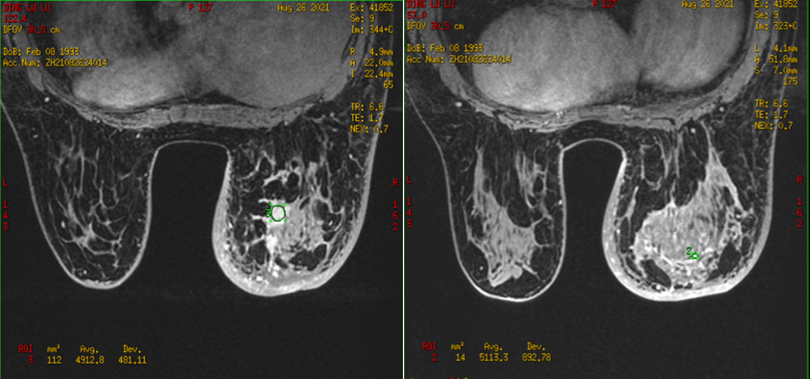
图1 乳腺MRI(2021-8-26)
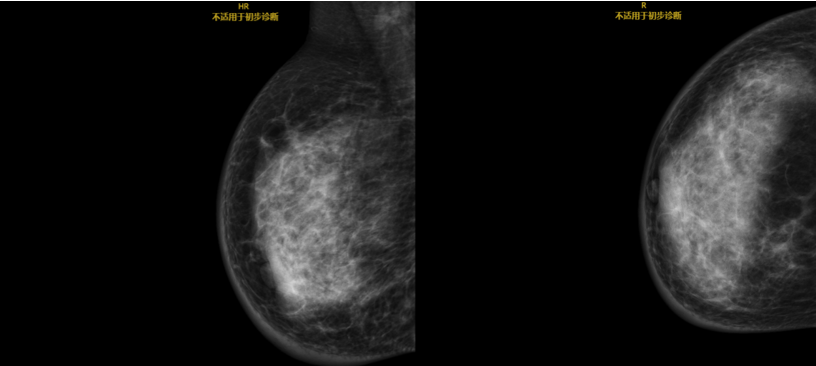
图2 乳腺钼靶(2021-8-27)
乳腺及腋窝淋巴结空心针穿刺病理及免疫组化示:
右乳穿刺标本病理:浸润性乳腺癌,待免疫组化进一步诊断。免疫组化:ER(2+,约80%),PR(1+,热点约20%),HER2(3+),Ki67(+,热点区约30%),E-cadherin(膜/质+),P120(膜+);
右腋窝淋巴结病理:镜下未见正常淋巴结构,纤维组织内见异形细胞巢,考虑为转性癌,待免疫组化进一步分析。免疫组化:ER(3+,约95%),PR(3+,热点约95%),HER2(3+),Ki67(+,热点区约30%),E-cadherin(膜+),P120(膜+)。
临床诊断:右乳浸润性导管癌 cT4N2M0 Ⅲc期;分子分型:Luminal B型(HER2阳性型)
治疗经过:
一、 化疗+靶向新辅助治疗
2021年9月至2022年1月,行6周期的TCbHP方案治疗,具体为:TCb(多西他赛120mg+卡铂600mg)+曲妥珠单抗(首次8mg/Kg,之后6mg/Kg)+帕妥珠单抗(首次840mg,之后420mg)×q3w。化疗期间,给予卵巢功能抑制(OFS)治疗(戈舍瑞林3.6mg q28d IH)以保护卵巢功能。每周期治疗后复查乳腺彩超,每2周期治疗后复查乳腺MRI。
2021年9月30日,复查乳腺彩超示:右乳皮肤及皮下脂肪层水肿增厚,内象限为主;右乳探及多枚低回声结节,部分内示强回声,较大一枚位于3:30近乳头侧边缘距乳头3.8cm,距皮肤约1.0cm处,范围约1.8cm×1.4cm×0.9cm,边界不清晰,形态不规则,内示血流信号;右侧腋窝探及多枚淋巴结声像最大2.7cm×1.2cm,皮质增厚。疗效评估为:病情稳定(SD)。
2021年10月22日,复查乳腺彩超示:右乳3:30近乳头侧边缘距乳头3.8cm,距皮肤约0.9cm处,范围约0.8cm×0.8cm×1.0cm,边界不清晰,形态不规则,内示血流信号,弹性成像质地偏硬;右侧腋窝探及多枚淋巴结声像最大0.7cm×0.6cm,淋巴门可见,皮质增厚。疗效评估:PR。
2021年11月11日,复查乳腺MRI(图3)示:右侧乳腺较对侧增大,腺体结构不整;乳头后上方腺体结构扭曲,强化不均,可见条状点状强化灶时间-信号强度曲线呈流入型;右乳腺体实质信号不均,外上象限、内下象限可见多发斑片状异常信号,呈段样分布;右侧乳头凹陷,右侧腋窝可见多发小、中空淋巴结影,较前片(2021-08-26)右乳病灶强化程度减低,皮肤增厚程度减轻,右侧腋窝淋巴结减小。BI-RADS:6类。
2021年11月12日、2021年12月3日、2021年12月23日、2022年1月16日分别复查乳腺彩超,疗效评估:SD。
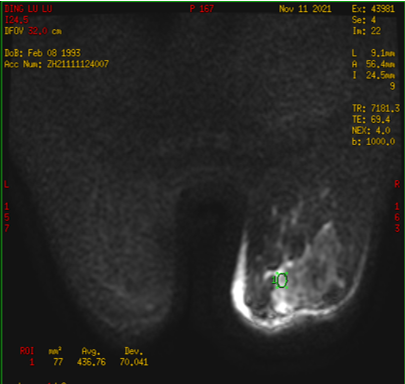
图3 乳腺MRI(2021-11-11)
一、 手术治疗
2022年1月17日,在全麻下行右乳癌改良根治术。
术后病理及新辅助评估:右乳新辅助治疗后,肿瘤侵犯范围:乳头(-)基底(-)神经侵犯(-)皮肤(-)脉管侵犯(-)。非肿瘤性乳腺组织:TDLU基底膜与小叶硬化;RCB系统:I级,淋巴结状态 无癌状态:伴治疗后改2,无治疗后改28。有癌状态:伴治疗后改2,无治疗后改0,总计32。转移最大径0.3cm。淋巴结2/32见癌转移。
二、 放射治疗
2022年3月,开始行一周期放疗,具体方案:右胸壁及腋窝引流区50Gy/25f。
三、 内分泌+靶向辅助治疗
2021年9月9日至2022年8月18日,完成1年的OFS(戈舍瑞林3.6mg q28d IH)+AI(依西美坦25mg qd po)+双靶治疗(曲妥珠单抗首次剂量560mg,维持剂量420mg;帕妥珠单抗首次剂量840mg,维持剂量420mg)。
四、 内分泌+奈拉替尼强化治疗
2022年9月1日至2023年8月31日,给予OFS(戈舍瑞林3.6mg q28d IH)+AI(依西美坦25mg qd po)+奈拉替尼(240mg qd po,完成1年)强化治疗。
患者在服用奈拉替尼后,出现腹泻,3-4次/天,后按需服用盐酸洛哌丁胺,服用后腹泻次数有所减少,持续2个月时间。每3月随访复查一次,末次复查时间为2023年8月22日,结果显示患者病情控制良好。
点评专家简介
乳腺、甲状腺外科前科主任
中华医学会会员
江苏省中西医结合学会乳腺病专业委员会委员
江苏省抗癌协会第一届乳腺病专业委员会委员
江苏省抗癌协会第一届甲状腺癌专业委员会委员
首届中国研究型医院学会乳腺专业委员会委员
江苏省妇幼保健专业委员会委员
徐州市抗癌协会乳腺癌专业委员会副主任委员
徐州市抗癌协会肿瘤康复专业委员会副主任委员
长期从事临床第一线工作,在乳腺疾病及甲状腺疾病的诊治方面,尤其是乳腺癌、甲状腺癌的规范手术治疗,经验丰富
专家点评
年龄是影响乳腺癌患者预后的重要因素,患者年龄越小,预后越差,这可能与年轻乳腺癌更具侵袭性的生物学行为,更具倾向于高复发风险特征有关[2]。一项探索乳腺癌患者长期随访复发风险的研究显示,晚期乳腺癌在在初次诊断后15年、20年、25年和32年的累积发病率分别为8.5%、12.5%、15.2%和16.6%,且年轻患者(<40岁)晚期复发的累积发生率更高[5]。因此,需要将年龄作为患者预后评估及治疗决策制定的考量因素之一。对于年轻乳腺癌患者,不仅要关注近期疗效,还应特别关注其对生活质量及长期生存的需求,为患者提供个性化充分治疗,预防复发,提高患者的生活质量。
术前新辅助治疗已经成为乳腺癌的主要治疗策略之一。对于有一定肿瘤负荷(T2期或N1期及以上)的三阴性或HER2阳性乳腺癌患者,应优选新辅助治疗[6]。HER2是乳腺癌重要的驱动基因和预后指标,以HP双靶为基础的新辅助治疗已经成为HER2阳性乳腺癌的首选方案[6]。本例患者在完善检查、明确诊断后,给予TCbHP方案进行新辅助治疗,最佳疗效为PR。在患者完成6周期的新辅助治疗后,即进行手术治疗。术后病理显示未达到病理完全缓解(pCR)。pCR是新辅助治疗的一项重要的预后指标,相较于pCR患者,新辅助治疗后未达到pCR的患者预后较差。NeoALTTO研究结果显示,与拉帕替尼和/或曲妥珠单抗新辅助治疗未达到pCR的HER2阳性早期乳腺癌患者相比,pCR患者具有更好的EFS(HR 0.48)和OS(HR 0.37),pCR患者在1~2年内的复发率几乎是未达到pCR的一半(HR分别为0.073 vs 0.121)[7]。既往研究数据显示[6,8],对于不同亚型的新辅助治疗后未达到pCR的患者采用相应的化疗、靶向治疗或内分泌治疗予以辅助强化,可显著改善预后。
一项探索曲妥珠单抗辅助治疗1年后序贯奈拉替尼强化辅助治疗的Ⅲ期临床研究——ExteNET研究结果显示[3,4],在HER2阳性乳腺癌患者中,与安慰剂组相比,曲妥珠单抗辅助治疗1年后再进行1年的奈拉替尼强化治疗可显著改善患者的2年无浸润生存率(iDFS:93.9% vs 91.6%)。对于non-pCR患者,进行奈拉替尼强化辅助治疗的5年iDFS率为85.0%(安慰剂组5年iDFS率为77.6%),绝对获益为7.4%;5年无远处转移生存期(DDFS)率为86.8%(安慰剂组为79.8%),绝对获益为7.0%;8年总生存(OS)率为91.3%(安慰剂组为82.2%),绝对获益为9.1%,降低疾病死亡风险达53%[4]。CSCO乳腺癌诊疗指南推荐[9],对于新辅助治疗未达到pCR的患者,无论患者术前采用曲妥珠单抗单靶还是HP双靶治疗,辅助阶段在HP双靶治疗后序贯奈拉替尼进行强化辅助治疗(Ⅲ级推荐2A级证据)。基于此,本例患者在进行一周放疗加强局部控制后,给予HP双靶辅助治疗1年,并继续进行1年的奈拉替尼强化辅助治疗。目前本例患者已经完成1年的内分泌联合奈拉替尼强化治疗。末次复查显示患者病情控制良好。
本例患者在服药后出现了3~4次/天的腹泻症状,后给予洛哌丁胺(按需服用),腹泻控制良好。腹泻是奈拉替尼最常见的不良反应,其中,3级腹泻的发生率为40% [3,4]。一项探索奈拉替尼强化辅助治疗过程中采用预防性止泻方式或剂量递增方式预防腹泻疗效的国际多队列Ⅱ期研究——CONTROL研究亦显示,采用洛哌丁胺预防治疗组(洛哌丁胺 第1~14天,4mg/次 tid,第15~56天, 4mg/次 bid)的腹泻发生率显著降低为20%。此外,采用剂量递增给药模式也可以显著降低腹泻的发生率。剂量递增方案(DE1队列,奈拉替尼第1~7天:120 mg/d、第8~14天:160 mg/d,此后240 mg/d;洛哌丁胺按需使用)治疗的3级腹泻的发生率最低,仅为13%,因腹泻导致的停药率亦最低,仅为3%[10]。本例患者在服用洛哌丁胺后,腹泻次数减少。可见,通过适当的预防和管理措施,奈拉替尼的腹泻不良反应可得到改善,这亦有利于提高患者的治疗依从性。
[1] New estimates of the global burden of cancer in2020 now published! #Globocan2020.IARC estimatesthat the cancer burden has risen to 19.3 million newcases 8 10.0 million deaths this year gco.iarc.fr/today/home
[2] Wang X, Xia CF, Wang Y, et al. Landscape of young breast cancer under 35 years in China over the past decades: a multicentre retrospective cohort study (YBCC-Catts study). EClinicalMedicine. 2023 Sep 22.
[3]Chan A, Delaloge S, Holmes F A, et al. Neratinib after trastuzumab-based adjuvant therapy in patients with HER2-positive breast cancer (ExteNET): A multicentre, randomised, double-blind, placebo-controlled, phase 3 trial[J]. The Lancet Oncology, 2016, 17(3).
[4]Chan A , Moy B , Mansi J ,et al.Final efficacy results of neratinib in HER2-positive hormone receptor-positive early-stage breast cancer from the phase III ExteNET trial[J].Clinical Breast Cancer, 2020.DOI:10.1016/j.clbc.2020.09.014.
[5]Nrgaard P R ,Esen Buket ztürk, Lene M ,et al.The Incidence of Breast Cancer Recurrence 10-32 Years After Primary Diagnosis[J].JNCI: Journal of the National Cancer Institute(3):3[2023-12-06].DOI:10.1093/jnci/djab202.
[6]《中国乳腺癌新辅助治疗专家共识(2022年版)》专家组,邵志敏.中国乳腺癌新辅助治疗专家共识(2022年版)[J].中国癌症杂志, 2022, 32(1):9.DOI:10.19401/j.cnki.1007-3639.2022.01.011.
[7] Nuciforo P , Townend J , Piccart M J ,et al.Ten-year survival of neoadjuvant dual HER2 blockade in patients with HER2-positive breast cancer[J].European journal of cancer: official journal for European Organization for Research and Treatment of Cancer (EORTC) [and] European Association for Cancer Research (EACR), 2023.
[8] HURVITZ S A, MARTIN M, JUNG K H, et al. Neoadjuvant trastuzumab emtansine and pertuzumab in human epidermal growth factor receptor 2-positive breast cancer: three-year outcomes from the phase Ⅲ KRISTINE study[J]. J Clin Oncol, 2019, 37(25): 2206-2216.
[9]2022版CSCO乳腺癌诊疗指南
[10] Chan A, Ruiz-Borrego M, Marx G,et al. Final findings from the CONTROL trial: Strategies to reduce the incidence and severity of neratinib-associated diarrhea in patients with HER2-positive early-stage breast cancer. Breast. 2023 Feb;67:94-101.
排版编辑:肿瘤资讯-Tracy











 苏公网安备32059002004080号
苏公网安备32059002004080号


